维持性血液透析患者腹主动脉钙化危险因素的相关性分析
符业,李灿,胡波
(攀钢集团总医院肾脏内科,四川 攀枝花 617023)
血管钙化是慢性肾脏病-矿物质和骨异常(CKD-MBD)重要组成部分,其发生率及严重程度与肾功能的恶化有关,也是患者发生心血管疾病的重要诱因[1-2]。对于长期进行血液透析治疗的患者,腹主动脉钙化(aorta abdominalis calcification,AAC)较为常见。了解AAC发生的危险因素,对有效防治ACC、改善患者预后具有重要作用。本文主要研究影响AAC发生的因素,现报告如下。
1 资料和方法
1.1 研究对象
研究对象为2015年6月至2017年6月于攀钢集团总医院行维持性血液透析治疗≥3个月的99例终末期肾脏病(end-stage renal disease,ESRD)患者。排除长期服用糖皮质激素、合并严重实质性脏器疾病、恶性肿瘤及各种原因导致长期卧床不起或者不能独立行走患者。99例患者中,男性62例,女性37例;原发病:慢性肾炎57例,糖尿病肾病20例,高血压肾病12例,狼疮性肾炎1例,紫癜性肾炎1例,泌尿系结核1例,梗阻性肾病1例,多囊肾4例,抗中性粒细胞胞浆抗体(ANCA)相关性肾损害2例。
1.2 方法
1.2.1 资料收集 记录患者性别、年龄、透析龄、体重指数(BMI)=体重 (kg) /身高(m2)、OSTA指数[即亚洲人骨质疏松自我筛查工具(OSTA)=(体质量—年龄)×0.2]、透析前后血压、检测透前血钙(Ca)、血磷(P)、血肌酐(SCr)、甲状旁腺激素(PTH)、铁蛋白及同型半胱氨酸(Hcy)水平、股骨颈骨密度(BMD)、腰椎BMD、髋关节BMD、股骨颈T值、髋关节T值。
1.2.2 血管钙化评估 应用腹部侧位X光片对患者进行腹主动脉钙化评分(AAC),X光片包括第11、12节胸椎骨、第l~5腰椎和第1、2节骶椎骨。根据kauppila等[3]报道的半定量积分方法,由两位放射科医师对患者第1节至第4节腰椎对应的腹主动脉钙化情况进行盲法评分,计算腹主动脉钙化(AAC)评分,最终得分取其平均值。血管钙化评分根据腹主动脉前壁和后壁钙化斑块的长度评估,采用Likert 4级(0~3分)评分法,0分、1分、2分和3分分别表示无钙化、轻度钙化、中度钙化和重度钙化。各患者腹主动脉钙化总积分为0~24分,根据AAC得分将患者分为无钙化组(AAC=0)、钙化组(AAC>0)。
1.3 统计学分析
所有数据采用SPSS统计软件完成。计量资料正态分布,两组比较使用方差分析,t检验;计量资料偏态分布,使用Kruskal-Wallis检验,计数资料使用χ2检验。采用Logistic回归分析进行多因素分析,以P<0.05为差异有统计学意义。
2 结果
2.1 维持性血液透析患者AAC单因素分析
99例患者中存在腹主动脉钙化者70例,占比70.71%。单因素分析显示,无钙化组与钙化组的年龄、OSTA指数、血Ca、血P、血SCr、PTH及腰椎BMD比较,差异有统计学意义(P<0.05)。

表1 维持性血液透析患者AAC单因素分析
2.2 多因素分析
对单因素分析存在统计学差异的影响因素进行多因素分析,结果显示年龄、血Ca、血P、血SCr、PTH是AAC危险因素,OSTA指数、腰椎BMD为保护因素。
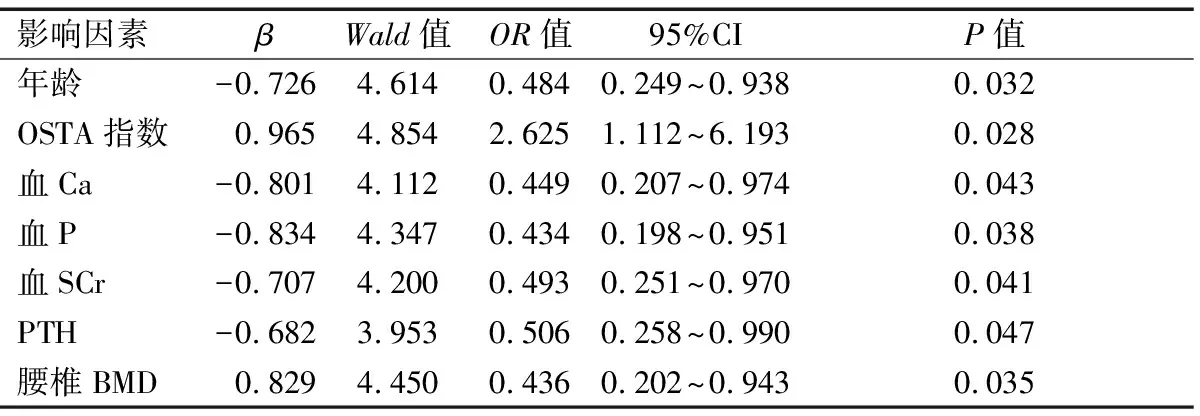
表2 多因素分析
3 讨论
随着CKD-MBD指南的发布,人们对维持性血液透析患者发生ACC的关注度也越来越高。相关资料[4-5]显示,相较于无ACC患者,ACC患者心血管疾病发生率及死亡率明显较高。ACC是长期进行血液透析治疗的患者重要并发症,其发生机制较为复杂,目前还未有统一结论。本次研究结果显示,70.71%的ESRD患者存在ACC,表明长期行维持性血液透析的ESRD患者ACC发生率较高。
对无钙化组与钙化组患者资料进行影响因素分析,显示年龄、血Ca、血P、血SCr、PTH是AAC危险因素。血管钙化是由与骨代谢相似的细胞机制参与调节,是常见的、与年龄相关的机体改变。马潭涌等[6]研究表明,年龄是ACC发生的危险因素,这是因为随年龄增长,血管中钙沉积增多,血管逐渐钙化,即使非维持性血液透析患者也会随着年龄增长而出现血管功能下降,血管钙化发生。研究表明,慢性肾脏病患者长期血Ca、血P水平异常,钙磷代谢紊乱,P可通过血管平滑肌膜上的磷酸协同转运蛋白进入到细胞内,对血管成纤维细胞进行诱导,继而产生骨钙素、I型胶原等成骨细胞因子,而这些特异性骨蛋白可诱导血管钙化发生[7-8]。此外,钙磷代谢紊乱还会引发继发性甲状旁腺功能亢进,PTH水平升高,而长期高水平PTH易诱发高转运骨病,进而使得破骨细胞数量及活性增加,骨吸收活跃性异常增强,这又会导致血Ca、血P升高,进而促进ACC发生[9-11]。付影等[12]研究也发现,高水平PTH可能参与了血管钙化的发生与发展。
本次结果还显示,OSTA指数及腰椎BMD为保护因素,而以往研究极少报道这两点。长期临床研究发现,骨质疏松症发病与血管钙化具有密切关系,血管钙化会促进骨质疏松发生和发展,骨质疏松患者同时也存在血管钙化[13]。分析原因:正常条件下,通过成骨细胞和破骨细胞交互作用,钙盐溶解和沉积处于动态平衡,而当骨吸收和骨形成打破平衡状态,骨吸收增加时,骨质疏松发生,骨钙融出进入血管,钙沉积于动脉管壁,造成血管钙化,使得动脉硬化等疾病发生[14]。OSTA指数作为骨质疏松症重要筛查指标,对评估骨质疏松症风险发生具有重要价值,OSTA指数越低,代表发生骨质疏松症的可能性越高[15],即钙化风险也越高。而BMD也是骨质疏松的一种反映,松质BMD越低、骨量丢失越严重者患有ACC的可能性越高[16]。刘红敏等[17]研究中老年ACC与腰椎BMD的相关性,发现两者无显著相关性,可能是该研究与本次研究纳入者样本量及特点不同,相关研究表明,不同居住环境下,血管钙化的发生率也不尽相同。
综上所述,年龄、血Ca、血P、血SCr、PTH均是AAC发生危险因素,而OSTA指数、腰椎BMD为保护因素,临床可针对性采用有关措施进行预防。但本次研究亦存在不足,研究人群仅限于本院患者,样本量较少,且未探究不同检查方法对BMD测量的影响,因此还需在往后的研究中进一步探讨。

