舒肝宁注射液与10%葡萄糖注射液配伍稳定性研究
林小明,黄 敏,谢培德
0 引言
舒肝宁注射液(SGN)是以张仲景《伤寒论》中的名方“茵陈蒿汤”为基础方,依据该方随症加减化裁而成,组方由茵陈、栀子、板蓝根、灵芝等药物的提取物及黄芩苷组成,具有清热解毒、利湿退黄、益气扶正、保肝护肝等功效,对机体免疫功能具有调节和增强作用[1],对脂肪肝具有改善作用[2-3],目前临床上主要用于肝炎、高胆红素血症、肝功能损害、脂肪肝、胆管炎等的治疗[4]。作为一种保肝护肝药物,临床上常将其与5%葡萄糖注射液(5%GS)、10%葡萄糖注射液(10%GS)、氯化钠注射液(NS)配伍应用。已有报道,舒肝宁注射液与NS配伍不溶性微粒符合规定[5],但与5%GS配伍≥10 μm的微粒数不符合标准,而SGN与10%GS的配伍情况至今未见有报道。为此,我们以配伍溶液的外观、pH值、不溶性微粒,以及绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷含量的变化为指标,考察其与10%GS配伍液的稳定性,为临床用药提供参考。
1 仪器与试药
高效液相色谱仪(岛津LC-10A Class-VP),pHS-2C型精密酸度计(上海雷磁仪器厂),GWF-5J 型微粒分析仪(天河医疗器械设备有限公司),SW-CJ-1FD洁净工作台(苏州净化设备有限公司),狮鼎SHB循环水式多用真空泵(郑州长城工贸有限公司),津腾溶剂过滤器。SGN(贵州瑞和制药有限公司,规格:2 ml,批号:20170312),10%GS(广东大冢制药有限公司,规格:500、250、100 ml,批号:B1612082、E1611141、B1708071)。对照品:绿原酸(批号:LYS2017041901)、黄芩素(批号:HQS2017071302)、野黄芩苷(批号:YHQG2017032301)、栀子苷(批号:MUST-17020401)、黄芩苷(批号:MUST-17031811)均购自南京春秋生物工程有限公司,所有对照品纯度均>98%。甲醇为色谱纯,其他试剂为分析纯。
2 方法与结果
2.1 实验用水制备 取注射用水,用0.45 μm微孔滤膜过滤,初滤液弃去,得实验用水。经检测符合中国药典2015年版(四部)通则项下微粒检查用水有关规定。
2.2 试验用具准备 于层流净化台上将实验用具用实验用水冲洗至洁净,备用。
2.3 配伍溶液制备 模拟临床用药浓度及操作,于层流净化台上进行配制。精密吸取规定量的SGN,置于规定的量瓶中,加10%GS 定容,摇匀,即得。配伍液的具体剂量和溶媒用量:①SGN 10 ml+10%GS至100 ml,②SGN 10 ml+10%GS至250 ml,③SGN 10 ml+10%GS至500 ml,④SGN 20 ml+10%GS至100 ml,⑤SGN 20 ml+10%GS至250 ml。上述溶液各5份。
2.4 稳定性考察 取“2.3”项下的配伍液分别于0、2、4、6 h观察溶液的外观,测定溶液的pH 值、不溶性微粒及绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷含量的变化情况。
2.5 不溶性微粒测定 按照《中国药典》2015年版(四部)通则项下不溶性微粒检查法,用GWF-5J型微粒分析仪测定。
2.5.1 空白试验 取试验用SGN 15支,10%GS每个规格取4袋,测定其不溶性微粒,取平均值。结果见表1。结果表明,本次试验所用药液均符合规定。
2.5.2 配伍溶液放置不同时间点的不溶性微粒测定 对“2.3”项下的25个样品溶液放置不同时间后,用GWF-5J 型微粒分析仪对溶液中的不溶性微粒进行测定,每个时间点的配伍液均重复测定5次,取平均值。结果见表2。
2.6 配伍溶液放置不同时间点其外观和pH值的检查 对“2.3”项下25个样品溶液不同时间点的溶液外观进行观察,并按照《中国药典》2015年版(四部)通则项下pH值测定法检查其溶液pH值的变化。结果显示,25个样品溶液外观放置6 h内未发生变化,均为棕黄色透明液;溶液pH值变化均未超过0.2。见表3。
2.7 配伍液有效成分的含量测定[6]

表1 SGN和溶媒的不溶性微粒数测定结果(个/ml)
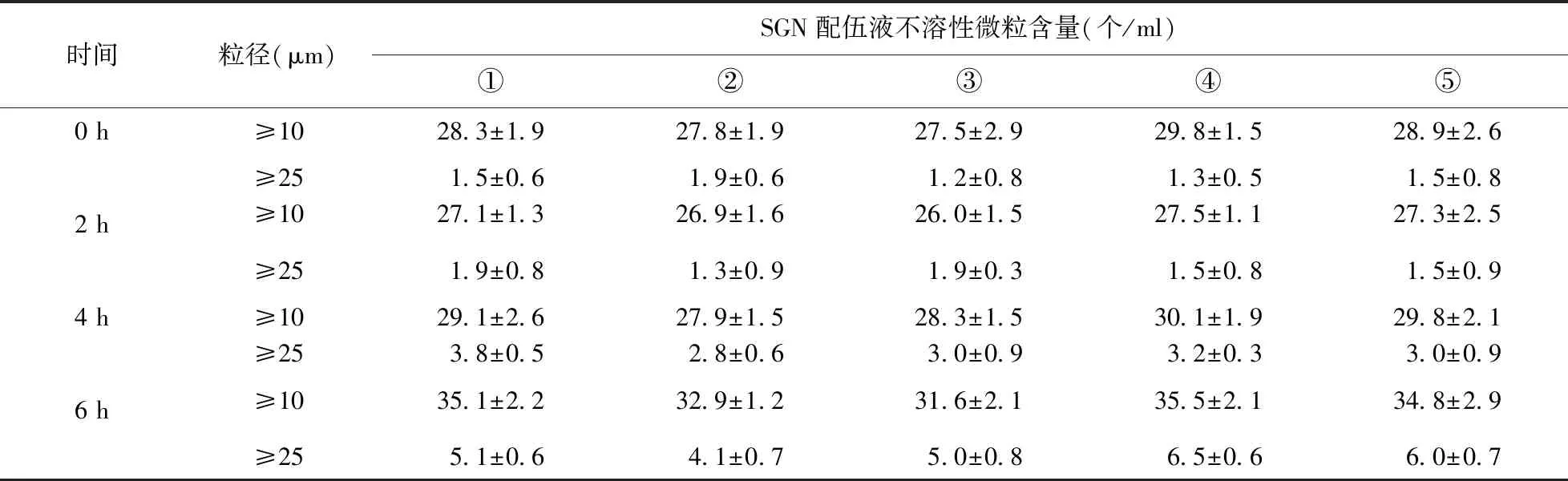
表2 配伍液不同时间点不溶性微粒的变化情况(n=5)
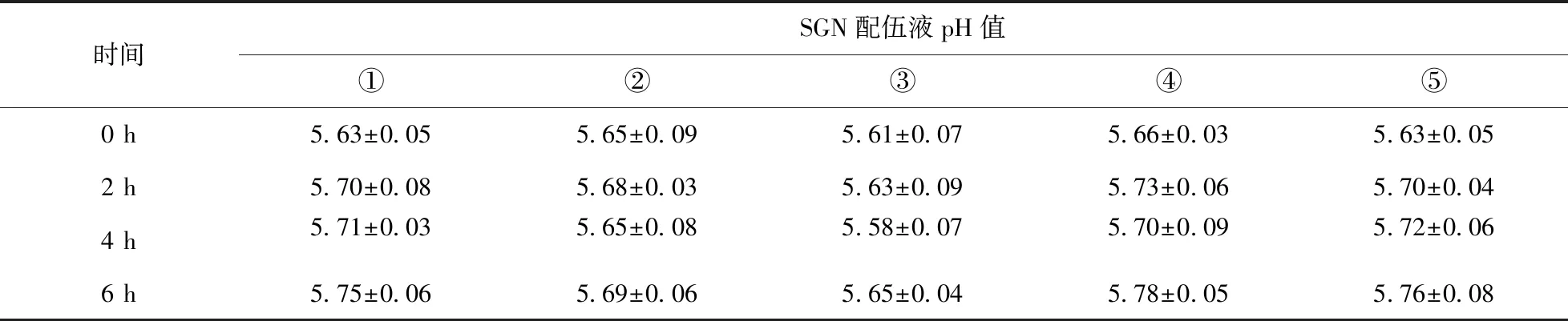
表3 配伍液不同时间点pH值的变化情况(n=5)
2.7.1 色谱分析条件 色谱柱:YMC-Pack ODS-A C18(250 mm×4.6 mm,5 μm),柱温30 ℃;流动相:0.4%磷酸溶液(A)-甲醇(B),梯度洗脱(0~23 min,75%→25%B),流速1 ml/min;进样量10 μl;检测波长:238 nm(黄芩苷、栀子苷)、327 nm(黄芩素、野黄芩苷、绿原酸)。
2.7.2 对照品溶液的制备 精密称取绿原酸14.12 mg、栀子苷70.65 mg、黄芩苷404.5 mg、黄芩素12.16 mg、野黄芩苷20.96 mg,置50 ml量瓶中,加甲醇25 ml溶解,加实验用水至刻度,摇匀。取此溶液25 ml,置500 ml量瓶中,加实验用水至刻度,摇匀即得对照品溶液。
2.7.3 标准曲线的制备 精密量取“2.7.2”项下对照品溶液2、20、40、60、80、100 ml,分别置于100 ml量瓶中,加实验用水至刻度,摇匀,制成系列不同浓度(即绿原酸0.282 4、2.824、5.648、8.472、11.296、14.12 μg/ml,栀子苷1.413、14.13、28.26、42.39、56.52、70.65 μg/ml,黄芩苷8.090、80.90、161.8、242.7、323.6、404.5 μg/ml,黄芩素0.243 2、2.432、4.864、7.296、9.729、12.16 μg/ml,野黄芩苷0.419 2、4.192、8.394、12.58、16.77、20.96 μg/ml)的溶液。按“2.7.1”项下的色谱分析条件对上述溶液依次测定,记录峰面积。以对照品的浓度X(μg/ml)为横坐标、峰面积Y为纵坐标进行线性回归,得绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷的回归线方程分别为:Y=(39.52 X+3.016)×103(r=0.999 8)、Y=(21.91 X+1.016)×103(r=0.999 7)、Y=(19.62 X+4.523)×103(r=0.999 9)、Y=(38.25 X+3.152)×103(r=0.999 8)、Y=(29.51 X+1.765)×103(r=0.999 6),线性范围分别为:0.282 4~14.12 μg/ml、1.413~70.65 μg/ml、8.090~404.5 μg/ml、0.243 2~12.16 μg/ml、0.419 2~20.96 μg/ml。
2.7.4 精密度试验 精密量取“2.7.2”项下对照品溶液40 ml,置于100 ml量瓶中,加实验用水至刻度,摇匀,按“2.7.1”项下的色谱分析条件,测定其待测成分的含量,连续重复进样6次。结果绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷含量的RSD(n=6)分别为0.81%、1.21%、1.50%、0.96%、1.36%。
2.7.5 重复性试验 取舒肝宁注射液10 ml,加入100 ml的5%GS中,摇匀。精密量取5 ml,6份,分别置于10 ml量瓶中,加实验用水至刻度,用0.45 μm滤膜过滤,取续滤液,按“2.7.1”项下的色谱分析条件,测定其待测成分的含量。结果绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷含量的RSD(n=6)分别为0.98%、1.51%、1.62%、0.86%、1.69%。
2.7.6 回收试验 精密吸取已知含量的舒肝宁注射液(绿原酸33.56 μg/ml、栀子苷595.7 μg/ml、黄芩苷19563 μg/ml、黄芩素50.60 μg/ml、野黄芩苷139.5 μg/ml)1、2、4 ml,分别置于50 ml量瓶中,各精密加入“2.7.2”项下对照品溶液1 ml,加实验用水至刻度,摇匀,用0.45 μm滤膜过滤,取续滤液,按“2.7.1”项下的色谱分析条件,测定其待测成分的含量。结果绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷含量(低、中、高浓度)回收率分别为>99%、>99%、>99%、>98%、>99%,RSD(n=3)分别为<1.8%、<1.4%、<1.4%、<1.6%、<1.7%。
2.7.7 配伍液有效成分的含量测定 精密吸取“2.3”项下放置不同时间的配伍液适量(①、②、③取5 ml,④取2 ml,⑤取5 ml),置于10 ml量瓶内,加实验用水定容,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,按“2.7.1”项下色谱分析条件进行测定,记录峰面积并计算其含量,见表4。
3 讨论
3.1 配伍溶媒的选择 SGN说明书于用法用量项下规定:静脉滴注,10~20 ml/次,用10%GS 250 ~ 500 ml 稀释后静脉滴注。已有报道,舒肝宁注射液与NS配伍不溶性微粒符合规定,但同5%GS配伍≥10 μm的微粒数不符合标准[1],而SGN与10%GS的配伍情况至今未见有报道,而且有少数医生使用溶媒的用量仅为100 ml。因此,本研究选择10%GS为溶媒,且溶媒用量选择在100~500 ml 范围对其配伍稳定性进行研究。
3.2 配伍液的不溶性微粒 表2结果表明,SGN与10%GS配伍0~6 h内配伍液的不溶性微粒均不符合规定,这可能与SGN pH值为6~8,而5%、10%GS pH值范围均低于SGN,从而造成SGN不稳定有关。另外,本研究结果提示,2 h内配伍液的不溶性微粒不但未随放置时间延长而增加,相反还有下降趋势;但4~6 h内配伍液的不溶性微粒随放置时间延长而增加。究其原因可能是配伍液放置后不溶性微粒出现复溶现象,而随着放置时间延长,配伍液内部又发生某些理化反应的缘故。
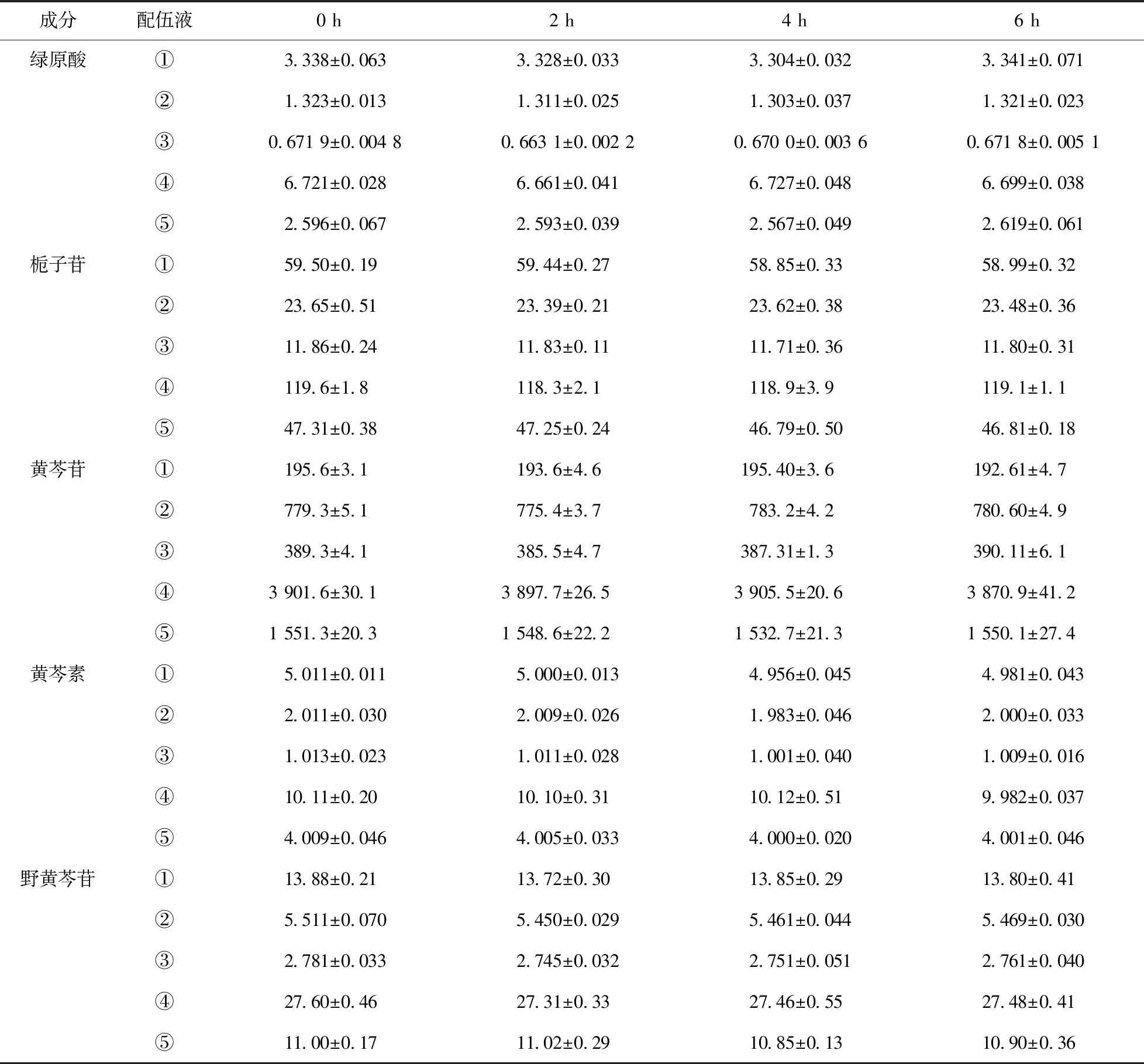
表4 配伍液不同时间点有效成分含量的变化情况(μg/ml,n=5)
3.3 配伍液的外观及pH值 结果表明,10~20 ml SGN用10%GS 100~500 ml稀释后,0~6 h内配伍液的外观均为棕黄色透明液体,各配伍液的pH值变化均未超过0.2,说明配伍液的pH值在6 h内是稳定的。但配伍液的pH值均不在SGN的质量标准(6~8)内。
3.4 有效成分含量 SGN是由茵陈、栀子、板蓝根、灵芝的提取物和黄芩苷组成。茵陈、栀子、板蓝根、灵芝的主要成分分别为绿原酸[7],栀子苷[8],尿苷、鸟苷、告依春和腺苷[9],尿苷和腺苷[10]。但在预试验中一直未找到尿苷、鸟苷、告依春、腺苷等成分的测定方法,而且在检测黄芩苷的同时检测到了野黄芩苷和黄芩素。因此,本实验仅以配伍液中绿原酸、栀子苷、黄芩苷、黄芩素、野黄芩苷含量变化作为配伍液稳定性的研究指标。表3实验结果表明,配伍液各有效成分6 h内其百分含量为98.5%~100.9%,说明在考察时间内各有效成分在配伍液中是稳定的。
综上所述,SGN与10%GS配伍后,配伍液的外观、pH值、各有效成分含量于6 h内无明显变化,但不溶性微粒数量于0~6 h内均不符合质量标准。因此,SGN与10%GS不宜配伍应用。

