儿童特发性肺含铁血黄素沉着症三例误诊及诊断思路分析
曾茂君,申婕,曾志辉,赵明一,旷寿金
特发性肺含铁血黄素沉着症(IPH)为一种弥漫性肺泡毛细血管出血性疾病,通常以反复咳嗽、气促等呼吸道症状作为首发表现,同时伴有贫血和肺部阴影。发病年龄主要为儿童期,因本病罕见,症状不典型,从而极易误诊,且病程长,反复发作,长期预后不良。本研究通过对3例IPH的临床资料进行分析,同时总结该病特征、诊断检查及误诊原因,以期为IPH的诊断提供依据。
1 病例简介
患儿1,男,11岁,因“发现皮肤黏膜苍白6年余”于2017-02-14收住中南大学湘雅三医院,患儿6年前无明显诱因出现皮肤黏膜苍白,以口唇及面色苍白为主,易疲乏,无咳嗽、咳痰、发热、盗汗,于2011年因“晕倒”在外院就诊,诊断“重度营养性贫血”,予输血、口服补铁等治疗后好转出院,出院继续治疗1个月后,血红蛋白水平升高,便自行停药。2013年再次因“重度营养性贫血”于外院住院治疗,胃镜示胃、食管、十二指肠黏膜正常,幽门螺杆菌阳性。骨髓穿刺示粒细胞系、巨核细胞系无异常,红细胞系增生明显活跃。血清铁蛋白水平正常。予阿莫西林克拉维酸钾、奥美拉唑、克林霉素、铁剂治疗10 d后,血红蛋白水平升高后出院,复查8次血红蛋白水平波动在73~112 g/L。发病以来,无消瘦,大小便正常,既往有反复上呼吸道感染史,无肝炎、结核、支气管扩张病史。以“贫血查因”入本院,体格检查示:体温36.4 ℃,脉搏110次/min,呼吸22次/min,体质量35 kg。慢性贫血面容,唇黏膜苍白,无黄疸,双肺呼吸音清,未闻及明显干湿啰音;心脏检查无异常;腹软,全腹无压痛及反跳痛,未触及明显包块,肝脾未扪及,甲床苍白,无杵状指。实验室检查:白细胞计数4.21×109/L〔参考范围:(5.00~12.00)×109/L〕,血红蛋白63 g/L(参考范围:110~160 g/L),红细胞平均血红蛋白量(MCH)16.2 pg(参考范围:27.0~34.0 pg),红细胞平均血红蛋白浓度(MCHC)253 g/L(参考范围:316~354 g/L),平均红细胞体积(MCV)64.7 fl(参考范围:82.0~100.0 fl),白小板计数185×109/L〔参考范围:(125~350)×109/L〕,网织红细胞计数0.030(参考范围:0.003~0.030)。尿常规、便常规正常,血清铁4 μmol/L(参考范围:9~32 μmol/L),总铁结合力90 μmol/L(参考范围:45~75 μmol/L),血清铁蛋白90 μg/L(参考范围:30~300 μg/L)。溶血性贫血全套(直接及间接抗人球蛋白试验、红细胞脆性试验、血红蛋白电泳)阴性、地中海贫血基因阴性,骨髓穿刺结果示红细胞系增生明显,粒细胞系、巨核细胞系无异常。胸部X线片示双肺纹理增多增粗,夹杂大量斑点样模糊影。高分辨率CT(HRCT)示双肺弥漫性病变并轻度间质改变,IPH?纤维支气管镜:肺部灌洗液示中等量柱状上皮细胞,少量淋巴细胞及中性粒细胞,另可见大量巨噬细胞,其胞质内含有金黄色或褐色颗粒。粪便寄生虫试验阴性。入院后予输注浓缩红细胞,T细胞斑点试验(T-spot)阴性,予泼尼松龙抗炎治疗后,血红蛋白84 g/L,出院后继续口服药物治疗。
患儿2,女,2岁9个月,因“面色苍白2个月,反复抽搐1 d”于2016-08-09入院。2015年10月—2016年1月因“发热、咳嗽、气促”在当地医院住院治疗4次。2016年4月再次因“喘息”口服药物及雾化治疗1个月。外院血常规示贫血,自行在家中服药治疗后无明显好转。入院前1 d无明显诱因抽搐,双眼凝视、牙关紧闭、四肢强直抖动、呼之不应,无大小便失禁及口吐泡沫,反复抽搐3次,分别持续5、30、10 min。外院经吸氧、止痉治疗,惊厥停止后意识清楚,实验室检查:白细胞计数12.62×109/L,血红蛋白24 g/L,中性粒细胞分数0.88(参考范围:0.40~0.75),淋巴细胞分数0.09(参考范围:0.20~0.40),白小板计数397×109/L。考虑“惊厥持续状态、极重度贫血”,予甘露醇减轻脑水肿,输注悬浮红细胞100 ml等对症治疗后,转入儿科。既往体质差,有反复呼吸道感染病史。体格检查示:体温37.2 ℃,脉搏130次/min,呼吸35次/min,体质量11.4 kg;贫血貌,肺部体格检查无异常;肝右肋下触及3 cm,质软;脾脏未触及,甲床苍白;病理征阴性。血常规:白细胞计数8.85×109/L,血红蛋白28 g/L,MCH 15.8 pg,MCHC 257 g/L,MCV 61.5 fl,白小板计数422×109/L,网织红细胞计数0.067。便常规正常,血清铁6 μmol/L,总铁结合力96 μmol/L,血清铁蛋白11 μg/L。溶血性贫血全套、地中海贫血基因阴性,骨髓穿刺结果示骨髓增生活跃,粒细胞系、红细胞系增生活跃,中幼粒细胞增加,巨核细胞系无异常。胸部X线片示双肺散在斑片模糊影,提示双肺感染。HRCT示双肺多发性病变,IPH?肺炎?肺部灌洗液示肺含铁细胞。T-spot阳性,考虑结核感染。脑脊液常规:总细胞10×106/L,白细胞计数2×106/L,脑脊液生化及颅脑CT未见异常。根据患儿疾病史、临床表现、实验室检查,最后诊断IPH、癫痫、结核感染。予激素及抗结核治疗后,血红蛋白水平升高后出院。
患儿3,女,3岁1个月,因“发现血红蛋白降低1年余”于2017-02-20入院,因皮肤黏膜苍白于外院就诊3次,无皮疹、出血点,无咳嗽、咳痰、黄疸。2016-02-14骨髓穿刺示骨髓增生明显活跃,粒细胞系增生减低,红细胞系明显减少,地中海贫血基因、血清铁正常。2016-05-09血红蛋白水平降至92 g/L。2016-05-10骨髓穿刺示骨髓增生明显活跃,粒细胞系、红细胞系增生活跃。2016-12-23外院血红蛋白51 g/L,诊断“营养性贫血”,予输血、补铁治疗后贫血改善,定期复查血红蛋白,维持在80~100 g/L,再次出现皮肤黏膜苍白加重,到本院门诊就诊,血常规:白细胞计数5.92×109/L,血红蛋白57 g/L,白小板计数382×109/L。胸部X线片示双肺弥漫性病变,肺含铁血黄素沉着症?感染性病变?以“重度贫血、肺含铁血黄素沉着症?”收入儿科。患儿既往无反复呼吸道感染病史,无结核病史。体格检查示:体温37.7 ℃(肛温),体质量12 kg,贫血貌,无黄染,肝右肋下可触及2 cm,其余无异常。支原体抗体1∶320(参考范围:〈1∶40)。血清铁5 μmol/L,
总铁结合力72 μmol/L,血清铁蛋白59 μg/L。溶血性贫血全套、地中海贫血基因阴性,纤维支气管镜:肺部灌洗液性质红色,可见肺含铁巨噬细胞。肺部CT示双肺野透亮度减低,双肺弥漫分布斑点状、斑片状磨玻璃样高密度灶。予激素治疗后血红蛋白维持基本稳定后出院,并继续口服药物治疗。
3例IPH患儿的临床表现及体征见表1,检验及检查结果见表2。
2 讨论
反复咯血、缺铁性贫血、弥漫性肺浸润影为IPH的典型三联征,但多数患儿无典型及特异性症状[1]。一项法国研究显示,儿童在IPH诊断中最常出现的临床特征是贫血和呼吸困难(分别为64%和68%),仅50%的患儿出现咯血[2],诊断依赖于常见临床症状、体征,同时排除其他疾病所致继发性肺含铁血黄素沉着症。该病的发病年龄有两个高峰,分别为〈5岁和〉11岁的儿童[3]。IPH发病率为(0.24~1.23)/105,但其病死率高达50%[4]。故及时诊断、早期治疗至关重要,可以改善预后。
IPH应与以下呼吸系统疾病相鉴别:(1)支气管肺炎:常见表现为咳嗽、咳痰、气促、肺部听诊可闻及干湿啰音,胸部X线片示肺部小点片状阴影。不同点在于,IPH常有贫血、咯血症状,病程长,经抗感染、输血及铁剂治疗后病情反复,而肺炎的呼吸道感染症状典型,不伴有贫血,病程短,抗生素治疗有效,当小儿肺炎合并营养性贫血时,需与之鉴别。(2)支原体肺炎:可出现痰中带血,肺部阴影,伴贫血,但支原体抗体阳性,易被误诊。(3)支气管扩张:支气管壁弹力组织、肌层及软骨破坏,导致其管腔形成异常的、不可逆性扩张、变形。主要表现为咳嗽、多痰,多见于晨起后或体位改变时。与IPH的相同点是咳嗽、咯血,但支气管扩张可有大量脓痰,痰液静置后出现分层现象,胸部X线片及CT常表现为杂乱不规则的高密度影,线状或双轨征,串珠样改变。
血液系统疾病为最易与IPH混淆的疾病。(1)缺铁性贫血:是儿童常见的血液疾病,与IPH均为小细胞低色素贫血,长期贫血可有气促、杵状指、心脏扩大[5],血清铁、铁蛋白降低,多数有网织红细胞计数正常或降低,少数可有网织红细胞计数升高。但缺铁性贫血无咯血、咳嗽,肺部无病变,胸部X线片无异常。当网织红细胞计数正常或降低时需行地中海贫血基因检查,与地中海贫血相鉴别[6]。(2)溶血性贫血:是因各种原因导致红细胞破坏超过骨髓造血代偿能力所致的一种贫血。慢性溶血性贫血,可有血红蛋白降低、网织红细胞计数升高,查体可见贫血貌,偶有皮肤黄染,肝脾大,铁剂治疗效果欠佳,需与IPH鉴别。但溶血性贫血常伴有血尿或血红蛋白尿,胸部X线片无异常,抗人球蛋白试验、红细胞渗透脆性试验、血红蛋白电泳可用于鉴别。(3)慢性失血性贫血:是由于长期出血所致的小细胞性贫血。儿童常见于肠道畸形、牛乳过敏、钩虫病等,无呼吸道感染表现,可行胃肠镜及大便隐血试验、粪便寄生虫检查、食物过敏原检查用于鉴别。
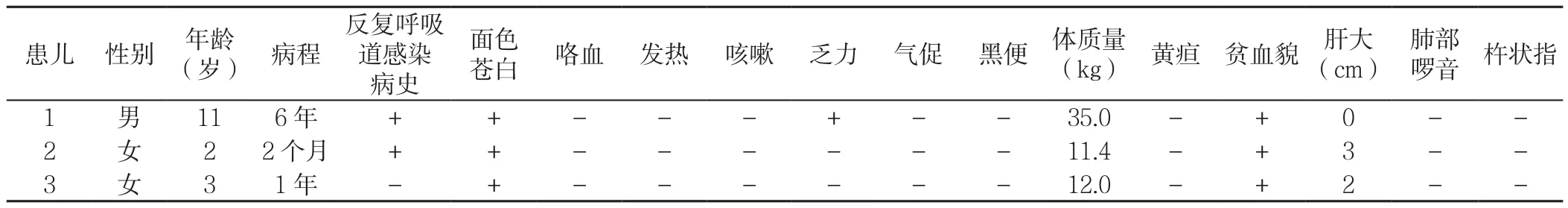
表1 3例IPH患儿临床表现及体征Table 1 Clinical manifestations and physical signs of 3 cases of pediatric idiopathic pulmonary hemosiderosis

表2 3例IPH患儿检验及检查结果Table 2 Examination results of 3 cases of pediatric idiopathic pulmonary hemosiderosis
诊断IPH时,同样要与继发性肺含铁血黄素沉着症进行鉴别,排除如IgA肾病、系统性红斑狼疮、肺出血-急性肾炎综合征、慢性心力衰竭等引起的继发性肺含铁血黄素沉着症[5]。
本文3例均误诊为缺铁性贫血,最长误诊时间达6年,主要原因是每次发生贫血时血清铁降低,铁剂治疗有效。IPH由于肺出血,铁沉积于肺泡巨噬细胞中,不能运转作为合成血红蛋白之用,血清铁和铁饱和度降低,易误诊为缺铁性贫血,且补充铁剂血红蛋白水平能升高。值得一提的是,铁蛋白常作为铁缺乏最敏感的指标,但在IPH中,血清铁蛋白水平升高或正常[6]。
本文3例患儿由于缺乏特征性三联征表现,被误诊为营养性贫血。首先,医生对该病认识不足为主要原因[7],与症状不典型、临床思维局限、临床经验不足有很大关系,详细询问病史就能否定营养性缺铁性贫血的诊断;同时出院后定期随访可降低误诊率,长期反复出现缺铁性贫血,应怀疑营养性贫血的诊断。另外家属重视程度不够,治疗后达到轻微疗效后即自行停药也是长期误诊的原因之一。
IPH常见年龄在16岁以下,6岁以下为发病高峰[8],年龄小,可无典型咯血症状,部分患儿可吞咽含血痰液[9],胃液检测肺含铁血黄素巨噬细胞可为阳性,但阳性率低,可多次复检。以往的研究显示,胃液检测含铁血黄素巨噬细胞的灵敏度为30%,而支气管或肺泡灌洗液的灵敏度为92%[10]。
长期贫血可导致患儿免疫功能下降,除以上检查外,同时需排除其他病原体感染。本文3例IPH患儿,1例合并支原体感染,1例合并结核感染,1例合并幽门螺杆菌感染,在激素治疗同时要控制感染,避免感染扩散。
综上所述,对缺铁性贫血原因不明或病情反复者,应考虑IPH可能,常规进行胸部X线片或进一步行肺部CT检查及纤维支气管镜检查,纤维支气管镜灌洗液检测到含铁血黄素巨噬细胞可排除其他原因导致的肺内出血和全身疾病,从而确诊[11]。

