Box-Behnken响应面法优化哈西奈德脂质体的制备工艺
林肖霞,蔡延渠,高建滨,蔡艳桃,苏少琴
(1.佛山市南海区妇幼保健院,广东 佛山 528200; 2.广东药科大学新药研发中心,广东 广州 510006)
哈西奈德是一种皮质类固醇,具有良好的抗感染、抗过敏、抗瘙痒和血管收缩作用[1]。局部应用不易引起全身性不良反应,目前的剂型以液体制剂、乳剂和涂抹剂等为主[2]。皮肤的角质层是药物经皮吸收的主要屏障,一般外用剂型通过添加促透剂增加经皮吸收效率,但促透剂又促进了药物的全身吸收,容易增加药物的不良反应[3]。脂质体是由两性分子双层膜包裹而成的具有一个或多个水性腔室的微泡,药物制备成脂质体后,可有效提高药物的稳定性和治疗指数[4],且脂质体具有皮肤组织靶向性、兼溶性、缓释性和无毒性,非常适合外用药物的剂型改造[5]。为了增加哈西奈德的经皮吸收率,降低促透剂的使用量,本研究制备了哈西奈德脂质体,采用Box-Behnken响应面法对其制备工艺进行优化,并考察其透皮性能。
1 材料与方法
1.1 仪器与试剂
SD大鼠,体质量(200±10)g,购于广州中医药大学实验动物中心,合格证号:SYXK(粤)2017-0125。
高效液相色谱仪(日本岛津);SHA-C水浴恒温振荡器(金坛市宏华仪器厂);BT25S电子天平(德国赛多利斯);YB-P6智能透皮试验仪(天津药典标准仪器厂);N-2110旋转蒸发仪(东京理化株式会社)。
哈西奈德(上海麦克林生化科技有限公司);胆固醇、VE、卵磷脂(上海阿拉丁生化科技股份有限公司);哈西奈德对照品(批号100146-201504,中国药品生物制品检定所)。
1.2 方法
1.2.1 哈西奈德脂质体的制备及其包封率测定方法 称取哈西奈德粉末100 mg,溶解于30 mL 0.05 mol/L PBS溶液(pH=7.5),搅拌均匀,将溶液加热至60 ℃,保持搅拌状态。卵磷脂、胆固醇和VE依据不同实验设计比例溶解于无水乙醇中,将此混合溶液使用滴管缓慢滴入哈西奈德溶液中,继续搅拌30 min。旋转蒸发去除乙醇后,超声波细胞破碎仪破碎5 min(功率150 W,超声5 s,停5 s)后,即可获得哈西奈德脂质体,置于4 ℃保存待用[6]。
哈西奈德脂质体甲醇破膜后,按《中国药典》收录的黄体酮内标法[7]测定哈西奈德的质量浓度,色谱条件:Kromasil C18色谱柱,流动相为甲醇-水-乙醚(体积比76∶20∶4),检测波长为238 nm。哈西奈德脂质体甲醇破膜后,测定的哈西奈德质量浓度即为哈西奈德脂质体中药物总量,超速离心法分离哈西奈德脂质体与游离哈西奈德,测定游离哈西奈德总质量,包封率=哈西奈德脂质体中药物总量-游离哈西奈德质量/哈西奈德脂质体中药物总量×100%。
1.2.2 单因素试验 以哈西奈德脂质体包封率为指标,对哈西奈德∶磷脂(质量比,下同)、胆固醇∶磷脂(质量比,下同)、VE∶磷脂(质量比,下同)和乙醇用量进行单因素试验。各因素选择范围分别如下:哈西奈德∶磷脂为1∶10、2∶10、3∶10、4∶10、5∶10、6∶10,胆固醇∶磷脂为1∶10、2∶10、3∶10、4∶10、5∶10、6∶10,VE∶磷脂为0∶10、0.5∶10、0.1∶10、0.15∶10、0.20∶10、0.25∶10,乙醇用量为1、3、5、7、9、11 mL。每个试验重复3次。
1.2.3 Box-Behnken响应面优化设计 依据单因素试验结果,采用Box-Behnken响应面优化制备工艺,选取A因素(哈西奈德∶磷脂)、B因素(胆固醇∶磷脂)、C因素(VE∶磷脂)和D因素(乙醇用量),设计4因素3水平试验方案,以包封率为响应值(Y),并以-1、0、1分别代表变量的因素编码,基于Box-Behnken响应曲面设计试验方案按表1进行试验,共29次试验,采用Design expert 8.0对试验结果进行分析。
表1Box-Behnken试验因素水平和编码
Table1Factor Level and Coding in Box-Behnken Test

因素水平-101A(哈西奈德∶磷脂)1∶102∶103∶10B(胆固醇∶磷脂)1∶102∶103∶10C(VE∶磷脂)0∶100.5∶101∶10D(乙醇用量/mL)357
1.2.4 体外透皮试验 分别配制2.5 mg/mL的哈西奈德溶液和哈西奈德脂质体溶液。大鼠脱颈处死后,苦味酸去毛,取腹部两侧皮肤,剔除皮下脂肪。将皮肤置于透皮扩散装置,皮肤角质层面对释放池,真皮层面向接受池,释放液为0.3 mL,接受液为5 mL,温度为(37.5±0.5)℃,振速为150 r/min,分别于2、4、6、8、10、12 h取样4 mL,并补足等量接受液,按下式计算累积透过量:
式中,Q为第n次取样时的累积透过量;A为扩散面积(cm2);Cn为n时间点取样浓度;Ci为1,2,3…n-1时间点取样浓度。
再按公式“累积透过率=累积透过量/哈西奈德总量×100%”计算累积透过率。
1.3 数据处理
2 结果
2.1 单因素试验结果
从图1的单因素试验结果可见,哈西奈德∶磷脂为2∶10、胆固醇∶磷脂为1∶10、VE∶磷脂为0.5∶10、乙醇用量为5 mL时,哈西奈德脂质体具有最高的包封率。因此,在设计4因素3水平响应面优化试验中,哈西奈德∶磷脂选择1∶10、2∶10、3∶10,胆固醇∶磷脂选择1∶10、2∶10、3∶10,VE∶磷脂选择0∶10、0.5∶10、1∶10,乙醇用量选择3、5、7 mL。
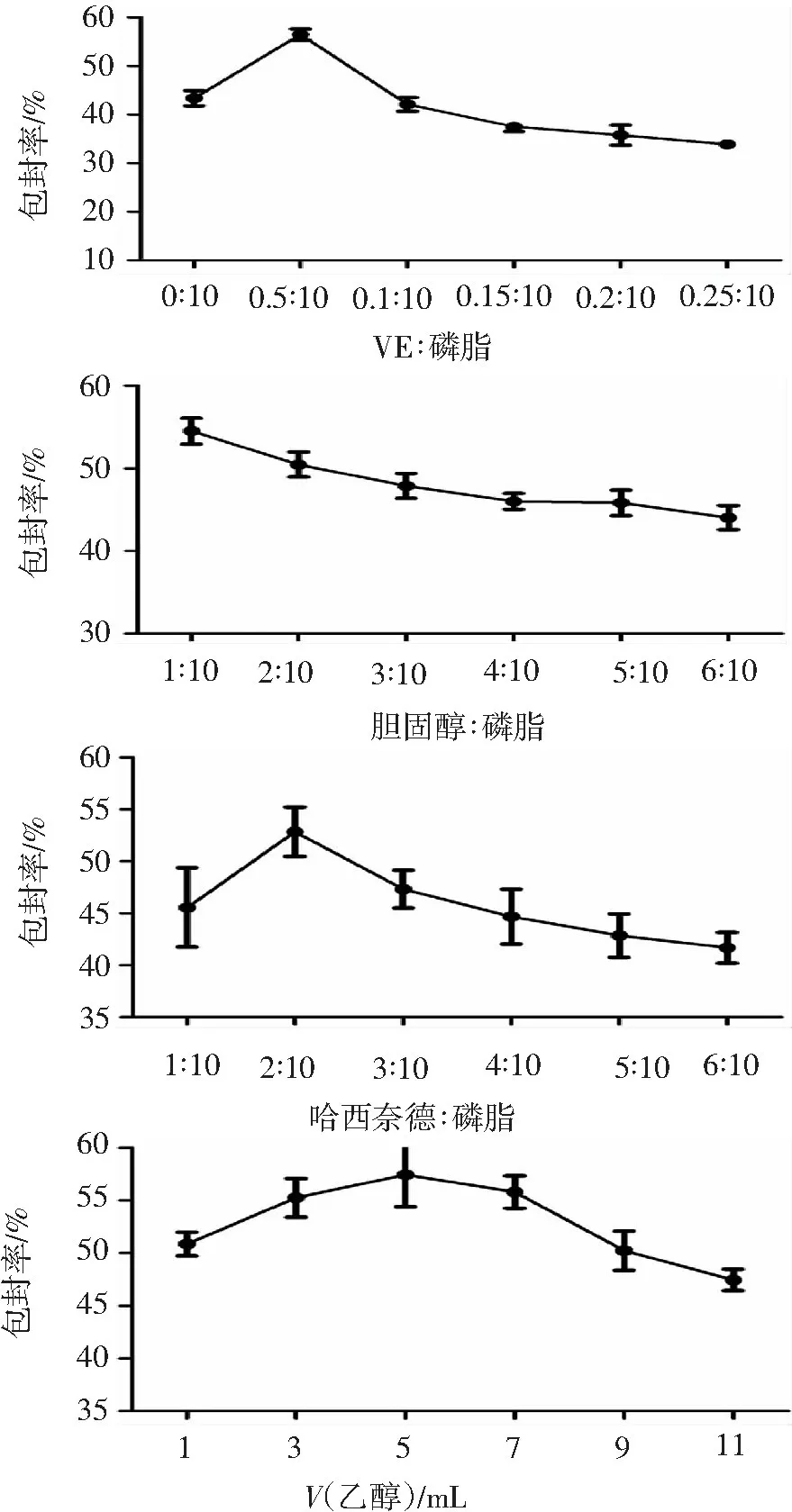
图1各因素对哈西奈德脂质体包封率的影响
Figure1Effects of various factors on encapsulation rate of Hassinide liposomes
2.2 响应面法优化制备工艺结果
2.2.1 Box-Behnken响应面试验设计优化结果
Box-Behnken试验方案及结果见表2。
表2Box-Behnken响应面试验设计与结果
Table2Design and results of Box-Behnken response surface experiments

编号因素ABCD包封率/%12∶102∶100.5∶10455.35222∶102∶100∶10558.03131∶102∶100∶10457.87242∶102∶101∶10344.72252∶101∶101∶10440.43462∶102∶101∶10552.65771∶102∶100.5∶10348.17683∶102∶100.5∶10564.21591∶103∶100.5∶10459.353101∶102∶101∶10449.707112∶101∶100∶10436.915122∶102∶100∶10338.744131∶102∶100.5∶10541.526143∶102∶100∶10439.790152∶101∶100.5∶10330.673162∶103∶100.5∶10344.55172∶102∶100.5∶10459.236182∶103∶100.5∶10450.107192∶101∶101∶10544.196202∶102∶100.5∶10458.059212∶103∶100.5∶10554.367222∶102∶100.5∶10451.157233∶101∶100.5∶10435.379243∶102∶100.5∶10332.129251∶101∶100.5∶10428.853263∶103∶100.5∶10443.478272∶102∶100.5∶10453.807283∶102∶101∶10451.812292∶103∶100∶10455.062
2.2.2 模型建立与回归分析 采用Design-expert 8.0.6.1对实验数据进行回归分析,建立的二次多元回归方程如下:
Y=81.61+2.02A-0.90B-1.09C-1.67D-2.67AB+3.38AC+1.94AD+2.89BC-1.63BD+0.21CD-9.91A2-4.65B2-4.71C2-3.94D2。
对方程的回归分析结果(表3)显示:模型的F值为5.98,P<0.001,表明模型具有显著性,只有0.10%的概率是由于噪声导致F值偏大;失拟项的数值为0.088 2,>0.05,表明失拟项对于误差不显著,回归方程拟合度较好。模型决定系数为R2=0.713 6,表明该模型可以解释响应面中85.68%的可变性;模型中,哈西奈德∶磷脂-VE∶磷脂、哈西奈德∶磷脂-哈西奈德∶磷脂、胆固醇∶磷脂-胆固醇∶磷脂、VE∶磷脂-VE∶磷脂、乙醇-乙醇之间的相互作用对哈西奈德脂质体包封率均具有显著影响(P<0.05或P<0.01)。
响应面曲线图可直观反映响应值和试验参数之间的相关关系,图2分别是哈西奈德∶磷脂、胆固醇∶磷脂、VE∶磷脂、乙醇用量之间的相互作用对脂质体包封率的响应面图。
2.2.3 验证试验 通过响应面分析,得到最优制备工艺如下:哈西奈德∶磷脂为2.1∶10,胆固醇∶磷脂为1.9∶10,VE∶磷脂为0.4∶10,乙醇用量为4.66 mL,预测包封率为81.95%。对最优制备工艺进行3次验证试验,得到实际包封率为(79.25±4.24)%,与理论值的误差为2.7%。
2.3 哈西奈德脂质体的表征
哈西奈德脂质体的表征结果显示,哈西奈德脂质体形态圆整,粒径分布均匀,平均粒径为(148.2±10.3)nm,Zeta电位为41.67 mV,见图3。
2.4 哈西奈德脂质体透皮性能分析
从表4可见,哈西奈德脂质体组的2、4、6、8、10、12 h累积透过量和累积渗透率均显著高于对照组。
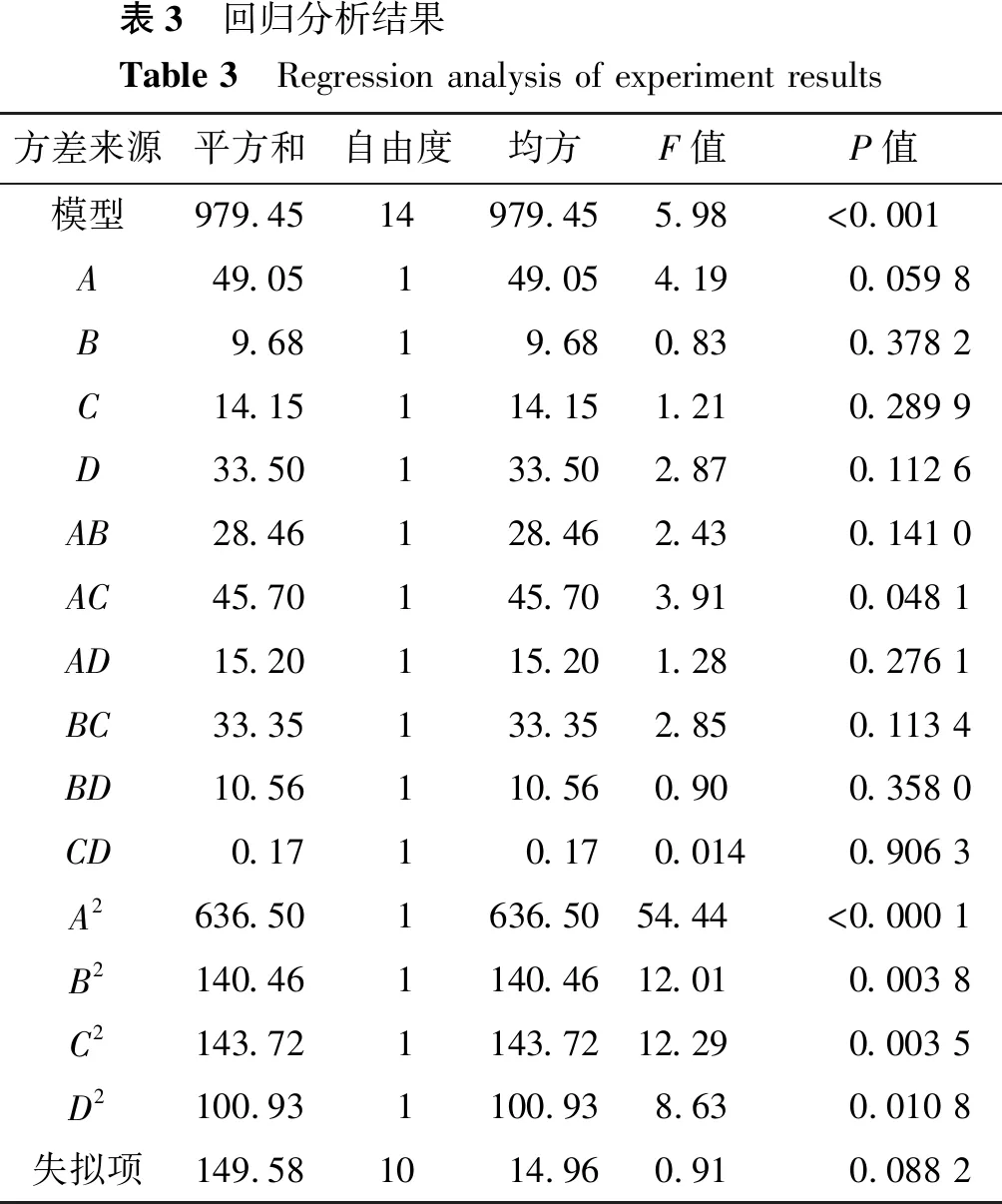
表3 回归分析结果Table 3 Regression analysis of experiment results方差来源平方和自由度均方F值P值模型979.4514979.455.98<0.001A49.05149.054.190.059 8B9.6819.680.830.378 2C14.15114.151.210.289 9D33.50133.502.870.112 6AB28.46128.462.430.141 0AC45.70145.703.910.048 1AD15.20115.201.280.276 1BC33.35133.352.850.113 4BD10.56110.560.900.358 0CD0.1710.170.0140.906 3A2636.501636.5054.44<0.000 1B2140.461140.4612.010.003 8C2143.721143.7212.290.003 5D2100.931100.938.630.010 8失拟项149.581014.960.910.088 2
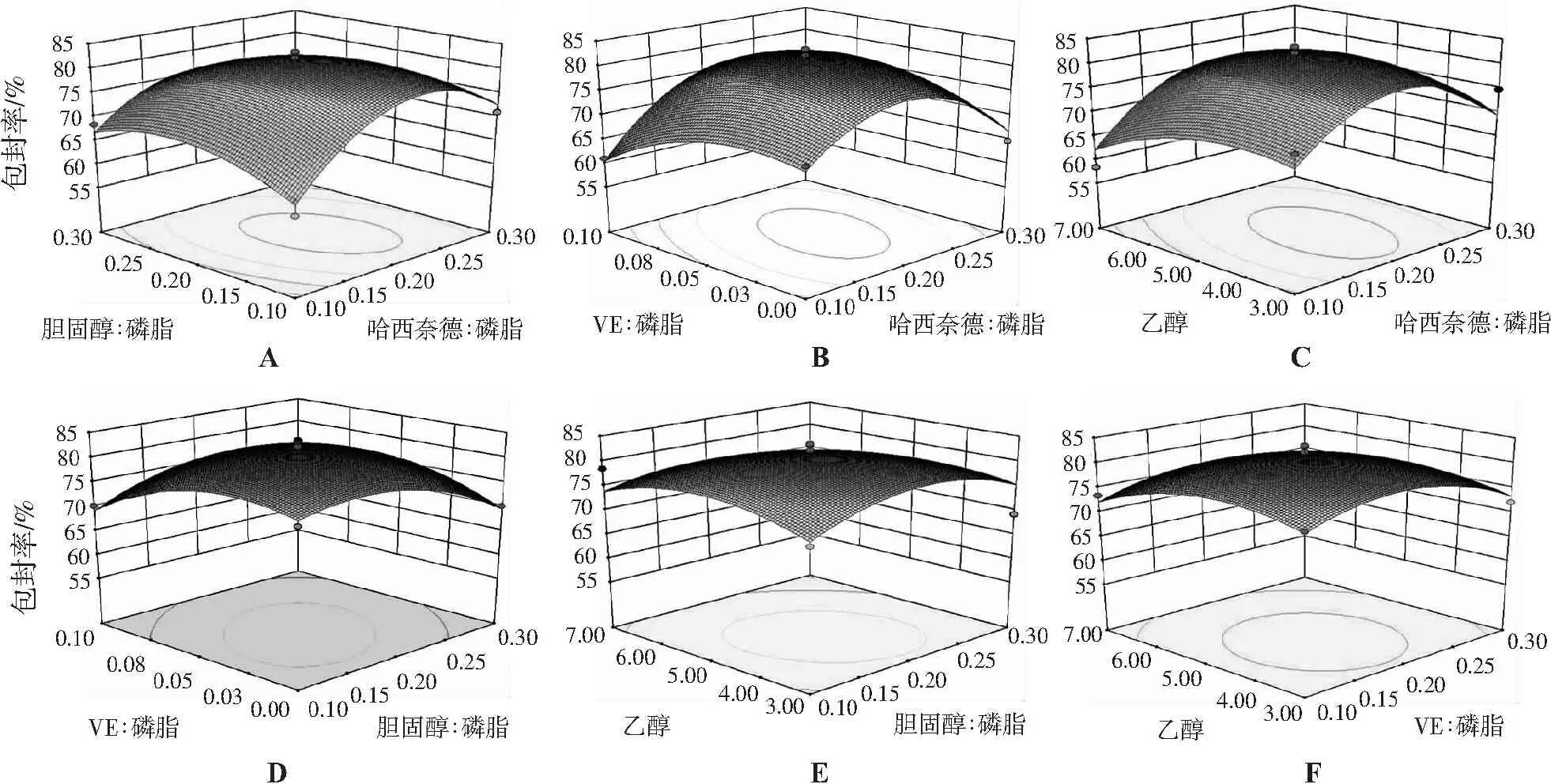
A.哈西奈德∶磷脂-胆固醇∶磷脂; B.哈西奈德∶磷脂-VE∶磷脂; C.哈西奈德∶磷脂-乙醇; D.胆固醇∶磷脂-VE∶磷脂; E.胆固醇∶磷脂-乙醇;F.VE∶磷脂-乙醇
图2各因素交互作用对哈西奈德脂质体包封率的影响
Figure2Response surface curves of encapsulation efficiency of Hassinide liposomes by two-factor interactions
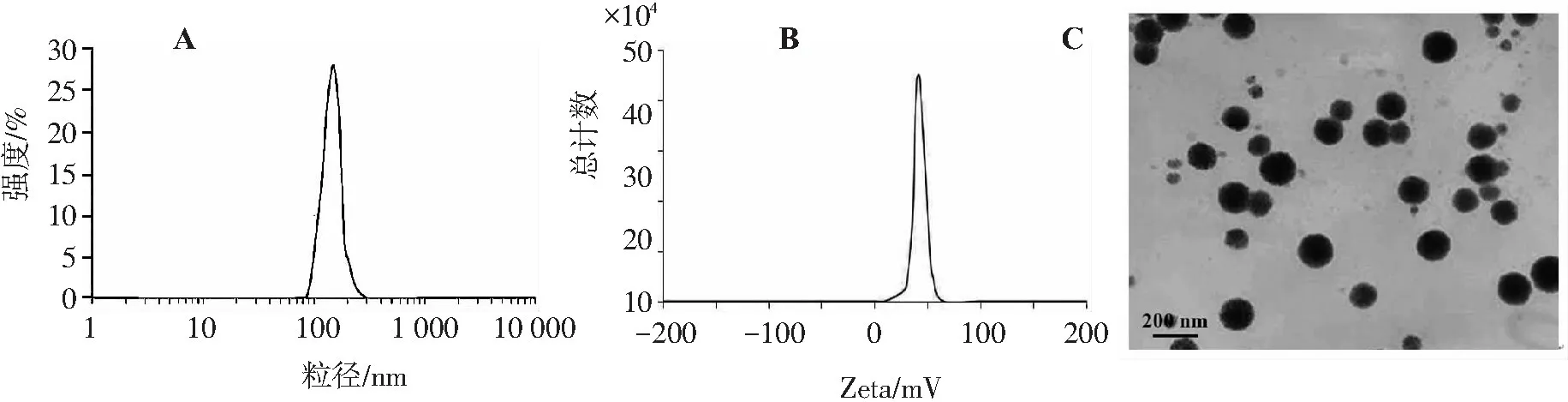

A.脂质体粒径分布图; B.脂质体电位分布图; C.脂质体透射电镜图。
与溶液组比较:**P<0.01。
3 讨论
目前,脂质体已被应用于多种外用药物,如丁卡因脂质体[8]、维甲酸脂质体[9]、鬼臼毒素脂质体[10]和氢化可的松脂质体[11]等。通过制备脂质体可有效改善药物的经皮吸收性能。本研究采用乙醇注入-超声法制备了哈西奈德脂质体。影响脂质体制备的因素众多,单因素实验不能考察因素与因素之间的相互影响,正交试验注重于科学的安排试验,寻找最佳的因素水平组合,但考虑因素之间的交互作用时,试验次数将显著增加。为此,本研究采用响应面分析法对工艺进行了优化。
响应面分析法是通过对响应面等值线的分析寻求最优工艺参数,采用多元二次回归方程来拟合因素与响应值之间函数关系,并通过对回归方程的分析来寻求最优工艺参数,解决多变量问题的一种统计方法[12],广泛应用于生物学、食品学及医药学等领域[13]。本研究以包封率为响应值,对哈西奈德脂质体的制备工艺进行了优化,通过单因素试验设定4因素3水平试验,共29次试验,为避免实验操作带来的异常误差,每次实验均测定了脂质体的粒径,使单次结果脂质体粒径变化控制在10%内。
传统脂质体制备采用三氯甲烷、乙醇和甲醇等有毒有机试剂,本研究采用了无毒的乙醇进行制备哈西奈德脂质体,乙醇可以降低脂质体之间的水合力,乙醇过量可导致脂质体的聚集融合[14]。脂质体膜的组成极大影响脂质体的包封率,磷脂加入一定比例的胆固醇可以增加脂质双分子膜中分子间的紧密程度,但过量导致膜不对称性,导致药物泄漏。磷脂中的不饱和酰基链易氧化,因此需在制备过程中加入一定的抗氧化稳定磷脂,VE是一种常见的脂质体抗氧化剂,但过量使用会使脂质体的形成难度增大[15]。因此,本研究分别选择了哈西奈德∶磷脂、胆固醇∶磷脂、VE∶磷脂和乙醇用量进行了优化。
脂质体具有双亲性,通过包封可增加药物的溶解度,促进药物的经皮吸收,并在角质层形成药物贮库,缓释药物,避免药物大量进入血液,引起全身性反应。为此,本研究考察了哈西奈德脂质体的经皮吸收性能,结果显示哈西奈德脂质体组2、4、6、8、10、12 h累积透过量均显著高于溶液组,累积渗透率可达到对照组的2.75倍,具有良好的经皮吸收性能。

