新疆地区多中心阿比特龙和多西他赛治疗转移性去势抵抗性前列腺癌的临床疗效和安全性的对比分析
冉安鹏,张立东,王玉杰,史振峰,毕 兴,吴 群,杨军昌,李前跃,邓小虎,何万鹏,王文光,李 钊,阿布都克尤木,摆俊博,安恒庆,8
(1.新疆医科大学第一附属医院泌尿中心,新疆乌鲁木齐 830054;2.新疆维吾尔自治区人民医院泌尿中心,新疆乌鲁木齐 830001;3.新疆医科大学附属肿瘤医院泌尿外科,新疆乌鲁木齐 830011;4.新疆医科大学附属中医医院泌尿外科,新疆乌鲁木齐 830000;5.新疆军区总医院泌尿外科,新疆乌鲁木齐 830000;6.新疆生产建设兵团总医院泌尿外科,新疆乌鲁木齐 830002;7.克拉玛依市人民医院泌尿外科,新疆克拉玛依 834000;8.新疆医科大学公共卫生与预防医学博士后流动站,新疆乌鲁木齐 830054)
前列腺癌(prostate cancer,PCa)是欧美国家男性发病率最高的恶性肿瘤。在中国,其发病率也逐年升高。据统计,我国2015年新确诊PCa病例大约60 300例,死亡病例大约26 600例,并且绝大部分PCa患者在初次就诊时就已经发生转移[1]。雄激素剥夺治疗(androgen deprivation therapy,ADT)是转移性前列腺癌(metastatic prostate cancer,mPCa)的标准治疗方法[2]。虽然绝大多数患者初期ADT有效,但治疗18~24个月后,几乎所有患者都会逐渐演变为去势抵抗性前列腺癌(castration-resistant prostate cancer,CRPC)[3-4]。直到现在,转移性去势抵抗性前列腺癌(metastatic castration-resistant prostate cancer,mCRPC)的治疗选择仍非常有限,中位生存时间不到2年[5]。多西他赛化疗已经被证实能够使mCRPC患者得到生存获益,成为主要的治疗手段[6-7]。近几年,其他几种药物也被证实能够使mCRPC患者得到生存获益,例如阿比特龙、恩杂鲁胺、卡巴他赛、镭-223、sipuleucel-T[5,8-12]。目前只有多西他赛和阿比特龙在我国上市,本研究探讨阿比特龙和多西他赛治疗去势抵抗性前列腺癌患者的临床疗效和安全性的差异,现报道如下。
1 资料与方法
1.1 一般资料收集新疆地区新疆医科大学第一附属医院、新疆维吾尔自治区人民医院、新疆医科大学附属肿瘤医院、新疆医科大学附属中医医院、新疆军区总医院、新疆生产建设兵团总医院、克拉玛依市人民医院7家大型医院泌尿外科2016年6月至2018年1月收治的mCRPC患者94例,其中48名患者应用多西他赛(75 mg/m2,每3周1次,共10次)联合泼尼松(5 mg,b.i.d.)+ADT治疗,46名患者应用醋酸阿比特龙(1 000 mg,q.d.)联合泼尼松(5 mg,b.i.d)+ADT治疗。入选标准:①年龄≥18周岁的男性;②每个患者均通过前列腺穿刺活检术或前列腺电切术取活检,经病理学检查确诊为PCa;③CRPC患者:经药物或手术去势,血清睾酮<50 ng/dL;对于未行手术去势的患者,药物去势治疗持续进行;④病灶转移的依据为骨扫描检查发现骨转移病灶;或者磁共振成像(magnetic resonance imaging,MRI)/计算机断层扫描(computerized tomography,CT)检查证实转移性病灶存在(但除外肝脏或其他内脏转移);转移只有淋巴结转移时,转移病灶直径必须≥2 cm;⑤美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分≤2。排除标准:①既往接受过化疗等其他治疗方案的mCRPC患者;②有慢性肝脏疾病、病毒性肝炎史或肝功能异常者;③肾上腺皮质或垂体功能减退者;④既往药物去势治疗期间未规律治疗及规律随访者。
1.2 治疗方法阿比特龙组患者给予醋酸阿比特龙(ZYTIGA,西安杨森1 000 mg,q.d.)联合泼尼松(5 mg,b.i.d.)+ADT治疗,多西他赛组患者给予多西他赛(75 mg/m2,每3周1次,共10次)联合泼尼松(5 mg,b.i.d.)+ADT治疗,化疗预处理:多西他赛组患者在每次接受多西他赛治疗前日、当日、后一日,口服地塞米松(7.5 mg,b.i.d.)。
1.3 观察指标治疗期间,所有患者定期复查肝肾功能、血常规、血糖、血脂、电解质和前列腺特异性抗原(prostate specific antigen,PSA)等,阿比特龙组患者每月复查1次,多西他赛组患者每3周复查1次,多西他赛化疗后1周复查血常规。所有患者每3个月行发射型计算机断层扫描(emission computed tomography,ECT)全身骨显像、盆腔CT或MRI,合并其他内脏转移时增加相应部位的CT或B超,问询并登记期间的不良反应;通过定期复诊、打电话和借助PC-Follow临床数据库长期密切随访。将影像学进展、PSA进展作为主要研究终点并观察两组PSA反应率(影像学进展、PSA反应、PSA进展定义符合列腺癌临床试验工作组2(Prostate Cancer Clinical Trials Working Group 2,PCWG2)(PCWG2标准)。影像学进展:骨扫描发现2个或2个以上的新病灶或符合实体瘤反应评价标准的软组织病灶增大。PSA反应:治疗开始后PSA由基线值降低至少50%。PSA进展包括以下3种情况:①相比基线下降且达到缓解标准,相较于最低值升高≥50%,绝对值升高至少达到5 ng/mL(或恢复到基线水平),并在≥4周后经再次PSA值确认;②相比基线下降但未达到缓解标准,相较于最低值升高≥25%,绝对值升高至少达到5 ng/mL,并在≥4周后经再次PSA值确认;③相比基线未下降,相较于基线值升高≥25%,绝对值升高至少达到5 ng/mL,并在≥4周后经再次PSA值确认。
1.4 统计学分析采用SPSS 21.0统计软件进行数据处理和分析,定性资料的比较采用χ2检验,定量资料的比较采用t检验,非正态分布的资料的比较用非参数检验。无进展生存期(包括rPFS、PSA PFS)指标采用Kaplan-Meier法进行生存分析。P<0.05表示差异具有统计学意义。
2 结 果
2.1 患者的基本情况多西他赛组纳入患者48名,中位年龄71.0(62.00~75.75)岁;ECOG评分0分的患者共30名(62.50%),ECOG评分1分的患者共11名(22.92%),ECOG评分2分的患者共7名(14.58%);Gleason评分≤7共9名(18.75%),Gleason评分7共39名(81.25%);维吾尔族患者19名(39.58%);内脏转移2例,骨转移48例,淋巴结转移14例。阿比特龙组纳入患者46名,中位年龄72.5(67.75~78.25)岁;ECOG评分0分的患者共31名(67.39%),ECOG评分1分的患者共7名(15.22%),ECOG评分2分的患者共8名(17.39%);Gleason评分≤7共10名(21.74%),Gleason评分7共36名(78.26%);维吾尔族患者10名(21.74%);无内脏转移,骨转移46例,淋巴结转移7例。基本情况两组之间无统计学差异(表1)。
表1 患者的基本情况[例(%)]

PSA:前列腺特异性抗原;ECOG:美国东部肿瘤协作组。
2.2 观察终点指标阿比特龙组相较多西他赛组中位前列腺特异性抗原无进展生存期(prostate specific antigen progression-free survival,PSAPFS)延长(13月vs.9月,HR:0.59,95%CI:0.49~0.69;P<0.001),中位影像学无进展生存期(radiographic progression-free survival,rPFS)延长(15月vs.11月,HR:0.61,95%CI:0.51~0.71;P<0.001),(表2,图1)治疗后3个月PSA反应率显著提高(63.04%vs.41.67%,P=0.038,表2)。
表2 两组患者观察终点指标的比较

观察指标阿比特龙组(n=46)多西他赛组(n=48)统计量P值PSAPFS[中位数(95%CI)](月)13.0(10.1~15.9)9.0(7.7~10.3)-4.892<0.001中位rPFS[中位数(95%CI)](月)15.0(12.1~17.9)11.0(8.8~13.2)-4.663<0.001治疗后3个月PSA反应率[%(例)]63.04(29)41.67(20)4.3010.038
PSAPFS:前列腺特异性抗原无进展生存期;rPFS:中位影像学无进展生存期。
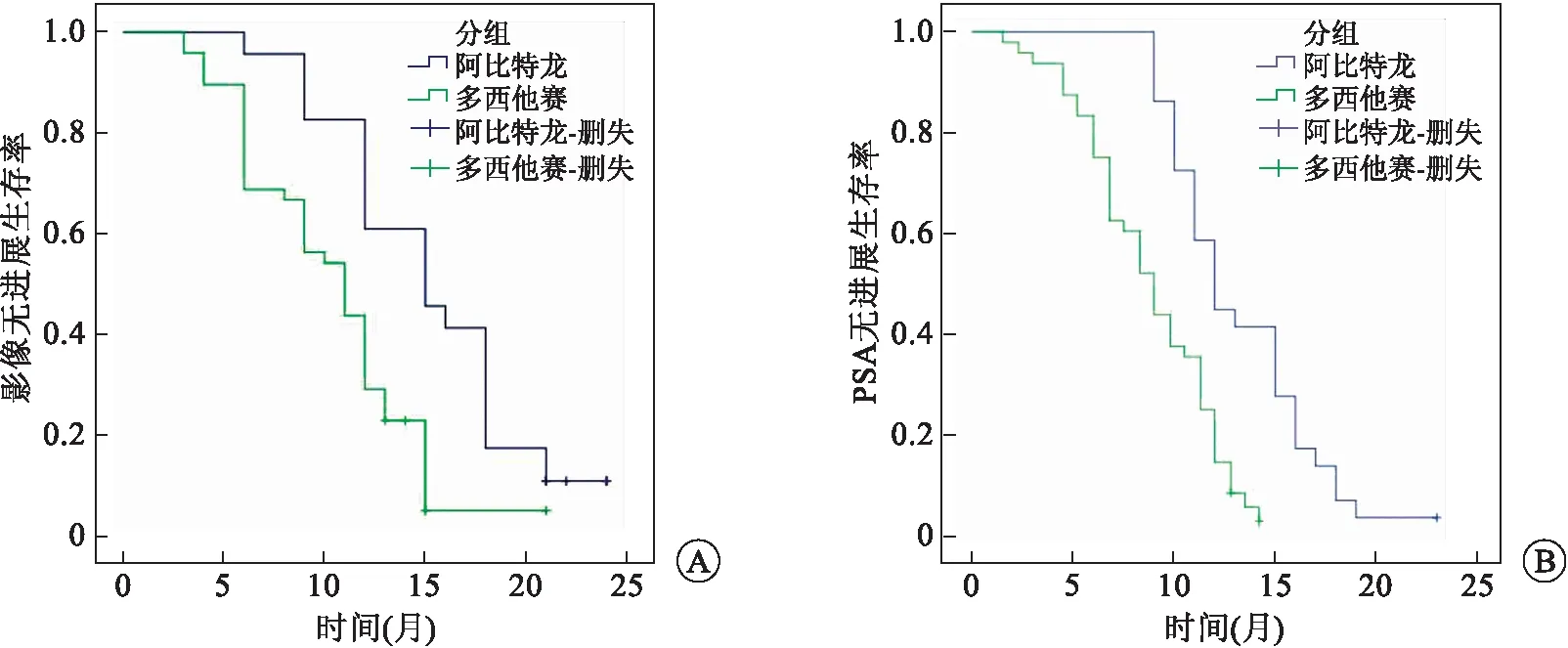
图1 阿比特龙组与多西他赛组的Kaplan-Meier生存分析曲线 A:影像无进展生存期;B:PSA无进展生存期。
2.3 不良反应两种治疗方案毒性模式差异很大,与药物的已知不良反应一致。发生至少1种3级或更严重不良反应的患者比例相似,阿比特龙组相比较多西他赛组为45.65%vs.47.92%,P=0.826。多西他赛组几乎所有患者均有不同程度的脱发,但3级以上所占比例较低。研究期间没有发生导致停药的严重不良反应,通过对症处理,不良反应均有所改善,可耐受治疗。两组3级及以上不良反应发生情况见表3。

表3 两组3级及以上不良反应[例(%)]
3 讨 论
PCa是欧美国家男性中最常见的恶性肿瘤。在我国,其发病率也逐年上升,绝大部分PCa患者在初诊时就已经发生转移,ADT是mPCa的标准治疗方案,但几乎所有患者在接受治疗18~24个月后都会进展为CRPC,其特点是ADT治疗无效。CRPC的发生机制极为复杂,主要包括雄激素受体(androgen receptor,AR)依赖性和AR非依赖性两类机制[13-14]。随着CRPC机制探索的不断深入,目前国内外已有许多研究表明多西他赛和阿比特龙能够使mCRPC患者获得生存获益,成为mCRPC的一线治疗方案。
多西他赛是一种有丝分裂抑制剂,主要在微管/微丝蛋白系统起作用,抑制微管解聚,促进微管蛋白聚合,最终诱导癌细胞凋亡[15]。根据国外TAX327随机对照、多中心、双盲的三期临床试验结果示[6],与米托蒽醌联合泼尼松治疗相比,多西他赛联合泼尼松3周方案治疗可显著延长mCRPC患者总体生存期(overall survival,OS)(18.9月vs.16.5月,HR:0.76,95%CI:0.62~0.94;P=0.009),同时能更好地改善患者的临床症状、有更高的PSA缓解率。不良事件多西他赛组较多,但仅有少数患者因不良反应导致治疗中断。多西他赛3周方案有效、安全、耐受性好。
PCa进展的主要原因是PCa细胞内的雄激素受体(androgen receptor,AR)被雄激素持续刺激。ADT治疗后,体内仍有少量雄激素持续刺激AR,导致CRPC继续进展,这部分雄激素来源于体内癌细胞自身合成。CYPl7A1限速酶调节体内雄激素的生物合成,PCa细胞中也存在此限速酶。理论上认为,通过抑制CYPl7A1酶就能降低体内雄激素水平,阻止CRPC的进展[16]。醋酸阿比特龙就是一种不可逆、高选择性、高亲和力的CYPl7酶抑制剂,能够阻断前列腺组织、睾丸、肾上腺组织中雄激素的合成。据国外COU-AA-302随机、对照、双盲、多中心三期临床试验显示[5],试验招募未化疗mCRPC患者1 088名,两组患者比例为1∶1,中位随访时间为27.1个月。治疗未经化疗mCRPC患者,与单纯泼尼松相比,阿比特龙联合泼尼松可显著延长患者OS(35.3月vs.30.1月,HR:0.79,95%CI:0.66~0.95;P=0.015 1)和rPFS(16.5月vs.8.2月,HR:0.52,95%CI:0.45~0.61;P<0.000 1)。同时,在身体状况恶化时间、前列腺特异性抗原无进展生存期、疼痛缓解等方面都有明显的改善。关于安全性方面,该研究发现应用阿比特龙联合泼尼松治疗的实验组3/4级不良反应的发生比率达48%,与对照组42%的发生比率相比,差异没有统计学意义。据国内一个回顾性研究报道结果显示,治疗未经化疗的mCRPC患者,与单纯泼尼松相比,阿比特龙联合泼尼松显著延长患者OS、PSAPFS与rPFS,并且具有良好的耐受性[16],为mCRPC患者提供了新的选择,值得推广。
最近,国外STAMPEDE临床研究对比阿比特龙与多西他赛治疗晚期或转移性前列腺癌疗效及安全性差异,共纳入患者566人,同时进行随机分组,多西他赛组189人,阿比特龙组377人,中位随访时间4年,中位PSA 56 ng/mL,中位年龄66岁,对于总体生存期HR=1.16(95%CI:0.82~1.65);对于前列腺癌特异性生存率HR=1.02(95%CI:0.70~1.49);关于不良反应,多西他赛组和阿比特龙组3级、4级、5级不良事件发生率分别为36%、13%、1%和40%、7%、1%。研究表明,对于这两种治疗方案,没有证据表明在总体生存期、前列腺癌特异性生存率及安全性方面存在差异[17]。
虽然目前国内外都在进行关于mCRPC的研究,但在当前药物之间如何选择及序贯问题上,仍然尚无定论。本研究对新疆地区应用阿比特龙联合泼尼松+ADT和多西他赛联合泼尼松+ADT治疗mCRPC患者,进行临床疗效和安全性对比。结果显示阿比特龙在rPFS、PSA PFS、PSA反应率方面均优于多西他赛;阿比特龙组相比较多西他赛组中位rPFS15月vs.11月,延长了4个月,中位PSA PFS 13月vs.9月,延长了4个月。治疗后3个月PSA反应率,阿比特龙组显著高于多西他赛组(63.04%vs.41.67%)。两种治疗方案的毒副反应构成有很大的差异,但发生3级及以上不良反应患者的比例相近。本研究中阿比特龙的主要毒副反应是高血糖、低血钾和肝功能损害;多西他赛主要的毒副反应是骨髓抑制、脱发和胃肠道反应,其中骨髓抑制中最为多见的是中性粒细胞减少症,几乎所有患者均出现不同程度的脱发,但较为严重的并不多。两组患者不良反应通过对症处理,均有所改善,可耐受治疗。
综上所述,这两种治疗方案均可显著改善mCRPC患者生存期,阿比特龙相较多西他赛可改善mCRPC患者rPFS、PSA PFS、PSA反应率,但没有证据显示在前列腺癌特异性生存率、总体生存期和安全性方面存在差异。两种治疗方案3级及以上不良反应发生率较高,但通过对症治疗,均可耐受。从目前的研究结果显示,阿比特龙优于多西他赛,且耐受性良好,是mCRPC的有效治疗选择,值得推广。由于随访时间的限制,此研究未将总体生存期作为主要研究终点,并且样本量较少,还需要大规模前瞻性研究进一步探讨。