清蒸和酒蒸九华黄精不同粒径粉的体外溶出度考察
吴其国,胡叶青,李文艳
(1.安庆医药高等专科学校药学系,安徽安庆246052;2.华润三九医药股份有限公司,广东深圳518110)
黄精为百合科植物滇黄精(Polygonatum kingianum Coll.et Hemsl.)、黄精 (Polygonatum sibiricum Red.)或多花黄精(Polygonatum cyrtonema Hua)的干燥根茎[1]。安徽九华山地区的黄精品种为多花黄精,在九华山地区生长范围较广,阴湿山坡和沟谷处较常见,云南、贵州、浙江、山东也有此品种分布,但药材质量都不如九华山地区,为突出其地方特色,取名为九华黄精[2]。
随着中药材资源越来越匮乏,通过中药粉碎技术,选择合适的粉碎粒径,使中药有效成分充分溶出变得尤为重要。目前黄精的炮制方法常用的有清蒸和酒蒸两种。
本文拟对九华黄精清蒸和酒蒸两种炮制品的不同粒径粉体进行初步的体外溶出特性考察,以期为清蒸和酒蒸九华黄精的有效利用提供支撑。
1 仪器与试药
1.1 仪器
仪器包括:1)HC-500YZ多功能粉碎机(永康市天祺盛世工贸有限公司);2)ZRS-8GD智能溶出试验仪(天津市天大天发科技有限公司);3)ZNHW-500型电加热套(上海越众仪器有限公司);4)SP-1920型紫外-可见分光光度仪(上海光谱仪器有限公司);5)FA1204B型电子分析天平(上海越平科学仪器有限公司)。
1.2 试药
试药包括:1)九华黄精生药材购于池州市大王洞中药材种植专业合作社;2)蒽酮(分析纯,国药集团化学试剂有限公司,批号20170222);3)无水乙醇(分析纯,上海中泰化学试剂,批号20161108);4)葡萄糖(分析纯,天津市大茂化学试剂厂,批号20160909);5)硫酸(分析纯,国药集团化学试剂有限公司,批号20170508);6)黄酒(浙江塔牌绍兴酒有限公司)。
2 方法与结果
2.1 清蒸和酒蒸九华黄精的制备
取九华黄精生药材,除去杂质,洗净,蒸至透心,切厚片,干燥,即得清蒸九华黄精;取净九华黄精,加黄酒(每100 kg九华黄精,用黄酒20 kg)拌匀、润透,再于锅内蒸透,取出,稍晾,拌回蒸液,再凉至六成干,切厚片,干燥,即得酒蒸九华黄精。
2.2 清蒸和酒蒸九华黄精不同粒径粉的制备
分别取一定量的干燥清蒸和酒蒸九华黄精炮制品,置于高速万能粉碎机中,粉碎3~5 min,分级过筛,分别得到清蒸九华黄精不同粒径粉:100目粉(过100目筛),200目粉(过200目筛),300目粉(过300目筛);酒蒸九华黄精不同粒径粉:100目粉(过100目筛),200目粉(过200目筛),300目粉(过300目筛)。
2.3 清蒸和酒蒸九华黄精总多糖含量测定
2.3.1 对照品溶液的制备
精密称取干燥至恒重的无水葡萄糖对照品12 mg,加入蒸馏水制成每毫升含0.136 1 mg的葡萄糖溶液,作为对照品溶液。
2.3.2 供试品溶液的制备
取清蒸和酒蒸九华黄精粉末(过2号筛)各1 g,精密称定,加入纯化水100 mL,称定重量,加热回流1 h(保持微沸),放冷,用水补足减失的重量,滤过,精密量取续滤液5 mL,加入无水乙醇30 mL,静置1 h,5 000 r/min离心15 min,沉淀加热水溶解,定容至25 mL,作为供试品溶液,备用。
2.3.3 标准曲线的绘制
精密吸取无水葡萄糖对照品溶液0.4、0.6、0.8、1.0、1.2 mL,分别置于10 mL具塞试管中,各管加水稀释至2 ml,精密加入硫酸-蒽酮溶液(精密称取0.2 g蒽酮,加80%浓硫酸溶解摇匀,即得。现配现用)5 mL,静置10 min,再于沸水浴反应10 min,取出,置冰水浴中冷却至室温,以水2 mL为空白,照2015年版《中国药典》(四部)通则0401紫外-可见分光光度法[3],在582 nm处测定吸光度A,以吸光度为纵坐标,葡萄糖质量为横坐标,得线性回归方程为

2.3.4 精密度试验
精密吸取无水葡萄糖对照品溶液0.5 ml,共6份,分别置于10 mL具塞试管中,按2.3.3项下自“各管加水稀释至2 mL”起开始操作,在582 nm处测定吸光度A,计算RSD=1.7%(n=6),结果表明仪器精密度良好。
2.3.5 重复性试验
称取清蒸九华黄精药材粗粉6份(每份约1 g),精密称定,按2.3.2项下制备供试品溶液,精密吸取供试品溶液2 mL分别置于10 mL具塞试管中,自“精密加入硫酸-蒽酮溶液”起开始操作,在582 nm处测定吸光度A,计算RSD=2.5%(n=6),结果表明该方法重复性良好。
2.3.6 稳定性试验
精密量取清蒸九华黄精供试品溶液2.0 mL,置于10 mL具塞试管中,按2.3.3项下自“精密加入硫酸-蒽酮溶液”起开始操作,室温放置,分别在 0、30、60、90,120、150 min 测定其 582 nm 处吸光度 A,计算RSD=1.4%(n=6),结果表明供试品溶液在2.5 h内稳定性良好。
2.3.7 加样回收率试验
精密称定已知总多糖含量的清蒸九华黄精药材粗粉1 g,共6份,分别精密加入无水葡萄糖对照品50 mg,按2.3.2项下方法制备供试品溶液,精密吸取供试品溶液2 mL,置10 mL具塞试管中,按2.3.3项下“精密加入硫酸-蒽酮溶液”起开始操作,平均加样回收率为98.62%,计算RSD=2.8%(n=6),结果表明回收率良好。
2.4 清蒸和酒蒸九华黄精粉的体外溶出度测定
2.4.1 溶出度样品的制备
分别取不同粒径的清蒸和酒蒸九华黄精粉约2 g,精密称定,投入溶出仪中,按2015年版《中国药典》(四部)通则0931溶出度和释放度测定法(桨法)[3]进行测定,以已超声脱气的500 mL水为溶出介质,转速 100 r/min,温度(37.0 ± 0.5)℃,分别于 5、10、15、30、45、60 min 取样 10 mL,同时向溶出杯中补充相同温度和体积的介质,取出的样品溶液于5 000 r/min离心10 min,精密量取离心后的上清液5 mL,加入无水乙醇30 mL,摇匀,静置沉淀1 h,10 000 r/min离心8 min,倾去上清液,沉淀用少量热水溶解,放冷,定容至10 mL,摇匀,作为样品溶液,备用。
2.4.2 溶出度的测定
精密量取上述样品溶液2 mL,置于10 mL具塞试管中,再按照2.3.3项条件项下自“精密加入硫酸-蒽酮溶液”起开始操作,在582 nm处测定吸光度A,每种粉末样品平行测定3份,测得不同时间清蒸九华黄精100目粉、200目粉、300目粉和酒蒸九华黄精100目粉、200目粉、300目粉中总多糖溶出量,取平均值,计算累积溶出率。结果如图1与2所示。
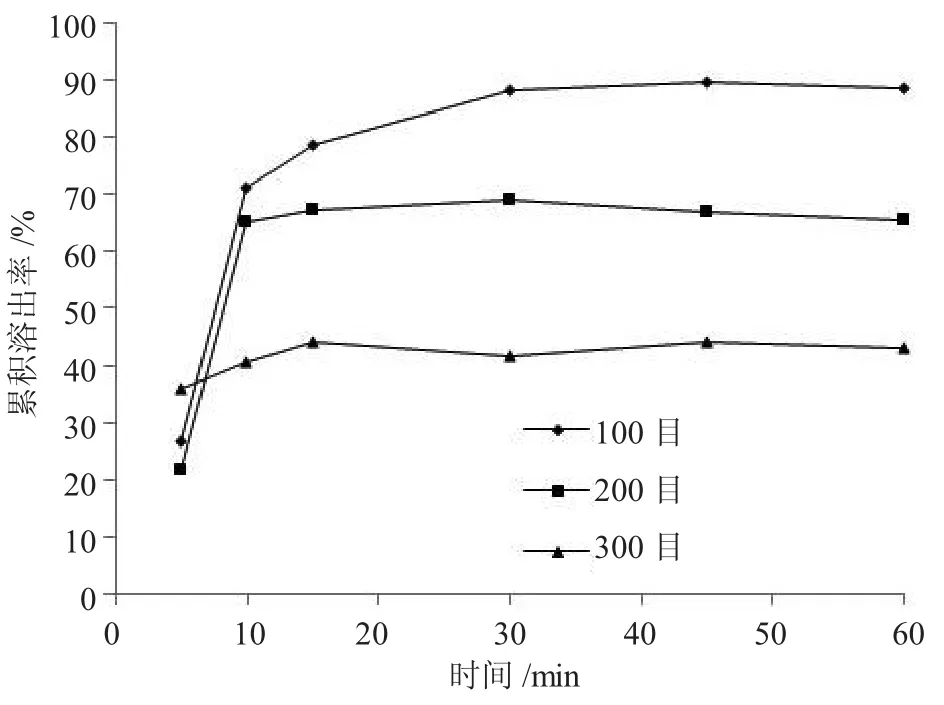
图1 清蒸九华黄精不同粒径粉的水介质体外溶出曲线

图2 酒蒸九华黄精不同粒径粉的水介质体外溶出曲线
3 讨论与总结
由图1可知,其不同粒径粉的累积溶出率由大到小的顺序分别为100目粉、200目粉、300目粉。由图2可知,其不同粒径粉的累积溶出率由大到小的顺序分别为200目粉、300目粉、100目粉。同一种九华黄精粉的不同粒径粉累积溶出率有较大差别,并不是粒径最小的300目粉累积溶出率最高,很早就有研究认为药材有效成分的溶出并不是随着粒径减小而无限增加[4],而是存在一个临界粒径,不仅每味药材的临界粒径不同,而且每种成分的临界粒径也存在差异[5]。
另外,黄精的炮制方法主要是清蒸和酒蒸两种,本研究分别制备了清蒸九华黄精和酒蒸九华黄精,从其外观形态来看,两种炮制品的表面和外观颜色、断面形态和气味均有显著差别,这些物理特性的差别也有可能会影响九华黄精在水中的溶出特性。清蒸和酒蒸九华黄精的最大累积溶出率分别是100目粉和200目粉,炮制方法不同,会影响中药材产品的质量,清蒸和酒蒸两种炮制方法对黄精多糖的含量影响是不一样的[6],炮制的各种因素会影响其含量变化,甚至会影响其溶出特性值得进一步研究。
总之,中药材的粉碎并不是越细越好,而应控制在一定的范围内,尤其是微粉操作,这可能是因为一方面超微粉体比表面积大、表面能增加,使颗粒处于非稳定状态,因而有强烈的相互吸引而达到稳定的趋向,这种倾向使粒子产生团聚而影响其溶出效果[7];另一方面粉末在溶出过程中存在溶出与吸附平衡,微粉溶出虽然稍多,但药材超微粉碎粒度过小,药材表面积急剧增大而使其表面能增加,药物粉体对多糖这类极性成分的吸附力增大,从而使其不易溶出[8-9]。而且高粉碎需要的能耗高、成本高,所以在医药工业生产中,偏高粉碎度的要求尤其要慎重选择[10]。

