丹参酮ⅡA-磺酸钠与牛血清蛋白的相互作用
陈凤英,杨林,黎祥妨
(商洛学院化学工程与现代材料学院/陕西省尾矿资源综合利用重点实验室,陕西商洛726000)
血清蛋白与药物小分子之间的相互作用,是生物化学领域的重要研究内容之一。血清白蛋白是生物体血浆中含量最丰富的运输蛋白质,能够与类别广泛的内源和外源性物质结合,将药物分子输送到人体各个部位。小分子药物被生物体吸收后,与血浆蛋白可逆性结合后进入血液循环系统,并且小分子药物与血浆蛋白的可逆性结合能够影响其在生物体内的分布、生物活性和毒性。因此,从光谱学角度研究小分子与蛋白质相互作用的过程和机理,对于深入研究小分子药物在生物体内的运输、分布以及在人体的代谢过程具有十分重要的意义[1-3]。丹参酮ⅡA是中药丹参中的活性成分之一,难溶于水,口服吸收效果较差。丹参酮ⅡA-磺酸钠是由丹参酮ⅡA经过磺化而成的盐[4],具有缩小心肌梗死面积、改善胃黏膜血液供应、抑制中枢神经系统降低血液粘度、抑制血小板集聚及抗血栓形成等作用,临床上主要用于心绞痛、冠心病、急性脑出血等病症的治疗[5]。目前,对丹参酮ⅡA-磺酸钠的研究主要集中在药效、药理以及含量测定等方面[6-8],与蛋白质的作用机理方面的研究未见报道。本文在模拟生理条件下,采用紫外光谱和荧光光谱两种方法研究了丹参酮ⅡA-磺酸钠与牛血清蛋白的相互作用机理,计算了不同温度下二者的结合常数以及反应过程的ΔG、ΔH、ΔS等热力学参数,推测了二者之间结合力的类型。
1 材料与方法
1.1 主要试剂与仪器
丹参酮ⅡA-磺酸钠和牛血清蛋白为生化试剂,三(羟甲基)胺基甲烷、浓盐酸和氯化钠均为分析纯,使用前未做任何处理。
pH精密酸度计(上海大普仪器有限公司),荧光光谱仪(日本日立高新技术公司),紫外可见光谱仪(上海恒勤仪器有限公司),超声波振荡仪(重庆市超声仪器有限公司)。
1.2 试验方法
1.2.1 紫外光谱法
在编号为1~10的10 mL的容量瓶中加入2×10-5mol·L-1的牛血清蛋白溶液1.0 mL,然后再依次加入体积分别为0、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9 mL的丹参酮ⅡA-磺酸钠溶液,用pH=7.40的0.1 mol·L-1的Tris-HCl缓冲溶液定容至10 mL,摇匀,分别在285.8、298、310 K温度下充分反应30 min。以Tris-HCl溶液为参比溶液,测量各溶液的紫外可见吸收光谱。
1.2.2 荧光光谱法
测试溶液的配制方法同1.2.1,固定荧光激发波长为280 nm,波长300~500 nm扫描的荧光光谱。
2 结果与讨论
2.1 紫外光谱法
285.8 、298、310 K时丹参酮ⅡA-磺酸钠与牛血清蛋白作用的紫外可见光谱见图1。由图1可以看出,丹参酮ⅡA-磺酸钠与牛血清蛋白的吸收峰峰形基本不变,随着丹参酮ⅡA-磺酸钠浓度的增加同一波长处的吸光度在不断增大。

图1 丹参酮ⅡA-磺酸钠与牛血清蛋白的紫外吸收光谱
由图2可得,在285.8 K时,丹参酮ⅡA-磺酸钠与牛血清蛋白作用的线性方程为y=5.9093×10-6x-1.677,R=0.9924;在298 K时,丹参酮ⅡA-磺酸钠与牛血清蛋白作用的线性方程为y=4.5709×10-6x-0.7981,R=0.9971;在310 K时,丹参酮ⅡA-磺酸钠与牛血清蛋白作用的线性方程为y=3.6550×10-6x+0.6271,R=0.9942,通过计算,在285.8、298、310 K时的结合常数分别为2.18×105、1.75×105、1.35×105L·mol-1,表明牛血清蛋白与丹参酮ⅡA-磺酸钠的结合常数随着温度的升高而降低。

图2 丹参酮ⅡA-磺酸钠与BSA结合的Lineweaver-Burk双倒数
2.2 荧光光谱法
2.2.1 丹参酮ⅡA-磺酸钠对牛血清蛋白的荧光猝灭
牛血清蛋白的内源荧光来自分子中的色氨酸、酪氨酸和苯丙氨酸等残基,荧光体在某些物质的作用下会发生荧光猝灭,许多药物或有机小分子化合物都是荧光猝灭剂。在285.8、298、310 K时牛血清蛋白与丹参酮ⅡA-磺酸钠的荧光光谱的变化情况见图3,随着丹参酮ⅡA-磺酸钠浓度的增加,牛血清蛋白的内源荧光强度降低,但它的峰位及峰形基本不变,表明丹参酮ⅡA-磺酸钠对牛血清蛋白的荧光有猝灭作用。
2.2.2 荧光猝灭的类型
荧光分子与其它分子相互作用引起荧光强度降低的现象称为荧光猝灭,可分为:动态猝灭和静态猝灭。静态猝灭是由于猝灭剂与荧光物质相互作用而生成了一定构型化合物,导致荧光物质荧光强度减弱的现象,静态猝灭过程符合Lineweaver-Bruk双倒数方程[9]:
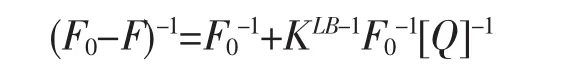
式中:KLB为猝灭剂与小分子药物的结合常数,F0为无丹参酮ⅡA-磺酸钠时的荧光强度,F为加入一定浓度的丹参酮ⅡA-磺酸钠后的荧光强度,[Q]为小分子药物的浓度。在298 K和310 K时丹参酮ⅡA-磺酸钠与牛血清蛋白相互作用的Lineweaver-Bruk双倒数曲线如图4所示。根据图4可以得到,在285.8、298、310 K时,丹参酮ⅡA-磺酸钠与牛血清蛋白的结合常数分别为1.71×105、1.69×105、1.22×105L·mol-1,结合常数随温度的升高而减小,说明丹参酮ⅡA-磺酸钠对牛血清蛋白的荧光猝灭属于静态猝灭。

图3 丹参酮ⅡA-磺酸钠对牛血清蛋白的荧光猝灭光谱
2.2.3 丹参酮ⅡA-磺酸钠与牛血清蛋白结合作用力
药物小分子与白蛋白大分子之间的作用力主要表现为:氢键、静电引力、范德华力和疏水作用力等。研究表明,若反应的焓变△H>0,熵变△S>0时,分子之间的相互作用力为疏水作用力;若反应的焓变△H<0,熵变△S>0时,分子之间的作用力为静电引力;若△H<0,△S<0,分子之间的相互作用力为氢键和范德华力[10]。丹参酮ⅡA-磺酸钠与牛血清蛋白结合过程的热力学参数见表1。由表1可见,丹参酮ⅡA-磺酸钠与牛血清蛋白相互作用的△H<0,△S>0,因此,丹参酮ⅡA-磺酸钠与牛血清蛋白之间的作用力主要为静电引力。
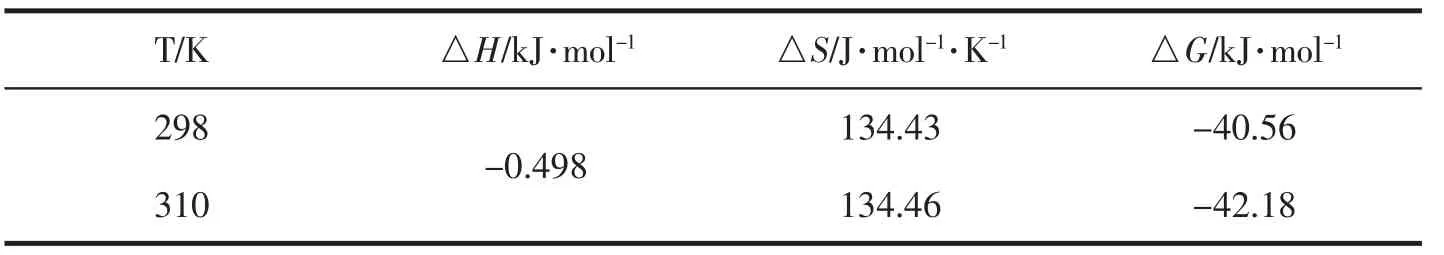
表1 丹参酮ⅡA-磺酸钠与牛血清蛋白相互作用的热力学参数

图4 丹参酮ⅡA-磺酸钠对BSA荧光猝灭的Lineweaver-Bruk
2.2.4 丹参酮ⅡA-磺酸钠与牛血清蛋白的结合位点数
静态猝灭过程的药物小分子和血清蛋白的结合位点数,可根据lg[(F0-F)/F]=lg K+n lg[Q]求算。其中,F0为未加入药物小分子时牛血清蛋白的荧光强度;F为加入猝灭剂药物小分子浓度为[Q]时的荧光强度。
图5是298 K和310 K时lg[(F0-F)/F]~l g[Q]曲线,通过线性拟合得到丹参酮ⅡA-磺酸钠与牛血清蛋白的结合位点数n分别为0.93、0.94和0.98,说明丹参酮ⅡA-磺酸钠与牛血清蛋白只有1个结合位点数。
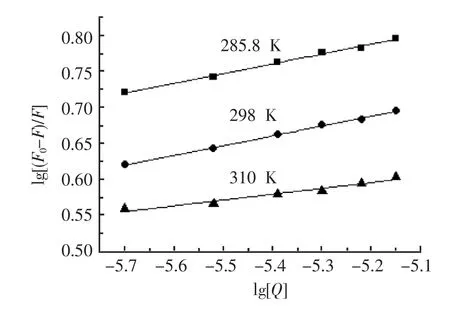
图5 丹参酮ⅡA-磺酸钠与牛血清蛋白的结合常数
3 结论
采用紫外光谱和荧光光谱两种方法研究了丹参酮ⅡA-磺酸钠与牛血清蛋白的相互作用,当反应温度为285.8、298、310 K时,紫外光谱法研究得到二者的结合常数分别为2.18×105、1.75×105、1.35×105L·mol-1,结合常数随温度的升高而降低。在反应温度为285.8、298、310 K时,荧光光谱法研究得到二者的结合常数分别为1.71×105、1.69×105、1.22×105L·mol-1,与紫外光谱法得到结果一致。丹参酮ⅡA-磺酸钠对牛血清蛋白的荧光猝灭方式属于静态猝灭,二者的结合位点数为1,主要通过静电引力作用结合。

