分光光度法同时测定油脂中氢过氧化物和醛含量
向思敏,朱振中,王巍巍
(江南大学 化学与材料工程学院,江苏 无锡 214122)
油脂在光、热、金属催化剂、微生物和水的影响下会发生氧化或水解,形成脂质氢过氧化物(初级氧化产物)。脂质氢过氧化物在高温或者金属存在时易分解形成醛、酮、酸、酯、醇和短链烃等次级氧化产物[1]。目前检测油脂初级氧化产物的方法有比色法[2]、化学发光法[3]、FTIR法[4-5]和电化学方法[6-7]等。其中比色法常用的有亚铁二甲酚橙法[2]、五磺基水杨酸法[8]和硫氰化铁法[9],此类方法均是利用氢过氧化物的氧化性;化学发光法主要是基于碱性鲁米诺与氢过氧化物的化学发光反应;FTIR 则是利用特征性光谱进行定性或定量分析;电化学方法中用得较多的是测电导率和阻抗。检测次级氧化产物的方法有液相色谱质谱联用法[10]和气相色谱质谱联用法[11],常用的衍生化试剂有2,4-二硝基苯肼和2-硫代巴比妥酸,均是利用羰基化合物与胺类的亲核加成反应。
目前国内外有关评价油脂氧化稳定性的方法主要是基于测定油脂的初级氧化产物(如氢过氧化物)或者次级氧化产物(如羰基类化合物),仅评价一种氧化产物使评价的可靠性或准确性难以保证。而分别测定油脂的初级氧化产物或次级氧化产物,将使分析评价过程较为烦琐费时和不经济。若能同时测定油脂的初级氧化产物和次级氧化产物,将使油脂氧化稳定性的评价结果更为可靠和准确。但有关同时测定油脂的初级氧化产物和次级氧化产物的研究鲜见报道。本文以N,N-二甲基对苯二胺为显色剂,利用胺的还原性和亲核性分别与氢过氧化物和羰基反应,以达到同时测定油脂氧化过程中氢过氧化物和醛的目的。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
鳄梨油由上海家化联合股份有限公司提供,大豆油购于超市。N,N-二甲基对苯二胺盐酸盐、乙酸、氯化铝、盐酸、无水乙醇、过氧化氢(30%)、三氯甲烷、甲醇、还原铁粉、无水氯化亚铁、硫氰酸钾、1,1,3,3-四乙氧基丙烷、硫代巴比妥酸、三氯乙酸和乙二胺四乙酸二钠,均为分析纯(国药集团化学试剂有限公司);实验用水均为超纯水。
1.1.2 仪器与设备
超声波清洗仪,数显式电热恒温水浴锅,双光束紫外可见分光光度计,721分光光度计,DHG-9033B5-Ⅲ鼓风干燥箱。
1.2 实验方法
1.2.1 溶液的配制
配制7.6 mmol/L N,N-二甲基对苯二胺乙醇溶液,8 mmol/L过氧化氢乙醇溶液,3.8 mmol/L丙二醛(MDA)溶液。
配制过氧化氢和丙二醛混合溶液:含0.67 mmol/L的过氧化氢和0.76 mmol/L的丙二醛。
1.2.2 过氧化氢和丙二醛标准曲线的绘制
取不同体积的过氧化氢乙醇溶液于5 mL比色管中,加入1 mL 2.74 mmol/L的乙酸溶液和2 mL 7.6 mmol/L N,N-二甲基对苯二胺乙醇溶液,用乙醇定容至5 mL,配制成0.08、0.12、0.20、0.40、0.67、1.00、1.33、2.00 mmol/L的过氧化氢标准溶液,40℃加热40 min后,以未加过氧化氢的溶液为参比,在340~410 nm处测定吸光度,在最大吸收波长处绘制过氧化氢溶液的标准曲线。
同样的方法配制0.15、0.23、0.38、0.76、1.26、1.89、2.53 mmol/L的丙二醛标准溶液,40℃加热40 min,以未加丙二醛的溶液为参比,在340~410 nm处测定吸光度,在最大吸收波长处绘制丙二醛溶液的标准曲线。
1.2.3 油脂中的氢过氧化物和醛含量的测定
取适量油脂于120℃烘箱中加热不同时间后取0.05 mL置于5 mL比色管中,用乙醇溶解,加入1 mL 2.74 mmol/L乙酸,2 mL 7.6 mmol/L N,N-二甲基对苯二胺乙醇溶液,用乙醇定容至5 mL,40℃加热40 min,分别在350 nm和408 nm处测定吸光度,根据标准曲线求油脂中氢过氧化物和醛的含量。
同时参考GB/T 5009.37—2003中的植物油过氧化值的测定方法和GB/T 5009.181—2003中丙二醛的测定方法,测定油脂中的氢过氧化物和丙二醛的含量。
1.2.4 双变量校准方法(Kaiser法)[12]
分光光度法测定选定波长(λi)下分析物A的线性校正回归函数为:
AAi=mAi·CA+eAi
(1)
式中:AAi为波长λi处的吸光度;mAi为线性回归的斜率;CA为分析物A的浓度;eAi为截距。
如果二元混合物(A,B)的测定是在两个选定波长(λ1和λ2)下进行的,则:
AAB1=mA1·CA+mB1·CB+eAB1
(2)
AAB2=mA2·CA+mB2·CB+eAB2
(3)
式中:AAB1为混合物A、B在波长λ1处的吸光度之和;AAB2为混合物A、B在波长λ2处的吸光度之和;eAB1和eAB2分别为λ1和λ2处线性校准的截距之和(eABi=eAi+eBi)。
联立式(2)和式(3),求得CA和CB的值:
CA=(AAB1-eAB1-mB1CB)/mA1
(4)
CB=[mA2(AAB1-eAB1)+mA1(eAB2-AAB2)]/(mA2mB1-mA1mB2)
(5)
为获得测定混合物(A,B)的最佳波长,用 Kaiser 法在两个选定波长下测定混合物的吸光度来解析二元混合物,并使用线性回归函数的参数在相同波长处评估每个组分,对每个二元混合物和每对预选波长创建一系列灵敏度矩阵K:
(6)
式中:mA1、mA2为组分A在选定波长(λ1,λ2)处的灵敏度参数的斜率;mB1、mB2为组分B在选定波长(λ1,λ2)处的灵敏度参数的斜率。计算此系列矩阵的分辨率,选择具有最高绝对矩阵行列式值的波长集为测定混合物(A,B)的最佳波长。
2 结果与讨论
2.1 紫外吸收光谱
分别将0.67 mmol/L的过氧化氢(H2O2)、0.76 mmol/L的丙二醛(MDA)及二者的混合物,以1 mL 2.74 mmol/L乙酸作催化剂,在40℃下与显色剂反应40 min,得到的紫外吸收光谱图如图1所示。
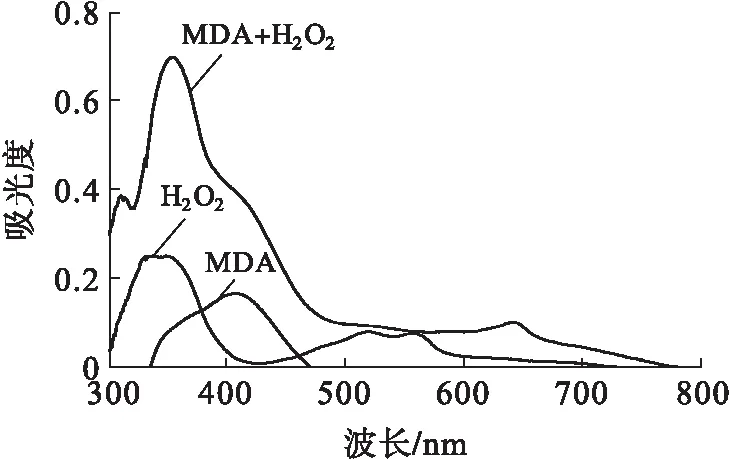
图1 MDA、H2O2、MDA+H2O2的紫外吸收光谱图
由图1可以看出,过氧化氢在348 nm处有较强的吸收,丙二醛在400 nm处有较强的吸收。但混合溶液在348 nm和400 nm处均存在光谱重叠,导致吸收峰不易观察,难以同时测定混合物中的分析物。为此,采用Kaiser方法选择混合物在这一段波长范围内测定最佳波长。
2.2 最佳波长的选择
按1.2.2分别绘制过氧化氢(348 nm)和丙二醛(400 nm)的吸光度(Y)随浓度(X)变化曲线。过氧化氢在0.08~2.00 mmol/L范围内与吸光度呈良好的线性关系,其线性方程为:Y=0.379 2X-0.000 7,R2=0.999 1,检出限为0.006 mmol/L。丙二醛在0.15~2.53 mmol/L范围内与吸光度有较好的线性关系,其线性方程为:Y=0.15X+0.028,R2=0.999 1,检出限为0.03 mmol/L。
用Kaiser方法在340~410 nm范围内选定11个波长,分别由式(1)和式(6)求过氧化氢和丙二醛的斜率及灵敏度矩阵行列式的绝对值,结果见表1和表2。
由表2可知,350 nm和408 nm处的灵敏度矩阵行列式的绝对值最大,故选择350 nm和408 nm作为同时测定混合溶液中过氧化物和丙二醛含量的最佳测定波长。
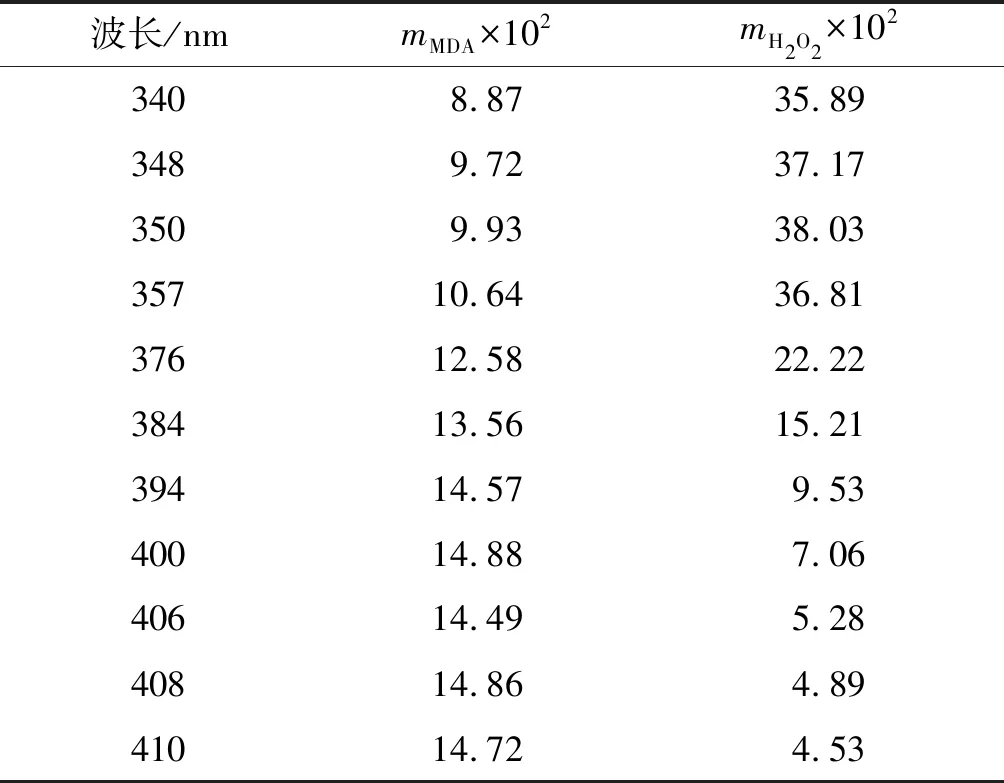
表1 H2O2和MDA的线性回归校准的斜率

表2 灵敏度矩阵行列式的绝对值(K×10-4)
2.3 反应条件的优化
2.3.1 催化剂的选择
取1 mL过氧化氢和丙二醛混合溶液,加入2 mL 7.6 mmol/L显色剂、1 mL 2.74 mmol/L不同种类的酸,用乙醇定容至5 mL,40℃反应40 min,以未加催化剂的溶液为参比,测定330~420 nm范围的吸收峰面积,结果如图2所示。
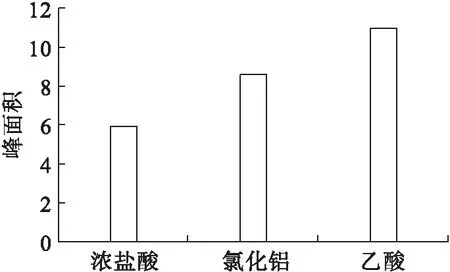
图2 不同种类的酸催化剂对反应的影响
由图2可知,浓盐酸能使显色的颜色迅速褪去,吸光度无明显增大,乙酸和氯化铝对吸光度的增加较为明显。其中,乙酸的效果最好,故选择乙酸作为催化剂。
2.3.2 显色剂最佳浓度的选择
取1 mL过氧化氢和丙二醛混合溶液,加入1 mL 2.74 mmol/L的乙酸、2 mL不同浓度的显色剂溶液,用乙醇定容至5 mL,以未加显色剂的溶液为参比,对混合溶液在40℃下加热40 min,在350 nm和408 nm处测定吸光度,结果见图3。
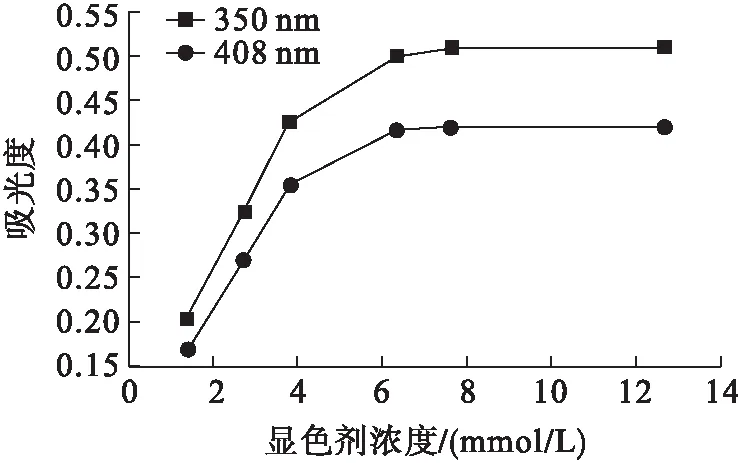
图3 吸光度随显色剂浓度的变化
从图3可以看出,350 nm和408 nm处的吸光度均随显色剂浓度的增加而增大。当显色剂浓度高于7.6 mmol/L后,吸光度的增加趋缓。故选择显色剂的浓度为7.6 mmol/L。
2.3.3 反应温度和反应时间的影响
取1 mL过氧化氢和丙二醛混合溶液,加入1 mL 2.74 mmol/L的乙酸、2 mL 7.6 mmol/L的显色剂溶液,用乙醇定容至5 mL,分别在30、40、50℃下加热不同时间,以不含混合液的溶液作参比,在350 nm处测定吸光度,结果见图4。
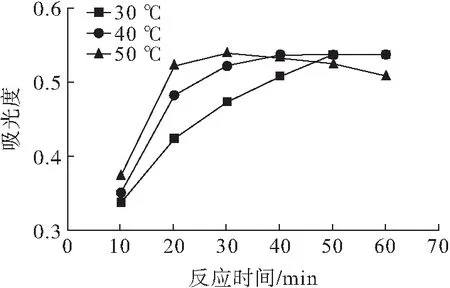
图4 反应温度和反应时间对吸光度的影响
由图4可知,随反应温度的升高,吸光度达最大值所需的时间越短,30℃为50 min,40℃为40 min,50℃为30 min。但反应温度越高,吸光度达到最高后经一段时间后会缓慢降低。故选择40℃反应40 min作为本方法的反应温度和反应时间。
2.4 油脂中氢过氧化物和丙二醛的同时测定
以350 nm和408 nm为混合溶液的测定波长,结合式(1)分别得出混合溶液中过氧化氢和丙二醛在不同波长处的线性回归方程,结果见表3。
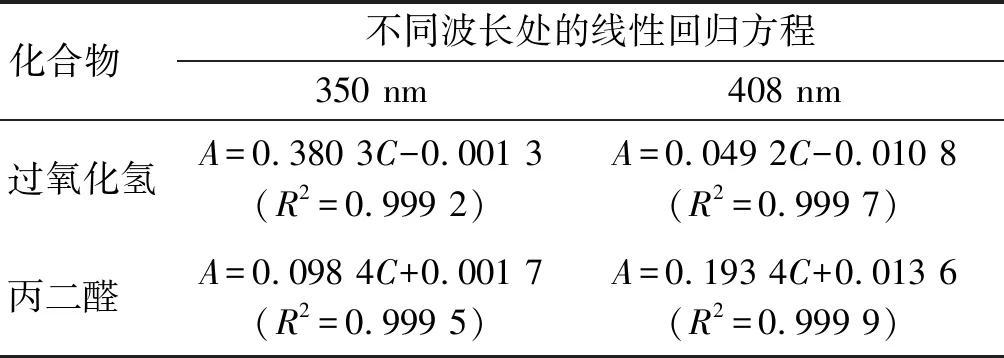
表3 混合溶液中过氧化氢和丙二醛的
根据表3中回归方程的相关参数及在350 nm和408 nm处分别测定的混合液的吸光度,由式(4)和式(5)即可求出氢过氧化物和醛的浓度。
按1.2.3分别测定大豆油和鳄梨油在120℃加热不同时间的氢过氧化物和丙二醛的含量,同时按国标法测定二者的含量,结果见表4。在置信度为95%下,计算F值和t值,比较两种方法的显著性,结果见表5。
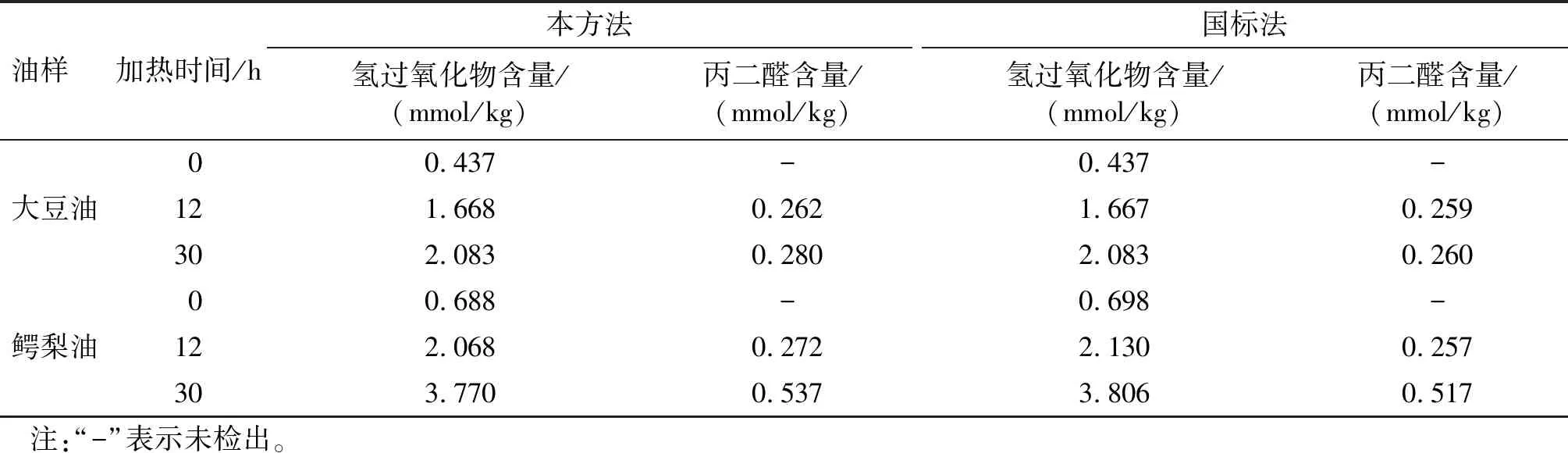
表4 大豆油和鳄梨油的氢过氧化物含量和丙二醛含量
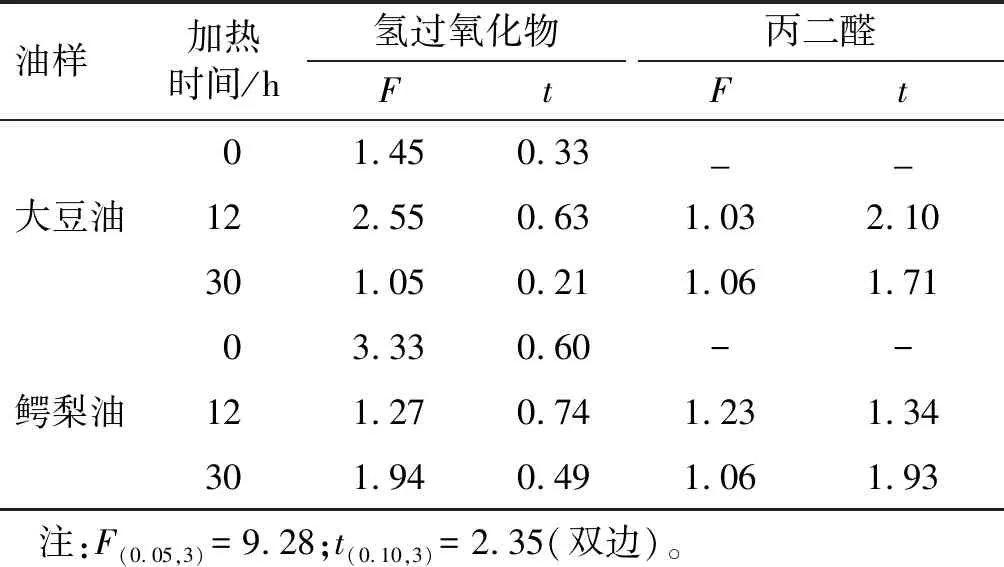
表5 方法的显著性检验
由表4可知,大豆油和鳄梨油的氢过氧化物含量和丙二醛含量均随加热时间的延长而增大,且鳄梨油的氢过氧化物含量和丙二醛含量的变化较大豆油的大,说明鳄梨油较大豆油更易氧化。从表4还可得出,丙二醛含量的增速较氢过氧化物缓,且丙二醛含量远小于氢过氧化物含量,可能是由于丙二醛是次级氧化产物再降解而形成的低相对分子质量的产物。此外,国标法所测的氢过氧化含量值与本方法的测定结果相近,而国标法所测的丙二醛含量均比本方法的测定值略小,可能是由于油脂氧化过程中除丙二醛外其他的单链醛也有吸收而引起。
由表5可知,在置信度为95%时,大豆油、鳄梨油的F值和t值均小于F(0.05,3)和t(0.10,3),说明两种测定方法之间不存在显著性差异。
3 结 论
本文建立了一种分光光度法同时测定油脂中氢过氧化物和醛含量方法,所测结果与国标法对比均无显著性差异。由于该方法能同时测定油脂的初级氧化产物和次级氧化产物,可为评价油脂氧化稳定性提供更为可靠和准确的参数,也可为构建预测油脂货架期模型提供新的思路。

