外电场下c-C4F8和C3F7CN分子福井函数与电负性研究
李亚莎, 周 筱, 谢云龙, 刘国成
(三峡大学 电气与新能源学院,宜昌 443002)
1 引 言
六氟化硫(SF6)因其优良的绝缘性能和灭弧性能被大量运用于电力行业,研究表明,SF6气体具有较强的温室效应[1];所以,电力行业正大量减少甚至完全替换SF6的使用[2]. 目前,新绝缘气体有三氟碘甲烷(CF3I)、全氟丙烷(C3F8)、六氟乙烷(C2F6)、八氟环丁烷(c-C4F8)、氟氯代烷、C3F7CN气体等等,多数是通过实验进行击穿特性、分解产物、混合气体等研究,但往往实验得到的现象和结果缺乏合理的理论解释.在高压绝缘技术领域可利用分子模拟技术从微观机制角度研究绝缘材料的性能,为实验手段提供有力的理论支撑与参考. 廖瑞金等[3]采用密度泛函理论[4-6]对绝缘纸抗热老化性能进行了量子化学研究.李亚莎[7]等采用密度泛函理论研究了电场下盐交联聚乙烯分子结构和能量变化,分析前线轨道在外场下的成分和红光光谱的变化.吴学科[8]等基于密度泛函理论研究了SF6在外电场作用下的分子结构和红外光谱.段逸群[9]等基于密度泛函研究了CF3I分子在外电场中的物理和光谱性质.张晓星[10]等采用反应分子动力学和量子化学相结合的方法,探究了 C3F7CN/CO2混合气体的分解路径及产物分布等特性.
绝缘气体需要承受电气设备运行环境的考验,如温度、湿度、电场、杂质等等,那么气体分子本身的化学稳定性十分关键,多种指标可以反应分子的化学活性,主要分为局部活性参数和全局活性参数,大多数化学反应主要与原子、原子团或分子中的特定位点有关,系统的化学反应活性由电子密度对扰动的敏感性决定,福井函数(Fukui function, FF)是较常用的局部反应参数之一,将福井函数收缩到每一个原子上则得到简缩福井函数(Condensed Fukui function, CFF).而全局反应参数有助于分析理解所研究系统的行为,并通过量化数据提供原理性的支撑,电负性(Electronegativity)就是一种全局反应参数,更重要的是绝缘气体为灭弧阻断放电需要具备高电负性,电负性是耐电强度、灭弧阻断放电能力的有效体现,也是替代型绝缘气体必须考察的绝缘性能之一,有研究表明分子结构中存在卤族元素、环状、双键或者三键都能够提升气体电气性能[11].目前,对绝缘气体反应位点以及电负性的量化研究鲜少.
本文采用密度泛函理论计算了c-C4F8和C3F7CN分子的电子密度和能量,进而计算出外电场作用下的福井函数、简缩福井函数和电负性,并分析了外电场对三者的影响,即量化了c-C4F8和C3F7CN在外电场作用下的化学稳定性与灭弧性能,为它们的工程应用提供了一定的数据、理论支撑,也为今后绝缘气体的相关研究提供了参考.
2 理论方法和模拟方法
2.1 理论方法
概念密度泛函理论(Conceptual density functional theory)[12]又称为密度泛函反应理论,是密度泛函的新化学活性理论,化学反应理论研究的是分子在不同类型试剂攻击下的变化趋势.
预测反应位点的理论方法有多种,第一类方法从头算动力学模拟对反应过程考虑全面,但计算成本太高;第二类方法过渡态理论计算反应势垒过程较为繁琐.所以采用基于反应物自身性质,仅考虑反应物自身电子结构特征来预测反应位点的方法尤为方便有效.在概念密度泛函中,福井函数主要与系统密度函数在恒定外势约束下对电子数变化的响应有关,它能够有效反应分子中不同局部的反应活性.福井函数早在1984年由Parr和Yang等人[13]提出,它比前线轨道理论(Frontier molecular orbital theory,FMO)表现出更良好的准确性,是由电子总数N的变化引起的电子密度的微分变化,也等效于系统的化学势μ对外部势能的响应,定义为
(1)
式中,N为当前体系的电子数,ρ(r)为该位点的电子密度,ν原子核对电子产生的吸引势.由于电子密度相对于电子数的不连续性,根据有限差分近似计算式(1)的左导数和右导数以及两者的平均值,即
f+(r)=ρN+1(r)-ρN(r)≈ρLUMO(r)
(2)
f-(r)=ρN(r)-ρN-1(r)≈ρHOMO(r)
(3)
(4)
ρN、ρN-1和ρN+1分别表示分子在中性状态、阳离子状态和阴离子状态的电子密度.f+(r)表征亲核反应,通过加入电子后电子密度变化的响应来测量,在(r)位点的f+(r)值越大,则在电子增益的亲核攻击中它可以接受的电子越多,因此分子在f+(r)较大的位点易受亲核攻击;同理,f-(r)表征亲电反应,通过失去电子后电子密度的变化来测量,f-(r)越大的位点易受亲电攻击;f0(r)表征自由基反应.福井函数值越大,相应位点的反应活性越大.
为了进一步定量比较原子层面的反应活性,计算出每个原子上的福井函数值,称之为简缩福井函数[14]. 分子中某原子a的简缩福井函数表示如公式(5)和(6),
(5)
(6)
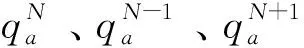
电负性在1932年由Pauling[16]首次提出,它量化了原子或官能团吸引电子朝向自身的内在能力,电负性计算依赖于原子或分子的其他性质.Parr 等人在1978年建立了密度泛函化学势和电负性之间的关系[17],即
(7)
χ为电负性,μ为化学势,E为能量,N为电子数,ν是所研究分子系统的外部电势,遵从电负性均衡原理,在定量DFT计算中存在计算化学势和电负性的实用方法,根据 Mulliken 方法[18],
(8)
这一标度简明直观,式中IE为分子的第一电离能(单位为eV, l a.u.=27.21138 eV),第一电离能是基态的气态原子失去最外层的一个电子所需能量,数值越小越容易失去电子;EA为电子亲和势,电子亲和势是基态的气态原子得到电子变为气态阴离子所放出的能量,数值越大得电子倾向越大.其中,
IE=E(N-1)-E(N)
(9)
EA=E(N)-E(N+1)
(10)
式中,E(N)、E(N-1)、E(N+1)分别是分子中性状态、阳离子状态和阴离子状态的能量.
2.2 模拟方法
在量化程序中搭建c-C4F8和C3F7CN的分子模型如图1所示,设置计算参数,其中泛函选择B3LYP,基组选择6-311G*,沿x轴方向施加步长为0.005 a.u.,范围为-0.03 a.u.至0.03 a.u.的电场,电场关键词为field=x-N nosymm,即N取值为-300至300,步长为50.使用关键词int=ultrafine增加积分的空间格点数来确保收敛,在计算窗口中对无电场中性分子进行几何优化,读取优化后的分子坐标在加电场条件下对中性分子进行几何优化,阳离子和阴离子计算单点.读取结果文件中的能量,计算分子的电负性,同时将结果文件输入到Multiwfn[19, 20]软件中计算福井函数以及简缩福井函数值,并利用可视化软件作等值面图.

图1 (a)c-C4F8分子模型;(b)C3F7CN分子模型Fig. 1 (a) molecular model of c-C4F8, (b) molecular model of C3F7CN
3 结果和分析
3.1 外电场对c-C4F8和C3F7CN分子化学反应活性的影响
福井函数是一个三维函数,考察其分布的最直观方法就是作等值面图,从福井函数计算公式可知其本质即电子密度差,在可视化软件中设置并将此密度差映射到初始状态电子密度上得到可反应福井函数大小的等值面图,称之为“福井函数投影到电子密度等值图”.c-C4F8分子和C3F7CN分子在无电场情况下的福井函数投影到电子密度等值图分别如图2和图3所示,图中蓝色越深的区域表示反应活性越强.
观察图2可知,c-C4F8分子内的F原子反应活性最强,亲电反应位点和亲核反应位点均在F原子上,即在化学反应中8个F原子容易得失电子.观察图3可知,C3F7CN分子内5N、4C、12F三个原子的反应活性比较强,且活性由强到弱依次为5N>4C>12F,即C3F7CN分子内亲电反应位点和亲核反应位点为5N、4C、12F.分别计算出上述反应位点的简缩福井函数值如表1、表2和表3所示.

图2 c-C4F8福井函数投影到电子密度等值图: (a) 正面的亲电反应活性;(b) 反面的亲电反应活性;(c) 正面的亲核反应活性;(d) 反面的亲核反应活性Fig. 2 Isograms of Fukui function projecting into electron density of c-C4F8: (a) electrophilic reactivity in the front, (b) electrophilic reactivity in the reverse, (c) nucleophilic reactivity in the front, (d) nucleophilic reactivity in the reverse
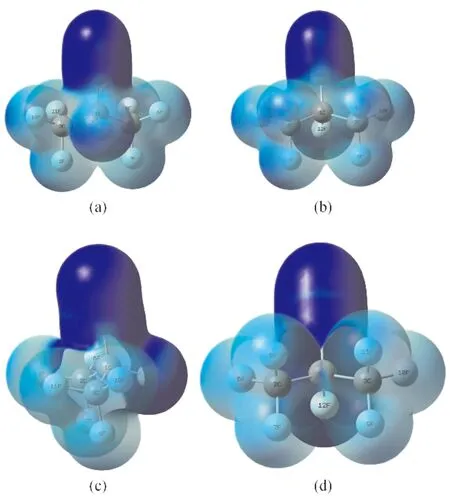
图3 C3F7CN亲电福井函数投影到电子密度等值图: (a) 正面的亲电反应活性;(b) 反面的亲电反应活性;(c) 正面的亲核反应活性;(d) 反面的亲核反应活性Fig. 3 Isograms of Fukui function projecting into electron density of C3F7CN: (a) electrophilic reactivity in the front, (b) electrophilic reactivity in the reverse, (c) nucleophilic reactivity in the front, (d) nucleophilic reactivity in the reverse
根据表1、表2和表3可以看出,分子内反应位点的反应活性对电场强度有一定的依赖性.在表1和表2中,当外电场为0时,所有氟原子的亲电简缩福井函数值和亲核简缩福井函数值分别相同,5F和6F、7F和8F、9F和10F、11F和12F的简缩福井函数以及随外电场的变化均两两相同,c-C4F8的分子结构有极高的对称性,每个C原子上两个F原子的变化保持一致.在-0.03 a.u.到0.03 a.u.电场范围内,5F与9F的简缩福井函数随外电场的变化互逆,而7F与11F的简缩福井函数随外电场的变化完全一致,这是因为外电场沿x轴方向变化,5F和6F、9F和10F在X轴向上,7F、8F与11F、12F关于x轴对称.综上,5F的简缩福井函数f-随着外电场的变化逐渐减小,即该位点失去电子愈发困难,亲电反应活性越来越弱,f+随着外电场的变化逐渐增大,即该位点愈发容易得到电子,亲核反应活性越来越强,其变化规律如图4所示;7F的简缩福井函数f-和f+均随外电场的变化先增大后减小,即该位点的亲电反应与亲核反应活性先增强后减弱,电场为0时达到最大值,最大值分别为0.092370和0.084616,整个变化过程较为缓慢,其变化规律如图5所示;9F的简缩福井函数f-随外电场的变化逐渐增大,即该位点亲电反应活性越来越强,f+随外电场的变化逐渐减小,即该位点亲核反应活性越来越弱,其变化规律如图6所示.
在表3中,电场从-0.03 a.u.变化至0.03 a.u.时,5N的简缩福井函数f-逐渐增大,且增幅较大,即该位点的亲电反应活性大幅增强,f+逐渐减小,减幅较缓,即该位点的亲核反应活性缓慢减弱,其变化规律如图7所示;4C的简缩福井函数f-大幅增大,即该位点的亲电反应活性大幅增强,f+逐渐减小,即该位点的亲核反应活性逐渐减弱,其变化规律如图8所示;12F简缩福井函数f-逐渐减小,即该位点的亲电反应活性越来越弱,f+逐渐增大,增幅较小,即该位点的亲核反应活性缓慢增强,其变化规律如图9所示.

表1 不同电场强度下c-C4F8分子内F原子的亲电简缩福井函数

表2 不同电场强度下c-C4F8分子内F原子的亲核简缩福井函数

表3 不同电场强度下C3F7CN分子内反应位点的亲电、亲核简缩福井函数

图4 c-C4F8中5F简缩福井函数随电场强度的变化Fig. 4 Variation of the CFF(5F in c-C4F8) with electric field intensity

图5 c-C4F8中7F简缩福井函数随电场强度的变化Fig. 5 Variation of the CFF(7F in c-C4F8) with electric field intensity

图6 c-C4F8中9F简缩福井函数随电场强度的变化Fig. 6 Variation of the CFF(9F in c-C4F8) with electric field intensity

图7 C3F7CN中5N简缩福井函数随电场强度的变化Fig.7 Variation of the CFF(5N in C3F7CN) with electric field intensity

图8 C3F7CN中4C简缩福井函数随电场强度的变化Fig. 8 Variation of the CFF(4C in C3F7CN) with electric field intensity

图9 C3F7CN中12F简缩福井函数随电场强度的变化Fig. 9 Variation of the CFF(12F in C3F7CN) with electric field intensity
3.2 外电场对c-C4F8和C3F7CN电负性的影响
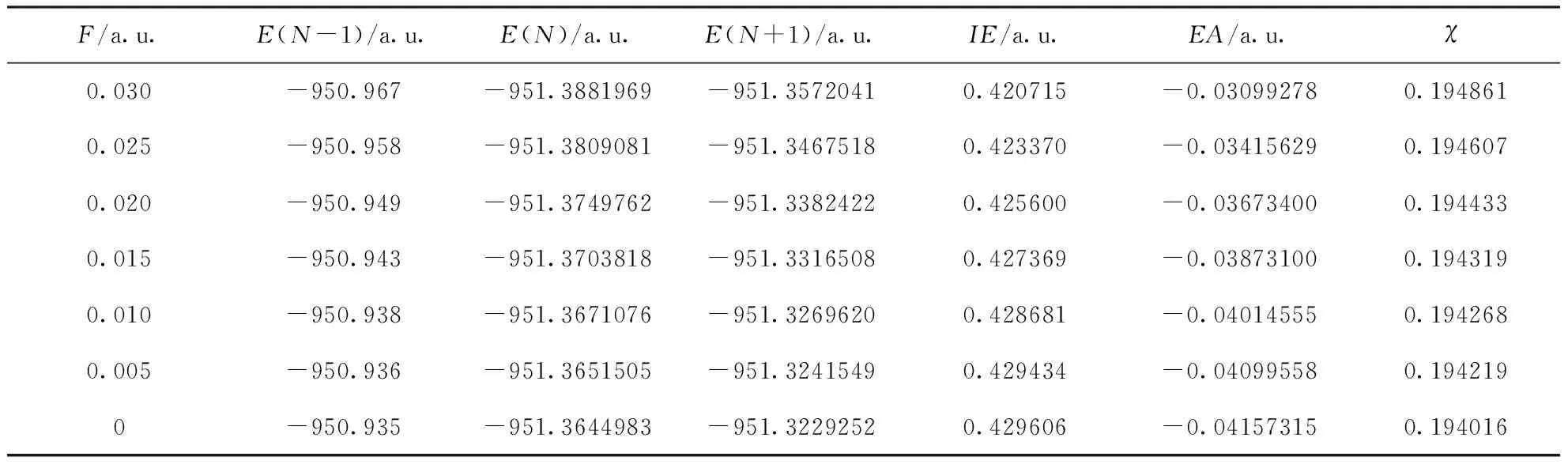
c-C4F8分子结构完美对称,随着外电场从-0.03 a.u.变化到0.03 a.u.,第一电离能、电子亲和势以及分子的电负性均与外电场方向无关,仅与外电场绝对值大小有关.表4为 c-C4F8在外电场作用时分子的总能量、第一电离能、电子亲和势以及电负性数据.电场绝对值越大,c-C4F8分子总能量越小,其主要原因是电场增大时原子上的电子发生偏移,电荷布局数发生变化,从而使得体系的哈密顿量H的势能增大,进而使得体系的总能量降低[21].随着电场绝对值的增大,第一电离能逐渐减小,电子亲和势逐渐增大.分子电负性逐渐增强,并且增幅逐渐加大,其变化规律如图10所示.
表4 不同电场强度下 c-C4F8的总能量、第一电离能、电子亲和势以及电负性
Table 4 Total energies, the first ionization energies, electron affinities and electronegativities of c-C4F8under different electric field intensities
F/a.u.E(N-1)/a.u.E(N)/a.u.E(N+1)/a.u.IE/a.u.EA/a.u.χ0.030-950.967-951.3881969-951.35720410.420715-0.030992780.1948610.025-950.958-951.3809081-951.34675180.423370-0.034156290.1946070.020-950.949-951.3749762-951.33824220.425600-0.036734000.1944330.015-950.943-951.3703818-951.33165080.427369-0.038731000.1943190.010-950.938-951.3671076-951.32696200.428681-0.040145550.1942680.005-950.936-951.3651505-951.32415490.429434-0.040995580.1942190-950.935-951.3644983-951.32292520.429606-0.041573150.194016
表5为C3F7CN在外电场作用下分子的总能量、第一电离能、电子亲和势以及电负性数据.分子总能量在电场强度-0.03 a.u.至0.01 a.u.范围内逐渐增加,且增幅逐渐变缓,在电场强度为0.01 a.u.时得到最大能量-906.2853531 a.u..在电场强度0.01 a.u.至0.03 a.u.范围内逐渐减小,且减幅增大.第一电离能逐渐减小,电子亲和势大幅减小.分子电负性逐渐减小,其变化规律如图11所示.
表5 外电场作用下 C3F7CN 的三种状态总能量、第一电离能、电子亲和势以及电负性
Table 5 Total energies, the first ionization energies, electron affinities and electronegativities of C3F7CN under different electric field intensities

F/a.u.E(N-1)/a.u.E(N)/a.u.E(N+1)/a.u.IE/a.u.EA/a.u.χ-0.030-905.8429993-906.3372064-906.3580.494207070.021238630.257723-0.025-905.8314587-906.3244745-906.3360.493015840.011427560.252222-0.020-905.8223367-906.3135608-906.3160.491224100.002097950.246661-0.015-905.8158367-906.3044427-906.2980.48860604-0.006780500.240913-0.010-905.8120238-906.2971025-906.2820.48507870-0.015155660.234962-0.005-905.8110024-906.2915276-906.2680.48052522-0.023093040.2287160-905.8128873-906.2877093-906.2570.47482203-0.030434440.2221940.005-905.8172776-906.2856513-906.2490.46837368-0.037048120.2156630.010-905.8246943-906.2853531-906.2420.46065884-0.043363380.2086480.015-905.834831-906.2868282-906.2380.45199720-0.049038120.2014800.020-905.8476948-906.2900963-906.2360.44240146-0.054060720.1941700.025-905.863201-906.2951872-906.2370.43198628-0.058383260.1868020.030-905.8812725-906.3021425-906.2400.42086999-0.061944910.179463

图10 c-C4F8电负性随电场强度的变化Fig. 10 Variation of the c-C4F8 electronegativity with electric field intensity

图11 C3F7CN电负性随电场强度的变化Fig. 11 Variation of the C3F7CN electronegativity with electric field intensity
所以,c-C4F8与C3F7CN分子的电负性受外电场影响有明显变化,且无外电场作用时,两者的电负性与SF6电负性的相对关系如表6所示,c-C4F8电负性达到SF6的0.67倍,C3F7CN电负性达到纯SF6的0.77倍,相比c-C4F8电负性,C3F7CN电负性有显著增强,表明在4个C的结构中碳氮三键相较于碳环更能提升分子电负性.
表6 无外电场作用时c-C4F8、C3F7CN、SF6的电负性以及相对电负性数据
Table 6 The electronegativities and relative electronegativities of c-C4F8, C3F7CN and SF6without electric field

F/a.u.χ(c-C4F8)相对电负性(相对于SF6)χ(C3F7CN)相对电负性(相对于SF6)χ(SF6)00.1940160.6747110.2221940.7727010.287555
4 结 论
本文采用DFT/B3LYP方法在6-311G*基组水平上对不同外电场下c-C4F8和C3F7CN分子的福井函数、简缩福井函数与电负性进行了计算研究,发现外电场对分子简缩福井函数和电负性影响明显,得到结论如下:
(1)无外电场作用时,c-C4F8分子内部亲电反应位点和亲核反应位点均在四周的F原子上,即分子化学活性主要在F原子上;C3F7CN分子内部亲电反应位点和亲核反应位点为5N、4C和12F,即这三个位点最容易得失电子.
(2)原子的简缩福井函数值对外电场的变化呈现出明显的规律.由于c-C4F8分子结构完美的对称性,关于电场方向对称的两组氟原子的CFF变化一致,而沿电场方向分布的两组氟原子的CFF随外电场的变化互为相反状态.同时电负性仅与电场绝对值大小相关,电场增大,电负性增强.而C3F7CN分子电负性受到电场大小和方向两者的影响,随着电场的变化逐渐减弱.
(3)无外电场时,c-C4F8电负性达到纯SF6的67%,C3F7CN电负性达到纯SF6的77%.基于两者的结构组成,碳氮三键相较于碳环对增强分子电负性有更好的效果.

