HPLC法测定地氯雷他定中的有关物质
李 龙,郭 伟,于秀丽,解春文
(山东达因海洋生物制药有限公司,威海 264300)
地氯雷他定是先灵葆雅公司于2001年开发上市的三环长效型的第3代组织胺拮抗剂。本品为氯雷他定的活性代谢物,可通过选择性地拮抗外周H1受体,快速缓解季节性过敏性鼻炎的相关症状,如打喷嚏、流涕和鼻痒;鼻黏膜充血/鼻塞;以及眼痒、流泪和充血;腭痒及咳嗽。还用于缓解慢性特发性荨麻疹的相关症状如瘙痒,并可减少荨麻疹的数量及大小[1-2]。
实验设计(design of experiments,DOE)是一种安排实验和分析实验数据的数理统计方法,通过对实验进行合理安排,以较少的试验次数获得理想的实验结果和正确的结论。近10年来,DOE在液相方法开发过程中受到广泛关注,通过实验设计可以以较少的实验次数对色谱条件进行开发与优化,并能确定合理的色谱参数区间[3-4]。
目前国内药典并未收录地氯雷他定原料的测定方法,欧洲药典(EP 9.1)和美国药典(USP 41)主要针对11-氟地氯雷他定(杂质A)、异地氯雷他定(杂质B)、氯雷他定等工艺杂质进行控制,但并未对降解杂质N-甲酰化地氯雷他定(杂质E)、N-乙酰化地氯雷他定(杂质F)、N-羟基地氯雷他定(杂质D)进行控制。
本实验首先使用定制设计确定分析方法的关键色谱参数,然后对关键色谱参数进行优化,建立了地氯雷他定有关物质检测方法,可同时对工艺杂质及降解杂质进行检测。本方法简单、可靠,可准确检测地氯雷他定中有关物质含量。
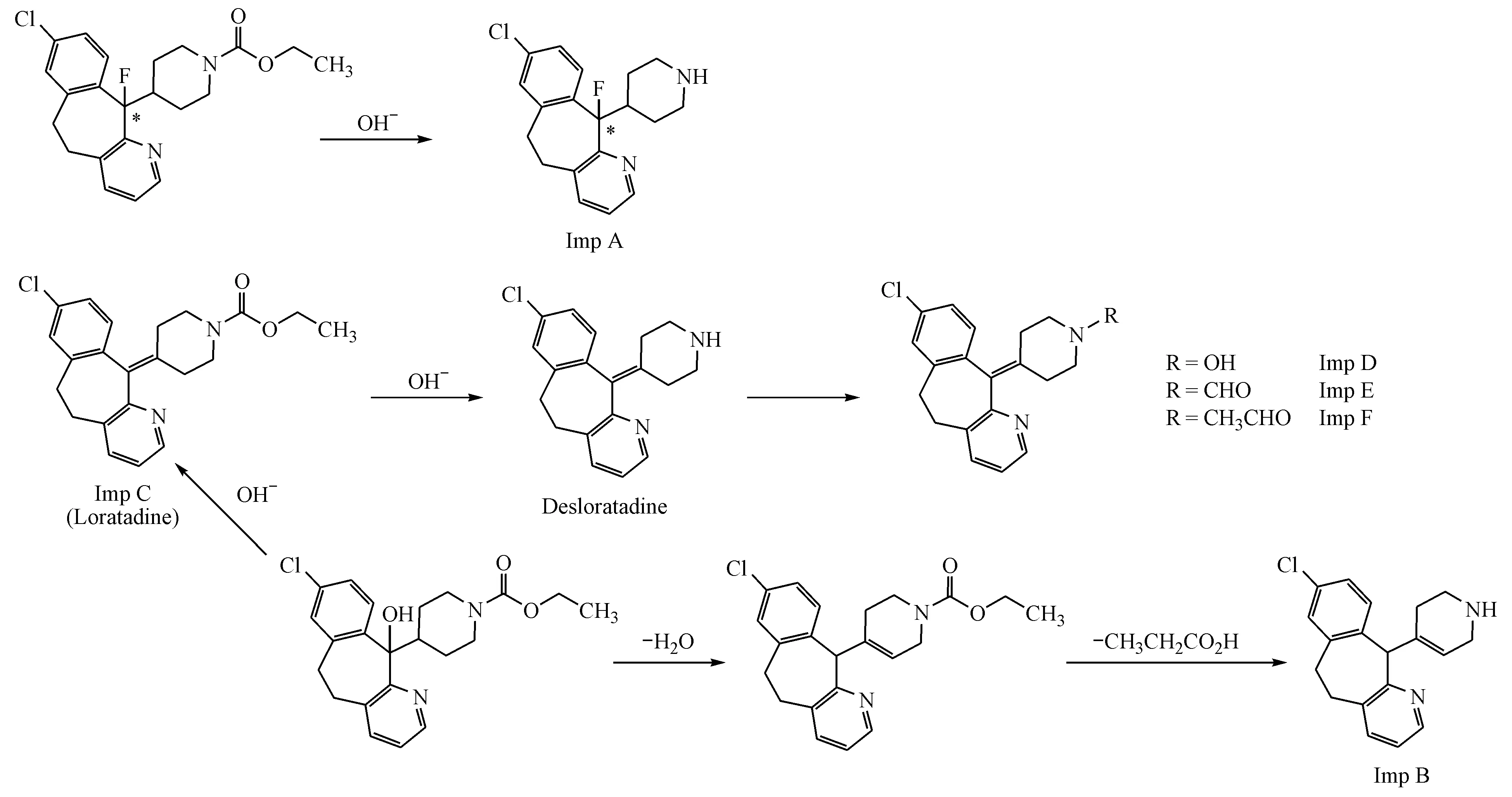
Figure 1 Origin of impurities in desloratadine
1 材 料
1.1 药品与试剂
杂质A对照品(批号1502-054A5,加拿大TLC Pharmaceutical Standards公司);杂质B对照品(批号CAX-14302-1702,美国Cato Research Chemicals公司);杂质C对照品(批号100615-201404,中国食品药品检定研究院);杂质D对照品(批号1-YHU-52-3)、杂质E对照品(批号1-KSK-17-2)、杂质F对照品(批号1-YHU-52-3)均购于加拿大Toronto Research Chemicals公司。自制地氯雷他定原料(批号170801、170802、170803),乙腈、乙醇均为色谱纯,其他试剂均为市售分析纯。
1.2 仪 器
安捷伦公司1200型高效液相色谱仪(美国安捷伦科技有限公司);XP205型电子分子天平(上海梅特勒·托利多仪器有限公司)。
2 方法与结果
2.1 色谱条件
色谱柱:YMC J′sphere ODS-M80(4.6 mm×250 mm,4 μm);检测器:UV检测器;检测波长:280 nm;柱温:35 ℃;流动相流速:1.5 mL/min;进样体积:40 μL;流动相:乙醇-0.003 mol/L十二烷基硫酸钠水溶液(取十二烷基硫酸钠0.570 g,三氟乙酸0.5 mL,加水稀释至1 000 mL)(47∶53)。
2.2 溶液的配制
各杂质对照品及地氯雷他定对照品储备液:分别取杂质A~F对照品及地氯雷他定对照品适量,精密称定,加流动相溶解并稀释制成质量浓度为0.1 mg/mL溶液。
杂质对照品溶液:分别精密量取杂质A~F对照品储备液适量,加流动相溶解并稀释制成质量浓度为2 μg/mL的溶液。
系统适用性溶液:精密称取地氯雷他定约 20 mg,再分别精密量取杂质A~F对照品储备液2 mL,同置100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀即得。
供试品溶液:精密称取地氯雷他定约20 mg,置于100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,作为供试品溶液。
2.3 专属性试验
2.3.1 已知杂质干扰试验 取按“2.2”项配制的各杂质对照品溶液与系统适用性试验溶液40 μL,分别注入液相色谱仪,记录色谱图(图2),结果各已知杂质之间的分离度均大于1.5,且不干扰主成分检测。
2.3.2 强制降解试验 取地氯雷他定适量,在酸、碱、氧化、高温、水解和光照条件下进行破坏实验,记录色谱图(图3)。结果表明,本品除氧化、酸、水解破坏条件外,其他破坏条件不发生降解。氧化、酸、水解破坏产生的降解产物与主成分、杂质之间分离度良好。各破坏条件(酸、碱、氧化、高温和光照)的物料守恒均在95.0%~105.0%,表明本方法无漏检杂质。
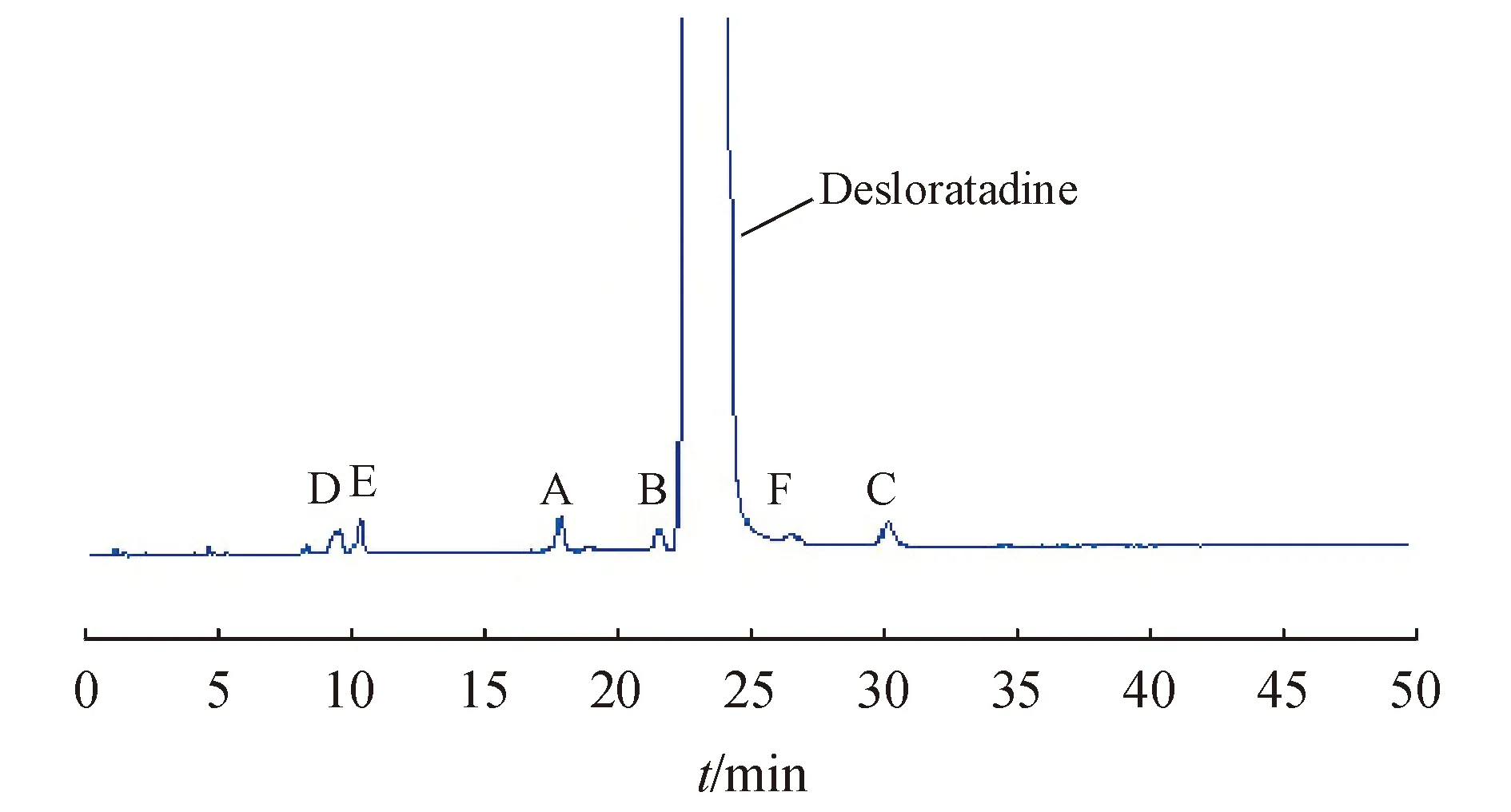
Figure 2 HPLC chromatogram of system suitability test of mixture of desloratadine and its impurities A-F
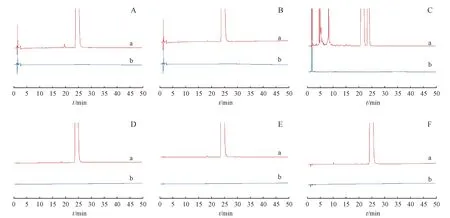
Figure 3 Chromatogram of stress test of sample (a),and dilute (b)
A:acid hydrolysis;B:basic hydrolysis;C:oxidative stress;D:photolytic degradation;E:thermal stress;F:water hydrolysis
2.4 线性、校正因子、检测限与定量限
精密量取“2.2”项下各杂质对照品及地氯雷他定对照品储备液稀释制成一系列对照品溶液。精密量取对照品溶液各40 μL,注入液相色谱仪,记录色谱图;以样品浓度(x)对测得的峰面积(y)作图,用最小二乘法进行线性回归,观察是否呈线性关系。通过地氯雷他定与杂质线性方程斜率比,计算杂质的相对校正因子,结果见表1。取地氯雷他定及各杂质对照品,用流动相不断稀释,在“2.1”项色谱条件下进样测定,定量限(LOQ)与检测限(LOD)结果见表1。
Table 1 Results of linearity test,LOQs and LODs results of desloratadine
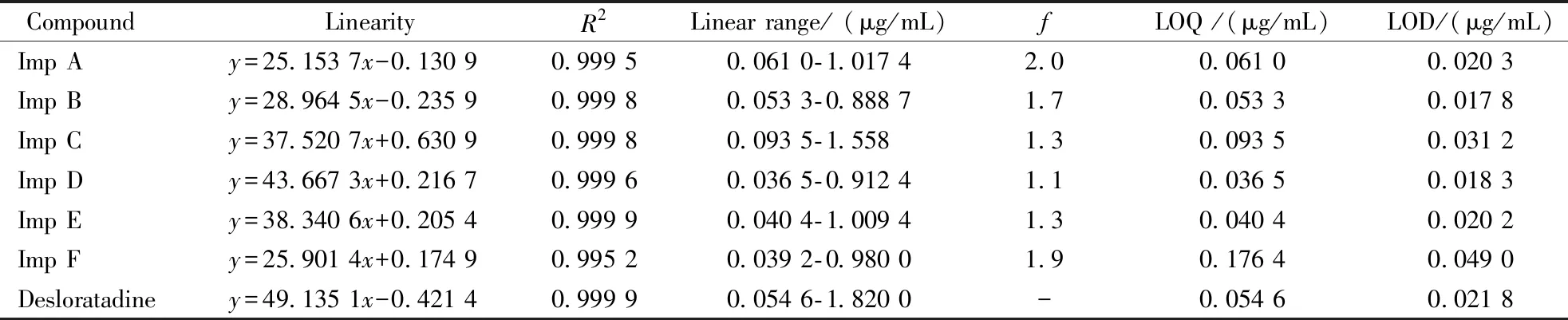
CompoundLinearityR2Linear range/ (μg/mL)fLOQ /(μg/mL)LOD/(μg/mL)Imp Ay=25.153 7x-0.130 90.999 50.061 0-1.017 42.00.061 00.020 3Imp By=28.964 5x-0.235 90.999 80.053 3-0.888 71.70.053 30.017 8Imp Cy=37.520 7x+0.630 90.999 80.093 5-1.5581.30.093 50.031 2Imp Dy=43.667 3x+0.216 7 0.999 60.036 5-0.912 41.10.036 50.018 3Imp Ey=38.340 6x+0.205 40.999 90.040 4-1.009 41.30.040 40.020 2Imp Fy=25.901 4x+0.174 90.995 20.039 2-0.980 01.90.176 40.049 0Desloratadiney=49.135 1x-0.421 40.999 90.054 6-1.820 0-0.054 60.021 8
2.5 回收率实验
精密称取地氯雷他定约20 mg,共10份,精密加入各杂质储备溶液(50%、100%、150%,各3份,其中一份不加各杂质储备溶液),置同一100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,作为供试品溶液。精密量取各供试品1 mL,置100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,作为对照溶液。按加校正因子的自身对照法测定,结果杂质A回收率为96.59%~102.23%,RSD为6.1%;B回收率为94.89%~104.41%,RSD为3.1%;杂质C回收率为97.99%~102.44%,RSD为3.4%;杂质D回收率为90.99%~102.80%,RSD为4.4%;杂质E回收率为94.17%~115.00%,RSD为6.1%;杂质F回收率为96.17%~108.45%,RSD为8.5%。
2.6 精密度及稳定性
取地氯雷他定原料适量,按照“2.2”项下方法平行配制6份供试品溶液,照“2.1”项下色谱条件检测,结果杂质A、杂质B、杂质C、杂质D、总杂E、杂质F的RSD分别为5.0%、3.6%、0.0%、8.8%、0.9%、8.8%。
取地氯雷他定原料适量,按照“2.2”项下配制供试品溶液,照“2.1”色谱条件分别在0、2、4、8、12、24、48 h内进行检测,结果杂质A的RSD(n=7)为2.2%;杂质B的RSD(n=7)为4.6%;杂质C的RSD(n=7)为5.1%;杂质D的RSD(n=7)为1.8%;总杂E的RSD(n=7)为2.7%;杂质F的RSD(n=7)为3.8%,表明供试品溶液在室温下48 h内保持稳定。
2.7 耐用性实验
通过改变柱温(±5 ℃)、流速(±0.1 mL/min)、色谱柱品牌[Weltch Ultimate XB C18(250 mm×4.6 mm,5 μm)]、流动相的有机相比例(±5%)、柱温(±5 ℃),评估杂质含量不受影响的承受程度。试验结果表明当微小改变柱温、流速、流动相比例等色谱条件,杂质含量没有发生显著变化,说明方法耐用性良好。
2.8 样品测定
取地氯雷他定原料3批,按“2.2”项下方法分别配制供试品溶液,进样测定,记录色谱图,按加校正因子(表1)的主成分自身对照法计算各供试品中杂质A~杂质F的含量,其他未知有关物质采用不加校正因子的主成分自身对照法计算,结果见表2。
Table 2 Result of impurities*
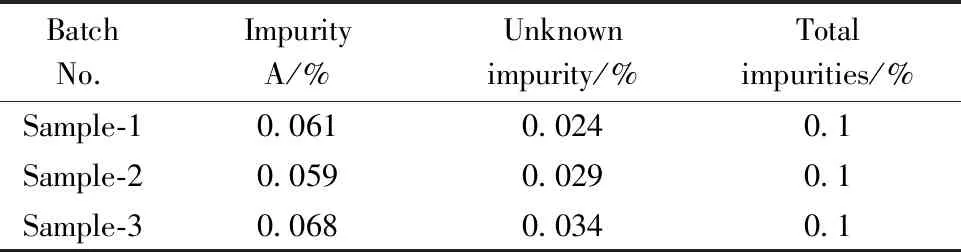
Batch No.Impurity A/%Unknown impurity/%Total impurities/%Sample-10.0610.0240.1Sample-20.0590.0290.1Sample-30.0680.0340.1
*Imp B-Imp F is not detected
3 讨 论
3.1 关键色谱参数筛选
对欧洲药典地氯雷他定原料[6]项下有关物质色谱条件进行分析,主要影响因素见图4。
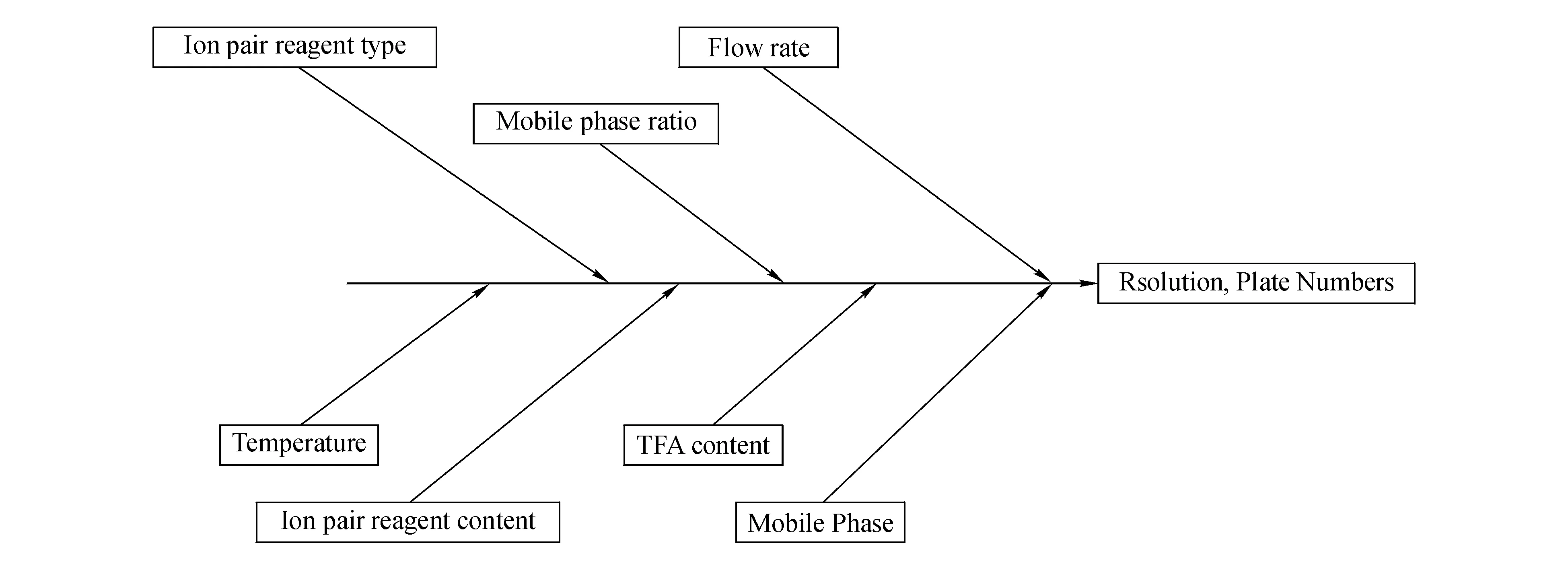
Figure 4 Fishbone of main factor of HPLC method for determination of desloratadine and its impurities
按照“2.2”项下方法配制系统适应性溶液,使用Plackett-Burman筛选设计,以杂质D、E色谱峰分离度(R1)、杂质B与主成分分离度(R2)及理论塔板数(N)为考察表指标,对流动相中离子对试剂含量(mol/L)(因素A)、柱温(℃)(因素B)、流速(mL/min)(因素C)、三氟乙酸含量(%)(因素D)、有机相比例(%)(因素E)、有机相种类(因素F)和离子对试剂种类(因素G)进行考察,按照表3进行试验,以确定色谱条件中关键色谱参数。
使用JMP软件对上述结果进行处理分析,采用最小二乘法进行效应筛选的模型拟合,得到各响应对应的参数估计与效应检验的结果,如表3所示。
Table 3 Experiment design and result
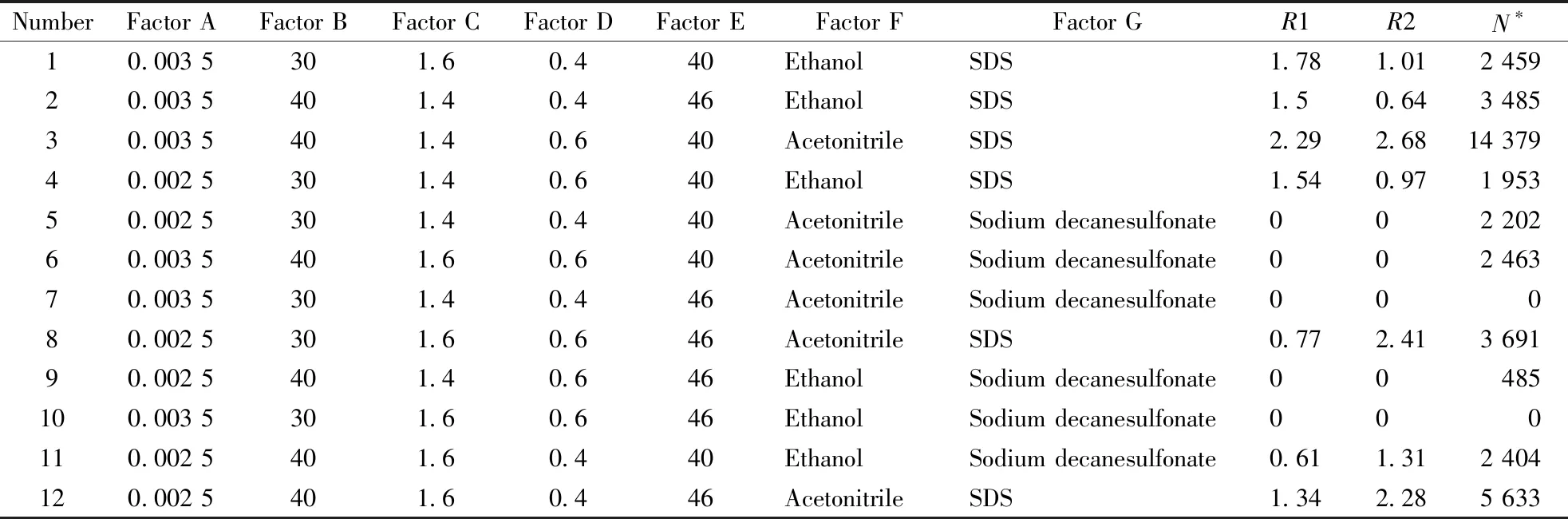
NumberFactor AFactor BFactor CFactor DFactor EFactor FFactor GR1R2N∗10.003 5301.60.440EthanolSDS1.781.012 45920.003 5401.40.446EthanolSDS1.50.643 48530.003 5401.40.640AcetonitrileSDS2.292.6814 37940.002 5301.40.640EthanolSDS1.540.971 95350.002 5301.40.440AcetonitrileSodium decanesulfonate002 20260.003 5401.60.640AcetonitrileSodium decanesulfonate002 46370.003 5301.40.446AcetonitrileSodium decanesulfonate00080.002 5301.60.646AcetonitrileSDS0.772.413 69190.002 5401.40.646EthanolSodium decanesulfonate00485100.003 5301.60.646EthanolSodium decanesulfonate000110.002 5401.60.440EthanolSodium decanesulfonate0.611.312 404120.002 5401.60.446AcetonitrileSDS1.342.285 633
*When the chromatographic peaks are overlapped,the resolution is defined as 0;when the main peak is split or deformed,the number of plates number is defined as 0
通过表4可以看出,以色谱峰分离度及主峰理论塔板数为考察指标,离子对试剂含量(mol/L,因素A)、流动相中柱温(℃,因素B)、流速(mL/min,因素C)、三氟乙酸含量(%,因素D)和有机相种类(因素F)和对考察指标未发现显著性影响;离子对试剂种类(因素G)和有机相比例(%,因素E)对考察指标有显著性影响。
Table 4 Result of data processing
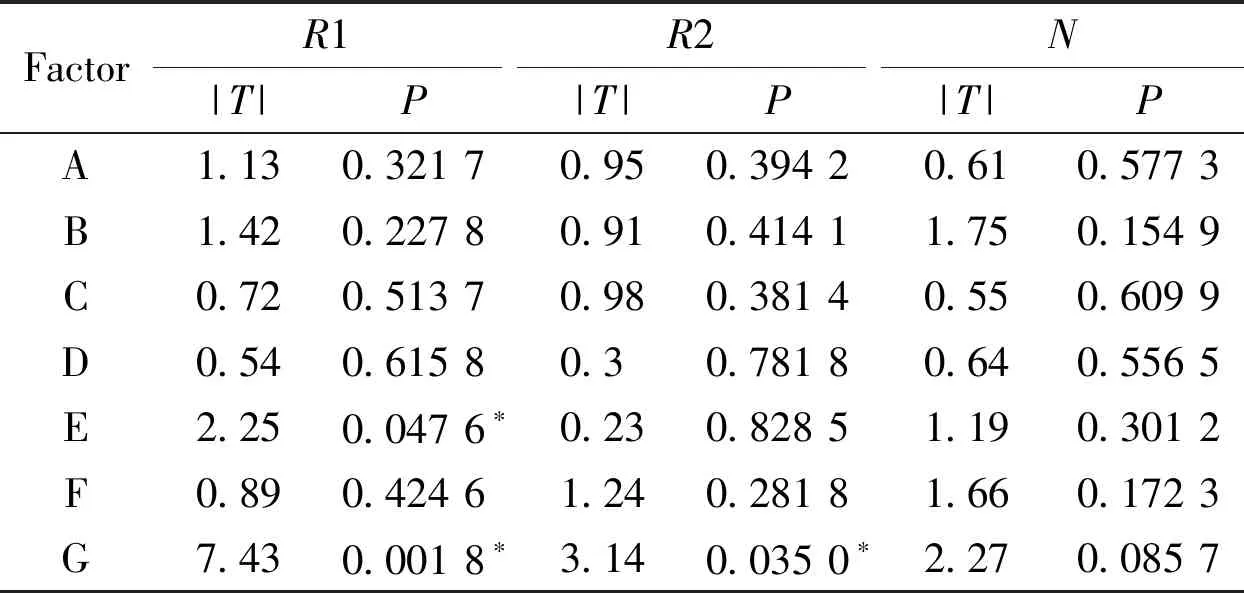
FactorR1|T|PR2|T|PN|T|PA1.130.321 70.950.394 20.610.577 3B1.420.227 80.910.414 11.750.154 9C0.720.513 70.980.381 40.550.609 9D0.540.615 80.30.781 80.640.556 5E2.250.047 6∗0.230.828 51.190.301 2F0.890.424 61.240.281 81.660.172 3G7.430.001 8∗3.140.035 0∗2.270.085 7
The smaller thePvalue,the more significant the statistical result,the “*” represents a significant effect.|T| is the absolute value ofTvalue
综合上述结果分析可知,关键色谱参数为离子对试剂种类与有机相比例。对十二烷基硫酸钠与癸烷磺酸钠进行对比发现,使用十二烷基硫酸钠配制流动相,主峰保留时间及杂质分离情况均符合要求,因此选择十二烷基硫酸钠作为离子对试剂。而有机相乙醇比例需进一步考察。
试验中使用乙醇代替乙腈进行考察,结果发现,分离度与理论塔板数等考察指标均符合要求,同时考虑到乙醇作为有机溶剂具有价格低廉、毒性低的优点,因此选用乙醇替换乙腈配制流动相。
3.2 十二烷基硫酸钠纯度的考察
按照“2.2”项下方法配制系统适应性溶液,分别对不同厂家[国药集团化学试剂有限公司(纯度85%)、麦克林(纯度99%)、阿拉丁(纯度99%)和中国食品药品检定研究院(纯度92.5%)]十二烷基硫酸钠配制的流动相进行考察。发现使用纯度较高的十二烷基硫酸钠可使主峰保留时间降低,杂质之间、杂质与主峰之间的分离度升高(图5)。这是由于十二烷基硫酸钠中主要杂质为十四烷基硫酸钠[7],该杂质含量高时会导致主峰保留时间增加且峰型严重展宽。根据实验结果,选用阿拉丁与麦克林生产的十二烷基硫酸钠配制流动相。
3.3 乙醇比例的选择
按“2.2”项下方法配制系统适用性溶液。使用色谱专家系统Drylab 2000模拟流动相中不同有机相比例下各色谱峰之间分离度。将其他色谱参数输入色谱专家系统Drylab 2000后,按照要求软件要求分别配制乙醇含量45%、50%与55% 3个比例的流动相,分别测定上述条件下地氯雷他定及各杂质的保留时间及峰面积。将测得结果输入Drylab 2000软件,对不同有机相比例下的保留行为进行预测,预测结果表明,乙醇比例在33%~60%之间,色谱峰最小分离度均大于1.5,同时考虑k[8]与保留时间最低要求,选择k应不小于1且色谱峰最大保留时间应不大于60 min,得到乙醇含量与分离度关系预测图,见图6。
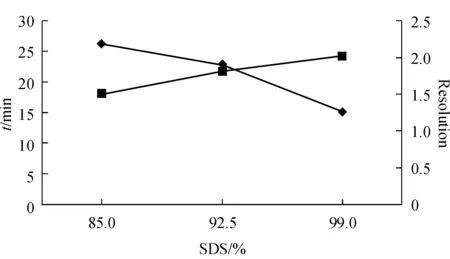
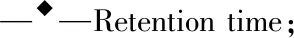
Figure 5 Effect of the assay of SDS on the resolution
Figure 6 Drylab software resolution map window
预测图中灰色部分为不符合给定条件区域,从图6可以看出,流动相中乙醇比例为44%~59%,均满足色谱峰最小分离度大于1.5,k不小于1且色谱峰最大保留时间不大于60 min(经耐用性验证后均符合要求),流动相中乙醇含量在大于47%后,色谱峰分离度数值基本达到最大且分析时间较短,因此确定流动相中乙醇比例应为47%。
3.4 检测波长的选择
取地氯雷他定杂质A、B、D、E、F对照品与地氯雷他定原料(批号:170801)适量,使用DAD检测器,在190~400 nm范围内扫描测定,地氯雷他定与各杂质在280 nm附近均有最大吸收,因此,确定有关物质检测波长为280 nm。
本研究建立的地氯雷他定有关物质检测方法,可同时对工艺杂质及降解杂质进行检测。本方法简单、可靠,可快速、准确检测地氯雷他定中有关物质含量。

