帕金森病非运动症状与血清铁代谢相关蛋白关系的研究
王 方, 钟丽珍, 张 佳, 王剑锋
帕金森病(Parkinson disease,PD)是一种中老年人常见的慢性、进展性神经变性疾病,PD主要病理变化为中脑黑质致密带多巴胺(dopamine,DA)能神经元变性、坏死,残存的DA能神经元内出现路易小体(Lewy bodies,LBs)。2003年,Braak等按照LBs出现的先后顺序对PD进行病理分期,从病理学角度证实了PD患者多种非运动症状的存在,并且证实在运动症状出现前,PD患者可因中脑外的其它脑组织损害而出现非运动症状。
越来越多的研究表明,PD患者黑质和其他核内的铁沉积过多,最终均可能导致α-突触核蛋白(α-synuclein)寡聚体的异常沉积及过度的神经免疫炎症反应,从而出现PD的运动症状及非运动症状[1,2]。近年来功能影像学研究表明铁沉积除了位于黑质纹状体以外[3],还广泛沉积于运动前皮质、前额叶、岛叶、小脑、脑桥等部位[4,5],而这些部位均与PD患者的多种非运动症状相关。有研究报道脑脊液铁及铁相关代谢相关蛋白可能与PD患者快动眼睡眠行为障碍(Rapid Eye Movement Sleep Behavior Disorder,RBD)及淡漠的发生有关[6,7],但PD患者非运动症状血清铁及其代谢相关蛋白的水平如何,国内外甚少有相关研究。本研究通过各种非运动症状量表评估PD患者焦虑、抑郁、淡漠、认知功能障碍、快动眼睡眠障碍、不宁腿综合征、嗅觉。通过检测PD患者铁、铁蛋白、转铁蛋白的水平,分析PD非运动症状与血清铁代谢相关蛋白水平之间的关系。
1 材料与方法
本课题已获得大连市中心医院伦理委员会及患者同意,入组患者均已签署参加临床研究的知情同意书。
1.1 研究对象的选择
1.1.1 PD组 连续选取2016年9月-2019年5月就诊于大连医科大学附属大连市中心医院神经内科符合以下入组及排除标准的PD患者60例。PD患者纳入标准:符合2016年中国帕金森病诊断标准(2016版)的PD诊断标准。入组排除标准:经详细的神经系统和其他方面的检查,排除脑血管病、脑炎、中毒、创伤等所致帕金森综合征;排除原发性震颤;排除多系统萎缩、进行性核上性麻痹、路易体痴呆等帕金森叠加综合征;排除严重痴呆、构音障碍等影响情感表达及其他精神疾病;排除各种原因引起的贫血;无铁和铁代谢相关性疾病,如缺铁性贫血、遗传性血色素沉着病等;排除恶性肿瘤、残疾及其他严重躯体疾病。
1.1.2 正常对照组 连续选取2016年9月-2019年5月就诊于大连医科大学附属大连市中心医院神经内科符合以下对照粗入组标准的健康对照组60例。其中年龄与性别组成与PD组相匹配。正常对照者入组标准:(1)无PD、继发性帕金森综合征、帕金森叠加综合征、遗传变性性帕金森综合征、特发性震颤等;(2)无阿尔兹海默病、血管性认知障碍、路易体痴呆等;(3)无快动眼睡眠行为障碍、发作性睡病等睡眠疾病;(4)无全身无感染性疾病;(5)无脑炎、脑膜炎、脑血管病及脑肿瘤等颅内疾病;(6)无颅脑外伤及手术史;(7)无铁及铁代谢相关性疾病,如缺铁性贫血、遗传性血色素沉着病等。
1.2 非运动症状的评价
1.2.1 汉密尔顿焦虑量表(Hamilton Anxiety Scale,HAMA) 评估患者的焦虑状况,≥14分为肯定有焦虑症状,分为PD焦虑组(PD-A组);≤7分为没有焦虑症状,分为PD非焦虑组(PD-NA组)。
1.2.2 汉密尔顿抑郁量表(Hamilton Depression Scale,HAMD) 评价患者的抑郁状况,>13分为存在抑郁症状,分为PD抑郁组(PD-D组);<8分为无抑郁症状,分为PD非抑郁组(PD-ND组)。
1.2.3 蒙特利尔认知评估量表(Montreal Cognitive Assessment,MoCA) 评价患者认知功能的情况,若受试者受教育年限小于12 y,则在测试结果上加1分,<26分为可能存在认知功能障碍(cognitive impairment,CI),分为PD认知功能障碍组(PD-CI组);≥26分为正常,分为PD非认知功能障碍组(PD-NCI组)。
1.2.4 快速眼动期睡眠行为障碍筛查问卷(Rapid Eye Movement Sleep Behavior Disorder Screening Questionnaire,RBDSQ) 评价PD患者的RBD症状,分值≥6分提示为很可能有RBD,分为PD-很可能的快速眼动期睡眠行为障碍组(PD-PRBD组);<6分提示不存在RBD症状,分为PD-非快速眼动期睡眠行为障碍组(PD-NPRBD组)。
1.2.5 PD改良淡漠量表(Modified Apathy Evaluation Scale,MAES) 总分>14分提示有淡漠症状,分为PD淡漠组(PD-AP组);≤14分为不存在淡漠症状,分为PD非淡漠组(PD-NAP组)。
1.2.6 阿根廷嗅觉减退评定量表(Argentine Hyposmia Rating Scale,AHRS) 总分≤22分提示存在嗅觉障碍(olfactory dysfunction,OD),分为PD嗅觉障碍组(PD-OD组);23或24分为嗅觉正常,分为PD非嗅觉障碍组(PD-NOD组)。
1.2.7 国际不宁腿综合征评定量表(International Restless Legs Syndrome Rating Scale,IRLSRS) 根据国际不宁腿综合征研究组(International Restless Legs Syndrome Study Group,IRLSSG)及IRLSRS评价PD患者有无不宁腿症状,将PD患者分别PD-RLS组及PD-NRLS组。
1.3 血清学标本的采集 在患者病情允许的情况下,停用与抗PD相关的药物10~12 h,并于次日清晨留取空腹静脉血4 ml,检测血清铁、铁蛋白及转铁蛋白的水平。
1.4 统计学方法 资料数据通过SPSS 23.0软件进行统计处理,以P<0.05为差异提示有统计学差异。计量数据为正态分布时采用均数±标准差表示;非正态分布时采用中位数、四分位间距表示。计量资料组间内比较时,采用t检验对正态分布数据进行分析;采用非参数检验对非正态分布数据进行统计分析。
2 结 果
2.1 PD患者与健康组血清指标水平的比较 本研究检测了60例对照组及60例PD组患者的血清铁、铁蛋白、转铁蛋白的水平。对照组与PD组血清铁、铁蛋白、转铁蛋白的比较结果(见表1)。结果显示PD组血清转铁蛋白的水平明显高于对照组;PD组铁蛋白水平明显低于对照组。
2.2 PD患者各非运动症状分组血清指标水平的比较 对PD不同运动症状进行分组,分别比较PD-A组和PD-NA组、PD-D组和PD-ND组、PD-CI组和PD-NCI组、PD-RBD组和PD-NRBD组、PD-AP组和PD-NAP组、PD-OD组和PD-NOD组、PD-RLS组和PD-NRLS组的血清铁、铁蛋白、转铁蛋白的水平,比较结果(见表2)。结果显示PD-D组铁蛋白水平明显低于PD-ND组;PD-AP组铁蛋白水平明显低于PD-NAP组;PD-RBD组血清转铁蛋白的水平明显高于PD-NRBD组。
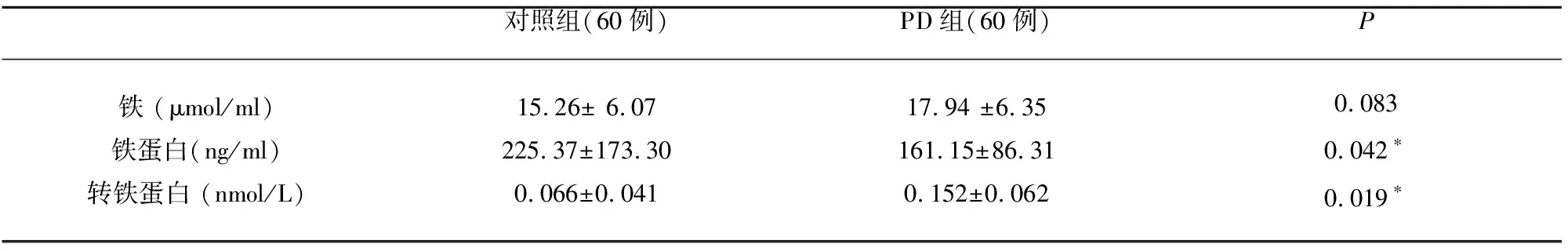
表1 对照组与PD组血清铁、铁蛋白、转铁蛋白水平的比较
*:P<0.05
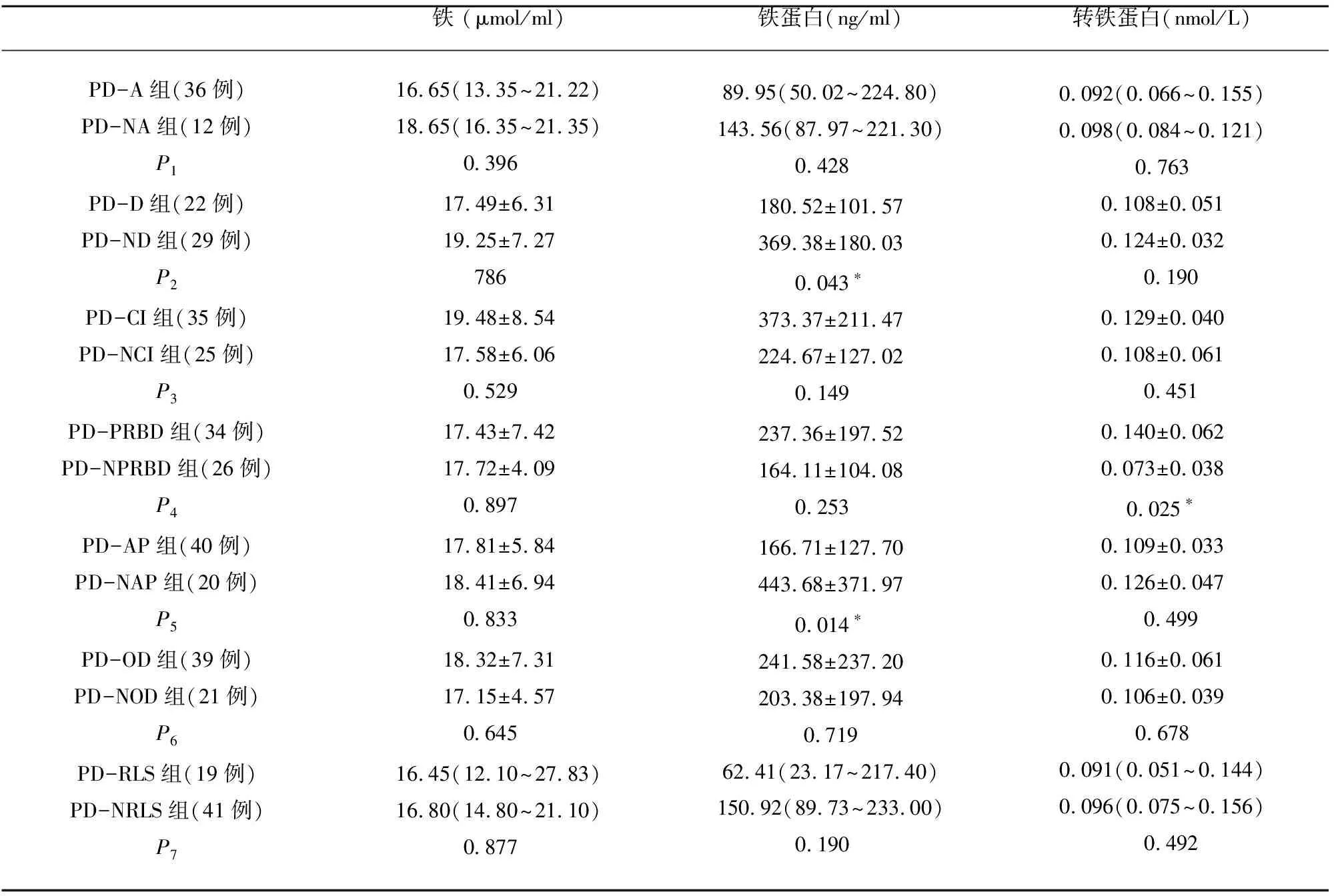
表2 PD患者各非运动症状血清铁、铁蛋白、转铁蛋白水平的比较
*:P<0.05
3 讨 论
铁在维持人体正常生理活动中起到非常重要的作用,尤其在神经细胞代谢、蛋白质合成、线粒体有氧呼吸、神经递质运输和髓鞘形成等过程中发挥重要作用。但过量的铁可以通过Fenton反应促进过氧化物的降解,并产生大量的羟自由基,从而造成神经细胞的死亡,同时过量的铁也可能导致α-synuclein寡聚体的异常沉积。如今越来越多的研究显示,PD患者脑内黑质及在特定大脑区域中存在铁的过度沉积[1]。有研究表明血液系统异常基因的表达可引起PD外周血的铁代谢异常[8],同时外周的铁可以透过血脑屏障进入脑内,故外周铁代谢紊乱也成为PD的发病机制之一[9,10]。铁蛋白被认为是铁的储存蛋白,正常情况下,血清铁含量的增加会导致铁蛋白的增加,脑组织也会增加铁蛋白。而转铁蛋白是铁运输的主要载体,能够有效地控制游离铁的水平,同时转铁蛋白也是铁通过血脑屏障从外周系统转运到中枢神经系统的主要转运体[11]。本研究发现PD患者转铁蛋白的水平明显高于对照组水平,而铁蛋白水平明显低于对照组水平,说明PD患者铁储存明显减少,而这些减少的储存铁可能是因过多的转铁蛋白将其转运至脑内所致,提示PD患者血清中转铁蛋白、铁蛋白的水平也可能间接反映了脑内铁的水平。
近年来有研究表明铁沉积除了位于黑质纹状体以外[3],还广泛沉积于运动前皮质、前额叶、岛叶、小脑、脑桥等部位[4,5],而这些部位均与PD患者淡漠、RBD等多种非运动症状相关,但血清铁及其代谢相关蛋白是否同样介导非运动症状的发生,目前国内外相关研究较少。有研究表明PD合并淡漠及PD合并RBD患者脑脊液中铁存在代谢紊乱[6,7]。也有研究发现血清铁与PD患者焦虑有关,但本研究未发现PD焦虑与非焦虑组有差别[12]。本研究发现PD-D组铁蛋白水平明显低于PD-ND组;PD-AP组铁蛋白水平明显低于PD-NAP组,提示PD抑郁患者、PD淡漠患者储存铁明显减少,这些减少的储存铁可能通过血脑屏障转运到脑内,沉积到与PD抑郁或淡漠发生相关的脑功能区如前额叶或岛叶,从而参与到PD淡漠和抑郁发生。同时本研究发现PD-RBD组血清转铁蛋白的水平明显高于PD-NRBD组。提示PD伴发RBD可能通过更多的转铁蛋白将铁转运至脑内,通过氧化应激等反应使得更多神经细胞变性、死亡,从而与PD患者RBD的发生、发展有关。
不宁腿综合征(RLS)也是PD常见的非运动症状,铁在RLS病理生理学中被证实具有重要作用,因此近年来对RLS治疗也出现了新的选择-补铁治疗[13],但铁代谢在帕金森病患者RLS的发病机制仍不尽相同。有研究发现PD伴有RLS患者与PD不伴RLS患者血清铁蛋白水平无显著差异[14]。本研究结果也未发现两组血清铁代谢相关指标有明显差异,这表明在PD患者中RLS的病理生理学机制与特发性RLS的发生机制可能是不同的,铁代谢异常并不一定发生在PD伴RLS患者中。但也有研究发现脑脊液铁代谢异常与PD患者RLS的发生进展有关[15],本研究未发现PD伴有RLS患者血清铁代谢相关指标有差异,考虑可能与样本量及所纳入的患者不同有关。
综上,外周铁代谢紊乱可能参与了PD非运动症状中快动眼睡眠行为障碍、淡漠及抑郁的发生、发展,铁蛋白、转铁蛋白可能是帕金森病快动眼睡眠行为障碍、淡漠及抑郁发生的外周血指标。但本研究存在样本量较小、对PD伴发非运动症状患者临床症状的评价存在一定的主观性等系统误差,有待于今后继续增加样本量及进一步采用客观评价方法以验证本研究的结果。

