锂电池磷酸铁锂正极材料的结构与性能相关性的研究进展
胡江涛,郑家新,潘锋
北京大学深圳研究生院新材料学院,广东 深圳 518055
1 引言
橄榄石结构过渡金属磷酸盐LiMPO4(LMP;M = Fe、Mn、Co、Ni;理论容量 170 mAh·g-1)被Padhi和Goodenough1发现后,一直是学术界和产业界研究的热点,特别是磷酸铁锂(LiFePO4),具有良好的热稳定性、低廉的成本(因为其所含元素在地球的丰度较高)、无毒、较高的理论容量和较好的放电平台2-4,已经投入商业应用,是动力电池首选的正极材料,其晶体结构如图1所示(Mn、Co和 Ni拥有相同的晶体结构)。橄榄石结构LiFePO4,是聚阴离子框架结构,其结构基元是LiO6八面体、FeO6八面体和PO4四面体,磷酸根中强的 P―O共价键在完全充电状态下稳定了氧原子,避免其被氧化生产氧气而释放,该结构的存在使得 LiFePO4成为一种安全的正极材料。而且由于其稳定的聚阴离子框架结构,LiFePO4的循环性能非常好。LiFePO4的不足之处在于电子电导率和离子电导率较低,分别为 10-9S·cm-1和 10-10-10-15cm2·s-1,作为正极材料应用于锂离子电池表现出较差的倍率性能。除此之外 LiFePO4的能量密度也不高5-8。因此,现阶段对该材料的研究主要集中在提高能量密度和倍率性能方面5,9-11,或者结合它的结构稳定优点来修饰高能量密度的层状材料12-14。

潘锋,1985年获北京大学化学学士学位,1994年获英国Strathclyde大学博士学位。现任北京大学深圳研究生院新材料学院院长、博导、“千人计划”特聘专家。研究方向为清洁能源及关键材料研发。国家材料基因组重点专项首席科学家。

图1 LiFePO4的晶体结构示意图Fig. 1 The crystal structure of LiFePO4.
对LiMnPO4的研究兴趣来自于它的高充放电电压平台(4 V),但是LiMnPO4面临比LiFePO4更加严峻的问题,它的电子导电性比 LiFePO4低四个数量级15。在充放电过程中形成的 MnPO4与LiMnPO4的晶格适配度很低,而且在Mn3+形成之后产生 Jahn-Teller效应引起严重的晶格形变,影响电化学性能16,17。同时在充放电的过程中Mn3+易发生歧化反应生成 Mn2+和 Mn4+,Mn2+极易溶出,导致材料中的能量因子丢失18,同时Mn4+具有极强的氧化性很容易氧化分解电解液,导致电化学性能下降18-20。研究表明,LiFePO4和LiMnPO4形成的固溶体 LiMnyFe1-yPO4也可以进行正常的充放电,LiMnyFe1-yPO4的晶格常数满足Vegard定律21,Fe3+-O-Mn2+之间的超交换相互作用可产生 Mn3+/Mn2+在 4.1 V的高电压22。在LiMnyFe1-yPO4中,当Fe元素出现在Mn附近位置时,会激活 Mn3+/Mn2+22。和 LiFePO4一样LiMnyFe1-yPO4的离子电导率和电子电导率都不高,其倍率性能也很差。
LiNiPO4和 LiCoPO4都具有非常高的放电电压,分别可达到5.2和4.8 V。LiCoPO4是一种非常具有竞争力的电极材料,可以实现接近于LiCoO2的能量密度23,24。但是LiCoPO4的电化学稳定性和热稳定性非常差,即使对其界面进行处理,几十次循环后容量衰减仍可达到50%25,26,其衰减原因不仅仅在于低的电子电导率和离子电导率27,与高电压下电解液的分解也有关系28。循环过程中 LiCoPO4的锂脱嵌机制与 LiFePO4和LiMnPO4不一样,它在循环过程中有中间相的形成29。上述种种原因成为 LiCoPO4商业化应用的障碍。为解决 LiCoPO4面临的问题比较有效的方法有元素替代30,31和界面修饰32,33等,这些方法在一定程度上可以提高离子和电子电导率,并提高稳定性,但不能从根本上消除这些影响。LiNiPO4在电化学过程中的问题很多,目前的研究结果表明充电电压达到 5.2 V时,甚至没有锂离子的脱出34,35。而且很难找到与LiNiPO4匹配的电解液,即使有适合的,计算表明 LiNiPO4和 NiPO4之间的体积变化很大,这可能会导致结构的畸变进而影响到材料的电化学稳定性34。
综上,LMP体系材料中最有商用价值且安全廉价的是LiFePO4和LiMnPO4或者它们混合形成的固溶体。为提高其电化学性能,就需要解决低电子和离子电导率的问题。改善LiMnyFe1-yPO4材料导电性能的方法主要有包覆和掺杂两种36。包覆法是在磷酸铁锂材料表面通过物理或化学方法包覆一层电子导体,以改善其电子传输性能。碳包覆是一种常用的磷酸铁锂改性方法,碳材料的引入一方面可增加粒子与粒子之间的导电能力,另一方面还可以抑制合成过程中颗粒的融合与长大,减小最终产物的粒径,同时还可以起到还原剂的作用,避免Fe3+的生成,这就实现了从多方面改善磷酸铁锂类材料充放电性能的要求1,36-39。但是过多的碳包覆会降低最终产物中活性物质的比例和振实密度,进而影响到材料的体积能量密度。离子掺杂是改善磷酸铁锂导电性能的又一种有效方法,在LiFePO4晶格中掺入高价离子40-42,可很大程度上提高 LiFePO4的电化学性能。解决离子电导率低的问题,可以采取控制体相缺陷和缩短传输路径的手段。锂离子在橄榄石材料体相中主要沿着[010]方向一维扩散,扩散通道很容易被杂质堵塞或缺陷打断,导致磷酸铁锂材料实际扩散系数降低。所以通过设计LiMnyFe1-yPO4的材料结构和降低 LiMnyFe1-yPO4的缺陷浓度可以改善锂离子扩散速率并提高电化学性能。颗粒纳米化可以缩短锂离子的迁移路径,降低颗粒内部的传输时间,提高倍率性能43。此时,磷酸铁锂电池倍率性能的决速步不再是锂离子在颗粒内部的脱嵌,而是锂离子或者电子在界面的传输速率起到决定性作用3,44,45。下面从磷酸铁锂材料体相晶体结构、界面结构及在不同的电解质环境下的界面重构和电极结构与锂电池性能的构效关系等方面进行总结,系统化的阐述并总结了影响磷酸铁锂类正极材料最新研究进展。
2 磷酸铁锂材料体相特征与锂电池性能的关系
2.1 磷酸铁锂相结构
2001年,Amador等46将α-LiFePO4置于极高压力下,晶体中原子位置发生了变化,空间结构由Pnmb变化成Cmcm,得到了β-LiFePO4。其晶体结构如图2所示,在β-LiFePO4中,锂离子与周围的氧原子配位形成畸变的四面体配位 LiO4,不同的 LiO4四面体既不共点和边,也不共面,不同锂原子之间距离很远以至于不存在锂离子传输通道。
2013年研究者将不同相结构的磷酸铁锂作为锂离子电池正极材料进行了较详细研究48,发现与传统的α-LiFePO4相比,β-LiFePO4的电子电导率较高,但由于其极低的锂离子迁移率,它几乎没有电化学活性的(在 2.0-4.2 V下容量仅有 15 mAh·g-1,且包碳后性能未得到明显提高),测得的少量容量也是归于β-LiFePO4中混杂的少量α-LiFePO4的贡献。而且其充放电曲线与传统的α-LiFePO4相比差距很大,磷酸铁锂在3.4 V左右特有的充放电平台消失了,而是在充放电电压区间内表现为斜线(这与β-LiFePO4锂离子迁移率低有关),之后的研究也证实了β-LiFePO4锂离子迁移率远低于α-LiFePO449。北京大学潘锋课题组50对β-LiFePO4进行了系统的研究,通过调控试验条件,可以实现磷酸铁锂两种相结构的可控制备。随后将β-LiFePO4与碳进行球磨引进的缺陷,最终产物打通了β-LiFePO4体相中锂离子的传输通道,实现了128 mAh·g-1的比容量47。且其充放电曲线和层状正极材料类似,磷酸铁锂的充放电平台消失了,表现出固溶反应的电化学特性,如图3所示。对β-LiFePO4进行了循环稳定性测试,循环 1000次基本没有容量衰减,表现出了非常好的循环稳定性。高容量β-LiFePO4的出现,以及其固溶充放电行为,为实现高倍率 LiFePO4电池性能带来了可能性。通过调控合成路线,潘锋课题组首次在LiMn0.5Fe0.5PO4固溶纳米晶体材料里面发现嵌入了亚纳米(2 nm尺度)β-LiMnxFe1-xPO4新相,它堵塞锂离子的扩散通道,在快速充放电时会影响电池的倍率性能51。

图2 β-LiFePO4的晶体结构示意图47Fig. 2 Schematics for structures of β-LiFePO4 47.
2.2 元素掺杂
元素掺杂是提高磷酸铁锂倍率性能的重要途径,考虑到橄榄石结构的一维离子传输特性,离子掺杂很有可能在提高电子导电性的同时降低体系的离子电导率52,因此在掺杂过程中一定要兼顾离子和电子的输运特性。掺杂通常分为四类,分别是金属铁位掺杂、金属锂位掺杂、铁锂位共掺杂以及非金属掺杂。关于金属锂位掺杂,研究比较深入的是MIT的Chiang等课题组37,他们在LiFePO4晶格中掺入高价离子,形成具有阳离子缺陷的Li1-xMxFePO4[M = Mg2+、Al3+、Ti4+、Nb5+、W6+等],使其电导率提高8个数量级左右,达到10-2S·cm-1,极大地提高了LiFePO4的电化学性能。上述过程提高电子电导率的重要原因是由于Li或Fe的缺陷出现了Fe的混合价,形成了p型半导体。中国科学院物理研究所施思齐等53采用第一性原理计算方法,用一定量的Cr3+取代LiFePO4中的Li,研究了 Cr3+对 LiFePO4电子结构的影响,同时从理论上解释了 Cr3+掺杂提高 LiFePO4电导率具体原因。之后,倪江锋等54采用不同的方法合成了两种 Cr3+掺杂 LiFePO4,证明了 Cr3+掺杂对于锂离子输运的重要作用。铁位掺杂也有相关的报道,Meethong等55,56开展了一系列工作证明高价掺杂对于倍率性能的作用。在Fe位还有Na+掺杂,Na的掺杂同时提供了氧空位57。吴宇平课题组58在Fe位进行了Zn2+掺杂,掺杂元素的“pillar”效应为锂离子的传输提供了更大的空间,提高了电子和离子电导率。铁锂位共同掺杂比较重要的工作是Wang等59进行的Mo元素掺杂,它同时占据了两个金属位点,结果显示 LiFePO4的导电性有所改善。非金属掺杂的工作有很多,比如说张中太课题组60采用的N、S、Cl和F等掺杂,杨勇课题组61进行的Ge、Sn、Se、Te或B掺杂,都起到了提高导电性的作用。LiFePO4中的金属位点包括锂位和铁位,但是掺杂元素的准确占位情况还不够明确,存在很多争议。Islam课题组62通过模拟的方法总结了二价到五价金属元素掺杂可能存在的掺杂位点,当然也存在一些例外的情况。

图3 β-LiFePO4在不同球磨时间条件下的充放电曲线47Fig. 3 Charge/discharge curves of β-LFPC with different ball-milling time 47.
2.3 颗粒纳米化
LiFePO4颗粒纳米化是解决锂离子传输问题的有效手段。计算62和实验63证明LiFePO4的传输主要路径是沿着[010]方向的一维传输,其本征扩散系数大约为10-8-10-12cm2·s-164。根据Fick扩散定律,颗粒纳米化可缩短锂离子传输路径减少传输时间从而提高传输效率。纳米化后锂离子在颗粒中的传输距离(锂离子是沿着[010]方向1D传输,在该方向的30 nm距离中传输小于1 s),并且颗粒与电解液的接触面积增加,提高了电化学反应面积,从而提高锂离子进出颗粒的速度;颗粒纳米化也增加了与导电颗粒的接触,提高了电子输运特性。总之,LiFePO4颗粒纳米化后可以大大提高电池的倍率性能65。例如,通过控制LiFePO4颗粒的生长方向,缩短[010]上的传输距离提高锂离子传输速率,亦可实现高倍率性能。Golden等66通过分子动力学模拟的方法证明了如果控制晶体沿着[100]方向生长,会增强离子在[010]方向上的传输。Huang等67通过水热的方法合成了两种生长方向的 LiFePO4,实验证明b方向传输路径缩短,锂离子扩散速率会增大。
2.4 体相缺陷
LiFePO4颗粒纳米化后,其传输的微观机制会发生改变,例如Amin等68研究了150 °C条件下LiFePO4的锂离子扩散系数,结果为 10-9-10-10cm2·s-1,同时也测定了a、b和c方向上的扩散系数,这个时候三个方向上的各向异性表现的不是那么明显,其传输模式已经从传统的1D传输扩展到了2D和3D。1D的锂离子传输模式有很大的缺点,传输的过程中锂离子很容易被通道内的缺陷所阻挡,但是如果是2D或者3D传输通道,锂离子可以利用缺陷实现多维传输。当反位量足够大的时候,就容易实现多维离子传输,这时候磷酸铁锂的两相变化就成为了固溶反应机制,这样有利于实现高的倍率性能。如果想让1D通道上被堵塞的锂离子继续传输,需要临近的1D维通道位置存在空位,形成网络促进传输,如果是完美的晶体结构,3D锂离子传输是不可能实现的。一般情况下我们遇到的缺陷类型包括:Li+在 Fe2+位、Fe2+在Li+位、Fe2+空位等。Ceder课题组69研究了粒径、反位和容量之间的关系,如图4所示。
对颗粒电化学性能影响最大的是 Fe2+/Li+反位缺陷,此时锂离子的传输通道被堵塞,影响到锂离子的正常脱嵌,表现出差的倍率性能,当缺陷含量较多的时候,会导致一部分锂离子失去电化学活性,导致容量下降。为了实现不错的LiFePO4倍率性能,相关课题组采用了很多种方法来抑制材料中的反位现象,比如说Guo等70合成的材料仅有小于0.3%的反位量,因此表现出了不错的电化学性能。但是缺陷的含量和电池的电化学性能不是线性的正相关关系,已经有研究者证明,当Fe2+/Li+反位缺陷达到2%以上时,锂离子的传输通道就会从1D扩展到2D或者3D3,69,其倍率性能不会受到太大影响,甚至会比同尺寸完美晶体的性能要好。潘锋课题组51设计了合适的合成流程得到了高 Fe2+/Li+反位量(5.27%)的α-LiMn1-yFeyPO4材料,促使锂离子的1D传输通道扩展到2D和3D,实现了非常好的倍率性能。反位量增加可以使橄榄石结构的两相反应机制成为了固溶反应机制,为倍率性能提高起到了很大作用71。
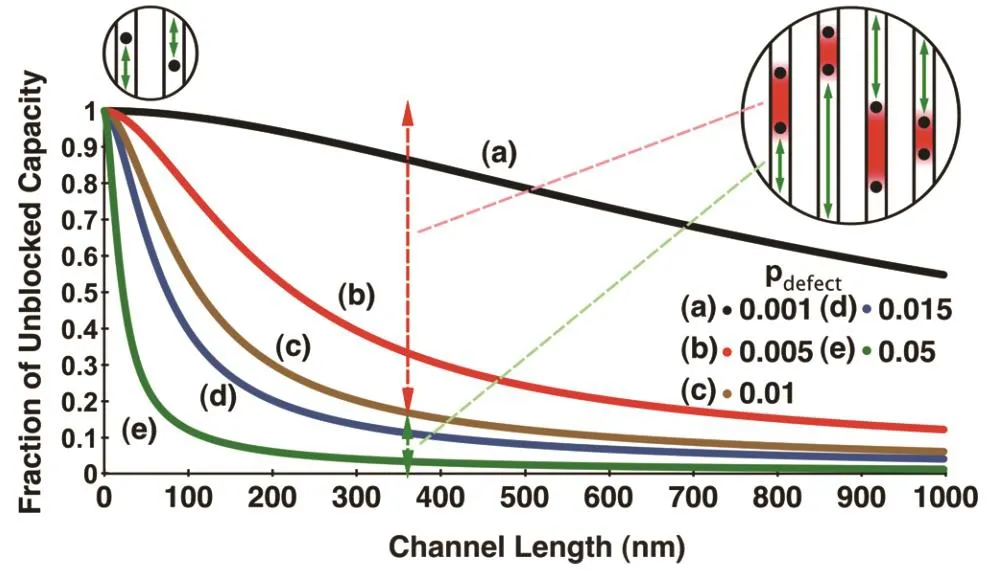
图4 LiFePO4颗粒的粒径、反位和容量之间的关系69Fig. 4 Expected unblocked capacity vs channel length in LiFePO4 for various defect concentrations 69.
2.5 锂离子传输机理
磷酸铁锂中锂离子的传输机制探讨一直是重要的研究课题,比较成熟的模型是Goodenough等1提出的Shriking-shell模型和Andersson等72提出的Mosaic模型。Shriking-shell模型73主要是指充放电过程中会形成LiFePO4/FePO4两相界面,该界面会随着锂的脱嵌发生动态变化。
Mosaic模型是指活性材料内部存在多个电化学活性中心,两相界面在活性中心同时产生,然后以活性中心为核心向外扩散。考虑到锂离子脱嵌的各向异性问题,Newman等74对Shriking-shell模型进行了改进,即在富锂和贫锂的两种状态下存在 LiαFePO4和 Li1-βFePO4这两种相。Delmas等75结合高分辨透射电镜,提出了Domino-cascade模型,认为新相形核后,其生长速率将远远超过新相的形核速率,锂离子沿两相界面的脱嵌可以像多米诺骨牌一样瞬间完成,不需要借助外力。目前对于橄榄石结构正极材料的锂离子脱嵌机理还没有统一的认识,因此近几年对该体系锂离子传输机制的研究一直没有停下。Tang等76运用原位硬X射线波谱成像技术和相场模型揭示了锂离子的混合传输机制,并讲到这是由于表面反应和锂离子不同方向扩散的相互作用引起的。William等77用X射线显微成像技术揭示了锂离子电池在循环过程中电极内部颗粒成分和反应速率的纳米级变化过程。锂离子的脱嵌机制一直处于完成的过程中,同时LixFePO4体系中也有很多新的发现。Wang课题组78实时观察到锂离子在磷酸铁锂颗粒内部的不均匀插入行为,同时还发现了锂离子在颗粒内部分布情况的瞬间反转现象,并通过计算给出了解释。
3 磷酸铁锂界面结构与锂电池性能的关系
3.1 界面包覆
纳米化的 LiMnyFe1-yPO4并不能改变其较低的电子导电性(< 10-9S·cm-1),这也是限制其倍率性能的重要因素,解决上述问题的一种途径就是界面包覆导电层,例如导电与导离子介质包覆、离子导体包覆、惰性介质包覆等。当颗粒的导电性解决之后,影响材料电化学性能的决速步就变成了锂离子在颗粒和电解液界面的传输了。已有很多文献报道,界面传输对于材料的倍率性能起到了很大的作用79,80。
导电介质中常用的包覆物质有碳和导电聚合物,包覆处理之后可以改善颗粒之间的电接触,提高导电能力38。关于碳包覆层,它的物理特征对于最终的电化学性能有很大的影响,比如说碳层的含量和碳层厚度81、碳层的石墨化程度82、碳的形态和分布83、碳表面积和多孔性84以及碳前驱体的种类85,86等等。在碳包覆的过程中要考虑到上述因素,这样得到的包覆层会表现出很好的导电性。颗粒纳米化在缩短传输路径提高倍率性能的同时也会引起一系列的问题,例如低的振实密度导致低的能量密度87,大的比表面积可能会促进金属离子的溶解88,可能会增强催化副反应89等。面对上述问题,潘锋课题组90利用 LiFePO4界面Fe的对称性破缺(在体相中Fe是以FeO6八面体配位的对称性,但在界面少了最外层的O成为对称性破缺的FeO5的五面体),利用―CO-与界面对称性破缺的FeO5的Fe配位形成Fe―O―C,重构了FeO5(OC―)界面对称性的特殊碳包覆方式(该 C链接成有缺陷的氧化石墨烯,其外层的导电性好的多层类石墨烯),使得该界面因为Fe―O―C中O-提供的额外负电子可以多存储Li离子,实现了超过理论容量的电化学性能,该超容量的大小正比于纳米颗粒比表面积的大小。Sun等91也同样通过对 LiFePO4界面修饰实现了 LiFePO4超容量的结果。离子导体的相关研究也很多,它们在界面提高了磷酸铁锂材料的离子传输特性和界面稳定性。Li3PO4在表面的包覆也起到了非常好的效果,很大程度上提升了倍率性能37。特别是玻璃态的Li3PO4,其具备很高的离子电导率92。惰性介质包覆的种类有很多,基本的作用是稳定界面,进而提高电化学活性。例如惰性介质AlF3与LiFePO4有很好的适配性,不仅可以减少材料的转移阻抗,还可以提高电化学性能和表面结构稳定性93。
3.2 界面环境
Gaberscek等79证明LiFePO4电极材料周围的电解质离子和溶剂等环境因素要比导电性物质的包覆作用大,因为离子界面的传输速度很慢。也就是说在颗粒纳米化之后,倍率性能的决速步是界面反应而不是体相离子传输。电解液在电化学过程中扮演着重要角色,不仅仅体现在溶液中离子的传输,在界面溶剂化的Li离子要脱去溶剂实现Li离子脱嵌,因此脱溶剂化过程也是很重要的作用。目前用到的电解液主要是有机电解液和无机水系电解液,对与水系电解液的研究越来越多94,95,因为水电解质可以阻止燃烧具有高安全性的特点,是一种有可能代替有机电解液的电解液。吴宇平课题组96在硫酸锂水性电解液中对大孔磷酸铁锂电极进行了电化学测试,该电池体系实现了很高的能量密度。潘锋和吴宇平课题组合作5在有机无机两种电解液体系下测试了磷酸铁锂颗粒电化学特性,通过对比发现水系下的倍率性能(可以实现6秒钟实现50%以上的充放电)比有机体系下的性能好很多。他们通过理论计算对两种电解液环境下锂离子的脱嵌锂机制进行了研究,发现LiFePO4与水溶液接触后通过 H2O与界面Li的界面对称性破缺(界面的LiO3)重构了LiO3(H2O)3的八面体,形成了一层既像LiFePO4体相对称性又像溶液锂离子溶剂化(Li(H2O)4)的配位环境,称为 Janus水合固液界面,这将降低锂离子在界面处锂离子在界面的溶剂化和去溶剂化的能垒,从而的锂离子在充放电时的脱嵌能垒,有利于锂电池的快速充放电过程(图 5)。潘锋课题组97进一步开发 Li离子在固液界面的扩散性质的方法,例如开发了用脉冲法研究,发现充电时有颗粒之间互充电,以及开发了LiFePO4单纳米颗粒(把单个纳米颗粒分散在碳纳米管的导电网络中,消除纳米颗粒界面的相互作用引发颗粒之间互相充放电)锂电池电化学测试体系98,首次揭示了在锂电池材料在电解质中锂离子的扩散与界面反应的动力学方程(ka=Aexp(-Ea/kT),ka是速率常数,A是指前因子,Ea是活化能)的活化能与界面结构的相关性及指前因子和锂离子溶剂化和脱溶剂化的关系,并解释了水和有机这两类电解液环境下锂离子界面反应常数差异性的原因。上述工作系统的阐述了LiFePO4锂离子电池在水系电解液中倍率性能表现非常好的原因是形成的Janus水合固液界面使得Li离子脱溶剂化能低,这对我们制备高倍率锂离子电池有重要指导意义。
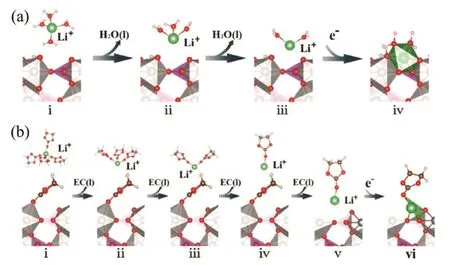
图5 (a)锂离子在磷酸铁和水界面的反应机理图,(b)锂离子在磷酸铁和EC界面的反应机理图5Fig. 5 Reaction profiles for Li+ transport across the(a) FePO4/water interface and (b) FePO4/EC interface in the discharge process 5.
4 磷酸铁锂电极结构与锂电池性能的关系
从电池设计和制造工程角度考虑,电极结构的设计与优化对电化学性能也有重要的影响,例如电极厚度、空间结构和多孔性等。最为熟知的提高倍率性能的方法是调节电极中活性材料、导电炭黑和粘结
剂的比例,当炭黑的比例增高时,倍率性能会有很大提升99,因为形成了更加健全的导电网络,降低了系统阻抗100,可缓解磷酸铁锂颗粒低电导率的问题,但同时也降低的电池的体积和重量的能量密度。当然,导电炭黑的物理特征对电化学性能的影响也比较大,潘锋课题组通过选择合适的导电炭黑,发现活性材料和“软”炭黑的大面积软接触,可以大大减弱了极化现象并提高了电化学性能101。
关于电极厚度与电池性能关系的研究非常多。Zhang等102制备了不同物质载量LiFePO4,研究了电极厚度和倍率性能的关系,发现电极越厚倍率性能越差,同时其功率密度也随之降低。Denis等103发现LiFePO4的电极厚度增加会增加电极阻抗和降低锂离子在电解液中的传导速率,影响倍率性能。有机电解液本身具有安全隐患,所以使用水系电解液的研究非常多,这样即解决安全问题,同时降低了成本。Guyomard等104在水系电解液体系中研究了电极厚度对电化学性能的影响,并寻找了水系电解液中实现高能量密度的方法。
为提高能量密度而增加电极厚度,一般来讲这不利于锂电池实现高倍率性能,但也有解决矛盾的办法,不仅可以增加厚度提高能量密度也可以表现出不错的电化学性能。Seznec等105使用NaCl作为模板,制造了非常厚的LiFePO4多孔电极,增大了电解液和电极的接触面积,促进了锂离子的传输,不仅提高了能量密度,同时也实现了很好的电化学性能。Chen等106通过使用不同规格的尿素甲醛树脂作为模板,得到了毫米级的三维多孔 LiFePO4电极,实现了优越的倍率性能和更高的能量密度。潘锋课题组107通过3D打印的方法实现了LiMn0.21Fe0.79PO4@C超高的倍率性能,不仅研究了厚度对倍率性能的影响,同时通过多物理场模拟的方法探究了孔隙率对磷酸铁锰锂电极倍率性能的影响,提出通过设计具有大的“有效孔空隙率”的电极可以大大提高电池的高倍率充放电的性能。Lestriez等108通过喷墨打印的方法制备了薄且多孔的电极,实现了非常好的倍率性能。Lewis等109通过3D打印的方法组装了微电池,在内部为正负极互插式3D结构,充分利用了空间,同时也得到了不错的功率密度。
5 结论
我国对新能源汽车的政策支持为动力锂电池的未来发展营造了非常好的氛围,这也对磷酸铁锂正极材料产业的快速发展起到了促进作用。磷酸铁锂正极材料的高安全性、高循环稳定性以及无污染等优势,使之成为动力电池的首选材料已经无需置疑,如何进一步提高锂电池的能量密度、功率密度是扩大其应用范围的必经之路,产业界和学术界应该以之为奋斗目标进行深刻探讨。
本文对影响锂离子电池磷酸铁锂正极材料电化学性能的因素进行了总结,从颗粒体相特征(相结构、掺杂、纳米化、缺陷和锂离子传输机制)出发,拓展到颗粒界面环境研究,最后到电池电极结构的设计,进行了系统化的分析,为我们设计高倍率锂离子电池提供了参考。如果想要实现高的能量密度和功率密度,应该如何设计材料、如何选取电解液、如何设计电极,本文为我们提供了重要参考。
材料设计方面,我们可以在界面进行对称性破缺的重构,使得界面储存额外更多的Li离子。纳米材料颗粒的尺度越小,表面积越大,额外储Li超容量就越大,可以把这个机理应用于改良现有磷酸铁锂材料,以提升其容量。
电解液选取和改良方面,从水系电解液能实现超快速充放的机理得到启发,电池充放电的倍率性能与锂离子脱溶剂化的过程和固液界面结构有紧密的关系,电极材料在界面对称性会产生破缺,电解液溶剂要补上这个缺位,一般是通过溶剂的极性基团与界面的过渡金属配位并与Li离子结合,像H2O这种体积小的分子还能在磷酸铁锂界面的 Fe配位,并与Li离子结合形成既像晶体中Li-O八面体又像溶剂化的Li-O四面体的Janus界面,使得Li离子的界面溶剂化/脱溶剂化都变得容易,进而实现快速的界面动力学。因此,电解液中添加不同功能和大小的溶剂分子重构界面,可以提高Li离子脱嵌速率和界面的稳定性。这不仅可以提高功率密度,而且可以保证电池的安全性。
电极结构设计方面,如何设计电池电极结构能同时提高电池的能量密度和功率(正比于倍率)密度是一个巨大的挑战,我们知道通常要提高电池单位体积的能量密度就要把电极的极片要压得密实并且极片要做的很厚,这样就会引起严重的浓差极化,导致Li离子从电解液到电极材料内部的脱嵌速率降低。从3D打印极片研究影响电池倍率性能的机理可以得到启发,设计增加“有效孔隙率”的电极是一个有效的途径,可以在三维结构上进行努力,建立快速离子传输的通道,在保证能量密度不损失的情况下实现电极材料和电解液的最大接触。
除此之外,要提高磷酸铁锂材料性能并应用于电动车动力电池,同时需要兼顾材料的合成流程、电池组的设计以及对电极的选择等,这些对最终的能量密度和功率密度性能表现都有非常大的影响,想要实现大幅度的性能提升,还需要进一步深入地研究机理,优化影响电池性能的各个部分。

