沙美特罗氟替卡松对抗COPD患者线粒体氧化磷酸化功能障碍的研究
,
(焦作煤业集团有限责任公司中央医院呼吸科,河南焦作 454000)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)属于一种渐进性、慢性呼吸系统疾病,同时它也是一种机体多脏器多系统的慢性炎症性疾病。COPD全球倡议(GOLD)2006年首次提出COPD具有明显的肺部病变特征的同时还存在典型的肺外表现,其中骨骼肌的功能障碍就属于其中一种。有研究人员证实COPD患者骨骼肌的氧化代谢能力明显下降,其中表现最为突出的线粒体的功能明显障碍。明前尚未有明确的病因学对此过程进行解释,但是有文献指出,肿瘤坏死因子((Tumor Necrosis Factor α,TNF-α)在COPD患者体内具有高表达,TNF-α作为一种重要的炎症因子,可以改变骨骼肌细胞糖代谢,使细胞内pH降低,影响细胞的氧化代谢能力,甚至导致细胞死亡。因此我们认为如果某种干预手段可以对抗TNF-α的高表达,那么将有可能改善COPD患者骨骼肌的氧化代谢能力,从而提高患者骨骼肌的耐力。
沙美特罗氟替卡松是目前临床对中重度COPD稳定期的推荐用药,更有文献报道沙美特罗氟替卡松可通过作用于多靶位多通路对COPD患者发挥抗炎、扩张气管的效应,但尚未有资料对沙美特罗氟替卡松对COPD患者线粒体氧化磷酸化功能障碍的影响进行报道,本研究以COPD患者为研究对象,探讨沙美特罗氟替卡松能否通过对抗TNF-α从而上调线粒体氧化磷酸化功能,并对机制进行研究。
1 对象与方法
1.1对象 将本院2010年4月至2013年8月100例COPD稳定期患者纳入本研究并进行为期1.5年的随访,所有入组患者诊断均符合2010年中华医学会呼吸病学分会修订的COPD诊治指南[1],其中男性52例,女性48例,年龄54~73岁,平均(58.4±2.9)岁。随访结束后其中坚持使用沙美特罗氟替卡松的44例设为观察组,其中男性24例,女性20例,年龄54~72岁,平均(57.6±3.1)岁;余下56例设为对照组,男性28例,女性28例,年龄55~74岁,平均(57.9±3.3)岁;将同期健康体检的50例设为健康组,男性27岁,女性23例,年龄50~72岁,平均(57.7±4.2)岁。三组在年龄、性别等一般情况比较无统计学差异(P>0.05),具有可比性。本研究方案经过医院伦理学委员会审查批准。
1.2排除标准[2](1)合并严重心脑肾等重大脏器病变、肿瘤或重症感染者;(2)入组前3个月接受糖皮质激素药物治疗者;(3)合并自身免疫性疾病者;(4)不予签署知情同意书者。
1.3治疗方法 两组患者均行平喘、止咳、祛痰、补液、吸氧等常规治疗。在常规治疗基础上,COPD患者给予沙美特罗氟替卡松(注册证号:H20120015,进口药品:法国Laboratoire GlaxoSmithKline)吸入,1喷/次,2次/d。
1.4检测方法
1.4.1肺功能检测 采用便携式肺功能仪(AS-505型,日本美能公司)于治疗前后行肺功能检测,令患者配合操作者口令,以最大可能吸气,然后以最大力量、最快速度呼出,注意夹住患者鼻子,嘱患者含紧口嘴,避免测试过程中漏气,以此获得FEV1 %预计值。
1.4.2主要试剂 RPMI 1640和胎牛血清(美国Thermo公司);人淋巴细胞分离液 (天津市灏洋生物制品科技有限责任公司);Western Blot实验单克隆抗体和二抗(上海达为科生物科技有限公司);透射电镜检测电子显微镜(日本,JEM-2100);Reverse transcriptase first stand cDNA synthesis(Takara,Japan);Trizol试剂、TaqDNA聚合酶(Promega公司)。
1.4.3单核细胞的提取 取健康组、对照组及观察组治疗前后前臂外周抗凝血5 mL,用人淋巴细胞分离液提取外周血单核细胞(PBMC,1×106/ml)200 μL,置于含10 %胎牛血清的RPMI 1640培养基中进行培养。
1.4.4透射显微镜检测 用于单核细胞细胞受沙美特罗氟替卡松作用前后线粒体的变化。将细胞用胰酶消化后收集于1 mL EP内,然后采用1 mL透视电镜专用戊二醛固定2 h后,按照常规电镜标本处理途径——脱水、浸润、包埋和切片。最后由专业操作者使用透射电子显微镜观察线粒体改变。
1.4.4Western Blot 收集适量经消化重悬的单核细胞于1 mL EP管后,用PBS洗涤2遍;然后加入细胞裂解液,充分裂解后置于4 ℃ 12 000 r/min离心机离心10 min;取上清液获取总蛋白,考马斯亮蓝法测定蛋白浓度;进行SDS-PAGE电泳分离蛋白后转印到硝酸纤维膜上,封闭后加入相应的单抗轻摇孵育1.5 h,用PBS洗涤膜条3次;接着加入HRP-二抗,置于室温轻摇1 h后取出再用PBS洗涤3次;最后进行曝光、显影、定影、拍照和统计分析。
2 结果
2.1沙美特罗氟替卡松能提高COPD患者肺功能 治疗前两组患者肺功能检查结果显示两组无差异(P>0.05),随访结束时患者再次接受肺功能检查,观察组与对照组FEV1在治疗后均有所下降,治疗后观察组FEV1下降程度较对照组要多,且差异均具有统计学意义(P<0.05);观察组与对照组FEV1/FVC(FEV1 %)在治疗后均有所下降,治疗后观察组FEV1/FVC(FEV1 %)下降程度较对照组多,且差异均具有统计学意义(P<0.05)。见表1。
2.2沙美特罗氟替卡松能显著抑制COPD患者外周血TNF-α的表达 对不同组别外周血TNF-α进行ELISA检测,结果显示100例COPD患者入院治疗前TNF-α浓度均高于健康组,经过治疗后虽然COPD患者TNF-α有所下降,但是其中观察组下降的趋势大于对照组,见图1。

表1 两组治疗前后肺功能情况比较
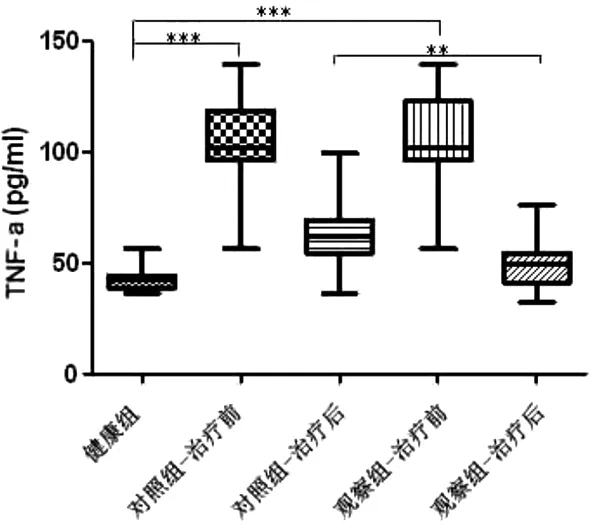
图1 各组外周血TNF-α的表达变化
2.3沙美特罗氟替卡松提高了COPD患者单核细胞线粒体氧化磷酸化复合体的表达 线粒体氧化磷酸化酶复合体Ⅰ、Ⅱ、Ⅲ是细胞线粒体功能的重要指标,通过western blot检测COPD患者治疗前单核三个复合体Ⅰ、Ⅱ、Ⅲ都有不同程度的浓度下调,经过沙美特罗氟替卡松治疗后复合体表达虽均有所提升,但浓度仍小于健康组,其中观察组浓度上调的较明显。
2.4沙美特罗氟替卡松能改善人单核细胞超微结构 健康对照组细胞结构基本正常,细胞膜结构清晰、完整,细胞核圆而饱满,细胞核膜完整,未见受损征象,常染色质均匀分布,可见各类完整的细胞器。对照组治疗后细胞结构仍存在被明显破坏,空泡样病变明显增多,部分细胞膜破裂,细胞器溶解后分辨不清,染色质流失,可见线粒体肿胀,粗面内质网减少。观察组治疗后受损情况较对照组明显好转,可见完整的细胞膜及细胞核,核膜完整,线粒体空泡病变明显减轻,粗面内质网部分扩张。
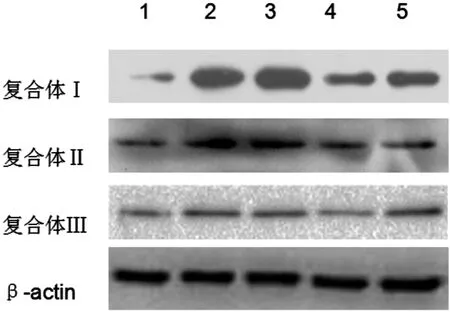
图2 各组单核细胞线粒体氧化磷酸化复合体的表达
注:Western blot法检测各组复合体Ⅰ、Ⅱ、Ⅲ的表达水平;β-actin可视为内部参照;“1”表示健康组;“2”表示观察组治疗前;“3”表示对照组治疗前;“4”表示观察组治疗后;“5”表示对照组治疗后。
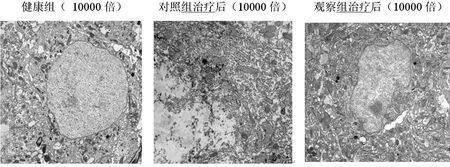
图3 各组单核细胞超微结构变化
3 讨论
COPD是一种可引起机体多脏器慢性炎症的呼吸系统疾病,全身骨骼肌在长期炎症效应影响下,其氧化表型可出现明显的退化与缺失,最终引起COPD患者骨骼肌耐力下降,运动功能减退。目前多数研究COPD药物对其的影响研究多停留在动物实验或者单纯临床疗效观察,临床分子生物学层面的报道并不多[3-5],本课题将COPD患者的外周单核细胞做为研究对象,对沙美特罗氟替卡松对COPD患者发挥抗炎机制进行研究。结果发现COPD患者外周血TNF-α的表达明显上调,TNF-α[6]是一种多功能的促炎因子,它能够诱导线粒体的损伤和破坏,同时抑制线粒体复合物的活性。线粒体是机体能量供应的主要场所,当线粒体形态和功能受到破坏时,各类细胞将失去能量供应来源而无法维持正常形态结构甚至死亡。本研究中COPD患者外周单核细胞形态结构的确出现明显的破坏效应,包括电镜下观察到线粒体退化和固缩,且这一过程伴随着TNF-α浓度的增加,这说明TNF-α浓度的增加可能是引起COPD患者外周血单核细胞线粒体破坏的主要原因。
沙美特罗氟替卡松属于长效β受体激动剂,能对细胞膜上的β受体产生特异性结合,激活细胞内腺苷酸环化酶(AC),激活其下游的环磷酸腺苷cAMP活性,同时激活鸟苷酸环化酶,使支气管平滑肌细胞内环磷酸鸟苷(CGMP)的含量减少,CAMP/CGMP比值上升而致支气管扩张。另一方面,沙美特罗可将机体无活性的GR(糖皮质激素受体)激活,增强了GR与糖皮质激素的结合能力,上调其抗炎能力。故其具有明显消炎、降低气道高反应的作用[7-8]。从动物实验研究结果[9]中我们了解到沙美特罗氟替卡松可以通过影响机体多个靶位和信号通路而产生多种生物效应。所以本研究尝试探讨沙美特罗氟替卡松对COPD患者的影响机制,结果发现沙美特罗氟替卡松在明显提高COPD患者肺功能的同时还可以在修复COPD患者外周单核细胞结构方面发挥重要作用,且降低了患者TNF-α的浓度,避免了机体线粒体遭受TNF-α的“攻击”而维持形态学和结构学的完整。
综上所述,随着COPD患者体内TNF-α水平的升高,患者外周单核细胞形态受到明显破坏,而沙美特罗氟替卡松可明显纠正这一过程,因此我们认为沙美特罗氟替卡松保护了COPD患者的线粒体,运用此药预防和减轻COPD病人骨骼肌功能障碍并提高患者生存质量是科学可行的。

