术前穿刺置管冲洗引流联合手术治疗复发性脊柱结核的效果分析
刘思源 窦吉辰 饶涛 赵衡 高康 周奕 李锦峰 郑刚 寸新华
作者单位:650041 昆明市第三人民医院骨科
脊柱结核是最常见的肺外结核之一,若未行有效治疗,极易引起椎体破坏,导致后凸畸形和脊柱不稳,致残率很高。随着外科技术的进步,通过病灶清除术联合化学治疗脊柱结核,取得了较好的临床疗效。但一些综合医院对结核病认识不足,以及不规范的化疗、清创不彻底、术后制动不严格、手术策略不适当等原因[1],以及耐药菌的出现,导致时有脊柱结核术后复发的病例报道。脊柱结核复发,常伴有内固定失效、脊柱不稳,严重威胁到患者的脊髓神经安全;此外,顽固性皮肤窦道形成会导致混合感染,因此脊柱结核复发的治疗风险高、难度大,无论化疗方案的制定还是手术方式的选择都面临很多困难[2-3]。昆明市第三人民医院骨科对术前穿刺置管冲洗引流联合手术治疗复发脊柱性结核患者的效果进行了分析,为临床治疗复发性脊柱结核提供安全有效的治疗方案和经验。
资料和方法
一、资料收集
1. 研究对象:回顾性分析2015年1月至2017年12月在昆明市第三人民医院骨科接受外科治疗的20例脊柱结核复发患者。其中,外院手术后复发到我院接受治疗的患者14例;男8例,女12例;年龄25~70岁,平均(45.6±2.5)岁;复发时间6~42个月,平均(13.5±5.7)个月。
2. 临床资料:全部患者均经影像学及实验室检查等证实为脊柱结核。20例患者中,腰椎结核10例,胸椎结核5例,胸腰段结核4例,腰骶段结核1例;并发肺结核5例,并发胸腹腔结核3例,并发糖尿病1例;耐药结核病患者5例,其中耐多药结核病患者2例;切口下存在脓肿性包块6例,窦道形成7例,椎旁及腰大肌脓肿18例,内固定松动失效4例。所有患者均得到良好随访,平均随访时间(1.9±0.8)年。见表1。
二、脊柱结核治愈及复发标准
1.治愈标准[4]:(1)结核感染中毒症状,病椎疼痛消失时间超过6个月;(2)血红细胞沉降率(ESR)和C反应蛋白(CRP)持续正常(ESR<40 mm/1 h,CRP<10 mg/L)时间超过6个月;(3)CT检查显示椎间植骨融合时间超过6个月;(4)抗结核药物治疗结束12个月后结核病灶无复发。
2.复发标准:治疗后全身及局部症状明显缓解,病灶一度消失,但在初次手术后≥6个月时出现局限性包块、冷脓肿积聚或窦道形成,植骨块吸收或破坏。
3.穿刺置管引流的标准:脊柱结核复发患者经影像学评估需行手术干预的患者;入院时年龄大、营养状况差、基础疾病多者;伴有脓肿形成者,怀疑耐药菌株感染的可能。
三、治疗方法
1. 围手术期的处理:所有患者均在诊断明确后在CT引导下行病灶处的穿刺置管引流,每日采用1000~1500 ml生理盐水进行冲洗,并加强营养支持治疗,纠正贫血、低蛋白血症,行规范的抗结核药物治疗,所有脊柱结核复发患者术前
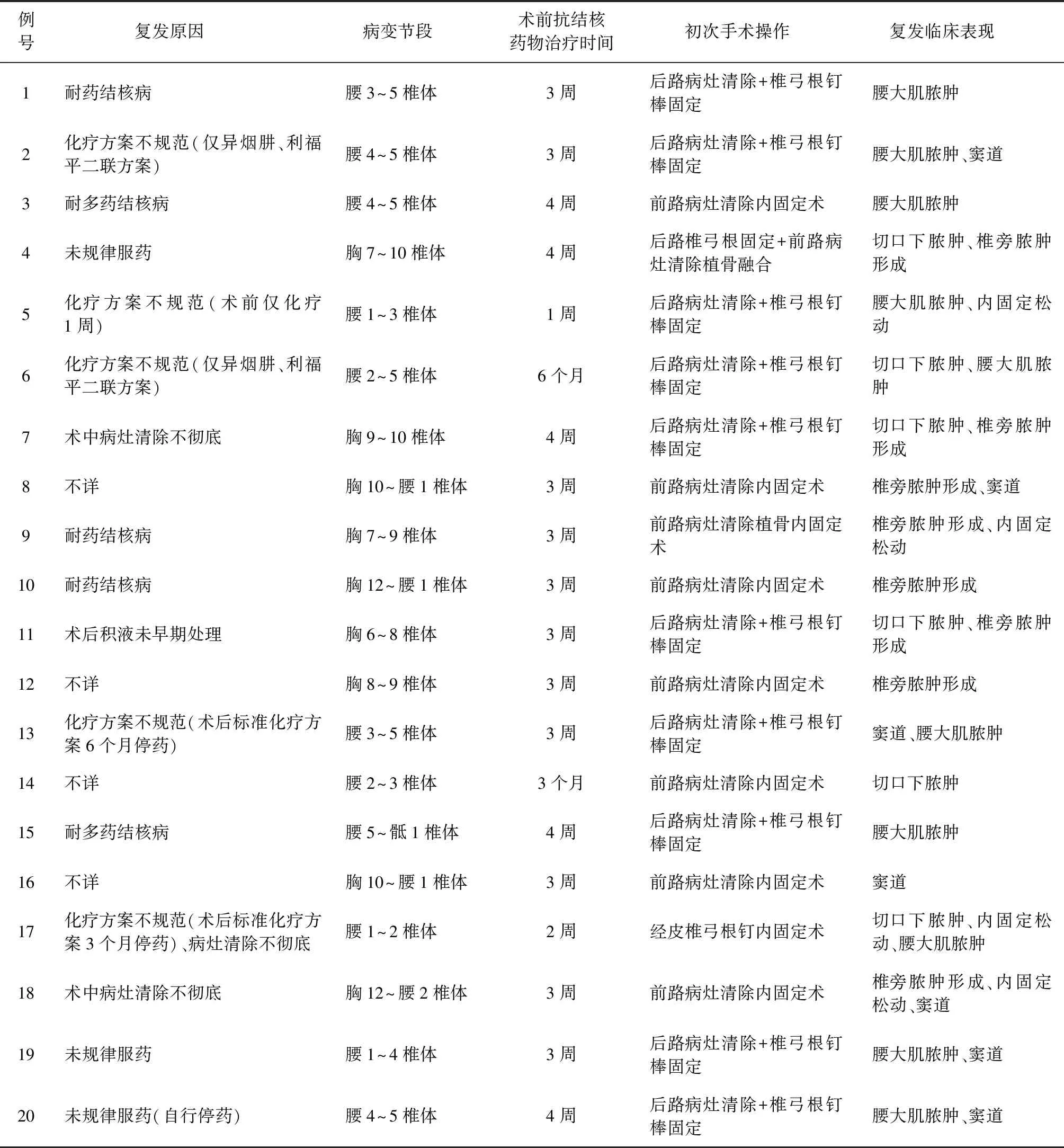
表1 本组脊柱结核复发患者的具体信息
均给予抗结核药物治疗(主要包括异烟肼、链霉素、利福平、吡嗪酰胺、乙氨丁醇),并根据穿刺引流出的标本做结核分枝杆菌培养及药物敏感性试验(简称“药敏试验”),根据试验结果调整或加用二线抗结核药物[5]治疗2~4周;2例患者经穿刺引流液行GeneXpert MTB/RIF检测及培养证实为耐多药结核病,给予环丝氨酸、左氧氟沙星或莫西沙星、阿米卡星、吡嗪酰胺、乙氨丁醇治疗;有窦道的患者行窦道内分泌物多次培养(均为阴性)。待体温恢复正常,血清白蛋白>35 g/L,血红细胞沉降率<40 mm/1 h,CRP下降后行手术治疗,于手术前1~2 d拔出穿刺引流管,平均带管时间(17.2±3.7) d。术后在常规外支具保护下1~4周后可离床下地活动,并继续行抗结核药物治疗。

图1 患者在CT引导下穿刺,大量脓液被吸出 图2 患者CT扫描图片,显示置管于椎旁脓肿处 图3~8 例1,男,30岁。在外院行后路椎弓根钉棒内固定,前路病灶清除髂骨支撑植骨,术后6个月,以切口下脓肿形成来我院就诊。图3~6为患者入院时脊柱X线正侧位和CT冠状面、矢状面图片,显示患者病椎破坏严重,植入髂骨吸收,且CT扫描显示椎旁脓肿形成。图7为患者置管冲洗后,手术切除病椎,放置钛笼。图8为患者随访6个月时CT复查,显示钛笼位置良好,植骨融合良好
2. CT引导下穿刺置管引流:取侧卧位或俯卧位。常规消毒铺单,CT薄层扫描根据核心病灶及脓肿所处的最佳引流位置确定具体进针点,若核心病灶与脓肿最佳引流位置相隔较远,则分别进行多部位穿刺。在体表皮肤做好标记,同时测量确定进针深度。采用2%利多卡因局部麻醉后,切开穿刺点皮肤0.3 cm左右的切口,先经皮用同轴套管针穿刺病灶处,可多次扫描确定穿刺针深度即时修正穿刺角度,确定穿刺位置理想后,置入导丝,在导丝引导下放入双腔引流管,抽出导丝,用注射器抽取脓液,行脓液GeneXpert MTB/RIF检测和结核分枝杆菌培养+药敏试验,再次行CT扫描确认位置后,于皮肤上固定好引流管,接好引流袋(图1,2)。
3. 手术方法:均采用全身麻醉,根据初次手术入路,进行手术规划,病灶清除取前路前外侧切口,逐层分离至病灶处,吸引器吸尽脓液后,用刮匙和骨刀等将死骨、炎性肉芽组织等切除,椎体间用钛笼椎间融合器填充自体肋骨或髂骨颗粒,并根据药敏试验结果混合链霉素2 g、注射用利福平0.45 g或左氧氟沙星0.4 g,重建前柱稳定性。若有内固定松动,更换内固定,延长固定范围。最后用过氧化氢、淡碘伏及生理盐水反复冲洗创面,并止血。于病灶处放置引流管后,逐层关闭切口。手术原则:若脊柱稳定性未发生明显改变,仅行病灶清除或窦道切除术;若发现明显不稳定,则行病灶清除+植骨融合内固定术。
四、记录及观察指标
记录患者性别、年龄、疼痛程度、神经功能、手术时间、术后再次复发情况、血红细胞沉降率、骨融合时间。于术后1、3、6、12个月复查血常规、肝肾功能、血红细胞沉降率,以及进行X线摄影、CT平扫加矢状面和冠状面二维重建、MR扫描等检查。
神经功能评级:采用Frankel脊髓损伤分级法[6]。疼痛程度评分:采用视觉模拟评分(VAS)方法记录术前、术后及末次随访疼痛程度,以0~10分记录,评分越高表明疼痛越剧烈[7]。
结 果
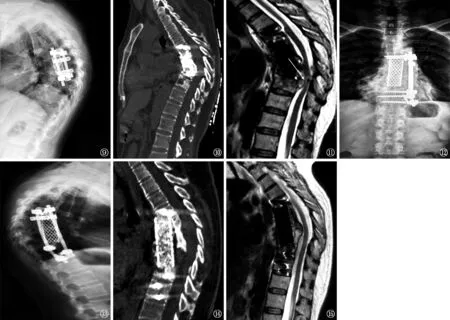
图9~15 女,43岁。因“胸椎结核术后7年,胸背部疼痛并双下肢不能活动超过2个月”来我院就诊。Frankel分级为C级。图9,10为患者术前X线和CT检查图片,显示后凸畸形,局部Cobb角约70°,未见内固定松动、断裂。图11为患者MRI图片,示脊髓受压严重,脊髓信号改变。图12,13为患者术后X线复查,显示内固定稳定,位置良好,脊柱后凸改善,Cobb角约52°,矫正率为26%。图14为患者术后4个月时CT复查,显示植骨融合良好。图15为患者术后4个月时MRI复查,显示脊髓无受压,脊髓信号恢复正常;患者Frankel神经功能恢复为E级
本研究中20例患者均顺利完成手术,平均手术时间(154.6±32.7) min。所有患者均获得有效随访,平均随访时间(12.0±3.6)个月。术前3例患者Frankel脊髓损伤分级为C级,2例为D级,末次随访时均恢复至E级。植骨融合时间平均(5.9±1.2)个月。穿刺置管引流术前患者VAS得分为(7.52±1.09)分,置管引流术后降低至(3.11±0.28)分,二次手术升高至(4.32±0.79)分。所有患者术后及随访过程中均未出现内置物松动、断裂等情况(附2例典型患者。例1:图3~8;例2:图9~15)。所有患者均未发现逆行性感染、窦道,均一期愈合。5例患者术前培养出耐药结核分枝杆菌(其中2例为耐多药结核分枝杆菌),根据药敏试验结果调整为二线抗结核药物进行治疗(停用检测为耐药的药物,可供选择的更换药物为左氧氟沙星、阿米卡星、丙硫异烟胺),随访过程中均未发现再次复发情况。
讨 论
脊柱结核为最常见的肺外结核,约占骨关节结核的50%。由于对脊柱结核认识的不深入,病灶清除的不彻底;不合理及不规范的抗结核化疗和手术方式选择不能有效抑制和(或)清除骨病灶内的结核分枝杆菌;以及部分患者存在营养状态差、自身免疫功能低下等原因,导致结核具有难治性和复发性[1]。Lan等[8]报道脊柱结核复发率为1.28%~25%。脊柱结核复发往往起病隐匿,常常在内固定和植骨区有明显的脓肿形成,表现为脊柱畸形、内固定失效、脊柱不稳,甚至伴有脊髓受压。因此,在使用抗结核药物治疗的同时,手术干预必不可少。结核是慢性消耗性疾病,复发脊柱结核患者术前常表现为对治疗缺乏信心、营养状况差、围手术期并发症多、骨质条件不好,甚至并发巨大脓肿,故制定良好的治疗策略,增强患者治疗的信心十分重要。
一、脊柱结核复发的治疗难点
复发患者由于既往至少经历了一次手术,身心均遭受过重大创伤,其治疗难度较初治脊柱结核更大、风险更高。脊柱结核复发的主要原因是治疗不规范,长时间不规范化疗导致耐药菌株的产生,甚至产生多耐药结核病、全耐药结核病[9-12]。耐药结核病、耐多药结核病和广泛耐药结核病成为困扰脊柱外科医生的重大难题[4]。本组患者中,5例(25.0%)术前诊断为耐药结核分枝杆菌感染,其中2例为耐多药结核分枝杆菌感染。然而,这一问题尚未得到部分脊柱外科医生的重视,尤其对于综合性医院。
此外,复发患者伴有手术区域组织解剖结构重建,严重的组织粘连,骨质破坏严重,病变范围较初次治疗前进一步扩大,原有内固定失效等情况。同时,脊柱结核作为一种慢性高消耗性疾病,营养状况不理想,对于围手术期患者的预后可能产生严重的不良影响[13]。此外,此类患者对于再次手术治疗往往存在心理畏惧,并对再次治疗的临床效果存在怀疑。因此,对于脊柱外科医生而言,脊柱结核复发的治疗是一个巨大的挑战。
二、术前穿刺置管引流的必要性
CT引导下穿刺置管引流治疗脊柱结核已经成功运用多年,是一项成熟的技术。对于复发的脊柱结核患者而言,笔者认为术前穿刺可获取标本做结核分枝杆菌药敏试验,指导个体化用药,保证手术成功率和治疗效果。李力韬等[9]已指出早期诊断对治愈耐多药脊柱结核、预防继发性耐药非常关键。本组患者中通过术前穿刺成功诊断出耐药性脊柱结核5例,其中2例为耐多药脊柱结核。并且,该微创治疗方式的禁忌证少,对椎体病灶或脓腔实行精确定位,手术安全性高。我科通过置管引流治疗脊柱结核累计患者已超过150例,最高置管于颈1椎体水平,尚未观察到严重并发症。同时由于局部置管引流后脓腔内压力降低,减轻了对周围神经组织的压迫,周围神经组织水肿减轻,且由于引流局部毒性物质浓度降低使炎症介质释放减少,从而减轻了局部疼痛等不适症状;局部血液循环改善,局部组织细胞水肿减轻,有利于提升药物在病灶周围的渗透能力,使局部的药物浓度进一步提高。组织水肿减轻导致局部细胞活力增强,从而也使局部组织的抗感染能力提升;引流使病变范围局限,减少受累椎体的数量。本组患者穿刺前VAS评分为(7.52±1.09)分,穿刺后降低至(3.11±0.28)分,VAS评分明显降低。
患者全身中毒症状及局部症状的减轻,有助于缓解患者的应激状态,随着自觉症状、进食能力、睡眠及自身心理焦虑等状态的改善,患者将更加有信心康复,并能更好地应对再次手术的创伤打击。
三、手术补充的必要性
对于脊柱结核的治疗,目前公认的原则是:(1)规范化的抗结核药物治疗必须早期、联合、足量、规律、全程[14];(2)彻底进行病灶清除,包括脓液、死骨、窦道、干酪样物质、结核肉芽组织和坏死椎间盘组织。国内一些学者报道通过经皮穿刺置管引流联合局部化疗冲洗治疗脊柱结核取得了很好的临床疗效[15-16]。但脊柱结核微创手术治疗也存在局限性,对严重的脊柱畸形及存在明显的脊髓压迫患者并不适用[16]。另外,笔者在应用该方法治疗脊柱结核过程中发现,很多患者坏死组织过于稠厚,置管冲洗无法将坏死组织引出;另外,对于有死骨形成、巨大脓腔形成的患者,单纯置管引流冲洗(局部化疗药物灌注或不灌注)治疗效果均有限,且由于置管后无法在家中实行护理,住院时间明显延长。目前,国内外学者主张对有适应证的脊柱结核患者均采取积极的外科治疗[17-18],在有效应用抗结核药物治疗的基础上采取彻底清除病灶和植骨消灭死腔,通过加强内固定矫正畸形,重建脊柱稳定性,促进局部结核病灶的控制和骨性愈合,可达到结核病灶静止+修复的目的。而复发性脊柱结核患者属于特殊的一类患者,其生理、心理均无法再次承受过大、过长时间及反复多次的治疗方式。因此,笔者认为,对于无绝对手术禁忌的复发性脊柱结核患者,均应行手术治疗。另外,脊柱前路手术对于病灶清理更为彻底,且已成为了治疗脊柱结核的经典术式[19],本组患者病灶清除均选择了前路,随访过程中尚未发现有结核病灶再次复发的情况。因此,对于复发性脊柱结核患者,在医师技术允许的条件下,手术翻修入路应该尽量选择前路。
四、本研究的局限性
本研究为根据临床治疗效果进行的描述性分析,由于样本量较少,故未行详尽的统计学分析。本组患者例数较少,还需要继续扩大样本量或进行多中心对照研究。由于耐药结核病患者抗结核药物治疗的时间长,本研究需要进一步对患者进行随访,同时对于置管指征、置管时间、不同手术入路应做进一步探讨。
综上所述,脊柱结核复发患者的治疗难度大、风险高。CT引导术前穿刺置管引流能获取脊柱结核复发患者的药敏试验结果,指导调整化疗方案,保证手术治疗效果;同时能迅速减轻患者疼痛症状,提升患者治疗信心,是对于开放手术治疗的有益补充。因此,术前置管引流冲洗联合开放手术治疗复发性脊柱结核是一种可供选择的治疗方法。

