纳米Al2O3分离富集环境样品中的铅
黄婷,米竟,梁媛媛,薛盼
(1.安康学院 化学化工学院,陕西安康 725000;2.陕西省富硒食品质量监督检验中心,陕西安康 725000)
目前已经发现了很多分离富集铅的吸附剂,如柚子皮生物吸附剂[1]、黑曲霉-稻草秸秆复合吸附剂[2]、聚乙烯亚胺杂化硅胶吸附剂[3]、大蒜茎叶生物吸附剂[4]、污泥基吸附剂[5]、MnO2/Fe3O4复合吸附剂[6]等。纳米粒子非常小,有很大的比表面积,所以纳米材料能够在表面吸附很多的物质,具有很强的吸附性。本文采用ICP-AES测量铅,研究纳米氧化铝的吸附性能,试图建立一种分离富集铅的新方法,该方法必须具有简便、效率高、无污染、成本低、吸附剂易再生等优点。确定了最佳吸附条件,在最佳吸附条件下将其应用环境水样中痕量铅的分离富集。
1 实验部分
1.1 仪器设备及工作条件
ICP-AES(Plasma1000型,钢研纳克);ICP发生器,频率40 MHz;等离子体焰炬观察高度为工作线圈以上15 mm;氩载气流量0.5 L/min,氩冷却气流量12 L/min,氩工作气体流量1.0 L/min,试液提升量2.6 mL/min;积分时间短波10 s,长波5 s,积分次数3次;铅的测定波长220.35 nm。
1.2 试剂及标准溶液
铅标准溶液(1.000g/L):称取0.399 6 g Pb(NO3)2溶解后,定容于100 mL容量瓶中,摇匀,备用。
纳米Al2O3(γ型,10 nm),由陕西中科纳米有限公司提供。其他试剂均购于天津化学试剂厂,用水为三重蒸馏水。
1.3 实验方法
1.3.1 吸附-解吸
取一定量的铅标准溶液,调节到最佳pH,加入一定量的纳米Al2O3,摇匀,静置15 min,离心(1 500 r/min),15 min后,移取上层清液2.00 mL,用ICP-AES测定,计算铅的含量和吸附率。
将吸附后的纳米Al2O3用三重蒸馏水洗至中性,干燥,加入洗脱剂0.01 mol/L NaOH 5.0 mL,摇匀,静置10 min后离心,取上层清液2.00 mL,用ICP-AES测定铅的浓度,计算回收率。
1.3.2 水样的处理
采集汉江水和实验室自来水为样品,用纤维素滤膜(孔径0.45 μm)过滤,将一定浓度的铅标准液加入到水样品中,调至最佳pH备用。
2 结果与讨论
2.1 酸度的影响
pH对纳米材料吸附铅有重要的影响,由于纳米材料在水溶液中表面羟基化作用,这些表面羟基将因溶液pH值的不同而发生质子化或去质子化,在pH值较高时,纳米材料表面带有负电荷易于吸附阳离子,随着pH值的降低,纳米材料表面逐渐变为中性,最后带正电荷易于吸附阴离子。实验考察了不同酸度条件下,纳米Al2O3对Pb(Ⅱ)吸附率的影响,如图1所示。随着pH值的增大,Pb(Ⅱ)的吸附率先增大后减小。实验结果表明,在室温下pH=6时吸附效果最佳,所以本文选择pH=6作为最佳吸附酸度,纳米Al2O3的吸附率达到92.03%。
2.2 吸附等温线和吸附容量
考察了不同温度下纳米Al2O3去除Pb(Ⅱ)的吸附等温线(见图2),由图3可以看出在4种温度下,热力学实验数据与Freundlich等温吸附模型有较好的拟合(R≥0.97),表明纳米Al2O3对Pb(Ⅱ)的吸附符合Freundlich模型,为多分子层的吸附。最佳的吸附条件下,在0 ℃、20 ℃、40 ℃和60 ℃下测得纳米Al2O3对Pb(Ⅱ)的饱和吸附容量分别为2.31 mg/g、2.70 mg/g、2.93 mg/g和3.32 mg/g。

图1 溶液pH对纳米Al2O3吸附Pb(Ⅱ)的影响
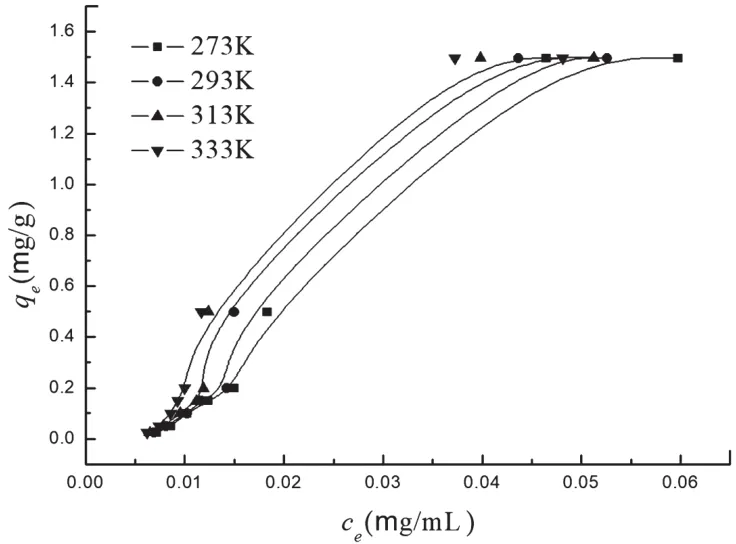
图2 纳米Al2O3对Pb(Ⅱ)离子的吸附等温线
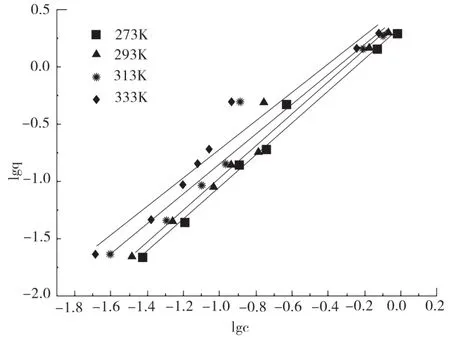
图3 不同温度下的Freundich吸附等温线
2.3 洗脱方法的试验
根据试验2.1,溶液pH值对Pb(Ⅱ)离子吸附影响分析,从图1可以看出,在较高或者较低pH值时纳米Al2O3吸附Pb(Ⅱ)离子的吸附率很低,因此采用一定浓度碱或酸将吸附的Pb(Ⅱ)离子洗脱下来,结果发现,当溶液中加入5.0mL 0.01 mol/L NaOH时,回收率达到95.34%,可将吸附的Pb(Ⅱ)离子基本洗脱。
2.4 水样品的分析
用汉江水和实验室自来水为样品,根据实验1.3.2处理样品后,调至pH为6.0备用。根据实验1.3.1过程进行吸附-解吸实验,平行做7次,实验结果如表1所示。

表1 水样品中Pb(Ⅱ)离子含量的分析结果(n=7)
2.5 检出限和精密度
在实验条件下该方法的检出限为0.145 5 μg/mL,计算相应的相对标准偏差RSD(n=7)为4.55%。
3 结论
用纳米Al2O3分离富集样品中的铅,此法具有简单、快速、高选择等的特点,在pH=6的条件下,用纳米Al2O3能够快速、定量的吸收铅,吸附容量大;易于洗脱,回收率达到95.34%;该方法成功用于环境水样和自来水中铅的测定,分析结果令人满意。

