二氧化硅负载氧化亚铜的制备及其光催化性能研究
孙红梅 贾林艳 孙冬雪
(1.牡丹江大学食品药品学院,黑龙江 牡丹江;2.牡丹江师范学院,黑龙江,牡丹江 157011)
1 前言
光催化氧化法是一项新型废水处理及净化高级氧化技术,具有降解完全、高效、价廉、稳定和可以利用太阳光等优点,具有良好的应用前景。[10]
Cu2O是一种P型半导体材料,具有很大应用前景的光催化材料。[11-14]将Cu2O负载在合适的载体上,不但提高Cu2O的比表面积,提高催化活性,还方便回收以及有效的循环使用。SiO2无定型粉末,一种无毒,无污染的无机非金属材料,具有特殊的孔径结构、大比表面积和优良的热稳定性,广泛用作吸附剂、干燥剂和催化剂载体等。[15-19]本文采用SiO2负载Cu2O,通过对甲基橙的降解率来研究SiO2负载Cu2O的最佳负载量以及制取SiO2负载Cu2O反应的最佳温度和加热时间。
2 实验部分
2.1实验试剂及仪器
2.1.1 实验试剂

表2-1 主要实验试剂
2.1.2 实验仪器

表2-2 主要实验仪器
2.2 实验内容
2.2.1 氧化亚铜的制备
分别配制5mol/L的氢氧化钠溶液0.5mol/L的硫酸铜溶液和0.75mol/L的葡萄糖溶液。在磁力搅拌机的搅拌下缓慢地将50mL氢氧化钠溶液添加到50mL硫酸铜溶液中,在60℃时,与50mL葡萄糖溶液混合,在搅拌器的持续搅拌下反应40min。[20]得到的Cu2O微粒悬浮液经抽滤后,在60℃的烘干箱中干燥,产物密封装袋标记好备用。
2.2.2 二氧化硅负载氧化亚铜的制备
沉淀法制备SiO2负载Cu2O,设定温度不同的恒温水浴锅,准备15个500mL的烧杯,做好标记,均加入83.4mL蒸馏水、20mL无水乙醇5mLCuCl2(0.5mol/L)溶液,搅拌均匀;烧杯中依次加入质量不同的SiO2;搅拌均匀测量烧杯内温度,温度接近水浴温度时,分别交替加入9mL的NaOH(1.0mol/L)溶液和30mL的无水乙醇溶液,然后在5s内加9.8mL的盐酸羟胺溶液并搅拌一定时间后包好保鲜膜静置1.5h。然后水浴中搅拌10min后取出烧杯,待溶液分层,用注射器抽取出上层清液,用体积比1:1的蒸馏水和无水乙醇溶液清洗沉淀,接着将沉淀放在无水乙醇中,转移至坩埚,60℃下烘干沉淀,得到一系列的SiO2负载Cu2O样品。
2.2.3 二氧化硅负载氧化亚铜最佳负载量的研究
取2.2.2中加入质量分别为1.900g、2.400g、3.230g、4.900g、9.900g的SiO2,制备得到Cu2O含量为1%、3%、5%、7%、10%的SiO2负载Cu2O催化剂,加入10mg/L甲基橙溶液中,在200W的白炽灯下以降解甲基橙溶液为目标,在甲基橙的最大吸收波长465nm下使用721分光光度计记录加入纯Cu2O和不同负载量的SiO2负载Cu2O的甲基橙溶液随时间变化的吸光度,计算出降解率,[21]比较降解率找到最佳负载量,其中A0为甲基橙初始时刻吸光度值,A1为甲基橙在不同催化时间下的吸光度值。
2.2.4 二氧化硅负载氧化亚铜最佳制备温度研究
在Cu2O最佳负载量的前提下,取2.2.2中水浴温度为30℃、35℃、40℃、45℃、50℃的SiO2负载Cu2O催化剂,加入10mg/L甲基橙溶液中,在200W的白炽灯下以降解甲基橙溶液为目标,在甲基橙的最大吸收波长465nm下用721分光光度计记录不同制备温度下的甲基橙溶液随时间变化的吸光度,比较降解率找出最佳制备温度。
2.2.5 二氧化硅负载氧化亚铜最佳加热时间的研究
在最佳负载量和最佳制备温度的前提下,取2.2.2中水浴加热搅拌时间分别为6min、8min、10 min、12min、14min的SiO2负载Cu2O催化剂,加入到20mg/L甲基橙溶液中,在200W的白炽灯下以降解甲基橙溶液为目标,在甲基橙的最大吸收波长465nm下用721分光光度计记录不同制备时间下的甲基橙溶液随时间变化的吸光度,比较降解率找出最佳制备时间。
2.2.6 二氧化硅负载氧化亚铜的催化寿命研究
在最佳负载量、最佳加热温度和最佳加热时间条件下得到的SiO2负载Cu2O样品,用721分光光度计,在200W的白炽灯下以降解甲基橙为目标,在甲基橙的最大吸收波长465nm下以此样品为催化剂测定吸光度,将此样品循环使用5次比较甲基橙溶液的降解率。
2.2.7 氧化亚铜及二氧化硅负载氧化亚铜的红外光谱测定
分别取Cu2O粉末和SiO2负载Cu2O粉末2g,分别与200mgKBr粉末混合均匀放入研钵中充分研磨,研磨好的药品放入到压片机中,保持15MPa的压力下3分钟,取出制好的药品片。将压好的药品进行红外光谱扫描,得到相应数据和红外光谱图。
3 实验结果及讨论
3.1 氧化亚铜最佳负载量研究
表3-1,表3-2为纯Cu2O和SiO2负载Cu2O(5%)的吸光率和降解率。白炽灯为光源,分别将0.20g SiO2负载Cu2O(5%)和0.01gCu2O加入到50ml 10mg/L的甲基橙溶液中,每隔15min用721分光光度计对甲基橙吸光度检测。计算出降解率。
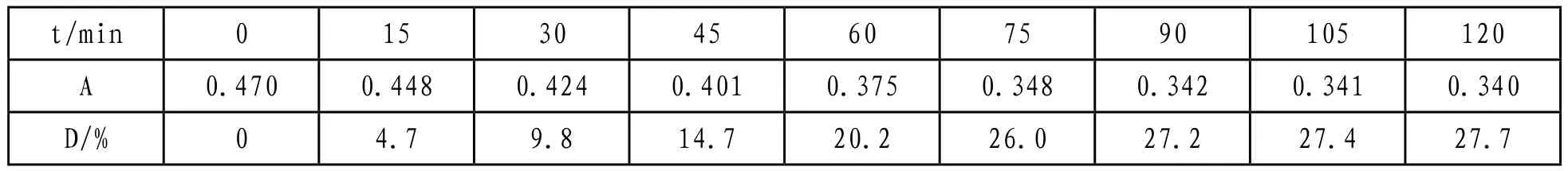
表3-1 纯Cu2O的吸光率和降解率
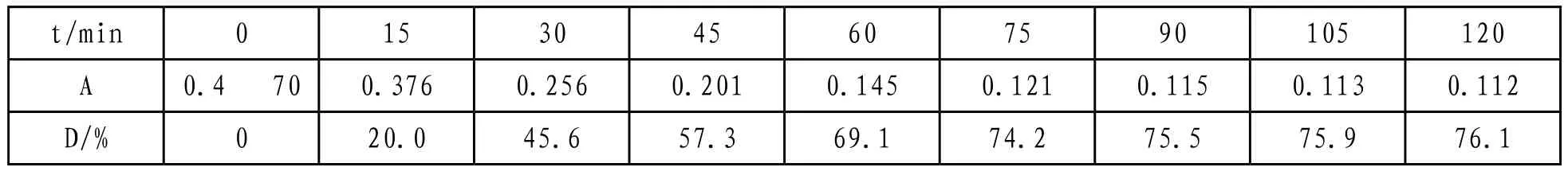
表3-2 SiO2负载Cu2O(5%)的吸光率和降解率

图3-1 不同掺杂量的脱色曲线
图中比较SiO2负载(5%)Cu2O比纯Cu2O的催化性能要好,充分说明SiO2是一种优良的吸附剂,增加了Cu2O的比表面积,提高了对甲基橙的催化效率。
表3-3和表3-4为Cu2O负载量分别为1%、3%、5%、7%、10%、的SiO2负载Cu2O对甲基橙的光催化降解的吸光度和降解率。白炽灯为光源,分别将0.10g五种不同掺杂量的催化剂加入到50ml 10mg/L的甲基橙溶液中,同等条件下以Cu2O负载量5%作为对照,每隔15min用721分光光度计对甲基橙吸光度检测。并计算出降解率。
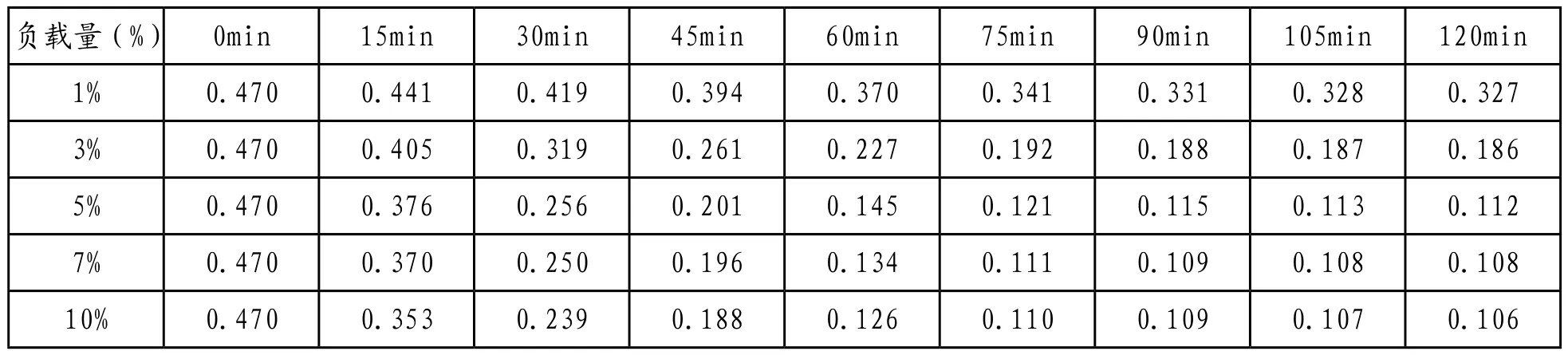
表3-3 不同Cu2O负载量甲基橙吸光度测量值
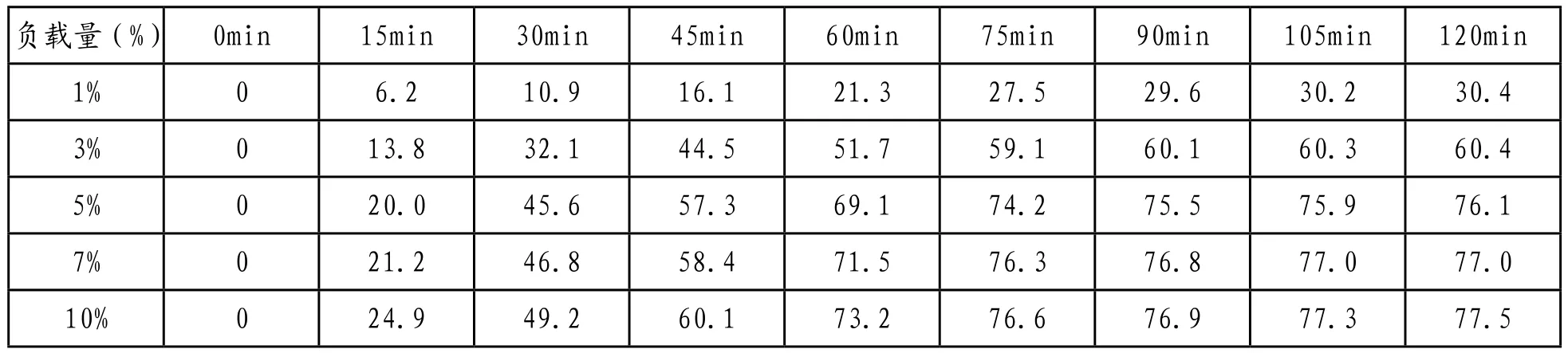
表3-4 不同Cu2O负载量甲基橙降解率值
以时间为横坐标,降解率为纵坐标,由上表数据绘制在不同负载量的SiO2负载Cu2O催化下,甲基橙的脱色曲线。
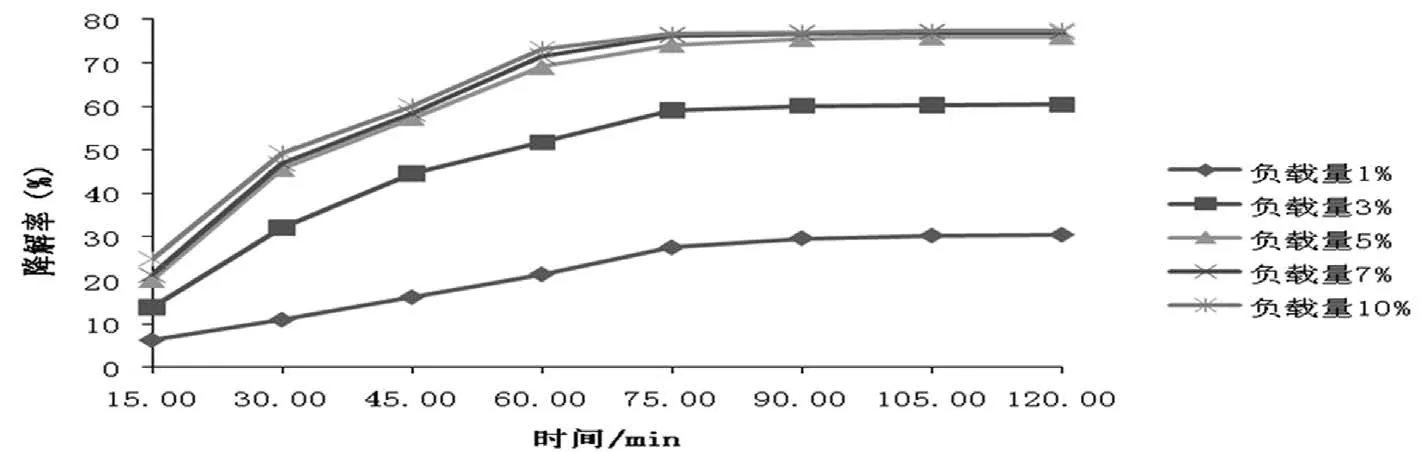
图3-2 不同负载量的脱色曲线
图3-2中可以看出,样品中Cu2O含量逐渐增大,Cu2O在SiO2上的负载量也随之增大,催化效果有所提高,但是催化的幅度不是很大,从节约成本方面考虑,负载量控制在5%左右最合适。
3.2 二氧化硅负载氧化亚铜最佳加热温度研究
表3-5和表3-6为加热温度不同的Cu2O负载量为5%,加热时间为10min的SiO2负载Cu2O对甲基橙的光催化降解的吸光度和降解率。白炽灯为光源,分别将0.10g五种不同加热温度的催化剂加入到50ml 10mg/L的甲基橙溶液中,每隔15min用721分光光度计对甲基橙吸光度检测。并计算出降解率。

表3-5 SiO2/Cu2O不同加热温度甲基橙吸光度值

表3-6 SiO2/Cu2O不同加热温度甲基橙降解率值

图3-3 不同加热温度的脱色曲线
从图表中可以看出随着加热温度的增大,相同时间内原子自身的扩散速率加大反应进行的较完全,催化剂的合成效果越好,但是温度过高,Cu2O的晶形发生了变化,使产物粒径增大,团聚现象严重,与SiO2的负载效果反而不好,因此,加热温度控制在40℃最适宜。
3.3 二氧化硅负载氧化亚铜最佳加热时间研究
表3-10和表3-11为加热时间不同的Cu2O负载量为5%加热温度为40℃的SiO2负载Cu2O对甲基橙的光催化降解的吸光度和降解率值。白炽灯为光源,分别将0.10g五种不同加热时间的催化剂加入到50ml、10mg/L的甲基橙溶液中,每隔15min用721分光光度计对甲基橙吸光度检测,并计算出降解率。

表3-7 SiO2/Cu2O不同加热时间甲基橙吸光度值

表3-8 SiO2/Cu2O不同加热时间甲基橙降解率值

图3-4 不同加热时间SiO2负载Cu2O催化下,甲基橙的脱色曲线
由图可知,加热时间为十分钟最佳,加热温度相同时,加热时间越长反应越完全,但随着时间过长,溶液浓度减小,新形成的晶形受到了阻碍,颗粒的晶粒尺寸继续增大,与SiO2负载效果变差。
3.4 二氧化硅负载氧化亚铜的使用寿命研究

表3-9 为循环次数1-5次的二氧化硅负载氧化亚铜对基橙的吸光度和降解率值

图3-5 不同循环次数的脱色曲线
从图中可以看出SiO2负载Cu2O循环次数增加,其催化活性降低,经过五次循环降解后,其降解率仍能达到70%以上,说明复合SiO2不仅提高了Cu2O的催化活性,也改善了催化剂的稳定性。
3.5 氧化亚铜及二氧化硅负载氧化亚铜的红外光谱分析

图 3-6 二氧化硅负载氧化亚铜红外光谱图
谱图形状相似,对比发现SiO2负载Cu2O的红外光谱图比氧化亚铜的红外光谱图多了一些小峰。强度上,SiO2负载Cu2O的吸收峰明显高于Cu2O的吸收峰。在波长为620cm-1处的振动峰为Cu2O中Cu-O键的伸缩振动引起的;[22]SiO2负载Cu2O的吸收峰在1100cm-1处增强,可能是Si-Cu键的伸缩振动造成的;在1600cm-1处的吸收峰为H-O-H的弯曲振动导致的。在3450cm-1的宽吸收峰是由于Cu2O和SiO2/Cu2O表面水分子H-O-H的伸缩振动引起的。
结论
直接沉淀法制备SiO2负载Cu2O催化剂,实验确定制备SiO2负载Cu2O的最佳条件为:在40℃的恒温水浴中将83.4ml蒸馏水、50ml无水 乙 醇、5mlCuCl2(0.5mol/L)溶 液、9mL的NaOH(1.0mol/L)、9.8mLNH2OH.HCl(0.5mol/L)和0.100g的SiO2混合,搅拌三分钟后静置1.5h,在水浴中搅拌十分钟,清洗,烘干得到SiO2负载Cu2O。光催化反应中,白炽灯做光源以10mg/L的甲基橙溶液作为目标降解物,得负载量为5%、加热温度为40℃和加热时间为10min的SiO2负载Cu2O对甲基橙降解的催化效果最好,降解率达到76.1%,且循环五次降解后,其降解率仍能在70%以上。

