铝酸钴/蜂窝陶瓷催化剂的制备及其在印染废水处理中的应用
张兰河, 张明爽, 高伟围, 李 正, 贾艳萍, 高 敏, 凌良雄
(1. 东北电力大学 化学工程学院, 吉林 吉林 132012; 2. 吉林建筑大学 松辽流域水环境教育部重点实验室, 吉林 长春 130118; 3. 北京农业生物技术研究中心, 北京 100089)
臭氧氧化技术在污水深度处理中广泛使用,单独臭氧氧化的臭氧利用率和有机物去除率较低,运行不稳定[1-2]。非均相臭氧催化氧化克服了单独臭氧氧化的缺点,提高了难降解有机污染物的去除率,其中催化剂在臭氧催化氧化过程中起着关键作用[3-4]。催化剂的制备方法主要包括溶胶-凝胶法、共沉淀法、浸渍法和涂覆法等,其中涂覆法因工艺简单、成本低、催化剂成分稳定等优点被广泛应用。
催化剂主要由金属或金属氧化物组成[5],制备催化剂的影响因素较多,如催化剂种类、表面特性、活性组分添加量、焙烧时间和焙烧温度等[6-8]。金属钴(Co)是一种重要的催化剂活性组成成分,常见化合价有+2价和+3价,具有催化效率高、稳定性好等优点[9]。将金属或金属氧化物活性组分负载于催化剂载体上可延长催化剂的使用寿命,同时提高污染物的去除率。采用钴氧化物(CoOx)改性二氧化钛(TiO2)催化剂进行优化试验发现,过高或过低的温度均会影响催化剂的强度和活性,在300~400 ℃焙烧温度下催化剂的催化性能最优[10]。利用Ni/Al2O3-CeO2处理废水时,当二氧化铈(CeO2)掺杂量为10%时,催化活性最高[11]。李冰蕊等[12]通过研究发现,Ce3+会抑制TiO2结晶,焙烧温度越高,Ce3+掺杂量对催化剂结构和活性影响越显著。蜂窝陶瓷(Ceramic Honeycomb,CH)具有强耐久性、高耐腐性、高可靠性、高反复利用性、低压降等特性,作为催化剂的载体已成功用于污水处理。利用CuMn/ZrAlTi/堇青石蜂窝陶瓷催化剂处理含酚废水,当活性组分负载率为1%时,化学需氧量(COD)去除率高于94%[13];采用蜂窝陶瓷负载金属锰(Mn)的催化剂去除硝基苯时,Mn的负载量越大,越有利于硝基苯的去除[14]。影响制备蜂窝陶瓷催化剂的因素较多,如何优化工艺条件制备稳定高效的催化剂是增加催化效率的重要环节。
近年来利用臭氧氧化法处理染料废水成为研究的热点[15-16],对苯二酚是一种重要的合成染料原料,生产过程中产生大量的对苯二酚废水[17-18]。本文研究以对苯二酚模拟废水为目标污染物,采用涂覆法制备铝酸钴/蜂窝陶瓷(CoAl2O4/CH)催化剂。利用正交试验优化催化剂的制备条件,考察涂覆次数、活性组分投加量、焙烧时间和温度对对苯二酚和COD去除率的影响。通过X射线衍射仪(XRD)、场发射扫描电镜(FESEM)和N2-吸附/脱附等手段分析催化剂的结构,探索催化剂的催化效率和使用寿命,以期为CoAl2O4/CH催化剂的工业化应用奠定理论基础。
1 试验部分
1.1 试验材料
主要试剂:草酸,天津市永大化学试剂有限公司;六水合硝酸钴,天津市北方化玻购销中心;氢氧化铝,天津市大茂化学试剂厂;铝溶胶,大连斯诺化学新材料有限公司;对苯二酚,北京化工厂。以上试剂均为分析纯。
1.2 试验装置
臭氧催化氧化对苯二酚废水的工艺流程如图1所示。臭氧催化氧化反应器是一个有效容积为1.5 L的有机玻璃容器,臭氧发生器利用空气作为气源产生臭氧(流速为2 L/min),臭氧由反应器底部的曝气板通入反应器,臭氧进气质量浓度为2.5 mg/L,对苯二酚初始质量浓度为100 mg/L,pH值为7.0,温度为(293±3)K。尾气利用质量分数为2%的碘化钾溶液进行吸收。

图1 臭氧催化氧化对苯二酚废水流程Fig.1 Catalytic ozonation process of hydroquinone wastewater
1.3 催化剂的制备
采用质量分数为50%的草酸溶液对CH(尺寸为19.3 mm×19.3 mm×10 mm)进行预处理。冷凝回流,煮沸(时间为1 h),冷却后分别采用自来水和去离子水进行洗涤,直至洗涤液pH值达到7,再置于烘箱中干燥(100 ℃、24 h)备用。
分别称取1.973 g的Co(NO3)2·6H2O与10.000 g的Al(OH)3溶于50 mL去离子水中搅拌1 h,再滴入5 mL铝溶胶进行混合。将预处理的CH浸渍于上述溶液1 h后取出,利用吸耳球吹脱其孔道内的残液,置于烘箱中120 ℃下干燥2 h,反复重复以上步骤(2、4、6次),置于马弗炉中焙烧,即制备得到CoAl2O4/CH催化剂[19]。为分析涂覆次数、活性组分投加量、焙烧时间和温度对催化效率的影响,设计4因素3水平正交试验,如表1所示。

表1 正交试验表Tab.1 Orthogonal experiment table
1.4 测试方法
采用7000S/L型X射线衍射仪(日本岛津公司)分析催化剂的物相,管电流为30 mA,管电压为40 kV,扫描范围为10°~80°,扫描速率为10(°)/min,X射线源为Cu靶的Kα射线(λ=0.154 nm)。利用ASAP-2020 M型全自动比表面积和微孔分析仪(美国Micro-meritics公司)分析样品的比表面积、孔容和孔径,在温度为110 ℃的条件下将催化剂活化4 h,测定77 K下氮气的吸附/脱附曲线。采用BET(Brunauer-Emmett-Telle)方程计算催化剂的比表面积,采用BJH(Barrett-Joyner-Hallender)脱附模型计算催化剂的孔径及分布[20]。利用XL-30型场发射扫描电镜(美国FEI公司)测定催化剂的粒径和形貌。采用WDW-50型电子拉力机(上海协强仪器科技有限公司)测试催化剂(长、宽和高分别为19.3、19.3、10 mm)的力学性能,测试速度为2 mm/min。
根据CJ/T 3028.2—1994《臭氧发生器臭氧浓度、产量、电耗的测量》,采用碘量法检测气相臭氧浓度;每隔5 min从取样口取样,采用紫外分光光度法(λ=288 nm)检测对苯二酚浓度[21];采用5B-3BV8型多参数水质分析仪(北京连华永兴科技发展有限公司)直接测定COD浓度。
2 结果与讨论
2.1 催化剂制备条件的优化
表2示出催化剂制备正交试验结果。可以看出,9#催化剂对对苯二酚去除率和COD去除率均最高,分别达到84.63%和50.39%。按照极差大小排序:涂覆次数>焙烧时间>Co与Al的量比>焙烧温度。极差的大小能够反映影响催化效率因素的大小,涂覆次数的极差最大,表明它是影响催化效率的最主要因素。为保证对苯二酚和COD均达到较高的去除率,选取A3B3C2D3进行试验,对苯二酚去除率为84.51%,COD去除率为50.60%。由试验结果可得CoAl2O4/CH的最优制备条件为:Co与Al的量比为0.4∶5,涂覆6次,焙烧温度为700 ℃,焙烧时间为6 h。

表2 催化剂制备正交试验结果Tab.2 Results of orthogonal experiment for catalyst preparation
2.2 臭氧、催化剂投加量和pH值的影响
在臭氧催化氧化过程中,臭氧(O3)投加量与臭氧产生活性基团的数量密切相关[22],从而影响催化效率。考察了O3投加量(质量浓度分别为0、1.3、2.5、3.4、5.3 mg/L)对对苯二酚和COD去除率的影响,结果如图2所示。
从图2可以看出:当O3浓度较高时,对苯二酚去除率较大,这是因为高浓度的O3增强了氧化对苯二酚的能力,提高了对苯二酚和降解中间产物的去除速率;当水中O3浓度低时,有机物的去除率低,主要是因为水中O3浓度未达到污染物完全降解所需的浓度[23];当O3质量浓度分别为0、1.3、2.5、3.4、5.3 mg/L时,O3利用率分别为0、31.13%、52.36%、29.00%、18.03%。当O3质量浓度为2.5 mg/L时,臭氧催化氧化体系中臭氧利用率最高,反应体系中的溶解氧迅速达到了溶解平衡状态,充足的O3与对苯二酚反应,加速了对苯二酚的降解;当O3质量浓度高于2.5 mg/L时,O3利用率快速下降,对苯二酚和COD去除率增加较小。这是由于臭氧催化氧化体系中的O3质量浓度较高时,溶解氧在水中达到饱和,残余的O3由尾气排出。

图2 O3质量浓度对对苯二酚去除率和COD去除率的影响Fig.2 Influence of O3 concentration on removal rate of hydroquinone and COD
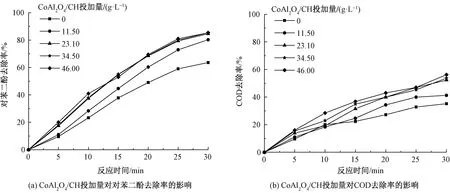
图3 CoAl2O4/CH投加量对对苯二酚去除率和COD去除率的影响Fig.3 Influence of CoAl2O4/CH addition amount on removal rate of hydroquinone and COD
考察了CoAl2O4/CH催化剂投加量(0、11.50、23.10、34.50、46.00 g/L)对对苯二酚和COD去除率的影响,结果如图3所示。与单独O3氧化相比,当催化剂的投加量为11.50 g/L时,COD和对苯二酚去除率变化小,加入的催化剂量不能使O3产生大量的·OH,O3直接氧化是降解对苯二酚主要原因;当CoAl2O4/CH催化剂投加量为23.10 g/L时,提高了O3、催化剂和对苯二酚的反应空间,对苯二酚的去除率大大增加,在反应时间为30 min的条件下,对苯二酚去除率为84.51%;但是,当CoAl2O4/CH催化剂投加量为46.00 g/L时,与CoAl2O4/CH投加量为23.10 g/L进行对比,对苯二酚和COD去除率仅提高0.74%,这是因为过多的催化剂影响了臭氧氧化分解产生的·OH与催化剂的有效接触面积。综合考虑,为既可获得较高的有机物去除率又可节约成本,选用CoAl2O4/CH催化剂的投加量为23.10 g/L。

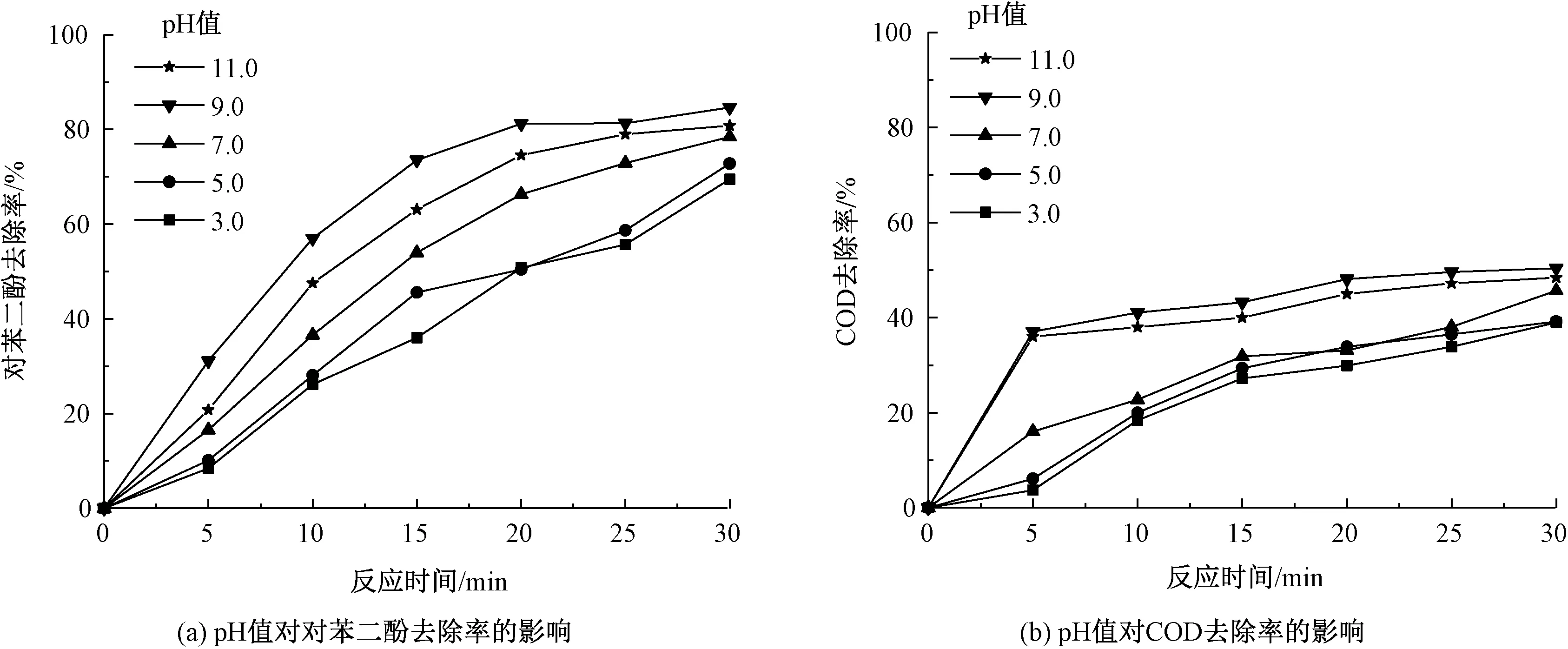
图4 pH值对对苯二酚去除率和COD去除率的影响Fig.4 Effect of pH value on removal rate of hydroquinone (a) and COD (b)

图5 1#和9#催化剂的N2吸附/脱附等温线Fig.5 N2 adsorption/desorption isotherms of 1# catalyst (a) and 9# catalyst (b)
2.3 催化剂的物理性能分析
催化剂的比表面积、孔径和孔容等物理性质均影响臭氧催化氧化效果。催化剂的低温N2-吸附/脱附等温线和粒度分布曲线(1#和9#催化剂)如图5所示。
9#催化剂的比表面积(45.47 m2/g)高于1#催化剂的比表面积(41.36 m2/g),涂覆的活性组分对CoAl2O4/CH催化剂的影响较大。1#和9#催化剂的孔径分布在4.00~4.60 nm之间,属于介孔结构,孔容分别为0.03、0.05 cm3/g。催化剂的比表面积和孔容越大,越容易将有机物吸附在其表面,从而进行有效的催化氧化反应[29-30]。9#催化剂较1#催化剂吸附量大,孔容孔径大,可吸附更多有机物,加速臭氧催化氧化过程,催化效率更高。
1#催化剂和9#催化剂的XRD谱图如图6所示。不同条件下制备的CoAl2O4/CH催化剂的主要晶型相似,在2θ为37.22°处均出现了非常尖锐的强峰。同时,在蜂窝陶瓷表面无其他杂质的衍射峰出现,与JCPDS no.44-0160保持一致,这说明制备的CoAl2O4结晶度好,属于典型的尖晶石结构(主要组分为CoAl2O4)。

图6 1#和9#CoAl2O4/CH催化剂的XRD谱图Fig.6 XRD patterns of 1# and 9# CoAl2O4/CH catalysts
图7示出1#催化剂和9#催化剂的FESEM照片。可以看出,蜂窝陶瓷表面粗糙,经焙烧后生成的活性组分均匀地附着在CH表面。图7(a)表明,1#催化剂表面为片层状结构;图7(b) 表明,9#催化剂的晶粒明显变小,呈现出海绵状微孔结构。这是因为Co(NO3)2·6H2O与Al(OH)3在高温焙烧下发生物理化学反应,生成具有催化活性的化合物CoAl2O4。

图7 1#催化剂和9#催化剂FESEM照片(×20 000)Fig.7 FESEM images of 1# catalyst (a) and 9# catalyst (b)(×20 000)
2.4 催化剂的稳定性分析
1#催化剂和9#催化剂力学性能的变化如表3所示。蜂窝陶瓷的最大压力和抗压强度分别为4 657 N和12.50 MPa。1#催化剂和9#催化剂的最大压力和抗压强度明显增强。这表明添加的活性组分CoAl2O4与CH紧密结合,催化剂的抗压强度增加。1#催化剂和9#催化剂使用前后的最大压力和抗压强度无明显变化,CoAl2O4/CH催化剂的抗压能力强,易于实现工业化。

表3 不同催化剂材料的力学性能Tab.3 Mechanical properties of different catalysts
CoAl2O4/CH催化剂(9#催化剂)稳定性的测定结果如图8所示。

图8 CoAl2O4/CH催化剂的循环利用次数对对苯二酚去除率的影响Fig.8 Effect of recycling utilization times of CoAl2O4/CH catalyst on removal rate of hydroquinone
催化剂重复使用5次后,对苯二酚去除率变化较小,这表明CoAl2O4/CH催化剂经过反复浸渍煅烧,活性物质与CH结合牢固,重复利用后催化活性未下降;因此,CoAl2O4/CH催化剂具有较高的催化活性和化学稳定性。
3 结 论
1)采用涂覆法制备了铝酸钴/蜂窝陶瓷催化剂,涂覆次数是影响臭氧催化氧化的最大因素。在涂覆6次、700 ℃焙烧6 h、Co与Al的量比为0.4∶5的条件下,铝酸钴/蜂窝陶瓷催化剂催化活性最高,COD和对苯二酚去除率最大,分别达到50.60%和84.51%。
2)在对苯二酚初始质量浓度为100 mg/L、pH值为7.0、温度为(293±3)K的条件下,随着臭氧和铝酸钴/蜂窝陶瓷催化剂投加量提高,对苯二酚和COD去除率提高。当臭氧和铝酸钴/蜂窝陶瓷催化剂投加量分别高于2.5 mg/L和23.10 g/L时,对苯二酚和COD去除率提高幅度减小,臭氧利用率下降。当pH值为9.0时,对苯二酚的去除率最高。
3)铝酸钴/蜂窝陶瓷催化剂的主要活性组分以CoAl2O4为主,是典型的尖晶石结构;CoAl2O4/CH(9#)催化剂呈海绵状结构,涂覆均匀且可吸附较多活性组分,比表面积和孔容最大,分别达到45.47 m2/g和0.05 cm2/g。
4)采用涂覆法制备的铝酸钴/蜂窝陶瓷催化剂具有较高的催化活性和反应稳定性,应用前景较好。
FZXB

