Lung-RADS分级和CT征象诊断孤立性肺结节的价值
单文莉, 柏根基,王亚婷,周围,郭莉莉
孤立性肺结节(solitary pulmonary nodules,SPN)在病理上主要包括肺部原发性和转移性肿瘤等恶性病变、良性肿瘤以及感染性病变等,低剂量筛查CT的应用大大增加了孤立性肺结节的检出率,但患者常因过度恐慌反复检查,为了帮助节省医疗资源以及给予临床相应的随访或手术建议,对孤立性肺结节的性质进行早期判断意义重大。本文研究分析240例孤立性肺结节患者的CT表现,探讨各个CT征象在良恶性病灶间的差异性分布,并比较肺部影像报告和数据系统(lung imaging reporting and data system,Lung-RADS)分级、CT征象及联合两种方法对孤立性肺结节的诊断效能。

表1 Lung-RADS分级2~4级标准
材料与方法
1.病例资料
搜集2016年10月-2017年10月淮安市第一人民医院孤立性肺结节患者240例,男131例,女109例,年龄32~81岁,平均(56.5±24.5)岁。所有病例均为首发单发病变(直径≤3 cm)、未行其他任何临床干预。病例均经手术或穿刺病理结果证实,其中良性45例,恶性195例,患者以咳嗽、咳痰、痰中带血为首发症状的27例,14例出现胸痛、胸闷或胸部不适,199例在健康查体时偶然发现。
2.CT检查方法
所有入组患者接受Siemens Somatom Defnition双源64排128层螺旋CT机胸部CT扫描,采用CARE Dose4D扫描条件:管电压80~140 kV,管电流60~100 mA,层厚为5 mm,层间距5 mm。所有受检者仰卧于检查床上,指导呼吸配合检查,扫描范围包括整个肺野,病灶的原始采集资料按1 mm标准算法重建后传到Siemens双源CT专用后处理软件Syngo Via工作站进行多平面重组、容积再现、最大密度投影等方法重组以利于观察病灶的特点。
3.图像测量与数据分析
所有病灶的影像资料均由两位高年资影像医生共同判读,观察病灶的边界是否光整、有无胸膜牵拉、毛刺、分叶、支气管截断、支气管充气、空泡、空洞及肿瘤血管征象,并测量病灶的大小,取病灶最大层面的最长径与最短径的平均值作为病灶的大小。根据Lung-RADS分级标准将病灶按密度分为纯磨玻璃病灶(pure ground-glass nodule,pGGO)31例、部分实性结节(mixed ground-glass nodule,mGGO)54例和实性结节(solitary solid nodule,SSN)155例。
所有病灶均按照Lung-RADS标准分类,并根据病理结果将资料划分为良、恶性两组,分析各CT征象在两组间是否具有差异性,有差异性征象恶性组大于良性组计1分/个,反之计-1分/个,而两组无明显差异的征象不计分,得出所有病灶的CT征象分值。
4.统计学处理
将通过上述方法得到的分析结果分别与病理比较,采用SPSS 22.0软件,通过卡方检验比较各征象在良恶性组别中的差异性。采用受试者操作特征曲线(receiver operating characteristic curve,ROC曲线),并根据约登(Youden)指数选取的两种诊断方法最佳界值将病灶划分为阳性组和阴性组。通过二元Logistic拟合得到两种方法联合对诊断孤立性肺结节的诊断效能,采用Z检验分析曲线下面积(area under curve,AUC)的差异性,以P<0.05认为差异有统计学意义。
结 果
1.病理诊断、Lung-RADS分级和CT征象积分
病理结果:240个病灶经病理证实良性45例,包括不典型增生28例,错构瘤10例,慢性机化性炎症3例,硬化性血管瘤2例;恶性195例,包括原位癌23例,鳞癌54例,腺癌117例。
Lung-RADS分级结果:按照Lung-RADS分级标准(表1)对每个病灶重新分类,结果为2级28例、3级25例、4A级17例、4B级121例。
CT征象积分:各征象在良恶性肺结节中的分布情况见表2,恶性组大于良性组的征象每个计1分,恶性组小于良性组的征象每个计-1分,病灶分值-1~7分(表3)。典型病例的CT表现见图1~4。

图1 女,71岁,右肺上叶后段高分化腺癌。a)CT平扫示病灶呈磨玻璃密度,大小约25.6 mm×23.3 mm,病灶内见空泡,边缘见毛刺,邻近血管移位并进入病灶内部(即肿瘤血管征,箭);b)CT平扫矢状面重组见分叶征,叶间胸膜牵拉(箭)。 图2 女,47岁,右肺上叶慢性炎症。a)CT平扫示病灶呈磨玻璃密度(箭),大小约12.9 mm×11.8 mm,边界欠清;b)矢状面重组示内部血管走形无异常(箭)。 图3 女,55岁,右肺上叶低分化腺癌。a)CT横轴面示病灶呈软组织密度,大小约24.6 mm×19.4 mm,病灶边缘可见毛刺、分叶,邻近胸膜牵拉(箭);b)MIP重组示肿瘤微血管征(箭);c)矢状面重组示胸膜牵拉增厚(箭)。 图4 女,47岁,右肺下叶高中分化腺癌。a)CT平扫横轴面示胸膜下病灶呈部分磨玻璃密度影,大小约18.1 mm×26.7 mm,与胸膜分界不清,边缘见毛刺、分叶,肿瘤内微血管不规则交通(箭);b)MIP重组后示肿瘤微血管征(箭);c)矢状面示病灶中央呈实性软组织密度,边缘晕状磨玻璃密度(箭)。
2.Lung-RADS分级、CT征象及联合两种方法诊断孤立性肺结节的结果比较
用ROC曲线分析Lung-RADS分级、CT征象及联合两种方法分别对孤立性肺结节良恶性进行初步诊断,三种方法的AUC分别为0.628、0.910、0.988,差异均有统计学意义。Lung-RADS分级的诊断效能明显低于CT征象评估(Z=8.483,P<0.001),联合两种方法对孤立性肺结节的诊断效能明显高于Lung-RADS分级(Z=8.403,P<0.001),且稍高于CT征象评估(Z=4.274,P<0.001),见图5。
根据约登指数计算每种方法的最优诊断界值,并计算其敏感度、特异度和符合率,与Lung-RADS分级方法比较,CT征象具有较高的敏感度(81.5%)、特异度(91.1%)和符合率(83.3%),而当联合两种方法诊断孤立性肺结节的敏感度、特异度和符合率分别可达到97.9%、95.6%、97.5%。

表2 不同CT征象在良、恶性孤立性肺结节中的差异 (例)
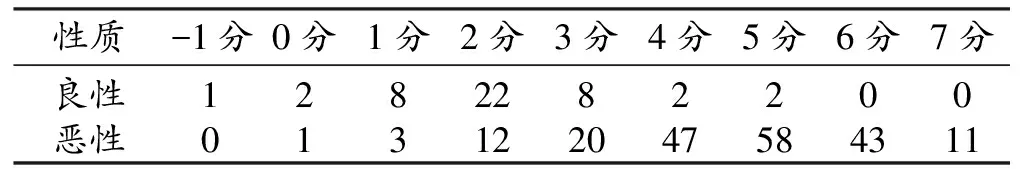
表3 良、恶性孤立性肺结节不同CT征象分值例数 (例)

图5 Lung-RADS分级、CT征象积分及联合两种方法诊断孤立性肺结节的ROC曲线分析。
讨 论
2014年美国放射学院(American College of Radiology,ACR)制定Lung-RADS分级标准用来规范肺癌基线筛查、影像报告书写、病灶处理建议,其鉴别依据主要是病灶的大小和成分。孤立性肺结节的大小和生长方式是评估结节恶性潜能的两大要素,恶性结节的可能性与结节直径呈正相关关系。磨玻璃结节的密度较正常肺实质稍高,但病灶内保留了支气管和血管等正常的肺结构,亚实性结节是磨玻璃密度中出现实性密度,当实性部分位于病灶中心时,周围的磨玻璃影常被称为“晕征”,该征象对病灶良恶性没有特异性。在恶性结节中,晕征是肿瘤细胞在局部扩散过程中仅沿着完整的肺泡壁表面增殖而没有间质或血管侵犯引起的,与常见的感染原因不同,这些结节通常在随访期间持续存在。相比较实性病灶,部分实性病灶具有更高的恶性风险[1]。根据Zhang等[2]的报道,恶性结节的进展过程可以仅表现为病灶内实性成分的增加,而不出现直径或体积的增大,杨智明等[3]同样报道对于磨玻璃密度结节,实性成分的含量与病灶的恶性程度呈正相关。陆青云[4]等的研究中良恶性肺结节的大小、内部实性成分具有差异性(P<0.05),且鉴别诊断的阈值分别为11.05 mm、4.55 mm。本组240个病例资料中,当病灶分级大于Lung-RADS 4A级时,诊断的敏感度、特异度、符合率分别为54.9%、68.9%、57.5%,ROC曲线的AUC为0.628(P<0.05),对孤立性肺结节的鉴别诊断存在一定的局限性。
虽然孤立性肺结节病灶的大小和实性成分对判断病灶良恶性具有重要价值,但很多研究发现孤立性肺结节形态学的价值同样不容忽视。李辉等[5]的研究结果显示鉴别孤立性肺结节良恶性最敏感的征象为毛刺、分叶及肿瘤血管征,联合毛刺及分叶征时鉴别孤立性肺结节良恶性的敏感度、特异度、符合率分别为100.0%、76.0%、92.0%。文献报道,孤立性肺结节病灶中与良性相关的特征包括内部可见脂肪和钙化,而提示恶性的征象包括边缘是否光整、毛刺、分叶、胸膜牵拉、支气管充气、肿瘤血管、空泡及空洞征等[6]。本组研究显示恶性征象主要有边界不光整、胸膜牵拉、毛刺、分叶、支气管截断、肿瘤血管及空洞征,良性征象主要为钙化,结果与文献大致相同。区别在于本组研究中支气管充气征和空泡征在良恶性孤立性肺结节间没有明显差异性(P>0.05),而支气管截断征的分布差异有统计学意义(P<0.05)。
王志鹏等[7]分析孤立性肺结节的危险因素的研究表明支气管充气征和空泡征在良恶性结节间无明显差异性(P<0.05)。李胜达等[8]做单因素分析孤立性肺结节病灶的CT表现时表明:胸膜牵拉、毛刺、分叶、支气管截断和肿瘤血管征在良恶性病灶中分布较多有统计学意义,上述结果与本组研究结果相同。Gaeta等[9]将支气管征分为五种类型:Ⅰ型,结节病灶突然阻塞支气管;Ⅱ型,结节周围环绕完整的支气管腔;Ⅲ型,结节压迫支气管;Ⅳ型,支气管穿入结节内增厚、变窄,管壁尚光整;Ⅴ型,支气管穿入结节内,管壁不规则增厚、变窄。也有较多学者[10-11]将Ⅱ型和Ⅲ型合并为一类,及分为四型。每种类型的支气管在良恶性病灶的分布略有差异,恶性结节多见的类型依次为Ⅰ、Ⅳ和Ⅴ型,良性结节中较常见的依次为Ⅱ型和Ⅲ型。本组资料中的支气管充气征大多属于Ⅱ和Ⅲ型,而支气管截断征多为Ⅰ型、Ⅳ和Ⅴ型,因此本组实验结果与文献结果不矛盾。本组资料中钙化是唯一的良性征象,文献[12]报道钙化多发生于错构瘤、结核球等,如果病灶内合并有脂质成分,则为诊断错构瘤的有力证据。恶性结节中的钙化多不规则或呈斑点状,具有离散性分布的特点,且范围很小[13-14]。
本研究中,当累计分值大于3时,CT征象诊断孤立性肺结节的敏感度、特异度、符合率分别为81.5%、91.1%、83.3%,AUC为0.910(P<0.001),与Lung-RADS分级方法相比,CT征象对孤立性肺结节的诊断价值更高,差异有统计学意义(P<0.001)。而两者联合诊断的的敏感度、特异度、符合率分别可达97.9%、95.6%、97.5%,AUC为0.988(P<0.001),联合诊断的价值大于Lung-RADS分级和CT征象(Z=8.403,P<0.001;Z=4.274,P<0.001)。该结果提示Lung-RADS分级在单独诊断孤立性肺结节时有局限性,但与CT征象联合诊断时,能明显提高诊断效能。这是因为联合两种方法时,相当于综合分析了病灶的大小、实性成分及形态学特征,因此为临床提供更全面、客观的影像依据。需要特别指出的是,ACR制定Lung-RADS分级主要应用于肺癌高危人群或伴有肺气肿、慢阻肺、职业及环境等各种危险因素,本文并未据此设置严格的纳入标准,故Lung-RADS分级评估孤立性肺结节良恶性的结果可能稍有偏差。
孤立性肺结节的良恶性评估仍然是一项具有挑战性的任务,病灶的大小、实性成分及形态学评估均为诊断难题不可分割的一部分。CT征象诊断孤立性肺结节的符合率优于Lung-RADS分级,但联合两种方法可以明显优化诊断效能,提高鉴别良恶性结节的符合率,帮助临床采取合理的处理措施。

