脱钙程度对浓缩乳蛋白功能性质的影响
刘大松,余 韵 ,李珺珂 ,徐雨婷,王 淼,周 鹏 *
(1.江南大学 食品学院,江苏 无锡 214122;2.食品科学与技术国家重点实验室 江南大学,江苏 无锡 214122)
浓缩乳蛋白 (milk protein concentrate,MPC)是牛乳先经脱脂处理,然后经超滤和洗滤脱除部分乳糖和盐之后,再通过真空浓缩和喷雾干燥脱水,所得到的一类高蛋白粉,其蛋白质的质量分数在40~90%之间[1-2]。MPC具有高蛋白质、低脂肪、低乳糖等特点,并具有良好的风味和口感,是酸奶、乳酪、婴幼儿食品、烘焙食品、运动营养食品、功能性饮料等食品的重要蛋白质配料[3-4]。MPC在食品中的具体应用是由其特有的功能性质所决定的,比如MPC中的酪蛋白分子具有无序的展开结构,并具有嵌段式的疏水和亲水区域,对液—液和气—液等界面的形成和稳定具有促进作用,因而MPC具有较好的乳化性和起泡性,可用于冰淇淋、慕斯蛋糕、搅打奶油、蛋奶酥等食品的研发和生产。此外,MPC的蛋白质组成与牛乳几乎完成相同,即主要含酪蛋白与乳清蛋白,且两者的质量比例约为4∶1,因而MPC可用于强化酸奶、乳酪等乳制品的蛋白组成,促进其在生产过程中凝胶结构的形成,从而提高最终产品的品质和得率等。
膜分离工艺具有非热、高效等特点,因而MPC能较好地保持了牛乳中蛋白质原有的结构和性质。MPC中主要的蛋白质是以酪蛋白胶束的形式存在的,胶束的结构特性决定了MPC的功能性质,而酪蛋白胶束的结构又受体系中钙的含量和存在状态的调控。目前,MPC在应用过程中存在的一个突出问题是其溶解性较差,而且蛋白质含量越高和贮藏时间越长,其溶解性较差的问题越严重[3,5-7]。MPC良好的溶解性是实现凝胶性、乳化性、起泡性等其它功能性质的先决条件,在工业生产中,通常要求MPC在常温条件下能够快速和完全的溶解[4]。前期研究表明,MPC溶解性较差的主要诱导机理是蛋白非共价聚集,即MPC中的钙离子会通过离子键介导蛋白质之间产生非共价交联,从而降低MPC的溶解度,而适当程度的脱钙预处理能提高MPC的溶解性和贮藏稳定性[7-10]。然而,脱钙预处理对MPC其它功能性质的影响却有待于进一步研究。
因此,作者以脱脂乳为原料,通过超滤、洗滤、离子交换脱钙和喷雾干燥,制备系列脱钙程度的MPC,探讨脱钙程度对MPC功能性质的影响,为调控和拓展MPC的功能性质提供理论依据,从而促进MPC在食品中的广泛应用。基于MPC在食品中的主要应用范围,作者在对脱钙MPC主要理化特性和功能特性(起泡性和起泡稳定性、乳化性和乳化稳定性)测定的基础上,进一步对脱钙MPC的凝胶流变、质构特性和微观结构特性及钙离子对其影响,进行了初步的探索研究。
1 材料与方法
1.1 材料与试剂
巴氏杀菌脱脂乳:上海光明集团产品;罗门哈斯Amberlite SR1L Na树脂:美国Dow’s化学品公司产品;异硫氰酸荧光素 (FITC)、葡萄糖酸内酯(GDL):美国Sigma公司产品;玉米胚芽油:西王集团有限公司产品。
1.2 主要仪器
SPPM-24S-1超滤系统:厦门三达膜科技有限公司产品;Spectr AA 220原子吸收光谱分析仪:美国Varian公司产品;B-290喷雾干燥仪:瑞士步琪公 司 产 品 ;HAAKE MARS Ш 流 变 仪 、Heraeus Multifuge XIR冷冻离心机:美国Thermo公司产品;TA-XT2质构分析仪:英国Stable Micro Systems公司产品;LSM-780激光共聚焦显微镜(CLSM):德国Zeiss公司产品;TM3030台式扫描电子显微镜(SEM):日本日立公司产品;UV-2700紫外可见分光光度计:日本岛津公司产品;T10高速分散机、T25高速分散机、C-MAG HS7磁力搅拌器:德国IKA集团产品;K1302凯氏定氮仪:上海晟声自动化分析仪器有限公司产品;SHP-250生化培养箱:上海森信实验仪器有限公司产品。
1.3 实验方法
1.3.1 脱钙MPC的制备 在脱脂乳中加入质量分数0.01%叠氮化钠以防止微生物生长,采用截留相对分子质量10 000的聚醚砜滤膜进行超滤,待体积浓缩3倍后,在截留液中补加水至原脱脂乳体积,经洗滤浓缩3倍后,再在相同条件下重复上述洗滤步骤2次,收集最终所得的截留液,并加入质量分数0.01%叠氮化钠。取1 kg截留液分别加入0、10、20、30、40 g离子交换树脂,在室温下搅拌2 h,然后在进口温度135℃和出口温度75℃的条件下进行喷雾干燥,收集MPC置于铝箔袋中。
1.3.2 总钙质量分数的测定 称取0.1 g脱钙MPC至250 mL高脚烧杯中,加入20 mL浓硝酸和5 mL高氯酸,高温消化至剩余体积约为2 mL,用超纯水定容至50 mL,取5 mL定容后样品与1 mL镧溶液(50 mg/mL)一起定容至50 mL,然后再采用原子吸收光谱法测定钙含量[11]。
1.3.3 总蛋白质质量分数的测定 称取0.2 g脱钙MPC、0.2 g硫酸铜、4 g硫酸钾于消化管中,加入20 mL浓硫酸,高温消化至澄清透明。采用凯氏定氮法测定脱钙MPC中的总蛋白质含量,所用的蛋白质换算系数为6.38。
1.3.4 起泡性和起泡稳定性分析 称取5 g脱钙MPC,加入100 mL超纯水,配制为5 g/dL的溶解液,25℃搅拌2 h后,在4℃冰箱中静置过夜。取5 mL溶解液置于15 mL刻度试管中,记录溶解液高度,然后用T10高速分散机和S10N-10G分散刀头(7.6 mm转子直径)在30 000 r/min下均质30 s,记录泡沫初始高度,待静置30 min后,记录泡沫终止高度,所得泡沫初始高度与溶解液高度的百分比即为起泡性,泡沫终止高度与泡沫初始高度的百分比即为泡沫稳定性[12]。
1.3.5 乳化性和乳化稳定性分析 取1.3.4中脱钙MPC的溶解液20 mL,置于50 mL烧杯中,加入5 mL玉米胚芽油,然后用T25高速分散机和S18N-19G分散刀头(12.7 mm转子直径)在11 200 r/min下均质2 min,立即取10 μL乳状液加入到5 mL磷酸缓冲液(0.1 mol/L、pH 7.0、质量分数 0.1%SDS)中,混合均匀后置于1 cm宽度的比色皿中,在500 nm波长处测定其吸光度值。乳液静置20 min后,再在相同条件下测定其吸光度值。乳化性和乳化稳定性的计算采用Manoi的方法[13]。
1.3.6 凝胶特性分析
1)凝胶的流变学性质分析 按照1.3.4中的方法配制两组脱钙MPC的溶解液(质量分数5%),在一组中添加氯化钙,使脱钙MPC溶解液中的钙含量与未脱钙MPC的溶解液相同。将溶解液置于95℃水浴中加热10 min,冷却至40℃,加入1 g/dL的葡萄糖酸内酯(GDL),搅拌2 min,取1 mL样品置于流变仪测试平台上,使用3.5 cm直径的探头进行动态振荡测试,测试频率为1 Hz,应变为1%,测试过程包含4个步骤:酸化阶段,40℃保持240 min;冷却阶段,样品以1℃/min的速度降温至10℃;退火阶段,10℃保持30 min;加热阶段,样品以1℃/min的速度升温至40℃[14]。同时,另取加入GDL的溶解液,置于40℃水浴中保持240 min,测定pH值的变化。
2)凝胶的质构特性分析 加入GDL的脱钙MPC的溶解液15 mL,置于25 mL平底烧杯中,40℃水浴中保持240 min,然后放入4℃冰箱,贮藏过夜后测定凝胶的质构特性,采用12.5 mm直径的圆柱形探头,下压速度为1 mm/s,下压位移为10 mm。在力与时间的关系曲线上,下压过程中的第一个破裂点所对应的力即为凝胶断裂力,最大下压程度所对应的力即为凝胶强度[14]。
3)凝胶的持水力分析 加入GDL的脱钙MPC的溶解液5 mL,置于15 mL离心管中,40℃水浴中保持240 min后于4℃冷藏过夜,在500 g和4℃条件下离心10 min,弃去上清后,所得剩余物的质量占凝胶初始质量的百分比即为持水力[14]。
4)凝胶的CLSM分析 加入GDL的脱钙MPC的溶解液,采用FITC(0.01 mg/mL)标记,然后取200 μL标记样品置于玻底培养皿中,盖上盖玻片,以AB胶密封,并包裹锡箔纸,避光放置于40℃培养箱中保持240 min,4℃冷藏过夜,然后在488 nm激发波长下观测凝胶的微观结构[15]。
5)凝胶的SEM分析 按照1.3.6.2中的方法制备凝胶,并将其切成1 mm3的立方块,用体积分数2.5%戊二醛在4℃固定过夜,然后用1%四氧化锇在4℃固定2 h,再用体积分数50%、70%、90%和100%乙醇梯度脱水,临界点干燥后将样品置于贴有导电胶的载物台上,喷金后于15 kV加速电压下观测凝胶的微观结构。
2 结果与讨论
2.1 脱钙MPC的基本组成
如表1所示,脱脂乳通过超滤、洗滤、离子交换脱钙和喷雾干燥等不同系列工艺处理后,各脱钙MPC的钙质量分数分别为27%、24%、22%、20%和17%,脱钙率分别为0%、11%、19%、27%和37%。各脱钙MPC的蛋白质质量分数约为78%,对应于食品工业中常用的MPC80。
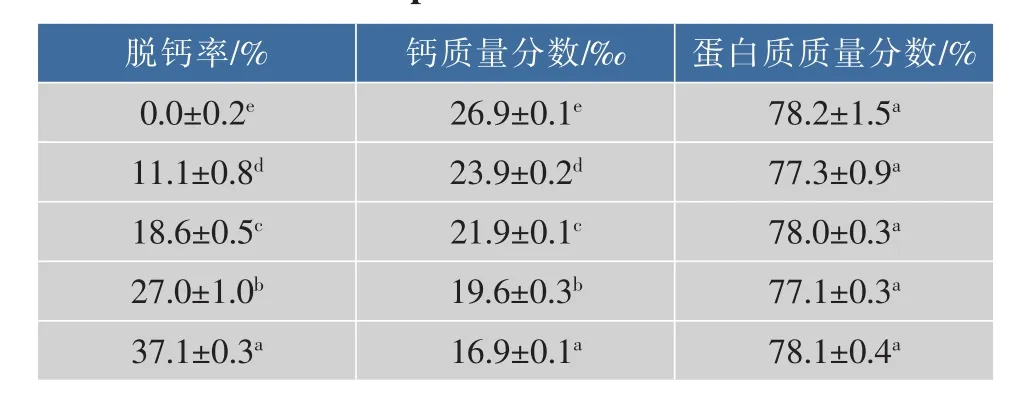
表1 脱钙MPC的基本组成Table 1 Composition of decalcified MPC
2.2 脱钙MPC的起泡性和起泡稳定性
泡沫是由连续的水相和分散的气相组成。蛋白质的起泡性是指蛋白质降低气-液界面的界面张力而促进泡沫形成的能力。MPC的起泡性是决定搅打奶油、冰淇凌、蛋糕等泡沫型乳制品品质的关键因素,微细的空气泡能赋予产品独特的质构和口感。MPC的起泡性和起泡稳定性随脱钙程度的变化如图1所示。从图中可以看出,起泡性随脱钙程度的增加而逐渐提高;起泡稳定性在脱钙率0~11%之间快速增加,在脱钙率11%~37%之间则缓慢增加。
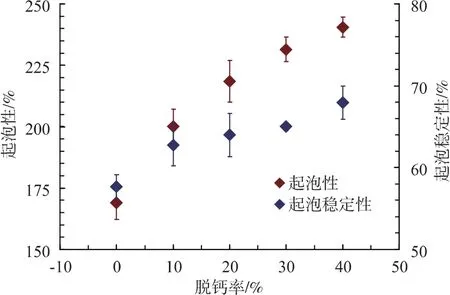
图1 脱钙MPC的起泡性和起泡稳定性Fig.1 Foamability and foam stability of decalcified MPC
2.3 脱钙MPC的乳化性和乳化稳定性
一些天然和加工食品,如牛乳、奶油、人造奶油、蛋糕等,都是乳状液类型的食品。乳状液为热力学不稳定体系,在贮藏过程中会发生相分离、絮凝、聚集等现象,蛋白质具有两亲特性,能起到乳化剂的作用,从而降低水油之间的界面张力。MPC的乳化性和乳化稳定性随脱钙程度的变化如图2所示。从图中可以看出,乳化性随脱钙程度的增加而逐渐提高;乳化稳定性在脱钙率0~19%之间保持几乎不变,在脱钙率19%~37%之间则快速增加。
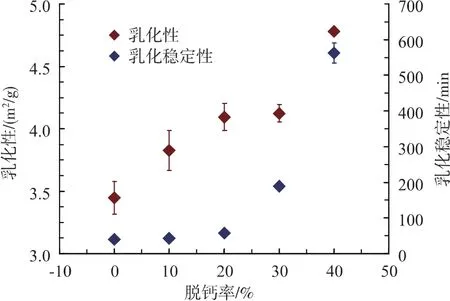
图2 脱钙MPC的乳化性和乳化稳定性Fig.2 Emulsifiability and emulsion stability of decalcified MPC
MPC中的酪蛋白主要是以球状胶束聚集体的形式存在的,胶束的粒径约为100 nm,胶束结构的完整性主要由胶体磷酸钙和疏水相互作用维持。酪蛋白都是磷酸化的蛋白,在胶束结构中,其磷酸基团与胶束钙之间相互作用形成离子键,从而起到维持胶束结构的作用。当脱脂乳的超滤截留液经过离子交换处理后,酪蛋白胶束中的钙离子被逐渐脱除,维持胶束结构的离子键被破坏,带负电的磷酸残基之间产生静电斥力,因而胶束结构逐渐被破坏,酪蛋白逐渐从胶束中解离,以单分子和小相对分子质量聚集体的形式存在[16]。相比酪蛋白胶束,单分子和小相对分子质量聚集体的酪蛋白能更快速地迁移到两相界面,更快速地展开并在界面上定向,更快速地在界面上与邻近分子之间发生相互作用,形成稳定的界面膜,从而更快速地降低界面张力,促进两相体系的分散,并提高两相体系(如泡沫和乳状液)的热力学稳定性。
2.4 脱钙MPC的凝胶性
2.4.1 凝胶的流变学性质 脱钙MPC凝胶的流变学性质测试模拟了酸奶从生产、贮藏、到食用的整个过程,分为4个步骤:酸化阶段,摸拟酸奶的发酵过程;冷却和退火阶段,模拟酸奶的后熟和贮藏过程;加热阶段,模拟酸奶入口食用的过程。
在动态振荡测试过程中,脱钙MPC凝胶的储能模量随时间和脱钙程度的变化如图3(a)所示。在加入GDL的酸化阶段,即0~240 min之间,体系温度保持在40℃,体系pH逐渐从6.74降到4.54,储能模量随时间逐渐增加。MPC中主要的酪蛋白为αs1、αs2、β、κ,其等电点分别为 4.4~5.0、4.9~5.0、5.2~5.4、5.4~5.6,因而随着体系 pH 值的降低,酪蛋白分子所带的净电荷逐渐减少,蛋白质分子之间的相互作用逐渐增强,产生蛋白聚集,并最终形成凝胶网络结构,因而储能模量逐渐增加。在冷却阶段,即250~270 min之间,体系温度从40℃降到10℃,储能模量随时间快速增加。在退火阶段,即270~300 min之间,体系温度保持在10℃,储能模量随时间变化不明显。在加热阶段,即300~330 min之间,体系温度从10℃升到40℃,储能模量随时间快速降低。在加热阶段结束时,脱钙MPC凝胶的储能模量略高于酸化阶段结束时的储能模量,说明经历冷却和退火阶段的熟化后,凝结的网络结构更稳固。
在动态振荡测试的4个阶段,脱钙率越高,凝胶的储能模量越低,这可能是因为钙离子的存在能够介导蛋白分子之间产生交联,并促进凝胶网络结构的形成。虽然前期研究表明适当程度的脱钙预处理能提高MPC的溶解性,但其凝胶性和贮藏稳定性降低[7-10]。然而,在工业生产中,通常要求MPC在常温条件下能够快速和完全的溶解。因此,可在脱钙MPC的溶解液中回补钙离子,使其钙含量与未脱钙MPC的溶解液相同,以探究储能模量的回复程度。脱钙MPC在回补钙后,其凝胶的储能模量随时间和脱钙程度的变化如图3(b)所示。对比回补钙前后的凝胶,可以发现在动态测试的4个阶段,其储能模量随时间而变化的趋势基本相同,但回补钙能显著回复其凝胶的储能模量,而且脱钙率越低,储能模量回复到的水平越高,其中11%脱钙率的MPC的储能模量完全回复到了脱钙之前的水平。
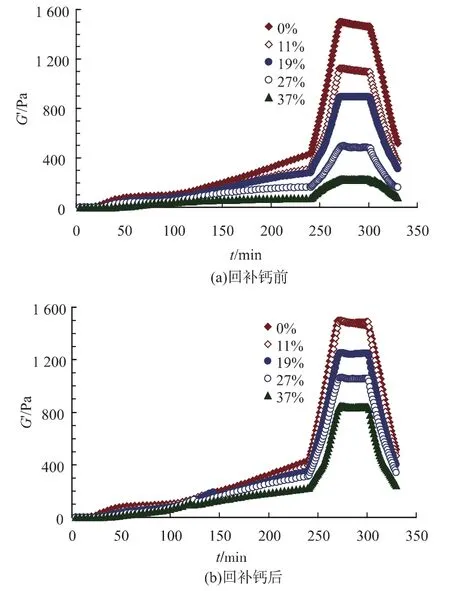
图3 脱钙MPC在回补钙前后其凝胶的储能模量(G’)变化图Fig.3 Changes in elastic modulus of decalcified MPC colloids/gels without and with calcium supplement
2.4.2 凝胶的质构特性和持水力 在回补钙前后,脱钙MPC的溶解液经酸化和熟化后,所得凝胶的断裂力、强度和持水力如表2所示。在回补钙前,MPC凝胶的断裂力和强度随脱钙程度的增加而逐渐降低;在回补钙后,凝胶断裂力和强度都得到了显著的回复,而且脱钙率越低,断裂力和强度回复到的程度越高,但仍略低于脱钙之前的水平。此外,在回补钙前,MPC凝胶的持水力也随脱钙程度的增加而逐渐降低;在回补钙后,凝胶持水力也得到了显著的回复,而且脱钙率越低,持水力回复到的程度越高,其中11%脱钙率的MPC的持水力完全回复到了脱钙之前的水平。
2.4.3 钙离子对MPC凝胶的组织结构的影响 对不同钙含量(即回补钙前后)的MPC的葡萄糖酸内酯凝胶组织结构进行了荧光显微和扫描电镜超微结构的对比观察。
在回补钙前后,脱钙MPC的溶解液经酸化和熟化后,通过激光共聚焦显微镜 (Confocal Laser Scanning Microscopy,CLSM)对所得凝胶的网络结构荧光显微观察结果如图4所示。图片中的绿色区域对应乳蛋白,黑色区域对应水相。从图片上可以看出,未脱钙MPC的凝胶,其网络结构致密均匀。在回补钙前,随着脱钙率的增加,MPC凝胶中的空隙逐渐变大且数量逐渐增加,凝胶网络结构逐渐变得疏松。在回补改后,MPC凝胶变得致密紧实,其孔隙率显著降低,凝胶的网络结构得到了显著的回复,而且脱钙率越低,凝胶网络结构回复到的水平越高,其中11%~19%脱钙率的MPC凝胶基本回复到了未脱钙MPC的凝胶网络结构(图4)。这也解释了MPC凝胶的储能模量、断裂力、强度和持水力,随脱钙率的变化趋势以及在回补钙前后的变化,即凝胶的网络结构越致密、稳固,其储能模量、断裂力、强度和持水力越大。
在回补钙前后,脱钙MPC的溶解液经酸化和熟化后,所得凝胶的微观结构在扫描电子显微镜(Scanning Electron Microscope,SEM)下的观察结果如图5所示。相比CLSM,SEM能更好的展现MPC凝胶的细微结构。从图中可以看出,未脱钙MPC的凝胶中,蛋白质分布均匀,凝胶结构致密。在回补钙前,随着脱钙率的增加,凝胶孔隙率逐渐升高,凝胶结构逐渐变得疏松和粗糙。在回补改后,MPC凝胶的孔隙率显著降低,凝胶的结构得到了显著的回复;而且脱钙率越低,补加钙后MPC凝胶网络结构回复到的水平越高,其中11%~19%脱钙率的MPC凝胶基本回复到了未脱钙的MPC凝胶结构。这一结果与CLSM显示的结果基本一致。
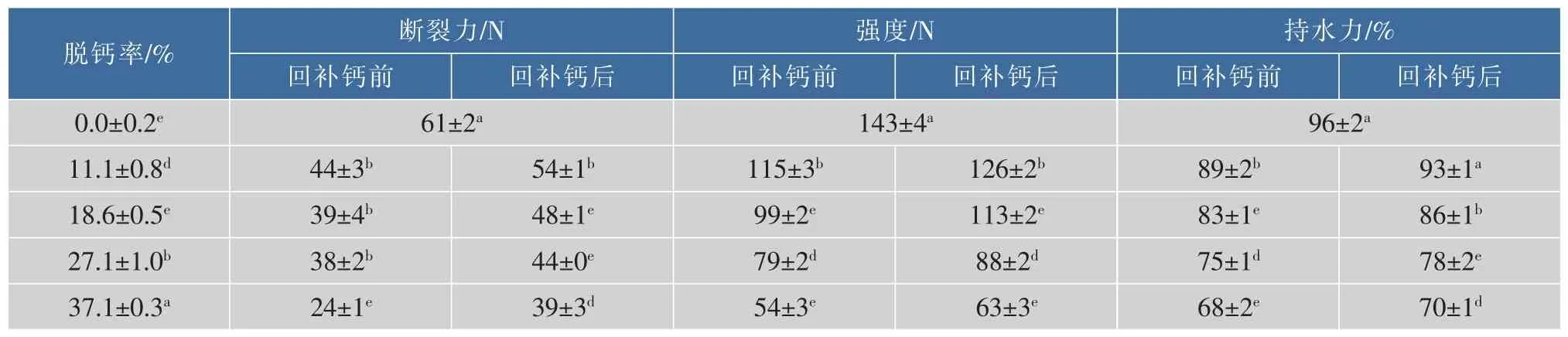
表2 脱钙MPC在回补钙前后其凝胶的断裂力、强度和持水力Table 2 Fracture force,hardness and water hold capacity of decalcified MPC gel without and with calcium supplement
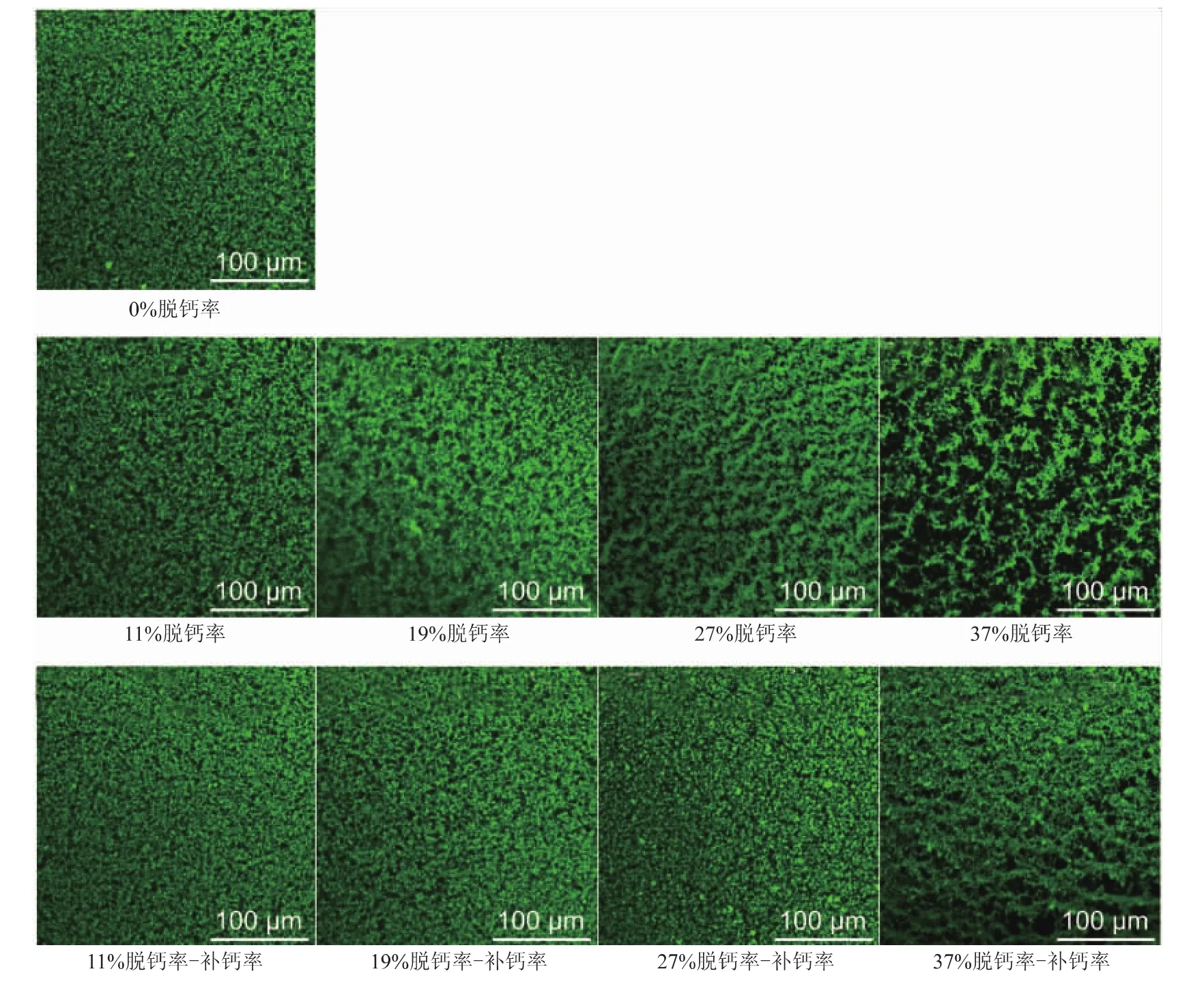
图4 脱钙MPC在回补钙前后其凝胶的CLSM微结构Fig.4 CLSM microstructure of decalcified MPC gel without and with calcium supplement
综合MPC凝胶流变学性质、质构特性、持水力和微观结构的结果,可以说明钙的回补能够在一定程度上回复脱钙MPC的凝胶性,其中11%脱钙MPC的凝胶性能够基本完全回复到脱钙之前的水平。这可能是由于钙离子的回补,增加了脱钙MPC溶解液中游离钙离子的含量,也提高了体系的离子强度,从而促进了蛋白质分子之间的交联以及凝胶网络结构的形成。
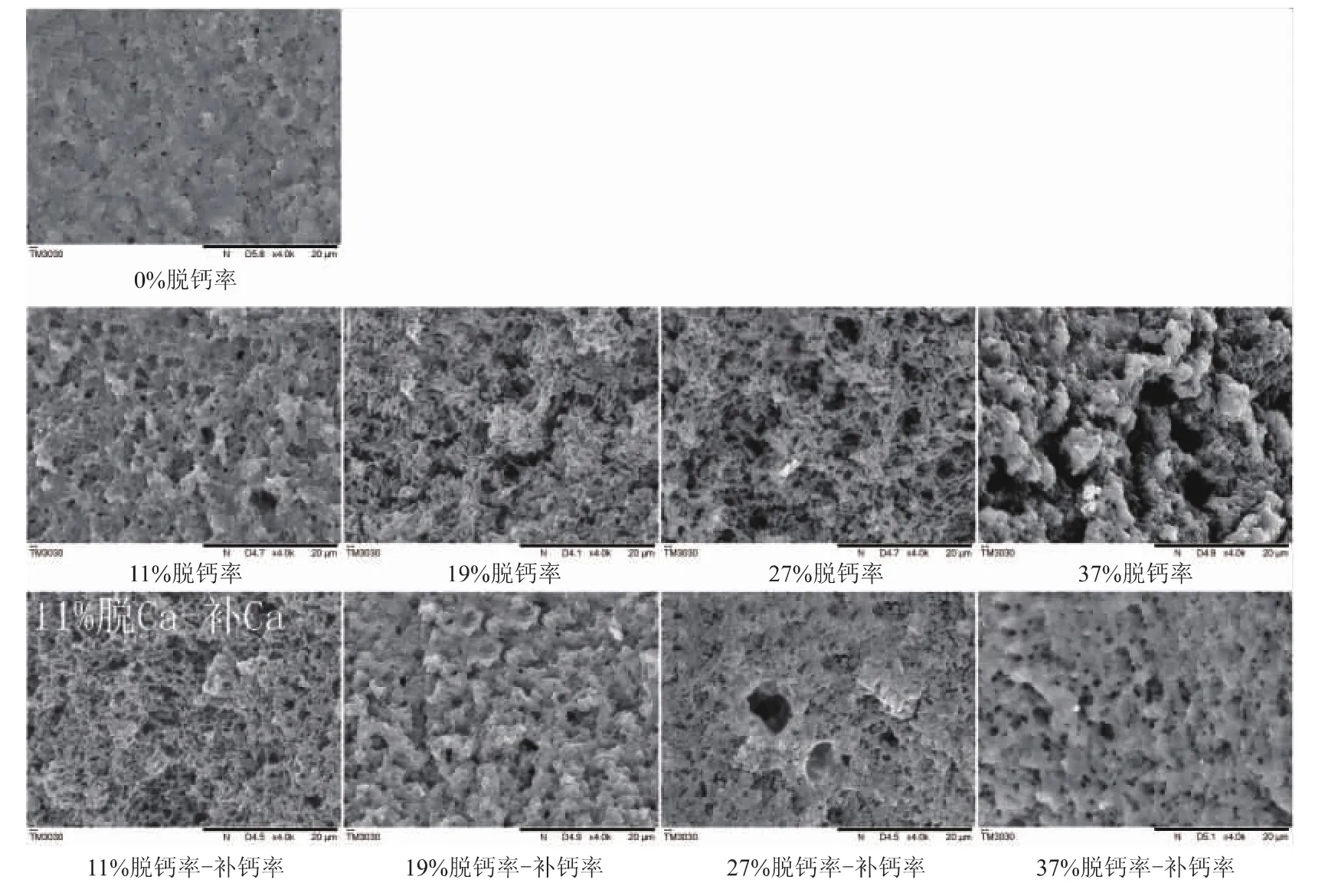
图5 脱钙MPC在回补钙前后其凝胶的SEM超微结构Fig.5 SEM micrographs of decalcified MPC gel without and with calcium supplement
3 结 语
采用离子交换树脂对脱脂乳的超滤截留液进行脱钙预处理,然后再通过喷雾干燥制备了脱钙率为0%、11%、19%、27%和37%的MPC。MPC溶解液的起泡性和起泡稳定性、乳化性和乳化稳定性都随着脱钙程度的增加而逐渐提高。此外,随着脱钙程度的增加,MPC凝胶的储能模量、断裂力、强度和持水力均逐渐降低,且凝胶网络结构逐渐变得疏松和粗糙;在脱钙MPC的溶解液中回补钙至未脱钙MPC的含量时,其凝胶的储能模量、断裂力、强度、持水力和网络结构均得到了显著的回复,且脱钙率越低,回复到的程度越高,其中11%脱钙率的MPC凝胶基本完全回复到了脱钙之前的水平。这说明离子交换脱钙可作为一种潜在的手段来调控MPC的功能性质,以拓展其在食品工业中的应用范围。

