当归补血汤治疗肿瘤化疗不良反应随机对照临床试验的Meta分析
庞小坤 韩梅 江心灿 赵宇昊
摘要:目的 系统评价目前当归补血汤治疗肿瘤化疗不良反应的疗效和安全性。方法 电子检索中国期刊全文数据库(CNKI)、万方数据库、中文科技期刊全文数据库(VIP)、中国生物医学文献服务系统(SinoMed)、美国国立医学图书馆(PubMed)、TheCochrane Library,截止2017年12月。应用Cochrane Risk of bias量表评价纳入研究的质量,釆用RevMan5.3软件进行Meta分析。结果 最终纳入14篇文献,包括1369例患者,Meta分析结局指标结果显示:白细胞水平升高[MD=1.25,95%CI(0.41,2.09),P<0.00001]、血红蛋白水平升高[MD=25.96,95%CI(15.59,36.34),P<0.00001]、血小板水平升高[MD=26.82,95%CI(23.33,30.31),P<0.00001]。IgG水平升高[ MD=2.78,95%CI (1.99,3.56),P<0.00001]、IgA水平升高 [MD=0.30,95%CI(-0.24,0.85),P<0.00001]、IgM水平升高[MD=0.29,95%CI(0.16,0.41),P<0.00001]、CD3+水平升高[MD=6.56,95%CI(3.79,9.34),P<0.00001]、CD4+水平升高[MD=5.77,95%CI(3.42,8.12),P<0.00001]、CD8+水平降低[MD=-4.73,95%CI(-6.62,-2.83),P<0.00001]、骨髓抑制Ⅲ級和Ⅳ级患者例数减少。结论 当归补血汤治疗肿瘤化疗不良反应可以增加血细胞、血清免疫球蛋白水平,使T淋巴细胞水平趋于稳定、减少骨髓抑制。当归补血汤减少肿瘤化疗不良反应有一定优势且安全性高。但结果异质性较大,还需更多高质量随机对照临床试验进行研究。
关键词:当归补血汤;肿瘤;化疗;不良反应
中图分类号:R730.53 文献标识码:A DOI:10.3969/j.issn.1006-1959.2019.02.021
文章编号:1006-1959(2019)02-0069-06
2006年WHO正式把肿瘤定为慢性可控制的疾病[1],随着人口老龄化加速、生活环境和方式的转变,预计未来几十年内,我国恶性肿瘤的发病和死亡人数将继续呈上升趋势[2]。随着医疗的不断发展,肿瘤患者的治疗不仅只延长生存时间,更要提高生存质量。恶性肿瘤主要采用手术、化疗、放疗、免疫治疗方法,其中化疗是使用最多、最广泛方法之一。肿瘤化疗药物通过干扰肿瘤细胞的增殖,从而发挥控制肿瘤生长的作用,但化疗药物大多选择性不强,不具有靶向性[3]。在抑制杀伤肿瘤细胞的同时,对正常细胞尤其是增殖旺盛的细胞同样具有抑制、杀伤作用,因此产生呕吐、口腔溃疡、皮肤过敏、骨髓抑制等不良反应,并对机体脏器有一定的毒性作用,影响患者的治疗计划和生活质量,甚至引起并发症导致死亡。当归补血汤出自李东垣的《内外伤辨惑论》,方用“黄芪一两,酒洗当归二钱”,是现今沿用的经典名方之一。其组方简单、药食两宜,现代药理学实验研究证明它能够促进细胞再生长,保护脏器,极大地减少化疗毒副作用和对机体的损害,是一种作用确切的化疗减毒增效剂[4]。此方临床使用广泛但关于当归补血汤对肿瘤化疗不良反应的系统评价较少,本研究通过Meta分析系统地评价当归补血汤治疗肿瘤不良反应的疗效与安全性,以期为临床诊疗提供循证医学依据。
1资料与方法
1.1纳入与排除标准 纳入标准:①研究对象:肿瘤化疗后产生不良反应者,肿瘤类型不限;②治疗组:单用或在对照组基础上加用当归补血汤或加味当归补血汤治疗;③对照组:使用西医常规化疗药物治疗;④主要结局:WBC、HB、PLT。⑤次要结局:血清免疫球蛋白水平(IgG、IgA、IgM)、T淋巴细胞亚群水平(CD3+、CD4+、CD8+);⑥研究类型:随机对照临床试验。排除标准:①重复发表的文献;②联合其他方剂治疗的研究;③动物及实验机理研究。
1.2文献检索 检索中国期刊全文数据库、万方数据库、中文科技期刊全文数据库、中国生物医学文献服务系统、美国国立医学图书馆、The Cochrane Library、Clinicaltrials.gov、临床试验注册库、WHO平台一级临床实验注册库,时限自建库至2017年12月。中文数据库进行主题词联合关键词(化疗)AND(随机)AND(当归补血汤/当归补血汤加味/黄芪当归汤/芪归)英文数据库检索策略为(chemotherapy)AND(random)AND(Angelicae Sinensis Decoctionor/Danggui Bu xue Decoctionor/Danggui Bu xue Tang / Angelic enrich blood soup /Chinese Angelicae Decoction)。
1.3文献筛选 由两名研究者独立完成并复核,将检索到的文献导入NoteExpress软件处理,先阅览题目摘要,获取符合或不确定是否符合标准的文献,再阅读全文,排除不符合纳入标准的文献。遇到有争议的文献时,进行讨论或与第三方商讨决定纳入与否。
1.4资料提取 ①纳入研究的基本信息:题目、作者、发表杂志的名称、类型、年卷期页码、基金支持;②研究方法和可能存在的偏倚;③研究对象的特征;④干预措施:治疗/对照药物的方法、联合用药情况,干预、对照类型;⑤结局指标:按照原始研究报告的指标和格式收集所有有效性结局和安全性结局的数据;⑥其他信息:重要引文,潜在利益冲突。由两名研究者按照纳入排出标准独立提取并核对。
1.5方法学质量评价 偏倚风险评估利用Cochrane风险评估工具:①随机分配方法;②分配方案隐藏;③对研究对象、方案实施者、结果测量者采用的盲法;④结果数据完整性;⑤选择性报告研究结果;⑥其他偏倚来源。以上6项,满足(yes)代表低风险偏倚;不满足(no)代表高风险偏倚;文献中未明确提供信息做出充分的是或否的判断时,把该条目判断为风险偏倚不清楚(unclear)。此项由两位研究者独立完成并交叉核对,产生分歧时进行讨论。
1.6安全性评价指标 骨髓抑制的分级采用的是世界卫生组织抗癌药物急性及亚急性毒性反应分级标准,分为0、Ⅰ、Ⅱ、Ⅲ、Ⅳ级,本次统计Ⅲ级和Ⅳ级的患者例数。
1.7统计学分析 定量分析采用Cochrane系统评价软件RevMan5.3进行Meta分析。连续性变量采用均差(Mean Different,MD)为统计量,给出95%可信区间(Confidence Interval,CI)。异质性检验采用同质性检验(Q test,Chi-square test),在此基础上借助I2分析临床异质性,不明显时采用随机效应模型合并。当I2≤30%且P≥0.1时,采用固定效应模型(fixed-effect model),当I2>30%且P<0.1时采用随机效应模型(random effects model)。若异质性太大(I2>75%),应查找异质性来源,考察Meta分析结果的稳定性。
2结果
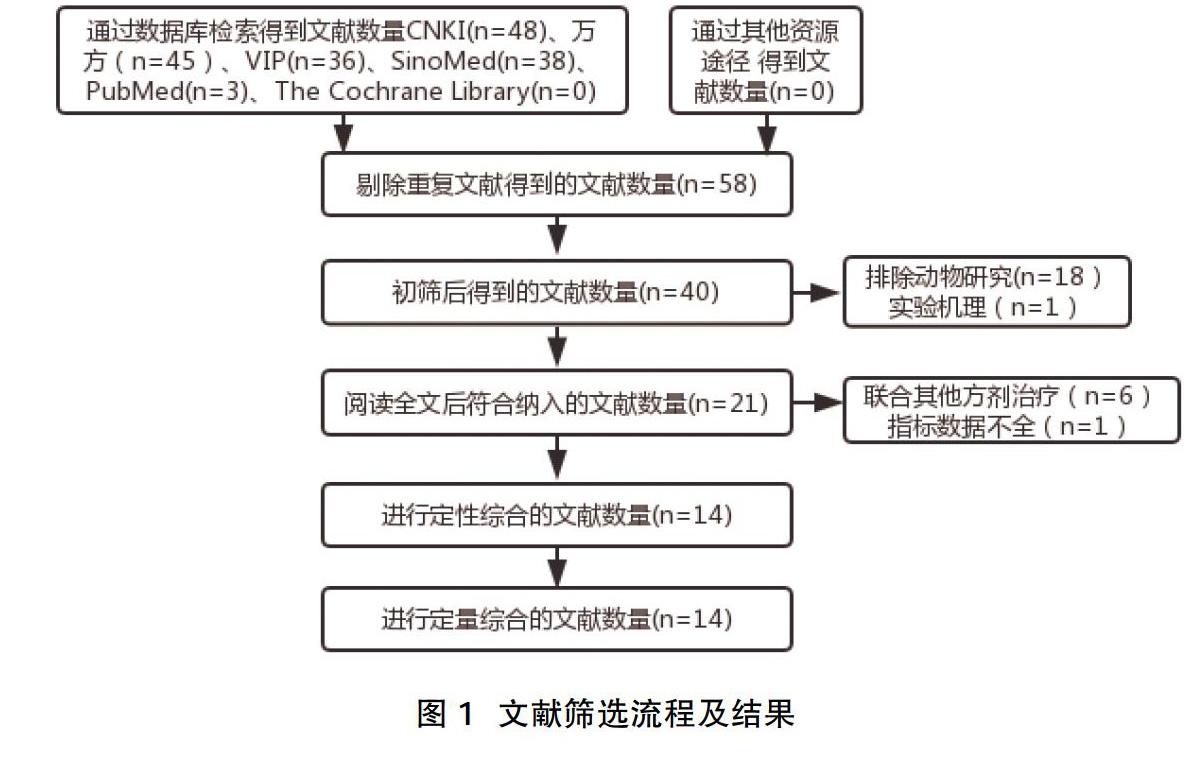
2.1文献筛选结果 初步检索获得相关文献204篇,经筛选最终纳入14个研究,包括1389例患者。文献筛选流程及结果,见图1。
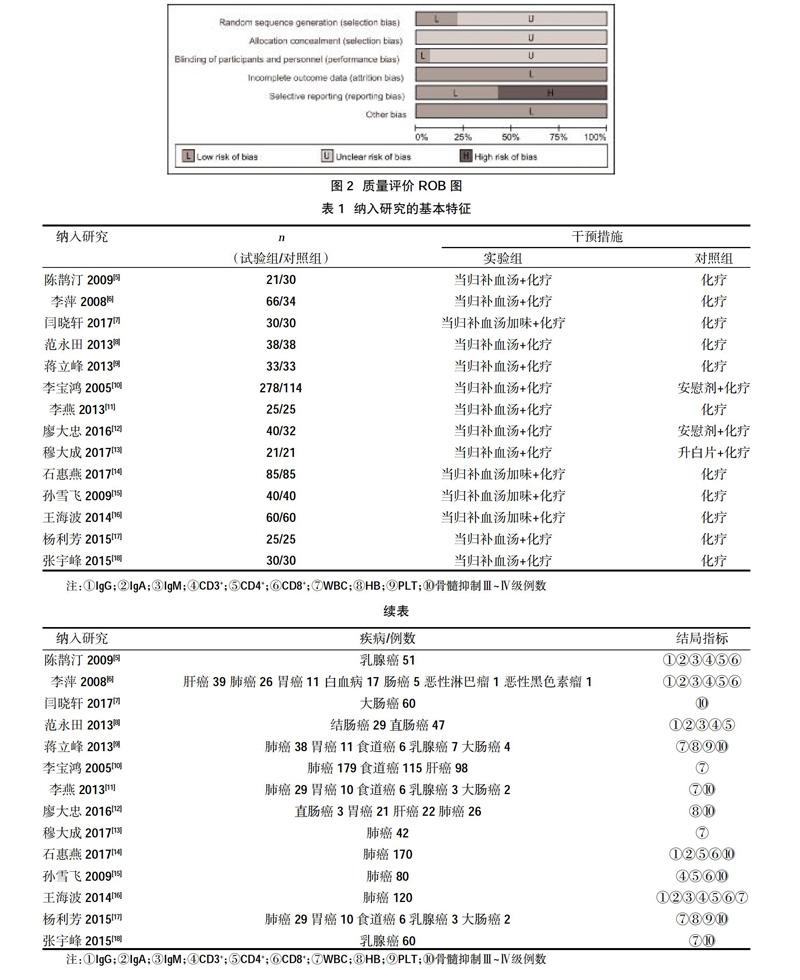
2.2纳入研究的基本特征 报告了主要结局指标的文献有8篇,占比44%。有4篇文献报告了随机方法。所有文献均未丢失数据,均具有明确的纳入排除标准、基线资料可比、没有资金支持与利益冲突,纳入研究的基本特征见表1。
2.3方法学质量评价 纳入14篇研究,有4篇[7,8,12,14]研究采用随机数字表法,其余10篇没有写明随机方法。有2篇[10,12]研究采用了双盲,其余12篇没有写明采用何种盲法。所有研究分配隐藏方法均不清楚(unclear)。无失访或退出。有9篇[7,9-13,15,17,18]研究对血细胞、血清免疫球蛋白、T淋巴细胞亚群水平三组结局指标报告不足两组,认为有选择性报告。其他偏倚来源均为无,见图2。
2.4 Meta分析结果
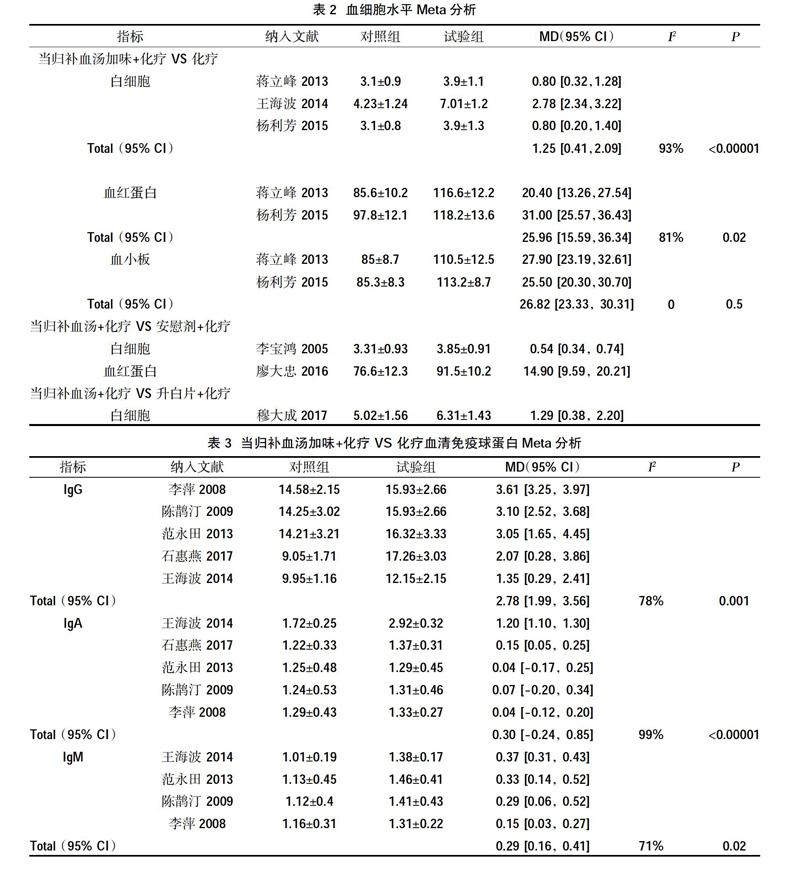
2.4.1血细胞水平分析 共纳入8篇研究[9-13,16-18]。分别对WBC、HB和PLT进行分析。随机效应模型显示当归补血汤加味+化疗对比化疗时,试验组WBC、HB和PLT大于对照组(P<0.05)。当归补血汤+化疗对比安慰剂+化疗时,WBC和HB大于对照组(P<0.05)。当归补血汤+化疗对比升白片+化疗时,WBC增多,见表2。
2.4.2血清免疫球蛋白水平分析 共纳入5篇研究[5,6,8,14,16]。分别对IgG、IgA、IgM水平进行分析。随机效应模型显示试验组的血清免疫球蛋白数目大于对照组(P<0.05),见表3。
2.4.3 T淋巴细胞亚群水平 共纳入6个研究[5,6,8,14,15,16]。分别对CD3+、CD4+、CD8+水平进行分析。随机效应模型显示试验组CD3+、CD4+细胞数目大于对照组(P<0.05)。CD8+细胞数目小于对照组(P<0.05),見表4。
2.5安全性评价 化疗治疗均伴有头昏、乏力、心悸等不良事件。有5个[7,9,11,17,18]研究报道了骨髓抑制度,随机效应模型显示当归补血汤加味+化疗对比化疗时,试验组的Ⅲ度和Ⅳ度的患者例数小于对照组(P<0.05),见表5。
2.6发表偏倚 每个结局指标下纳入的文章均不足10篇,因此不适宜用到漏斗图进行发表偏倚的评价。
3讨论
中医治疗肿瘤的原则以扶正为主,攻邪为辅,药物补肾健脾,益气补血,滋阴生津,兼以抗肿瘤药物治疗,是我国特有的治疗手段。以往治疗多为延长患者生存期,忽略了其治疗期间的生活质量。当归补血汤中黄芪健脾益气,当归养血活血,有助于改善患者生活质量。当归补血汤的现代研究表明,其有效成分为黄芪中所含黄芪甲苷、毛蕊异黄酮、芒柄花素、黄芪多糖和当归中所含阿魏酸、当归多糖、藁本内酯等[19]。阿魏酸与黄芪甲苷为促进造血与提高免疫的重要代表性成分[20]。当归多糖和黄芪多糖有抗肿瘤功效,可提高机体的免疫功能,增强机体的抗癌能力。当归补血汤联合化疗进行治疗可以减轻患者骨髓抑制度,保护脏器,减少恶心、呕吐、脱发[21],提高患者生活质量。可以成为预防和辅助治疗的优选药物,是优良的无毒性的免疫活化剂。
本研究发现使用当归补血汤联合化疗治疗能够增加患者的血细胞数量,提高机体抗氧化、抗血小板聚集等功能,刺激造血多能干细胞与造血主细胞的增殖分化,经过治疗后各项指标均由偏低达到正常。当归补血汤还可以增加机体血清免疫球蛋白数量,从而提高机体体液免疫水平。机体维持正常的免疫功能状态主要体现在T淋巴细胞亚群维持一定的比例上。恶性肿瘤会分泌因子使机体T淋巴细胞亚群数目发生紊乱,从而导致免疫反应下降。CD4+/CD8+比值降低则意味机体处于免疫抑制状态[22]。研究数据表明使用当归补血汤治疗后CD3+水平提高,CD4+/CD8+比值增大,免疫细胞数量增多并处于平衡状态,改善机体吞噬功能[23],有助于免疫功能的恢复。现用化疗药物大多有骨髓抑制的副作用,只是程度深浅不同。研究数据表明使用当归补血汤能够提高骨髓血细胞前体活性,骨髓造血等生化功能也随之提高,骨髓抑制Ⅲ度和Ⅳ度的病人明显减少。
本文由于纳入文献的样本量均较小,方法学质量偏低,仍需要更大规模的设计严谨的前瞻性随机对照双盲试验进一步证实当归补血汤可以减轻化疗不良反应。研究发现数据结果异质性较高,I2>75%,查找异质性来源为所研究的肿瘤类型不同,所用化疗药治疗不同,治疗时间不同,治疗所用当归补血汤药物比例不同,当归补血汤或有少量加味。但本文主要探讨发现当归补血汤治疗肿瘤化疗不良反应的疗效和趋势,所以仍进行合并分组研究。
目前,国内在当归补血汤抗肿瘤临床广泛应用,但科学实验研究并不多。未来应进行对更多双盲双模拟试验进行研究分析,也可对同一肿瘤疾病进行亚组分析,探讨当归黄芪不同比例时产生的差异。为肿瘤治疗的方案设计提供新思路。伴随着精准医疗、转化医疗的迅速发展,治疗思路从过去的单一放化疗发展向个体化的综合治疗。综上,当归补血汤可以减少肿瘤化疗不良反应,优势明显且安全性高。
参考文献:
[1]曾新颖,李镒冲,刘世炜, 等.1990—2015年中国四类慢性病早死概率与“健康中国2030”下降目标分析[J].中华预防医学杂志,2017,51(3):209-214.
[2]陈万青,孙可欣,郑荣寿,等.2014年中国分地区恶性肿瘤发病和死亡分析[J].中国肿瘤,2018,27(1):1-14.
[3]潘睿.中国慢性病前瞻性研究队列恶性肿瘤发病与死亡分析[D].南京医科大学,2017.
[4]周向明,周昕,李毅民.当归补血汤的研究进展[J].世界中医药,2013,8(6):705-707.
[5]陈鹊汀,刘智勤,朱惠学,等.当归补血汤对乳腺癌术后化疗患者免疫功能的影响[J].时珍国医国药, 2009,20(5):1207-1208.
[6]李萍,吴华.当归补血汤加味治疗化疗后白细胞减少症66例[J].陕西中医,2008(8):951-952.
[7]闫晓轩.当归补血汤加味对大肠癌术后化疗减毒增效作用的临床研究[J].四川中医,2017,35(2):94- 96.
[8]范永田,李德川,徐新亚.当归补血汤联合化疗对中晚期大肠癌术后患者免疫功能的影响[J].中华中医药学刊,2013,31(12):2843-2844.
[9]蒋立峰,刘怀民.当归补血汤防治肿瘤化疗后骨髓抑制临床观察[J].中医学报,2013,28(4):475-477.
[10]李宝鸿,廉南.加味当归补血汤对肿瘤患者放化疗增效减毒作用的临床观察附:392例病例报告[J].成都中医药大学学报,2005,28(2):7-9.
[11]李燕.当归补血汤防治肿瘤化疗后骨髓抑制的临床探讨[J].中国医药科学,2013,3(18):110-111.
[12]廖大忠,李静,鲁光洪,等.加味当归补血汤治疗肿瘤相关性贫血72例临床观察[J].四川中医,2016,34 (1):81-83.
[13]穆大成.探究加味当归补血汤治疗肺鳞癌化疗后白细胞减少的效果[J].内蒙古中医药,2017,36(14):23.
[14]石惠燕,张凌燕,田义洲,等.加味当归补血汤对中晚期非小细胞肺癌化疗患者免疫功能及生活质量的影响[J].新中医,2017,49(3):106-108.
[15]孙雪飞,陈景寒,孟龙,等.当归补血汤Ⅰ号在非小细胞肺癌术前BAI化疗中的作用[J].山东大学学报(医学版),2006,44(3):280-282.
[16]王海波,陈鹊汀,李鹤飞,等.当归补血汤对中晚期肺癌化疗后免疫功能的影响[J].中医学报,2014,29(11):1553-1554.
[17]杨利芳.针对肿瘤患者应用当归补血汤对骨髓抑制的预防效果观察[J].世界最新医学信息文摘,2015, 15(14):99-100.
[18]张宇峰,付培亭,刘秀宝,等.当归补血汤联合重组人粒细胞刺激因子防治乳腺癌化疗后骨髓抑制效果观察[J].临床合理用药杂志,2015,8(28):8-10.
[19]王艳杰,康芯荣,张雨薇,等.当归补血汤抗肿瘤作用研究进展[J].中国医学装备,2017,14(8):165- 169.
[20]寿迪文,马伟斌.当归补血汤的不同配比对黄芪甲苷、阿魏酸及芒柄花素含量的影响[J].新中医,2016, 48(6):274-276.
[21]黄朝忠,刘智,苏颖.当归补血汤对肿瘤化疗增效减毒作用的研究进展[J].吉林中医药,2014,34(9):962-964.
[22]严健,原永明,张舒,等.CD3+、CD4+、CD8+T淋巴细胞亚群在肿瘤患者外周血中检测的临床意义[J].检验医学,2013,28(10):901-903.
[23]王倩,侯改云.當归补血汤联合西药治疗对大肠癌术后细胞免疫功能及生存质量的影响[J].现代中西医结合杂志,2016,25(30):3339-3341.
收稿日期:2018-10-18;修回日期:2018-11-05
编辑/肖婷婷

