基于RCOO-+N(CH3)3R’型两性树脂法的MDEA溶液离子净化研究
郑金欣,沈紫薇,郭宏垚,苗正朋,李稳宏,李冬
(西北大学 化工学院,陕西 西安 710069)
天然气中所含CO2、H2S等酸性气体需净化处理才能达标[1-2],常采用胺液净化[3-4]。其中累积的阴阳离子及重烃组分严重影响胺液吸附能力,加剧了胺液降解、发泡及腐蚀[5],胺液中含有的缓蚀剂和固体颗粒等物质,使胺液在脱硫过程中形成泡沫,加重胺损失,严重影响脱硫系统正常运行[6-7]。范峥[8]、王军峰[9]、 徐飞[10]等探究了影响胺液失效的离子成分。胺液变质生成热稳定盐引起设备腐蚀、系统能耗增加等问题[11]。文献[12]介绍了OH-交换去除热稳定盐阴离子。文献主要见电渗析法,该方法成本较高,处理量小。基于单一交换树脂存在的弊端,我们提出两性离子交换树脂法深度净化劣化胺液。
1 实验部分
1.1 试剂与仪器
二氯甲烷、1,4-二氯甲氧基丁烷(BCMB)、无水氯化锌、丙酮、盐酸、丙烯酸、过硫酸钾、碳酸钠等均为分析纯;NKA-9树脂、XAD-2树脂均为工业品。
SFT-1004恒温加热磁力搅拌器;YT-0618真空抽滤装置;FTIR-650红外光谱仪;3H-2000PS2比表面积及孔径分析仪;LC-6微机盐含量测定仪;TMZ9-IC1000离子色谱仪。
1.2 两性树脂制备
以悬浮聚合法制备聚苯乙烯树脂微球(PS-1)[13],筛选35~45目的树脂微球,对其氯甲基化和胺基化,形成强碱型树脂(PS-2),然后与丙烯酸互贯聚合,得到强碱弱酸型两性交换树脂(PS-3)。
1.2.1 氯甲基化的聚苯乙烯微球制备 取80 g聚苯乙烯树脂微球PS-1、500 mL溶胀剂二氯甲烷、150 mL氯甲基化试剂1,4-二氯甲氧基丁烷(BCMB)于1 000 mL三口烧瓶中,静置溶胀8 h。在磁力搅拌下,分批加入10 g无水氯化锌,30 ℃下反应12 h。抽滤,用丙酮溶剂提取12 h,55 ℃真空干燥10 h,即得到氯甲基化的聚苯乙烯微球[14]。
1.2.2 强碱型交换树脂(PS-2)制备 取50 g氯甲基化聚苯乙烯微球置于1 000 mL三口烧瓶,在搅拌下依次加入600 mL二氯乙烷和一定浓度的三甲胺水溶液,再加入6 g无水氯化锌,在70 ℃下反应5 h后升温至95 ℃下反应10 h。冷却至30 ℃后,过滤,聚合物置于含有质量分数1% HCl的200 mL丙酮溶液中,搅拌1.5 h后过滤,再用丙酮提取12 h,55 ℃真空干燥10 h,得到胺基化树脂微球,即强碱型交换树脂(PS-2)。
1.2.3 强碱弱酸型两性交换树脂(PS-3)制备 取40 g强碱型交换树脂PS-2、20 mL超纯蒸馏水、10 mL 精制丙烯酸和200 g过硫酸钾,在80 ℃氮气气氛下反应10 h。加入10%Na2CO3溶液,将pH降至7。先抽滤,再丙酮提取12 h,最后在55 ℃下真空干燥10 h,得到羧基化-氨基化树脂微球,即强碱弱酸型两性树脂(PS-3)。
1.3 树脂等温吸附实验
分别配制以FeCl3、CaCl2、NaCl、Na2SO4和Na2C2O4为溶质的MDEA溶液,在pH为8,树脂用量为1 g树脂/30 mL胺液,吸附时间24 h,吸附温度298 K的条件下,用LC-6微机盐含量测定仪和TMZ9-IC1000离子色谱仪分别测定其在不同初始浓度c0条件下各离子的平衡吸附浓度ce。
1.4 吸附动力学与热力学
分别配制初始浓度0.1 mol/L的FeCl3和Na2C2O4的溶液,在温度为298 K的条件下,加入树脂用量为1 g干树脂/30 mL溶液,吸附一定时间,计算吸附量qt,并求解树脂吸附各离子过程的热力学参数,包括焓变ΔH、Gibbs自由能变ΔG和熵变ΔS。
配制含有不同初始浓度的FeCl3和Na2C2O4的溶液,分别在温度298,308,318 K条件下,吸附24 h后测定其平衡浓度ce。
2 结果与讨论
2.1 树脂表征
2.1.1 交换容量[15]分别测定两性交换树脂PS-3的总氢交换容量UH和总氯交换容量UCl,结果见表1。

表1 两性交换树脂PS-3的交换容量Table 1 Exchange capacity of amphotericion-exchange resin(PS-3)
由表1可知,UH≈UCl,表明树脂中两性基团含量基本相等,该树脂对阴阳离子的吸附容量相当。
2.1.2 孔结构与比表面积 分别以BJH法和BET法测定PS系列树脂的孔径分布与比表面积,结果见表2,其N2-吸/脱附曲线图见图1。
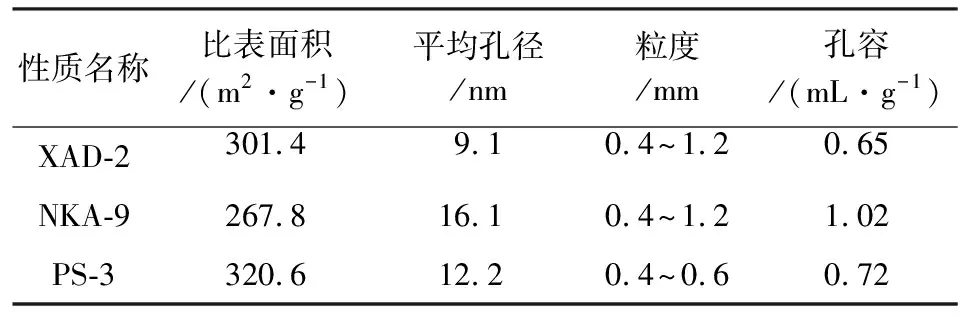
表2 PS-3与NKA-9及XAD-2的结构性质Table 2 Exchange capacity of amphoteric exchange resin
由表2可知,3种树脂的平均孔径依次为9.1,16.1,12.2 nm,均是以中孔(5~50 nm)为主。PS-3具有比XAD-2和NKA-9较高的比表面积。这与致孔剂的种类以及加量有密切关系。
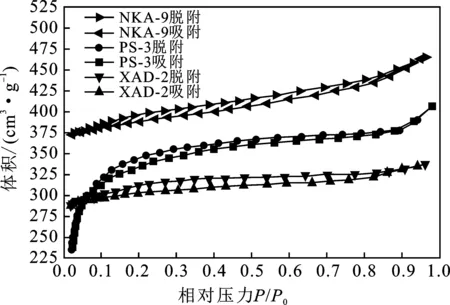
图1 PS-3、NKA-9与XAD-2的N2-吸附/脱附曲线Fig.1 N2-adsorption/desorption isotherms of PS-3,NKA-9 and XAD-2
由图1可知,随相对压力提高,各树脂对N2的吸附量未明显增大,且在脱附时均出现回滞环,这说明3种树脂在吸附过程中存在毛细凝聚现象,其孔结构均以中孔为主。此外,NKA-9和PS-3高压(P/P0>0.9)条件下,N2吸附量斜率增大,这表明该树脂内部可能出现颗粒的不均匀堆积,且有少量的大孔产生。
2.1.3 红外光谱 将干燥的树脂研磨成粉末与KBr混合压片,采用红外光谱仪分别测定PS-1、PS-2和PS-3树脂的分子结构,结果见图2。
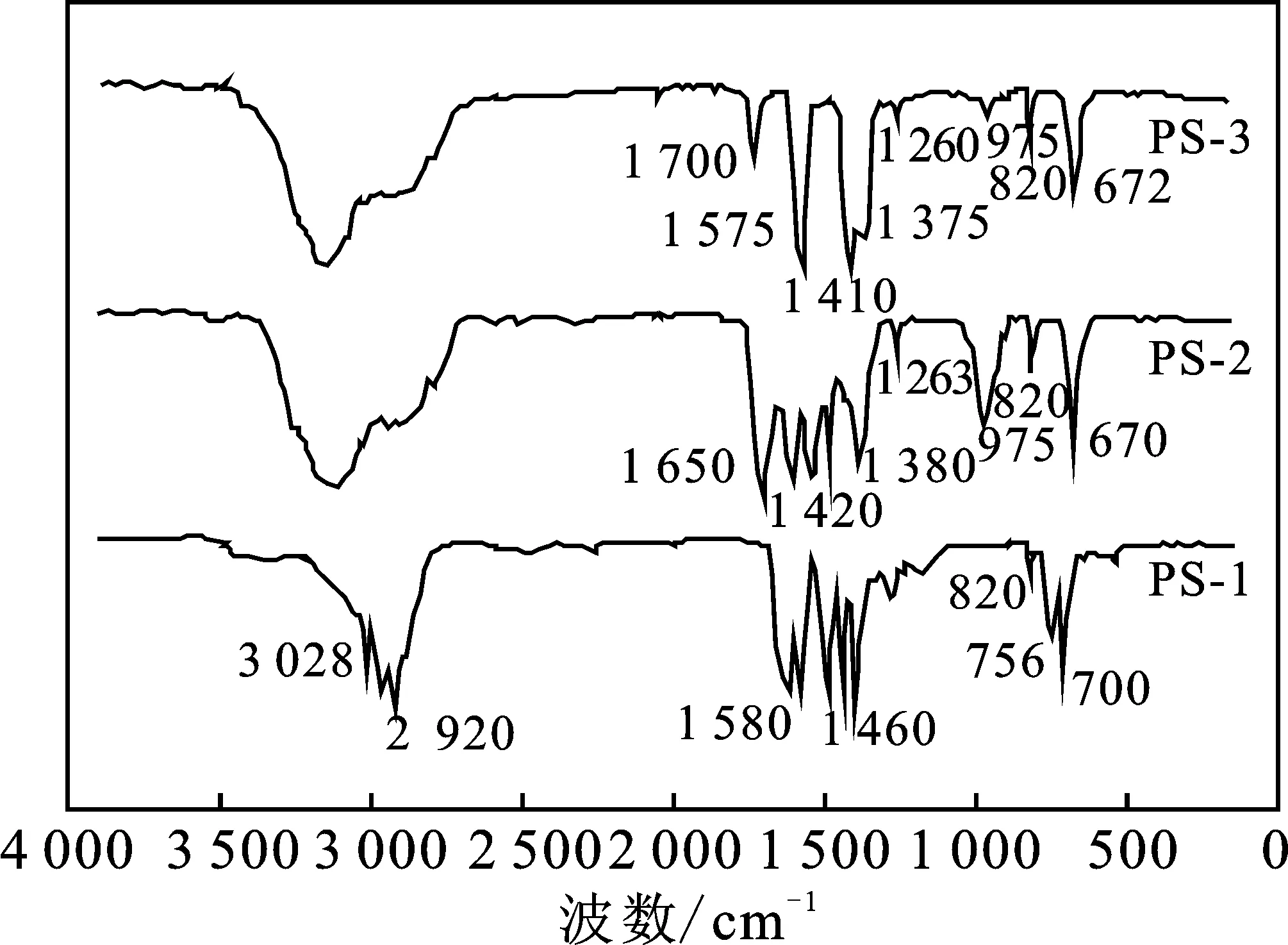
图2 PS系列树脂的红外光谱图Fig.2 FTIR spectra of resin series
由图2可知,PS-1在3 028,700 cm-1为苯环C—H伸缩振动和面内弯曲振动峰,1 580~1 460 cm-1为聚苯乙烯苯环骨架的振动峰,756,2 920 cm-1分别为—CH2—摇摆振动峰和不对称伸缩振动峰,这表明聚苯乙烯微球已成功制备。

PS-3的1 575,1 410 cm-1是RCOO(CH3)3NR’的特征峰,分别为—COO-的反对称和对称伸缩振动峰,1 700 cm-1为残余 —COOH峰且975 cm-1的+N(CH3)3峰明显减弱,这表明强碱弱酸型[RCOO-+N(CH3)3R’]两性交换树脂已成功制备。
2.2 等温吸附线
298 K下胺液中阴离子在两性树脂PS-3上的吸附等温线见图3。

图3 298 K下胺液中阴离子在两性树脂PS-3上的吸附等温线Fig.3 The adsorption isotherm of the anion in the amphoteric resin PS-3 at 298 K
由图3可知,随平衡浓度的增大,各类离子在两性树脂上的吸附量也增加,最终平衡吸附量趋于某一定值附近。这是由于随着各离子浓度的增大,溶液中有更多的可被吸附的离子,因而其平衡吸附量也增加,当浓度增大至某一值时,在该条件下的平衡吸附量已达到极值,因而吸附量又趋于平缓。
分别选择Langmuir模型和Freundlich模型对上述吸附数据进行拟合,结果见表3。

表3 298 K下各离子吸附等温方程拟合结果Table 3 Fitting of adsorption isotherm equation of ions at 298 K
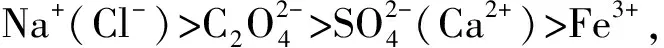

2.3 吸附动力学
吸附过程可分为内、外扩散两部分。当外扩散为吸附速率的控制步骤时,颗粒内的传质阻力即可忽略,可采用Lagergren拟一级或二级动力学方程来研究。
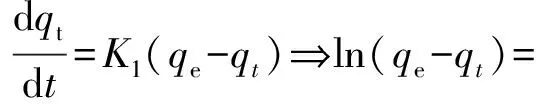
lnqe-K1t

式中qe——平衡吸附量,mmol/g干;
t——吸附时间,min;
qt——t时刻的吸附量,mmol/g干;
K1,K2——拟一级和二级速率常数,min-1和g干/(mmol·min)。
大部分吸附是内外扩散共同控制的,但也有主次之分。当主要控制步骤为内扩散时,可利用Kannan-Sundaram模型来拟合。


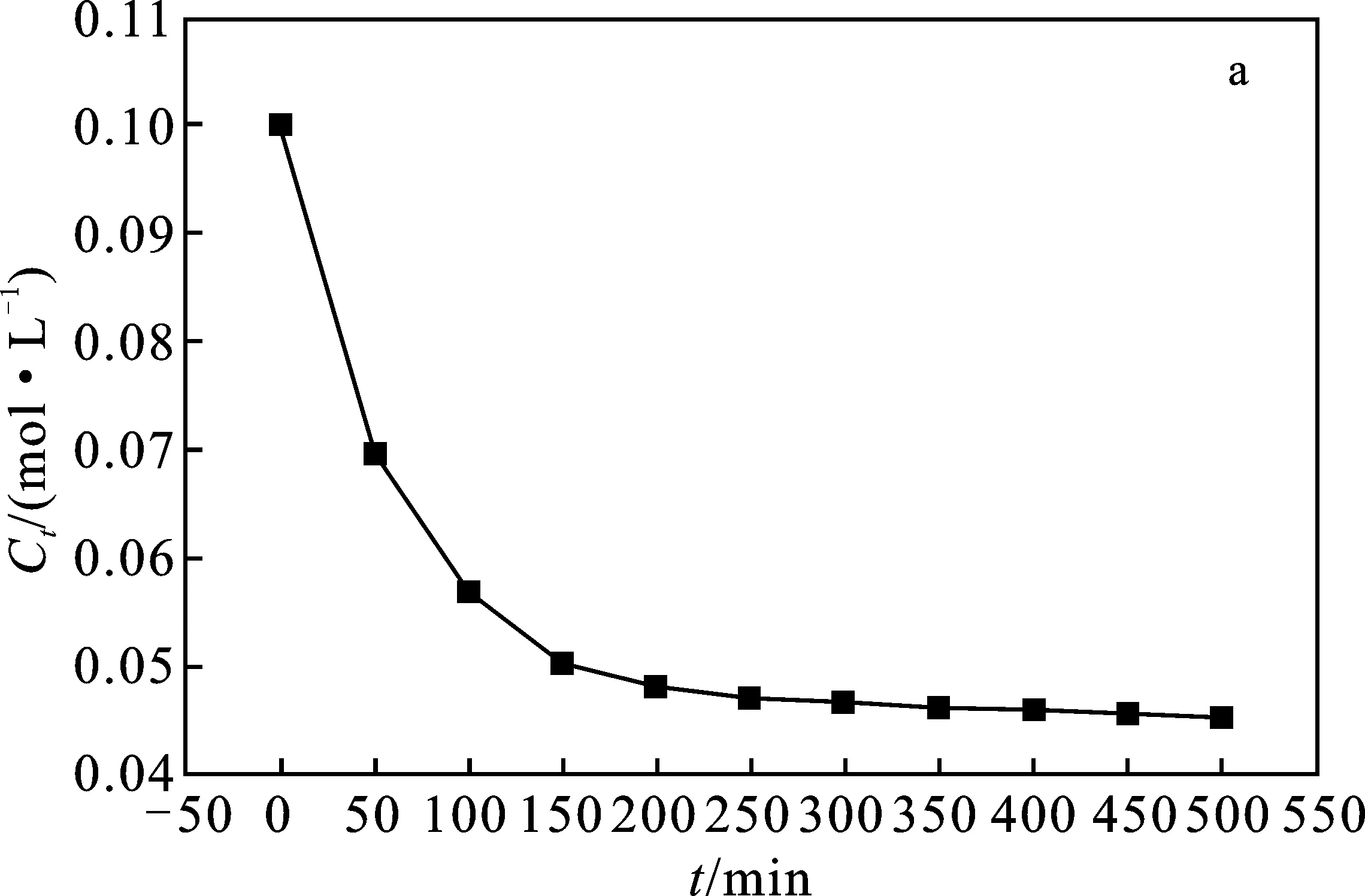
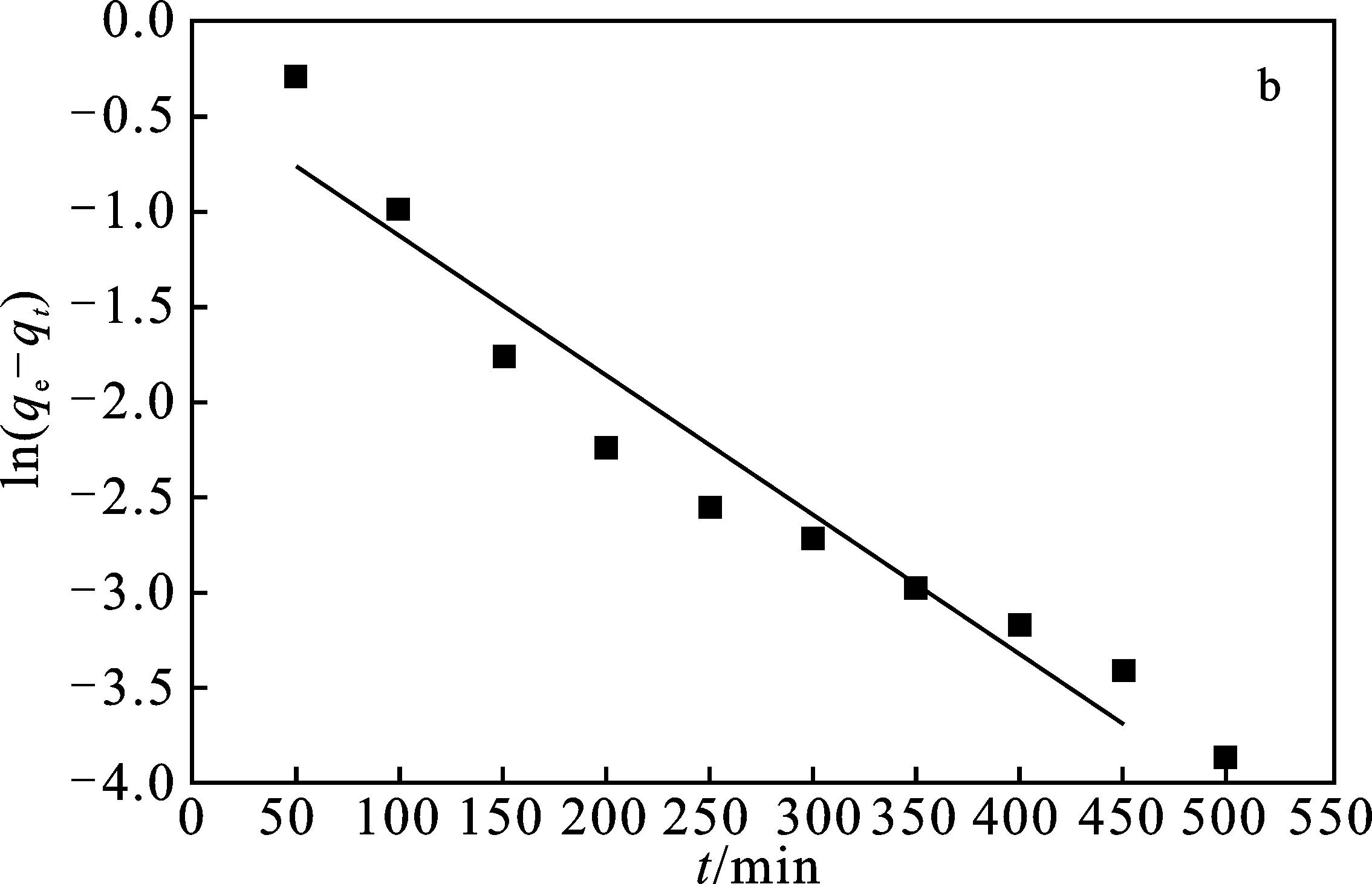

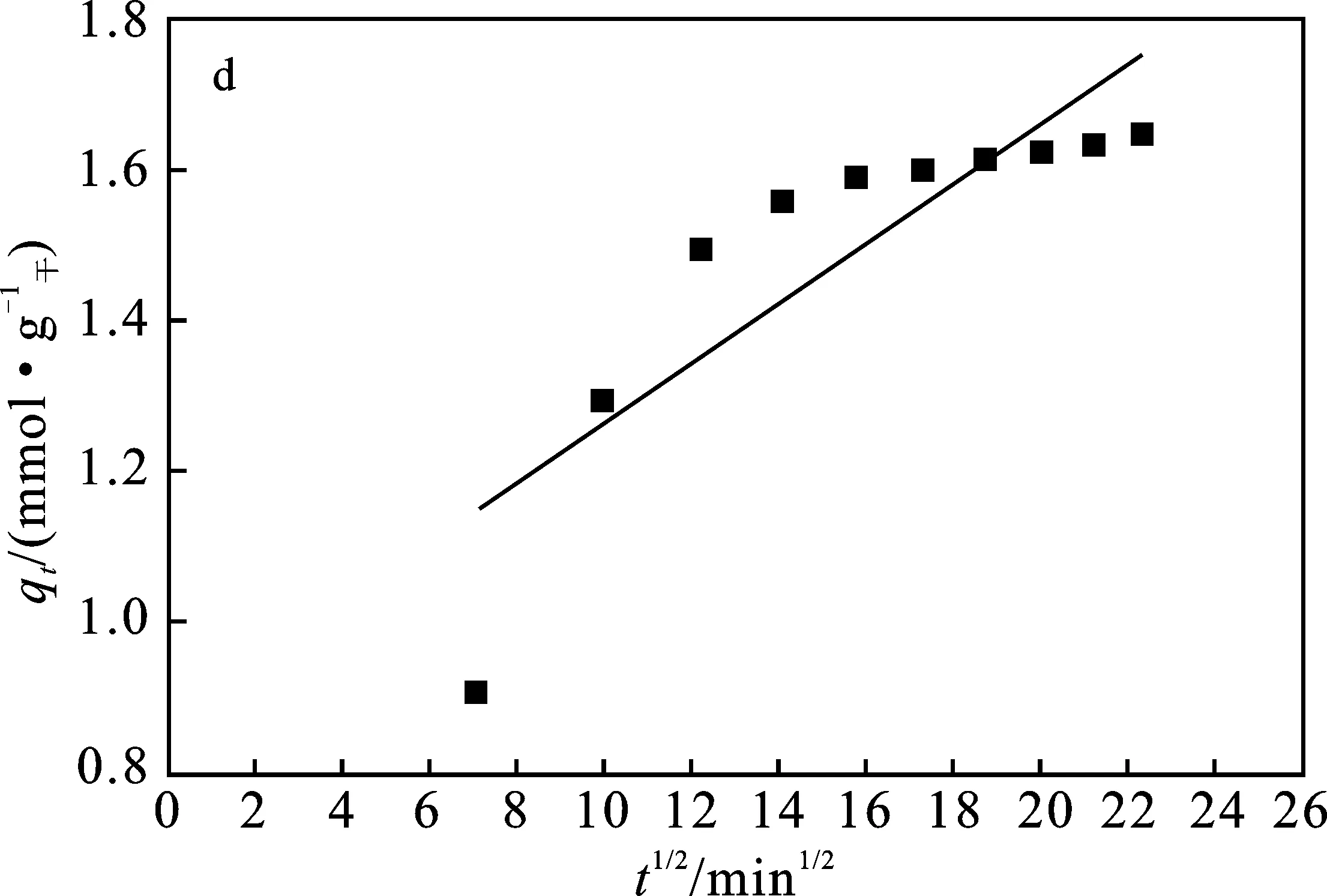
图4 298 K下不同模型Fe3+的吸附动力学拟合曲线图Fig.4 Fitting of adsorption isotherm of Fe3+ at 298 K under different modelsa.溶液中Fe3+浓度与时间关系; b.Lagergren拟一级动力学方程ln(qe-qt);c.Lagergren拟二级动力学方程t/qt-t; d.Kannan-Sundaram动力学方程qt-t1/2
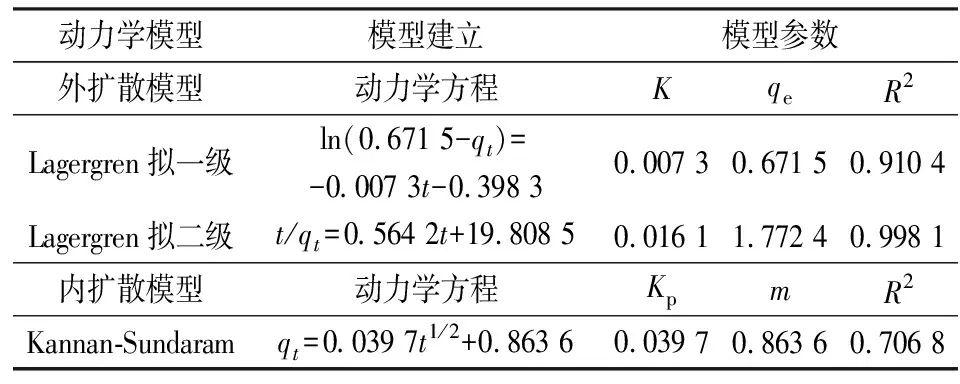
表4 298 K下不同模型Fe3+的吸附动力学参数Table 4 Adsorption isotherm parameters of Fe3+ at298 K under different models
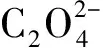
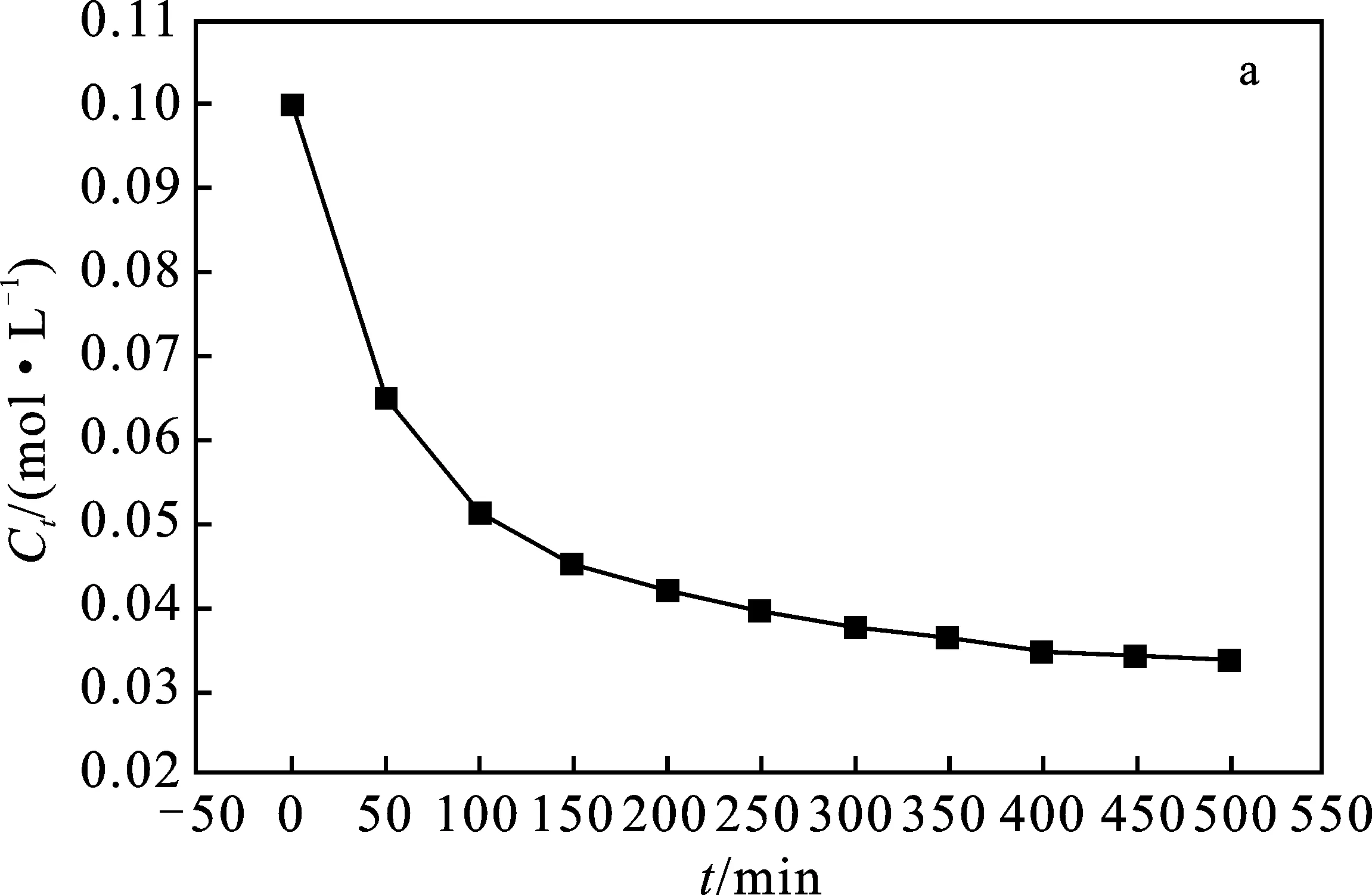

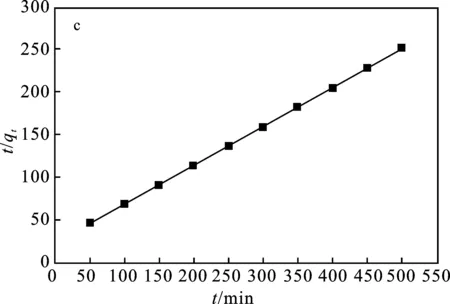

图5 298 K下不同模型的吸附动力学拟合曲线图Fig.5 Fitting of adsorption isotherm of at 298 K under different modelsa.溶液中浓度与时间关系; b.Lagergren拟一级动力学方程ln(qe-qt); c.Lagergren拟二级动力学方程t/qt-t; d.Kannan-Sundaram动力学方程qt-t1/2
2.4 吸附热力学
某一定值吸附量qe所对应的焓变为等量吸附焓变ΔH,反映吸附剂与吸附质分子或溶剂间作用力大小。吸附自由能变ΔG是判定吸附自发可能性的热力学参数,吸附熵变ΔS是判定体系混乱程度的热力学参数。分别采用Clausius-Clapeyron、Gibbs和Gibbs-Helmholtz方程式计算:
ΔG=-RTlnkD
其中,Ce为在特定吸附量qe下吸附平衡时离子浓度,mol/L;k0为常数;kD为分配系数,可通过kD=qe/Ce计算出kD,单位为mL/g干。
对lnCe-1/T进行作图,其结果见图6、图7和表6、表7。

图6 不同初始浓度下的Fe3+的焓变拟合图Fig.6 Fitting of Fe3+ enthalpy changes under different initial concentration
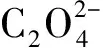
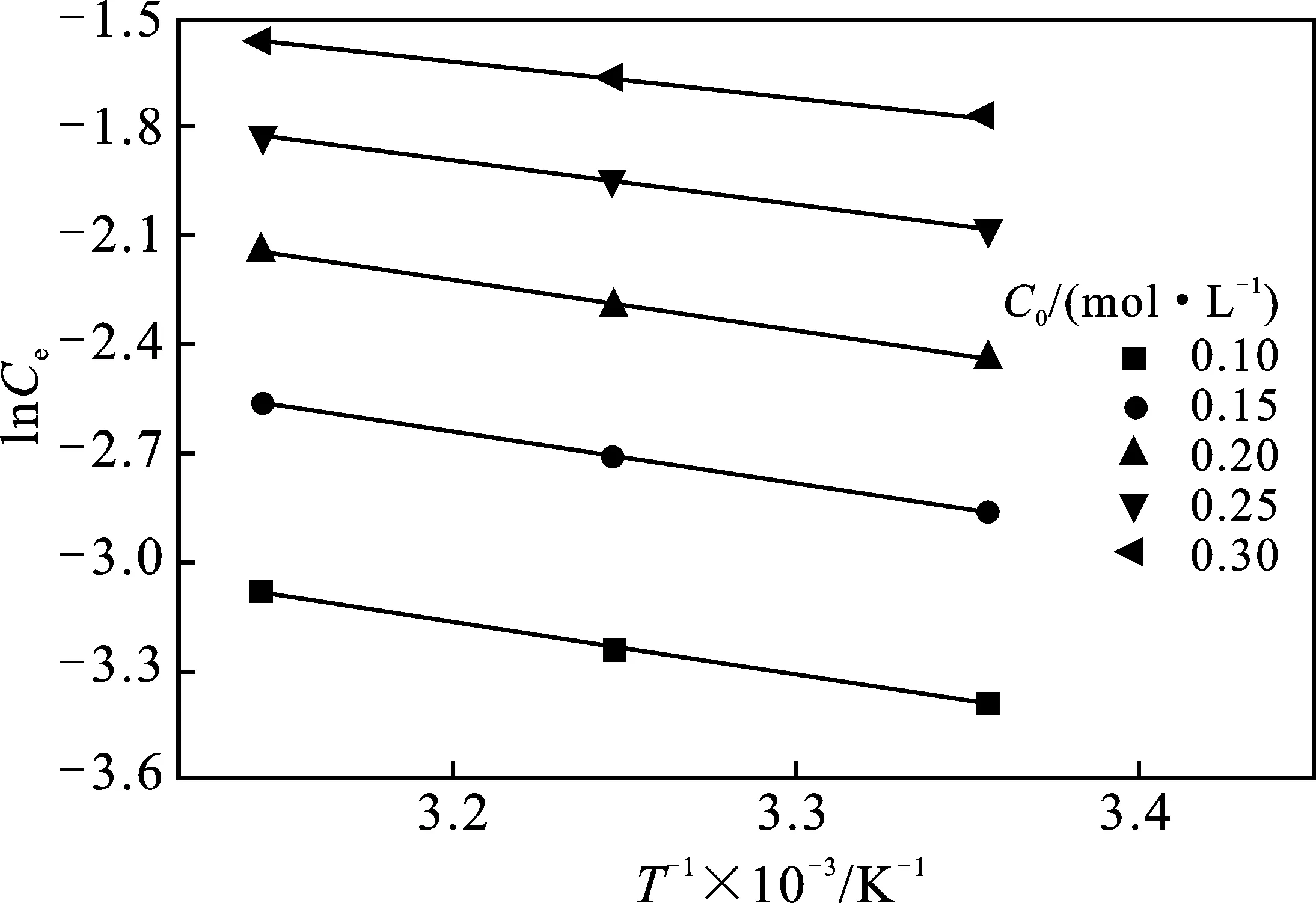
图7 不同初始浓度下的的焓变拟合图Fig.7 Fitting of enthalpy changes under different initial concentration
3 结论
(1)制备的RCOO-+N(CH3)3R’型两性树脂具有较高的比表面积和介孔结构,两性基团含量相等,总交换容量约为10.25 mmol/g。
(2)两性树脂上的离子吸附行为符合Langmuir模型,是以内盐键为主要吸附位点等当量的吸附阴阳离子,且对高价离子和有机酸根离子具有更高的吸附选择性。
(3)Fe3+和C2O42-的吸附为焓变ΔH均不低于-20 kJ/mol的放热过程,该吸附过程中体系混乱度减小,可自发进行,且低温更有利于离子吸附。
(4)Fe3+和C2O42-在两性树脂上的吸附行为符合以外扩散为控制步骤的Lagergren拟二级吸附模型。

表6 不同初始浓度下的Fe3+和的焓变求解拟合参数Table 6 Fitting parameters of Fe3+ and enthalpy changes under different initial concentration
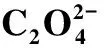
表7 不同初始浓度下的Fe3+和吸附热力学参数Table 7 Thermodynamic parameters under different Fe3+ and initial concentration

