中国西部地区泡型、囊型包虫病手术治疗方式与术后并发症的回顾性分析
苟 平, 王志鑫, 胡陈亮, 付世强, 樊海宁, 王海久
(青海大学附属医院 肝胆胰外科, 青海 西宁, 810000)
包虫病是流行于畜牧业发达地区的常见的人畜共患性寄生虫病,中国西部属高发地区,只发现有泡型(AE)和囊型(CE)感染。温浩等[1]曾报道,包虫病的患病率以CE较为常见,人接触或摄取被六钩蚴污染的水或食物而被感染,蚴虫通过胃肠道途径侵入门静脉系统,大部分停留在肝脏,少数进入肺及其他器官[2]。约70%的AE发生于肝右叶并造成严重损害, 40%可合并肝门部结构受侵[3]。本研究回顾性分析中国西部地区手术治疗肝包虫病相关报道及术后并发症的发生状况,现将结果报告如下。
1 资料与方法
1.1 一般资料
以“肝包虫病”“手术”“胆漏”“并发症”为关键词,在中国知网(CNKI)、万方、维普数据库中检索近1997—2017年中国西部地区(新疆维吾尔自治区、青海、西藏自治区、甘肃、宁夏回族自治区、内蒙古自治区、四川等)各中心(包括州/县、市、省级及地区级医院)有关手术治疗肝泡型、囊型包虫病的相关报道,对其中符合本研究分析目的者进行筛选(去除重复报道,同一时期报道以病例数多者为主,例数相近以近期报道为主),搜集并整理。
1.2 分析方法

2 结 果
共纳入1997—2017年中国西部地区32家中心手术治疗肝包虫病的相关报道38篇(去除重复报道、重要信息不全者后共34篇)。其中, AE 349例,为4家中心发表的共5篇报道所得,见表1; CE 3 658例,为近30家中心发表的共30篇报道所得,见表2。
*为第一作者所在医疗机构名称。
分析肝泡型、囊型包虫病术后主要并发症,结果显示胆漏、出血、黄疸、复发等并发症发生率的差异有统计学意义(P<0.05), 感染发生率的差异无统计学意义(P>0.05)。过敏为囊型特有,未进行比较。见表3。
肝泡型包虫病(HAE)共349例,年龄(36.9±1.8)岁。依据资料显示,手术方式可分为原位肝移植、根治性肝切除、姑息性肝切除及介入外引流,以及离体肝切除+自体肝移植。术后发生的并发症主要为胆漏、出血、感染、梗阻性黄疸、复发。不同手术患者术后并发症发生率比较,差异有统计学意义(P<0.05)。见表4。
肝囊型包虫病(HCE)共3 658例,年龄(37.8±1.4)岁。依据资料显示,手术方式可分为内囊摘除术、内囊摘除+外囊次全切除术、外囊完整剥除术、肝部分切除术、穿刺引流及硬化术。术后发生的并发症主要为胆漏、出血、感染、黄疸、过敏、复发。不同手术患者并发症发生率比较,差异无统计学意义(P>0.05)。见表5。此外,除6例中转开腹手术患者外,还有340例患者在腹腔镜下完成手术,术后主要并发症为胆漏、出血、感染、过敏、复发,未见梗阻性黄疸病例。见表6。
3 讨 论
根治性肝切除是HAE的首选手术治疗方式[38],其依据“无瘤原则”,能完整切除病灶组织,明显降低术后复发及转移率,有效改善预后。然而,肝切除术在带来较大获益的同时,也易引发各种术后并发症,胆漏就是最常见的一种。根据国际肝脏外科研究组(ISGLS)提出的胆漏标准[39],其被定义为术后第3天或3 d以后引流物中胆红素浓度至少3倍于同时期血清胆红素浓度。按严重程度分为A、B、C共3级: A级几乎不影响患者的临床管理及结局,不必进行额外的诊治操作;
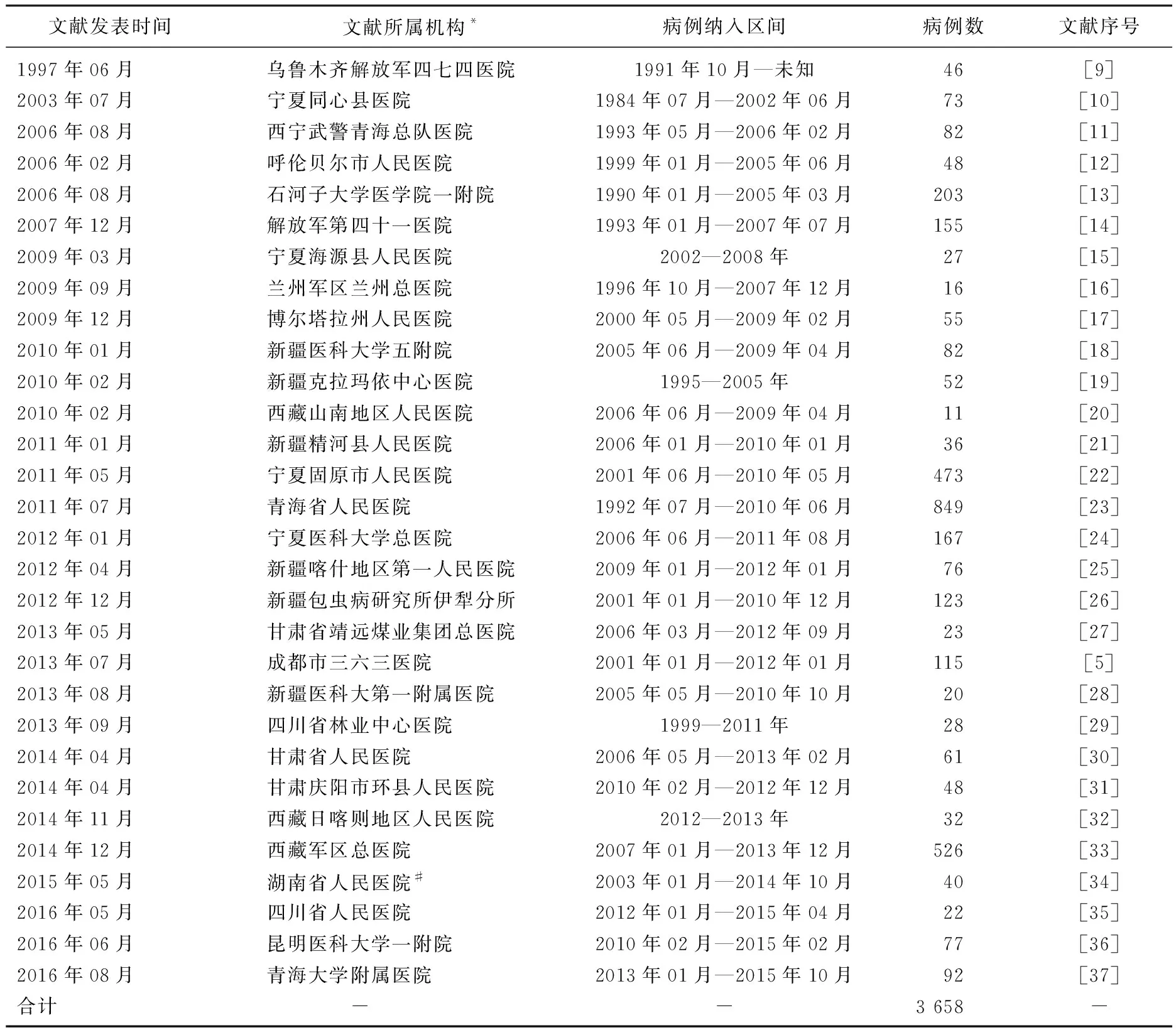
表2 中国西部地区近30家中心手术治疗CE包虫病相关文献数据
*为第一作者所在医疗机构名称; #病例资料来源于吐鲁番地区中心医院。

表3 泡型、囊型包虫病术后主要并发症比较[n(%)]
与CE比较, *P<0.05。
若A级胆漏需要调整临床管理方案,但不至于行再次手术,或A级持续时间超过1周以上则归为B级; C级胆漏则需再次手术以控制病情。温浩等[1]把术后3个月内未自行闭合且引流大于250 mL/d者称为顽固性胆漏。严重胆漏若继发胆汁性腹膜炎、腹腔脓肿等,病死率将明显升高。
肝切除术后胆漏发生率与诸多因素有关。Yang等[40]分析得出,直接胆红素(DBIL)、碱性磷酸酶(ALP)、丙氨酸转氨酶(ALT)及乳酸脱氢酶(LDH)水平是影响AE患者肝切除术后胆漏发生的独立危险因素。LDH由肝脏局部缺血、损伤导致肝细胞死亡后释放入外周血,故高水平LDH可能预示着肝损害程度较重,发生胆漏的可能性亦随之增加。另外,病灶直径大于10.5 cm[41]、术中出血量大于775 mL[42]等也可能是胆漏的危险因素。包虫病灶直径过大,侵犯或压迫重要管道结构,造成术中解剖困难,易损伤重要血管及分支胆管,组织局部缺血概率增大,无疑也会增加胆漏风险。这些影响因素体现了术前充分评估、术中精细操作的重要性。
临床上常在术前或术中发现包虫囊肿破入胆道的情形。本研究中内囊摘除术组术后胆漏发生率最高,其中有部分病例合并胆道侵犯而出现术前胆漏(共424例,占此术式总例数的近23.0%), 与Kilic等[43]报道的发生率(23.5%)近似。术前已合并胆道受侵与术后胆漏高发生率(本研究CE组发生率为15.8%)相比,是否有内在联系尚不得而知。理论上讲,若术中未及时发现并处理已有胆漏,术后胆漏发生率将明显增高。磁共振胰胆管成像(MRCP)、内镜逆行胰胆管造影(ERCP)及经皮肝穿刺胆管造影(PTC)可发现包虫囊肿破入胆道的情况,较超声、电子计算机断层扫描(CT)优势大,这为术前改善肝功能、充分预估术中情况等创造了条件。术中可结合直视或胆道镜观察内囊壁,胆漏试验,经胆囊管残端注入亚甲蓝,疑有包虫囊壁碎片或子囊进入胆道而行胆道探查、造影等方法,以协助术中及时发现胆漏口并予修补,促进漏口闭合,避免因术中遗漏而导致术后胆漏的发生。

表4 不同术式HAE患者术后主要并发症发生情况比较[n(%)]

表5 不同术式HCE患者术后主要并发症发生情况比较[n(%)]

表6 340例腹腔镜模式下HCE手术方式及术后主要并发症情况
胆漏的治疗亦是临床棘手的问题,保持术区通畅引流是防治术后胆漏的首要原则。将术区漏出的胆汁成分充分引流至体外,不仅可有效避免因胆汁积聚造成腹膜炎、腹腔感染等,还可促进术区小胆漏的自然愈合。郑建伟等[33]报道术后以通畅引流为主,辅以生长抑素或其类似物、抗胆碱药物等,可抑制胆汁分泌、降低胆道内压,进而促进胆漏愈合,同时也有降低因术区积液、出血等原因导致感染发生发展的潜在益处。鼻胆管引流、胆道支架及乳头括约肌切开(EST)等是内镜微创治疗胆漏的代表术式,其共同原理是通过降低胆道与肠腔或外界的压力梯度,降低胆道内压,促进胆漏的愈合。此外,针对C级胆漏的治疗,如因大量胆漏导致弥漫性腹膜炎,或每日胆汁引流量达数百毫升等情形,需适时手术探查、干预治疗以改善预后。

