环境因子对中国海矮拟帽贝种群遗传多样性的影响
李媛媛,王珊珊,郭晓雨,崔宇通,王云慧,王儒晓,李钊霞,蔡建平,张运发,曲江勇
(1. 烟台大学生命科学学院,山东烟台 264005; 2. 烟台大学数学与信息科学学院,山东烟台 264005)
生态遗传研究核心问题是探究生物在其分布边界的环境中形态、遗传变异趋势与规律[1-2],环境是种群遗传进化的一个重要因素,物种的分布、行为、生理与遗传分化受环境因子的影响显著[3]。生物形体变异是受环境影响最显著的生理学和生态学特征指标[4],空间尺度上的种内地理变异反映了物种适应当地环境变异趋向[5],贝格曼定律假定寒冷地区的同种体型较温暖地区的更小[6],此理论同时适用于恒温动物[7]和外温动物[8]。研究发现多变量形态度量学方法比传统的形态学分析方法在反映形态差异方面更有效[9],目前在海洋生物生态遗传研究领域上应用广泛[10]。在形态学差异反映种群间的遗传差异基础上,还需结合遗传变异等共同研讨种群遗传分化等问题,PEPIN[11]认为基于形态特征来进行种群的研究必须通过遗传学证据予以进一步证明,通过形态标记、遗传标记来共同阐明种群间的形态与遗传变异、种群间连续或隔离模式以及受环境、气候因子影响的种群分化是目前生态遗传研究的主要方法[11]。生物在适应环境过程中DNA、RNA均会随生态环境而变化,致使形态、遗传产生变异[12]。
DNA序列是可以直接从核苷酸序列上分析遗传变异的遗传标记,目前已广泛用于解决动物生态遗传等问题[13]。动物线粒体DNA (mt DNA)具有分子量小、进化速度快、结构简单、表现为母系遗传等特点,其中细胞色素c氧化酶亚基I (COI)基因突变速度较快且进化速率适中,可用于种群水平的遗传多样性分析[14]。
矮拟帽贝(Patelloidapygmaea)属于软体动物门(Mollusca)笠贝科(Acmaeidae)[15],中国海沿岸习见种。该种普遍分布于海岸带以上到浅层潮下带的整个潮间带,营附着生活,适宜生存的环境因子跨度大,受古地理历史事件及现今环境、气候因子影响明显,是研究种群生态遗传的模式物种[16-18]。目前矮拟帽贝研究主要集中在系统学和分类学等领域[19],对现今环境因子影响的遗传进化和形态变异并未得到进一步的研究[20]。本研究选取矮拟帽贝线粒体基因COI序列作为分子标记,探究环境因子对矮拟帽贝遗传多样性的影响,以期对中国海矮拟帽贝种群遗传多样性研究提供参考。
1 材料与方法
1.1 采样及测序
矮拟帽贝采集于中国海13个地域137个个体(图1),于无水乙醇中保存;并测量其形态量度[壳长(length,L)、壳宽(width,W)、壳高(height,H)、壳周长(perimeter,P)、短斜边(short hypotenuse,SH)、长斜边(long hypotenuse,LH)、干重(dry weight,DW)、壁厚(wall thickness,WT)]并计算头端角度(headend angle,HA)与尾端角度(end angle,EA)(表1,部分形态数据参考之前已发表论文[21])。
总DNA提取采用DNeasy®组织&血液试剂盒(GTIN:04053228006077,Lot:151046088,GIAGEN,德国)。使用COI通用引物进行PCR扩增(华大基因合成),COIForward:5-GGTCAACAAATCATAAAGATATTGG-3;COIReverse:5-TAAACTTCAGGGTGACCAAAAAATCA-3[22],25 μL的PCR扩增反应体系。PCR反应条件设置:94°C预变性2 min;94°C变性30 s,42°C退火40 s,72°C延伸50 s,35个循环;72°C延伸5 min。反应结束后利用琼脂糖凝胶电泳进行检测。PCR产物进行ABI PRIMS 3730双向测序。
1.2 环境因子
获取采样地近30年气象数据[年平均气压(annual average pressure,AAP)、年平均气温(annual average temperature,AAT)、年平均降水量(annual average precipitation,AAPR)、日照百分率(sunshine percentage,SP)、日照时数(sunshine hours,SS)、年平均水汽压(annual average vapor pressure,AAVR)]并计算各因子变异系数[年平均气压变异系数(annual average pressure variation coefficient,VAAP)、年平均气温变异系数(annual average temperature variation coefficient,VAAT)、年平均降水量变异系数(annual average precipitation variation coefficient,VAAPR)、日照百分率变异系数(sunshine percentage variation coefficient,VCSP)、日照时数变异系数(sunshine hours variation coefficient,VCSS)、年平均水汽压变异系数(annual average vapor pressure variation coefficient,VAAVR)],数据来源中国气象数据共享服务网(http://data.cma.cn/)并参考已发表论文[21]及各地的经度(longitude,LO)和维度(latitude,LA)。
1.3 统计分析
为排除个体生长周期等因素对研究结果的影响,以样本干重为基数换算各形态量度相对值,并统计计算平均数与标准差,通过SPSS 20.0[23]计算如下数据,单因素方差分析(ANOVA)测平均数差别的显著性检验、正态分布检验(Kolmogorov-Smirnov test)判断数据是否符合正态分布、形态变异主成分分析提取主成分及与环境因子相关性分析衡量两个变量因素的相关密切程度。
1.4 序列分析
得到的测序结果利用Conting软件进行拼接;CLUSTAL_X 1.83进行序列比对;DnaSP v5[24]获得单倍型信息;ARLEQUIN 3.5[25]软件计算群体遗传多样性指数;MEGA7计算序列变异(S)[26]。
2 结果与分析
2.1 形态变异分析
中国海13个地域137个个体的相对形态量度ANOVA分析结果显示各形态量度差异均为显著。主成分分析提取L/DW(92.21%)、W/DW(5.72%)、H/DW(1.60%)为形态变异主成分(表2),将其与样本量进行Pearson检验,提取的主成分均不受样本量影响,因此形态变异主成分可作为该物种形态变异的指标。
2.2 序列变异与遗传多样性
137个矮拟帽贝个体线粒体DNACOI部分序列(601bp)碱基含量:A: 24.10%、T: 37.27%、C: 16.53%、G: 22.10%,共发现217个多态位点,转换颠换比为1.25,无插入/缺失,界定30个单倍型,占样本总数的21.89%。AMOVA结果显示,矮拟帽贝遗传变异主要来源于种群间(89.57%,P<0.001)。各种群遗传多样性比较显示,汕头(ST)种群呈现较高的遗传多样性,威海(WH)种群呈现较低的遗传多样性(表3)。对COI分子标记的遗传多样性指数进行图示法和正态分布检验,所有遗传多样性指数都服从正态分布。与样本量之间的相关性分析结果显示,各多样性指数均不受个体数量的影响(P>0.05),正态分布检验和相关性分析的结果说明此数据可以用于表示各地理种群的遗传多样性高低。
2.3 遗传多样性和形态量度与环境因子的相关性分析
统计13个采样地的环境因子(表4)并进行正态分布检验,结果表明所有数据均为正态分布,具有统计学意义。遗传多样性与环境因子相关性分析结果表明(表5),矮拟帽贝种群单倍型多样性、核苷酸多样性以及序列变异与纬度、年平均气温变异系数、年平均降水量变异系数、日照百分率及日照时数呈显著负相关(P<0.05),
与年均气温、年均降水量及年均水汽压呈显著正相关(P<0.05)。

图1 矮拟帽贝采样图Fig.1 Sampling map of P. pygmaea注:“()”内为采样数量;JZ:锦州;ZH:庄河;DL:大连;YT:烟台;WH:威海;QD:青岛;LYG:连云港;ZS:舟山;XM:厦门;ST:汕头;MM:茂名;ZJ:湛江;BH:北海Note: Value in “()” is sampling number; JZ: Jinzhou; ZH: Zhuanghe; DL: Dalian; YT: Yantai; WH: Weihai; QD: Qingdao; LYG: Lianyungang; ZS: Zhoushan; XM: Xiamen; ST: Shantou; MM: Maoming; ZJ: Zhanjiang; BH: Beihai
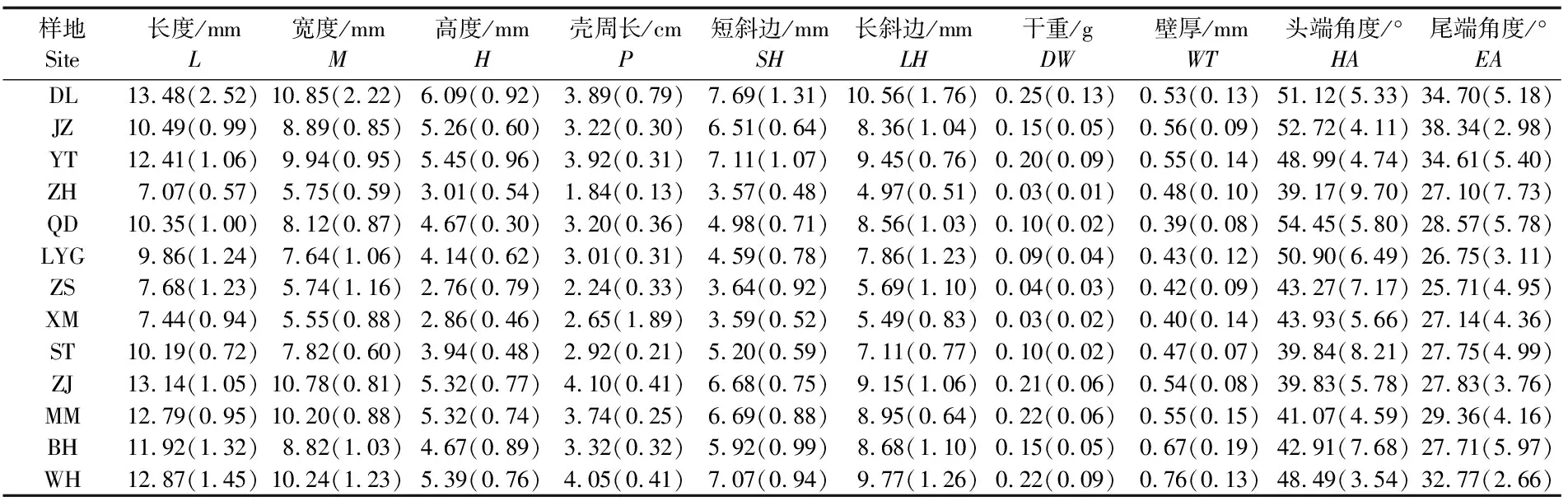
表1 矮拟帽贝形态数据的平均数(标准差)Tab.1 Mean values (standard deviation) of the morphological data of P. pygmaea populations
注:JZ:锦州;ZH:庄河;DL:大连;YT:烟台;WH:威海;QD:青岛;LYG:连云港;ZS:舟山;XM:厦门;ST:汕头;MM:茂名;ZJ:湛江;BH:北海
Note: JZ: Jinzhou; ZH: Zhuanghe; DL: Dalian; YT: Yantai; WH: Weihai; QD: Qingdao; LYG: Lianyungang; ZS: Zhoushan; XM: Xiamen; ST: Shantou; MM: Maoming; ZJ: Zhanjiang; BH: Beihai
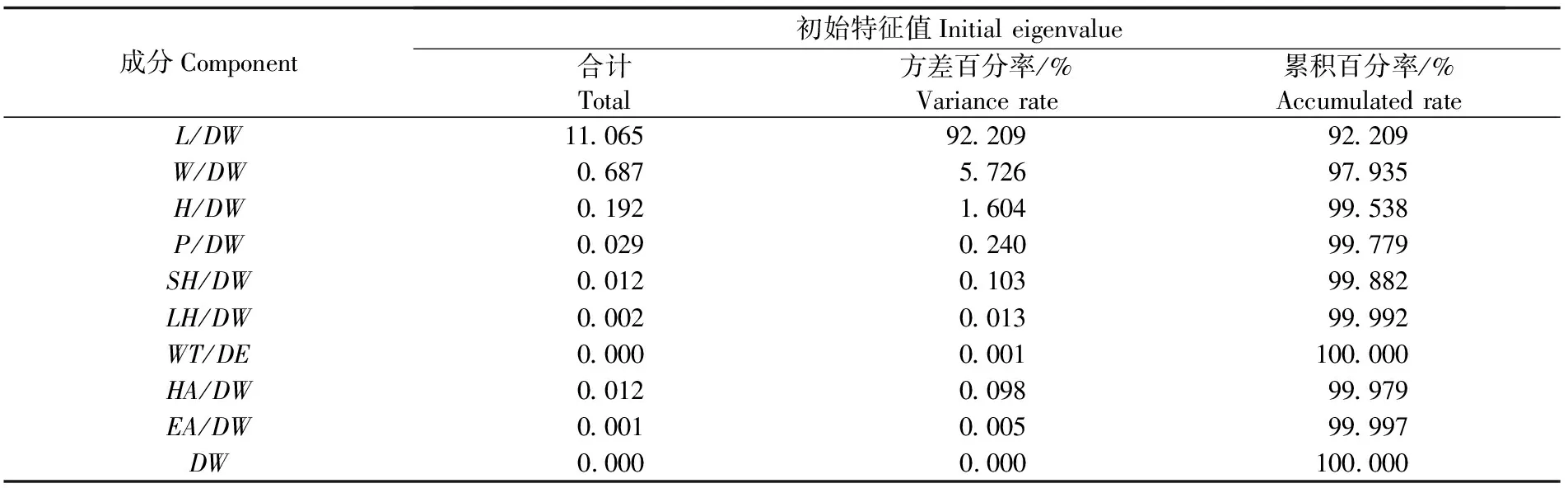
表2 矮拟帽贝形态变异的主成分分析Tab.2 Principal component analysis of P. pygmaea morphological variations
注:JZ:锦州;ZH:庄河;DL:大连;YT:烟台;WH:威海;QD:青岛;LYG:连云港;ZS:舟山;XM:厦门;ST:汕头;MM:茂名;ZJ:湛江;BH:北海
Note: JZ: Jinzhou; ZH: Zhuanghe; DL: Dalian; YT: Yantai; WH: Weihai; QD: Qingdao; LYG: Lianyungang; ZS: Zhoushan; XM: Xiamen; ST: Shantou; MM: Maoming; ZJ: Zhanjiang; BH: Beihai

表3 矮拟帽贝的遗传多样性(标准差)Tab.3 Genetic diversity of P. pygmaea(standard deviation)
注:JZ:锦州;ZH:庄河;DL:大连;YT:烟台;WH:威海;QD:青岛;LYG:连云港;ZS:舟山;XM:厦门;ST:汕头;MM:茂名;ZJ:湛江;BH:北海
Note: JZ: Jinzhou; ZH: Zhuanghe; DL: Dalian; YT: Yantai; WH: Weihai; QD: Qingdao; LYG: Lianyungang; ZS: Zhoushan; XM: Xiamen; ST: Shantou; MM: Maoming; ZJ: Zhanjiang; BH: Beihai
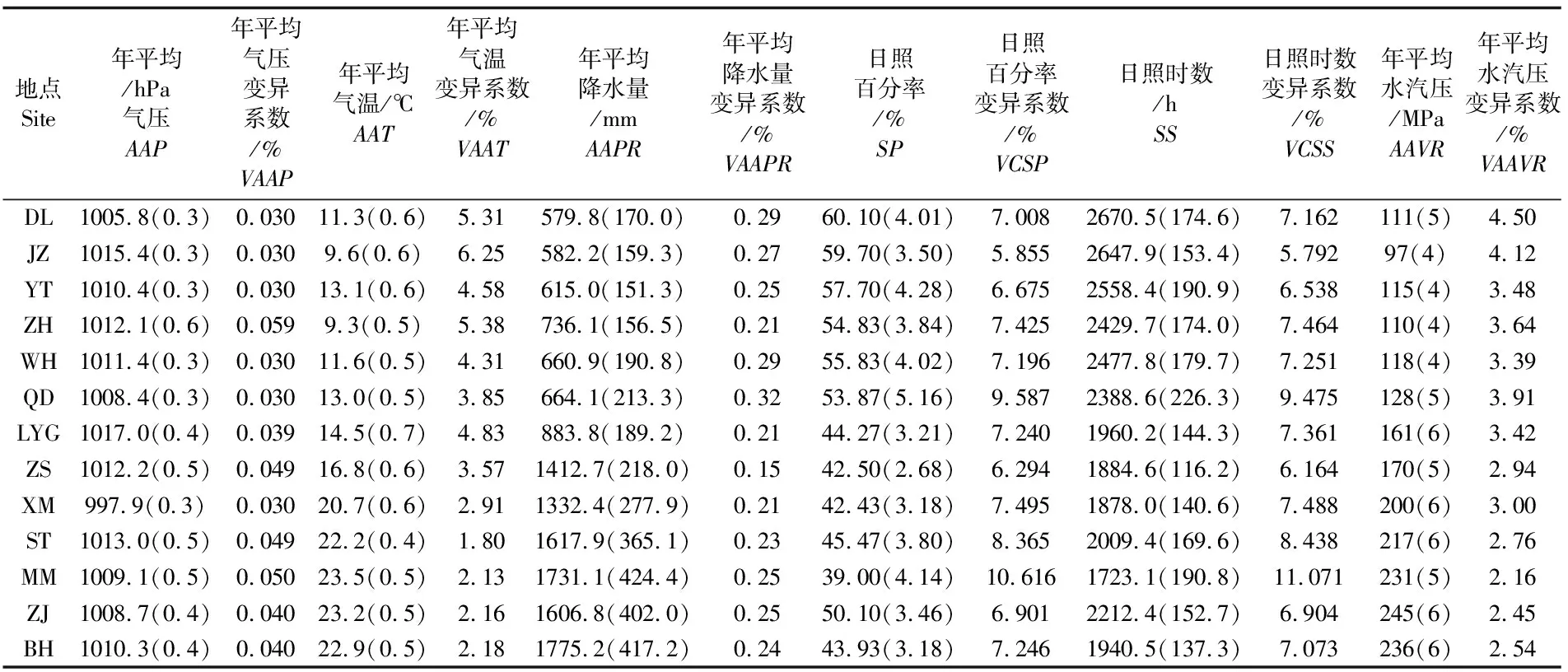
表4 13个矮拟帽贝地理种群近30年环境因子的平均值(标准差)Tab.4 Average values of environmental factors of 13 P. pygmaea populations in 30 years(standard deviation)
注:JZ:锦州;ZH:庄河;DL:大连;YT:烟台;WH:威海;QD:青岛;LYG:连云港;ZS:舟山;XM:厦门;ST:汕头;MM:茂名;ZJ:湛江;BH:北海
Note: JZ: Jinzhou; ZH: Zhuanghe; DL: Dalian; YT: Yantai; WH: Weihai; QD: Qingdao; LYG: Lianyungang; ZS: Zhoushan; XM: Xiamen; ST: Shantou; MM: Maoming; ZJ: Zhanjiang; BH: Beihai

表5 矮拟帽贝遗传多样性和形态量度与环境因子的相关性分析Tab.5 Relationship correlation between genetic diversity and morphology of P. pygmaea and environmental factors
注:*:P<0.05;**:P<0.01.
Note:*:P<0.05;**:P<0.01.
形态变异与环境因子相关性分析结果表明,主成分L/DW、W/DW、H/DW与年均降水量呈显著负相关(P<0.05)。
3 讨论
中国海矮拟帽贝各地理种群的COI序列研究表明,矮拟帽贝的单倍型多样性(0.200~0.867)较高且核苷酸多样性(0.000 7~0.091 4)较低,这一结果与GRANT等[27]提出的海洋类生物结果相符,说明该类型种群可能经历过历史扩张事件。
遗传结构分化和自然环境变迁之间的相互作用导致生活在不同环境下的矮拟帽贝存在地理变异[28-29]。环境因子对生物进化的影响显著,温度和降水量则是影响物种进化的两个最重要的环境因子[30]。
温度是贝类存活、生长、免疫、代谢的关键环境因子[31],研究发现太平洋牡蛎(Crassostreaglgas)、华贵栉孔扇贝(Chlamysnobilis)、虾夷扇贝(Mizuhopectenyessoensis)、马氏珠母贝幼虫(Pinctadamartensii)、栉孔扇贝(Chlamysfarreri)等遗传变异、分化均受气候变暖影响显著[32-33];海洋其它类生物研究发现,高温胁迫下紫色球海胆(Strongylocentrotuspurpuratus)蛋白代谢基因和信号传导基因的改变致使产生遗传分化[34],原绿球藻(Prochlorococcus)因生存温度不同,垂直分布的不同种群间遗传结构存在差异且温度越高遗传多样性越高[35]。矮拟帽贝遗传多样性与环境因子相关性分析表明,年均气温越高,种群遗传多样性越高,且随纬度的降低而升高。由此推测矮拟帽贝主要以岩石海床为栖息地,温度是影响物种代谢及性成熟的直接因素,继而影响种群遗传多样性,简而言之,温度越稳定遗传多样性越高,这与其它软体动物生态研究结果基本一致[36]。
矮拟帽贝遗传多样性与年均降水量、年均水汽压呈显著正相关,与日照百分率、日照时数呈显著负相关。降水量是影响生物遗传变异的另一重要因子[37],降水量直接反应空气环境中水分含量,水汽压间接代表大气中水汽含量,大气中水汽含量多时,水汽压越大[38];且日照越强,大气水汽含量越低,说明空气中水汽含量可能是影响矮拟帽贝遗传多样性的重要因素。矮拟帽贝作为潮间带生物,其生境可能更适于空气水分含量高的环境;且日照时数越短,遗传多样性越高,说明较退潮时裸露的日照环境,矮拟帽贝更趋向于海面下生存。另一种解释则为降水直接影响到矮拟帽贝生活区域的海水盐度,产生外界压力导致物种基因进化速率产生分歧。海水盐度是影响海洋生物生存生长至关重要的环境因子,受纬度(正相关)、降水量(负相关)、水气压(负相关)等多种因素的调节[39]。贝类生物对环境压力和环境盐度变化的适应性较差,环境因子可影响其生长发育进而导致遗传分化。SORIA等[40]的研究显示,随着盐度逐渐升高,智利扇贝(Argopectenpurpuratus)稚贝的氧循环和氮循环基因随之发生改变,导致遗传分化。由此得出盐度可以影响贝类能量和渗透压的变化。研究表明,在盐胁迫下贝类需要依靠能量代谢来维持体内渗透压的平衡,但是,盐度超出自身渗透压调节的范围,贝类的死亡率会升高[41]。外界非生物环境因素倾向于比内源的因素(如机体发育)变化更快,研究表明外源环境因素比内源机体因素更能促进遗传表达分化[42]。矮拟帽贝遗传多样性随纬度的降低而升高,与上述海水盐度(纬度与海水盐度呈正相关)降低导致遗传多样性升高结果一致,且从地理位置来看南部种群具有比北部种群有更深的遗传谱系、更高的遗传多样性。
海洋生物地理种群间的形态变异受到遗传因子和栖息地气候因子的双重影响[43],且形态量度主成分与年均降水量变异系数呈显著负相关,说明降水量是影响形态变异的主要因素,作为潮间带物种,落潮期暴露在空气中,受雨水的冲刷腐蚀导致形态产生差异,同时降水对生活区的水体盐浓度影响会导致摄食的变化而使形态产生差异。相对形态量度和其它环境因子的相关性分析表明其趋势与遗传分析的结果基本一致[44],与个别环境因子相关性趋势存在差异,其主要原因是自然选择导致物种基因遗传与形态变异的模式不同[45]。在稳定的环境中,自然选择压力的降低可以最大限度地保留基因型,遗传多样性升高;在不稳定的环境中,保留的种群适应多变环境,在选择压力下其有利的基因型被保留,遗传多样性则降低。

