卒中:回眸2018
王拥军,丁亚榕,戴丽叶,索阅
作者单位
1100070 北京首都医科大学附属北京天坛医院神经病学中心
2国家神经系统疾病临床医学研究中心
3北京脑重大疾病研究院脑卒中研究所
4脑血管病转化医学北京市重点实验室
2018年匆匆而过,脑血管病的临床和基础研究捷报不断,世界各地的研究为征服这个人类最重要的慢性病迈出了可喜的一步。盘点走过的一年,我们又见证了哪些给历史留下重要印记的研究呢?
1 全球卒中终身风险:难以承受之痛
2018年Lancet杂志刊登了来自全球疾病负担研究(Global Burden of Disease,GBD)的1990-2016年全球、区域和国家卒中终身风险报告[1]。该报告中利用GBD 2016的数据,评估195个国家中25岁以上人群的卒中、缺血性卒中或出血性卒中的终身风险,并以社会人口地理指数(sociodemographic index,SDI)进行分层。
终身风险这一概念是指在考虑了其他导致死亡的危险因素后,特定年龄、特定性别的人群在剩余寿命中发生某种疾病的累积概率。在报告中,主要呈现了两组重要的数据。
第一组数据是全球卒中风险排行榜。全球、区域和国家的卒中终身风险数据显示,在2016年,≥25岁的人群卒中终身风险为24.9%(95%不确定度区间为23.5~26.2),不同区域和国家之间存在差异。在21个GBD区域中,东亚风险最高(38.8%),其次为中欧(31.7%)和东欧(31.6%)。中国人群总体的终身卒中风险和男性的风险分别高达39.3%(95%不确定度区间为37.5~41.1)和41.1%(95%不确定度区间为39.2~42.9),在同项比较中均居于全球首位。将各国按照SDI进行区分,中-高指数国家居民的卒中终身风险最高,达31.1%,其次是中等指数国家(29.3%),高指数和低指数国家居民的卒中终身风险分别为23.5%和13.2%。
第二组数据是2016年与1990年的卒中终身风险对比。全球人群卒中的终身风险,从1990年的22.8%上升至2016年的24.9%,相对增加了8.9%(95%不确定度区间为6.2~11.5)。在全球不同区域,卒中终身风险的变化呈两极分化趋势。卒中终身风险增幅最大的是撒哈拉以南的东西部非洲地区、北非、中东部欧洲、东亚、南亚和东南亚地区。中亚、拉丁美洲南部和热带地区、高收入亚太地区和撒哈拉以南非洲地区的风险在同一时期大幅下降。这与全球经济发展情况趋势相同。
总体而言,全球卒中风险呈现出巨大的地区差异,东亚、中欧和东欧的卒中终身风险较高,卒中防治工作仍然任重道远(图1)。

图1 综合性别和年龄评估2016年全球人群卒中终身风险[1]
2 卒中基因研究:大队列合作的魅力
2018年,Nature Genetic杂志发表了一项超过52万人的队列研究结果,研究纳入的人群来自欧洲、美洲、亚洲、非洲及澳大利亚,这是全球合作的重要成果[2]。这项研究是由国际卒中遗传学联盟(International Stroke Genetics Consortium,ISGC)和MEGASTROKE联盟发起的。研究人员纳入了29项大规模研究的数据,收集了世界各地不同种族人群的DNA样品。在超过52万人中,约6.7万人已发生卒中,其余45.5万人作为对照。通过GWAS,该研究鉴定出了32个与卒中发病机制密切相关的基因,其中10个在国际研究中曾经被报道过,而其余22个是既往未经报道的卒中相关的基因区域。
这项研究将已知的与卒中相关的基因区域数量增至32个,它们具备两项重要特点:第一项特点是与其他血管疾病相关基因相互重叠,证实了这些基因区域与其他血管病变共享遗传变异。与这些基因相关的其他血管疾病因素包括脑白质高信号、高血压、脂代谢异常、颈动脉内中膜粥样硬化斑块形成、深静脉血栓、心房颤动等(图2)。这说明血管病并不是一个单基因病,而是多基因与环境相互作用的结果。第二项特点是这些基因区域与抗栓药物代谢的基因密切相关。这说明药物基因组与疾病的发病机制相互关联。卒中危险基因位点常常出现在抗血栓治疗的药物基因位点,对于卒中药物研发至关重要。

图2 卒中和其他血管疾病相关基因相互重叠[2]
这项研究通过鉴定新的卒中变异位点提示了既往未被深入研究的卒中机制,并且提出了进一步可靠的基因功能研究和实验随访的框架。这些发现是理解卒中遗传基础方面的重大进步。
3 缺血性卒中的再灌注治疗:拓宽的治疗窗口
急性期的再灌注治疗是缺血性卒中早期治疗最重要的原则。伴随着急性缺血性卒中血管内治疗的历史演变,再灌注领域研究的不断深入,科学家将再灌注治疗的时间窗不断拓宽。1995年,NINDS发表研究,确立了发病3 h为时间窗的以非强化CT为指导的静脉rt-PA治疗[3]。2008年,德国教授Werner Hacke[4]领衔的欧洲协作性急性卒中研究3(the European Cooperative Acute Stroke Study 3,ECASS 3)将静脉溶栓时间窗拓宽为3~4.5 h。2015年,多项临床研究证实发病6 h内多模式影像指导下静脉溶栓基础上的动脉取栓的有效性[5-8]。在2018年,两项大型研究进一步将机械取栓时间窗从6 h突破至24 h[9]。
第一项研究是应用MRI DWI或CTP联合临床不匹配治疗醒后卒中及晚就诊卒中患者用Trevo装置行神经介入治疗研究(DWI or CTP Assessment with Clinical Mismatch in the Triage of Wake Up and Late Presenting Strokes Undergoing Neurointervention with Trevo,DAWN)[9]。DAWN研究是一项多中心的前瞻性、随机、开放标签、结局盲法评价(prospective,randomized,open,blinded Endpoint,PROBE)的临床试验。研究在美国、加拿大、欧洲和澳大利亚的26家中心开展。患者的入组标准为:年龄≥18岁;最后看起来正常到随机的时间为6~24 h;卒中前mRS评分为0~1分;CTA或MRA证实的颈内动脉颅内段或MCA M1段或两段同时闭塞;存在临床症状的严重程度与梗死体积不匹配。人群采用1∶1随机对照分组,最终共纳入患者206例,其中107例接受机械取栓联合标准化药物治疗,另外99例患者接受了标准化药物治疗。
研究结果显示,在有效性结局方面,取栓组90 d mRS评分和神经功能独立(mRS≤2)概率都显著优于对照组(图3)。在不匹配分组、性别、年龄、基线NIHSS评分、血管闭塞部位、发病时间、发病形式等各亚组分析中,也均与总的结果一致。对于安全性结局,两组间24 h的症状性颅内出血和90 d任何原因所致的死亡没有显著差异。因此,对于发病距离最后正常时间为6~24 h且伴有临床与影像不匹配的急性缺血性卒中患者,取栓术联合标准治疗相比标准治疗,能改善其90 d功能结局。
第二项大型研究是由斯坦福大学发表的影像评估筛选缺血性卒中患者行血管内治疗研究3(Endovascular Therapy Following Imaging Evaluation for Ischemic Stroke 3,DEFUSE 3),该研究用PWI选择发病6~16 h的缺血性卒中患者行机械取栓治疗[10]。DEFUSE 3研究对于缺血性卒中患者的纳入标准为:最后看起来正常到随机的时间为6~16 h;NIHSS评分≥6分;卒中前mRS评分为0~2分;伴有颈内动脉和(或)MCA闭塞且RAPID软件定量评估显示最大梗死核心≤70 mL。将入组患者随机分配至血管内取栓组和单纯药物治疗组,其中取栓组92例,标准化药物治疗组90例。研究的主要终点是位移分析所示的干预90 d后mRS评分变化情况。

图3 DAWN研究主要结局
结果发现,与药物治疗组相比,取栓组患者随访9 0 d后的mR S评分显著改善,mRS 0~2分者的比例更高(45%vs17%,P<0.0001),mRS评分为5~6分者的比例更低(22%vs42%,P=0.0048)。此外,与药物治疗组相比,取栓组患者实现脑血流再灌注及血管再通的比例均更高(79%vs18%,P<0.0001;78%vs18%,P<0.0001)。就安全性而言,与药物治疗组相比,取栓组患者症状性颅内出血发生率并无显著差异(6.5%vs4.4%,P=0.75),死亡率有降低趋势(14%vs26%,P=0.05)。因此,对于MCA近段和颈内动脉梗死,并且组织还没有发生梗死的发病6~16 h的缺血性卒中患者,血管内取栓治疗加上标准治疗与单纯标准治疗相比,有更好的功能结局(图4)。
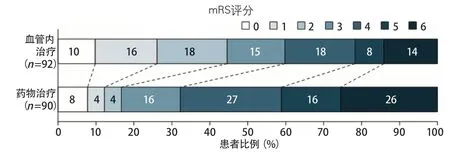
图4 DEFUSE 3研究主要结局
这两项大型临床研究为拓宽血管内取栓术在缺血性卒中患者中应用的时间窗提供了最新证据支持。基于这两项研究结果,在2018年2月美国AHA/ASA更新的急性脑血管病治疗指南中对于机械取栓增加了新的推荐意见:发病时间为6~16 h的急性缺血性卒中患者,如果存在前循环大血管闭塞,且满足DAWN及DIFFUSE 3研究的入选标准,推荐机械取栓(推荐级别:Ⅰ;证据水平:A);对于发病6~24 h的急性缺血性卒中患者,如果存在前循环大血管闭塞,且满足DAWN研究的其他入选标准,机械取栓是合理的(推荐级别:Ⅱa;证据水平:B-R)[11]。
同时,这两项研究还给我们带来了对于急性期脑灌注评价手段的启示,即阳性结果的关键在于通过适宜的手段评估可挽救脑组织的存在。因此,指南中同样更新了对于检查方法的推荐意见:对于一些经筛查的前循环大血管闭塞的急性缺血性卒中患者,如果最后正常状在6~24 h内,推荐进行CTP、DWI或PWI检查帮助筛选适合机械取栓的患者,但是必须严格符合随机对照研究中证实的可以获益的影像和其他标准的患者才可以进行机械取栓(推荐级别:Ⅰ;证据水平:A)。
以上两项研究针对的都是发病时间明确的缺血性卒中患者,然而在实践中部分患者发病时间不明确,这些患者是否有再灌注治疗的机会?2018年发表的针对再灌注治疗时间窗拓宽的大型研究还有第三项:醒后卒中患者基于MRI溶栓安全性及有效性(Efficacy and Safety of MRI-based Thrombolysis in Wake-up Stroke,WAKE-UP)研究[12]。
WAKE-UP研究采用MRI的DWI-液体衰减反转恢复序列(fluid-attenuated inversion recovery,FLAIR)影像的错配作为存在可挽救脑组织的组织学标准。研究共纳入503例患者,其中rt-PA溶栓治疗组254例,对照组249例。主要终点事件是90 d良好预后(mRS 0~1分)。结果发现,与对照组相比,静脉溶栓组优势明显,90 d随访后功能预后良好的患者比例更高(53.3%vs41.8%),统计学分析中校正后OR=1.61(95%CI1.09~2.36)。从安全性方面来看,静脉溶栓组中脑实质出血的风险也有增加(4.0%vs0.4%,P=0.03)。研究证实了对于未知症状发作时间的急性缺血性卒中患者DWI上表现为缺血性病变,而FLAIR相应区域无实质高信号的患者,与安慰剂相比,使用静脉溶栓能够为患者带来更好的功能预后。相应地,接受静脉溶栓的患者出血风险也有升高的趋势(表1)。
这3项研究的发表奠定了缺血性卒中急性期再灌注治疗时间窗的扩大,更多患者将因此获益。
4 新型rt-PA用于卒中治疗:迟来的证据
第三代组织型纤溶酶原激活剂替奈普酶(Tenecteplase/Metalyse/TNK-tPA)是阿替普酶(alteplase/rt-PA)的多点变异体,通过基因修饰合成,改变了rt-PA蛋白结构中T、N、K 3个碱基位置。相比于rt-PA,TNK-tPA具有更长的半衰期和更强的纤维蛋白结合特异性,是近年备受关注的新型溶栓药物。尽管TNK-tPA临床应用更便捷,但能否将它应用于急性缺血性卒中的临床治疗,仍需要临床试验的验证。
急性神经功能缺损患者扩展时间窗溶栓后联合动脉治疗(Extending the Time for Thrombolysis in Emergency Neurological Deficits with Intra-Arterial therapy,EXTEND-IA)TNK研究是一项多中心PROBE研究,在澳大利亚和新西兰的13家机构展开[13]。研究为非劣效性设计,如果研究显示出非劣效性,则进一步测试优效性。研究纳入了颈内动脉、基底动脉或MCA闭塞的缺血性卒中患者,患者发病时间为0~4.5 h,卒中前mRS≤3分,无静脉溶栓禁忌证。严重卒中前残疾(mRS≥4分)、造影剂过敏和随机化之前出现快速神经功能恢复的患者被排除在研究之外。
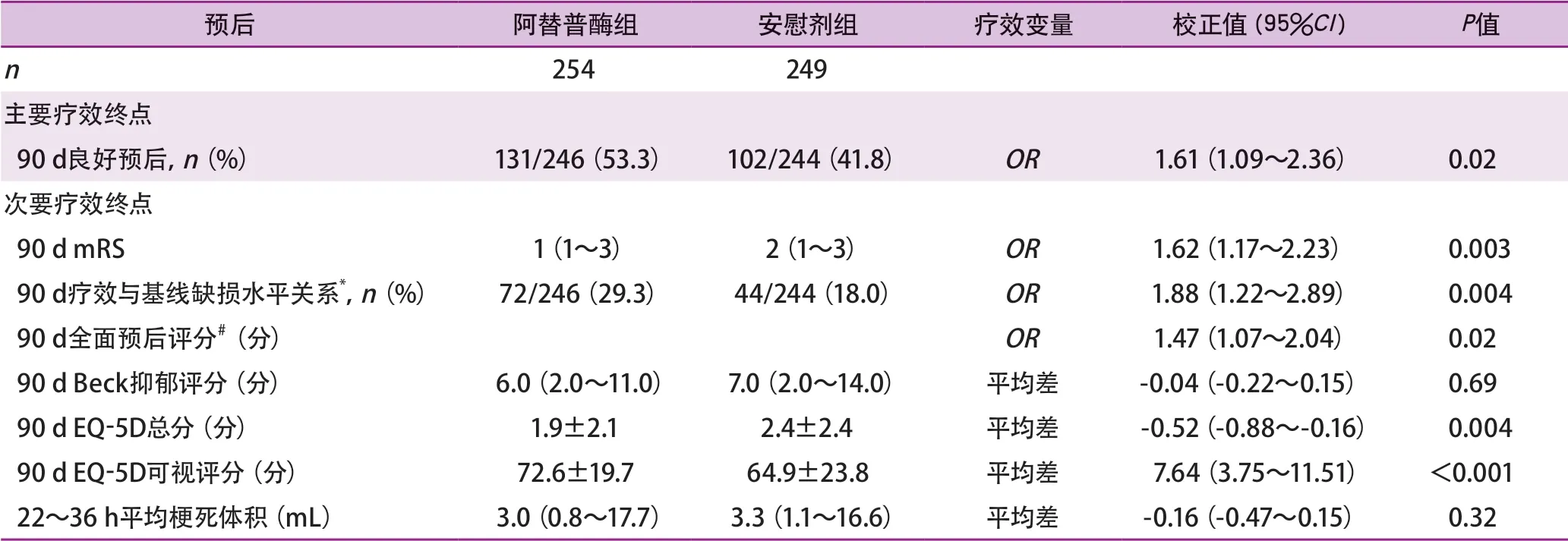
表1 WAKE-UP研究主要结局
研究结果显示,与rt-PA 0.9 mg/kg相比,TNK-tPA 0.25 mg/kg静脉溶栓可以带来初始血管造影时更多的再灌注,并且安全性与阿替普酶相当,可以作为血管内治疗前替代阿替普酶的有效药物(图5)。
在多项临床T N K 实验宣告失败之后,EXTEND-IA TNK研究的胜利大大增加了研究者对新型溶栓药物应用的信心[14-15]。新型溶栓药物的临床应用将使缺血性卒中急救更加便捷,给患者带来更多获益机会。
5 联合抗血小板治疗:并非多多益善
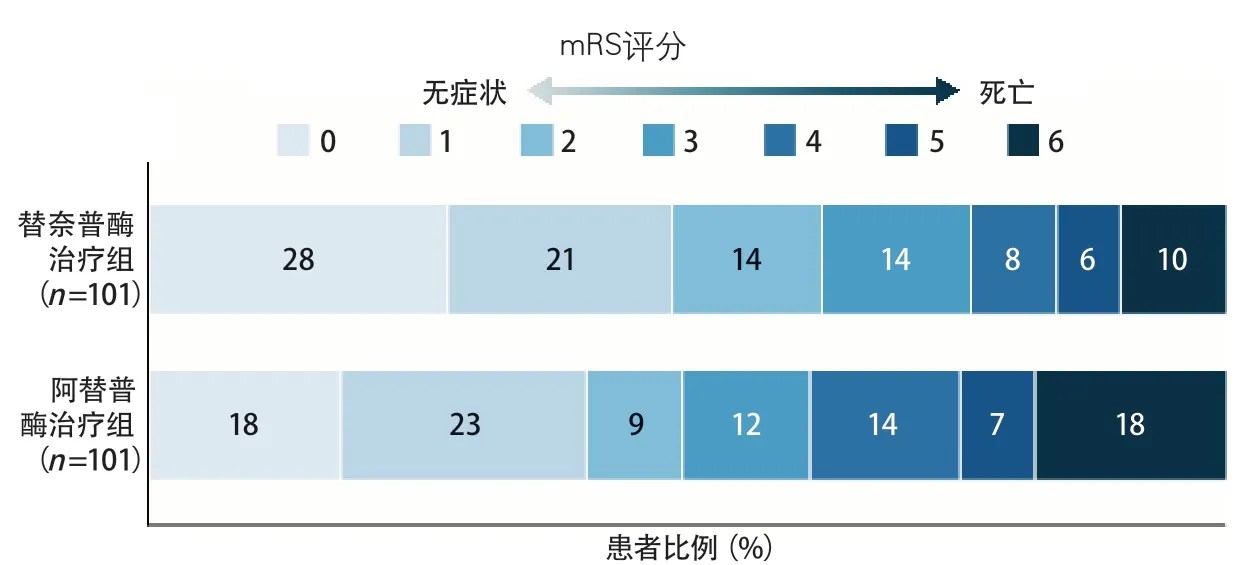
图5 EXTEND-IA TNK研究主要结局[13]
尽管再灌注治疗时间窗的扩大给更多的患者带来健康的机会,但是再灌注治疗多是针对中重度残疾的卒中患者,对于轻型卒中患者是否有效仍然是个悬而未决的问题。2018年发表了评价轻型卒中患者rt-PA溶栓有效性(The Potential of rt-PA for Ischemic Strokes With Mild Symptoms,PRISMS)试验结果。PRISMS研究原计划纳入948例发病3 h内NIHSS评分在0~5分的患者,1∶1随机化到静脉rt-PA溶栓治疗联合阿司匹林安慰剂组和口服阿司匹林325 mg联合rt-PA安慰剂静脉溶栓组。因赞助提前终止,最终在32个月内纳入313例患者。在随机化至rt-PA静脉溶栓组的患者中有78.2%在90 d达到良好预后(mRS评分0~1分);而在随机化至阿司匹林组的患者中有81.5%达到良好预后,两组间无显著差异[16]。在对主要安全终点的分析中,仅有5例患者在36 h内发生症状性颅内出血,并且这5例均为rt-PA溶栓组的患者。PRISMS研究提示,相比口服阿司匹林,静脉rt-PA溶栓治疗并不能改善轻型非致残性卒中的90 d功能预后,并有更高的症状性颅内出血风险。本研究中阿司匹林组的获益可能部分是由于比指南推荐的发病24~48 h更早期的阿司匹林治疗(75%本组患者平均在发病3.1 h口服了阿司匹林)。虽然研究提前终止并且有相对较高比例(8.9%)的90 d功能结局失访率,但结果仍有重要意义,rt-PA溶栓组的症状性颅内出血率接近轻型卒中临床试验的结果,且本研究结果进一步支持溶栓治疗并不能使轻型、非致残性卒中患者的功能获益。William J.Powers教授解读称,对于这些轻型非致残性卒中患者而言,阿司匹林治疗以及密切监测可能是适当方案[17]。
相比之下,对于非致残缺血性脑血管病患者,抗血小板治疗高歌猛进,取得了一项又一项循证医学证据的支持。2018年发表了新发TIA和轻型卒中血小板定向抑制研究(Platelet-Oriented Inhibition in New TIA and Minor Ischemic Stroke,POINT)[18]。POINT试验选择发病12 h内的轻型卒中和高危TIA患者,评价阿司匹林联合氯吡格雷与单用阿司匹林相比的有效性和安全性。抗血小板治疗选择问题上,POINT研究得到了与2013年氯吡格雷用于急性非致残性缺血性脑血管病事件高危人群的疗效(Clopidogrel in High-Risk Patients with Acute Nondisabling Ischemic Cerebrovascular Events,CHANCE)研究一致的结论[19]。在这项随机、双盲、安慰剂对照的国际多中心研究中,相比单用阿司匹林,氯吡格雷联合阿司匹林治疗能有效减低高危非致残性卒中患者90 d的复合血管事件(缺血性卒中、心肌梗死及缺血性血管性死亡)的发生率(6.5%vs5.0%,P=0.02)。在主要安全性终点方面,氯吡格雷联合阿司匹林治疗带来更高的主要出血风险(0.9%vs0.4%,P=0.02)。POINT研究与CHANCE研究的设计和结论异同总结在表2中。
两项试验疗效相似,但安全性相差很大,是否为POINT的联合治疗的时间过长所致?2018年的世界卒中大会上,美国南卡大学的Jordan Elm教授报告了POINT研究的时间序列分析。发现在治疗的前21 d,氯吡格雷联合阿司匹林双联抗血小板组发生主要缺血事件的风险相比阿司匹林单药治疗减低2%,风险比为0.65(P=0.0015),但在21~90 d双联抗血小板治疗并不减少主要缺血事件;在0~90 d双联抗血小板治疗均有更高的主要出血风险,在0~21 d出血风险相比阿司匹林组高0.5%。氯吡格雷联合阿司匹林治疗的获益主要发生在前21 d,超过了主要出血风险。治疗期间主要出血风险是持续存在且较低的。CHANCE研究中氯吡格雷联合阿司匹林治疗疗程为21 d,显示同样的获益且不增加主要出血[20]。结合CHANCE的结果一起考虑,POINT研究结果显示当氯吡格雷联合阿司匹林双抗治疗疗程限制为21 d时,可最大化增加获益并减少风险。

表2 CHANCE研究与POINT研究设计比较
在阿司匹林联合氯吡格雷治疗的基础上再增加抗血小板药物是否还能提高治疗效果?2018年发表了英国科学家发起的三联抗血小板治疗降低缺血性卒中后依赖性(the triple antiplatelets for reducing dependency after ischaemic stroke,TARDIS)试验结果。TARDIS研究是一项国际、前瞻性、随机、开放标签、盲法终点的临床试验,纳入的患者为发病48 h内的缺血性卒中或TIA[21]。参与者随机给予三联抗血小板(首次为负荷剂量阿司匹林300 mg,氯吡格雷300 mg;随后阿司匹林75 mg,氯吡格雷75 mg,双嘧达莫200 mg,每日2次)30 d,或按照指南抗血小板治疗(包括负荷量,单独氯吡格雷,或阿司匹林联合双嘧达莫)[22]。主要终点是90 d内的卒中和TIA复发率、严重程度,严重程度用mRS来评价,分为轻度(mRS 0~1分)、中度(mRS 2~3分)、重度(mRS 4~5分)及死亡。研究纳入的3096例患者中1556例随机化入三联抗血小板组;1540例随机化入标准指南推荐的抗血小板治疗组。两组间卒中/TIA的复发率或复发事件的严重程度并不存在显著差异,但三联抗血小板组有明显更高、更严重的出血事件(OR2.54,95%CI2.05~3.16)。本研究提示对于近期脑缺血的患者,强化抗血小板治疗未降低复发性卒中或TIA的发生率和严重程度,但是显著增加了严重出血的风险,因此不能把三联抗血小板治疗作为常规的临床实践。Pierre Amerenco教授分析了有关TARDIS研究设计可能对结果造成的影响:TARDIS研究的纳入标准为TIA和各种严重程度的卒中,其中11%患者为中重度卒中(NIHSS评分>6分);另有10%的患者在接受抗血小板治疗前曾经进行过溶栓治疗,这部分经过溶栓的患者具有明显更高的出血风险(包括颅内出血、出血转化等)。研究中70%的患者是在发病24~48 h内入组的[23];研究的三联抗血小板疗程为30 d(超出了复发风险最高的时期),纳入人群的病因分型有40%为小动脉闭塞性,而大动脉粥样硬化性卒中仅占16%。这些因素可能影响三联抗血小板有效性与出血风险的权衡。更具针对性地选择研究纳入人群可能有助于更好的评价三联抗血小板治疗。
6 非致残性缺血性脑血管病:从证据到指南
2018年,循证医学(evidence-based medicine,EBM)概念的提出者Gordon Guyatt教授团队在BMJ上发表题为《评估氯吡格雷加阿司匹林双联抗血小板治疗对预防急性轻型缺血性卒中或T IA 患者卒中复发和出血事件的有效性和安全性》系统评价和Meta分析[24]。系统评价共纳入3项研究,卒中和TIA发作快速评估以预防早期复发(The Fast Assessment of Stroke and Transient ischemic attack to prevent Early Recurrence,FASTER)、CHANCE和POINT,共计10 447例患者。在急性轻型缺血性卒中或TIA患者症状出现后24 h内开始使用氯吡格雷和阿司匹林双联抗血小板治疗可降低非致死性卒中复发的风险(HR0.70,95%CI0.61~0.80)。主要结论是:在双联抗血小板治疗开始后21 d内,甚至可能10 d内,停用双抗治疗可最大限度地提高治疗效益并最大限度地减少危害(图6)。
基于此项系统评价,BMJ同期发表了BMJ临床指南快速推荐意见,推荐对于急性轻型缺血性卒中或高危TIA患者,应在症状发作后24 h内尽快给予氯吡格雷联合阿司匹林双联抗血小板治疗,并且持续治疗10~21 d[25]。两条快速推荐的核心证据来源于CHANCE研究:对于高危TIA和轻型缺血性卒中,建议在发病24 h内启用阿司匹林加氯吡格雷的双重抗血小板治疗;对于高危TIA和轻型缺血性卒中,建议双重抗血小板治疗的时间是10~21 d,而不要超过21 d。依据建议评价、发展和评估分级(grading of recommendations assessment,development and evaluation,GREAD),双重抗血小板治疗可降低卒中复发风险为高质量证据;21 d以后继续双联抗血小板治疗不额外降低卒中复发为中等质量证据;21 d以后继续双联抗血小板治疗额外增加中重度出血风险为高质量证据。
2018年底,韩国国立大学医学院神经内科脑血管病中心在Stroke杂志上在线发表了的韩国一项的登记研究,连续纳入5590例CHANCE样(轻型非心源性栓塞性卒中和高危TIA)患者,年龄(64±13)岁,男性62.6%,氯吡格雷联合阿司匹林治疗占总体人群的66.1%。在CHANCE样人群中,氯吡格雷联合阿司匹林治疗相比阿司匹林单药治疗可减少发病90 d的卒中、心肌梗死、血管性死亡事件(表3)[26]。亚组分析发现双联抗血小板治疗在既往有抗血小板药物应用史、更高龄患者(>75岁)、非小血管闭塞性病因的人群中效果更佳。这项登记研究再次支持CHANCE和POINT双联抗血小板治疗的循证医学结论。
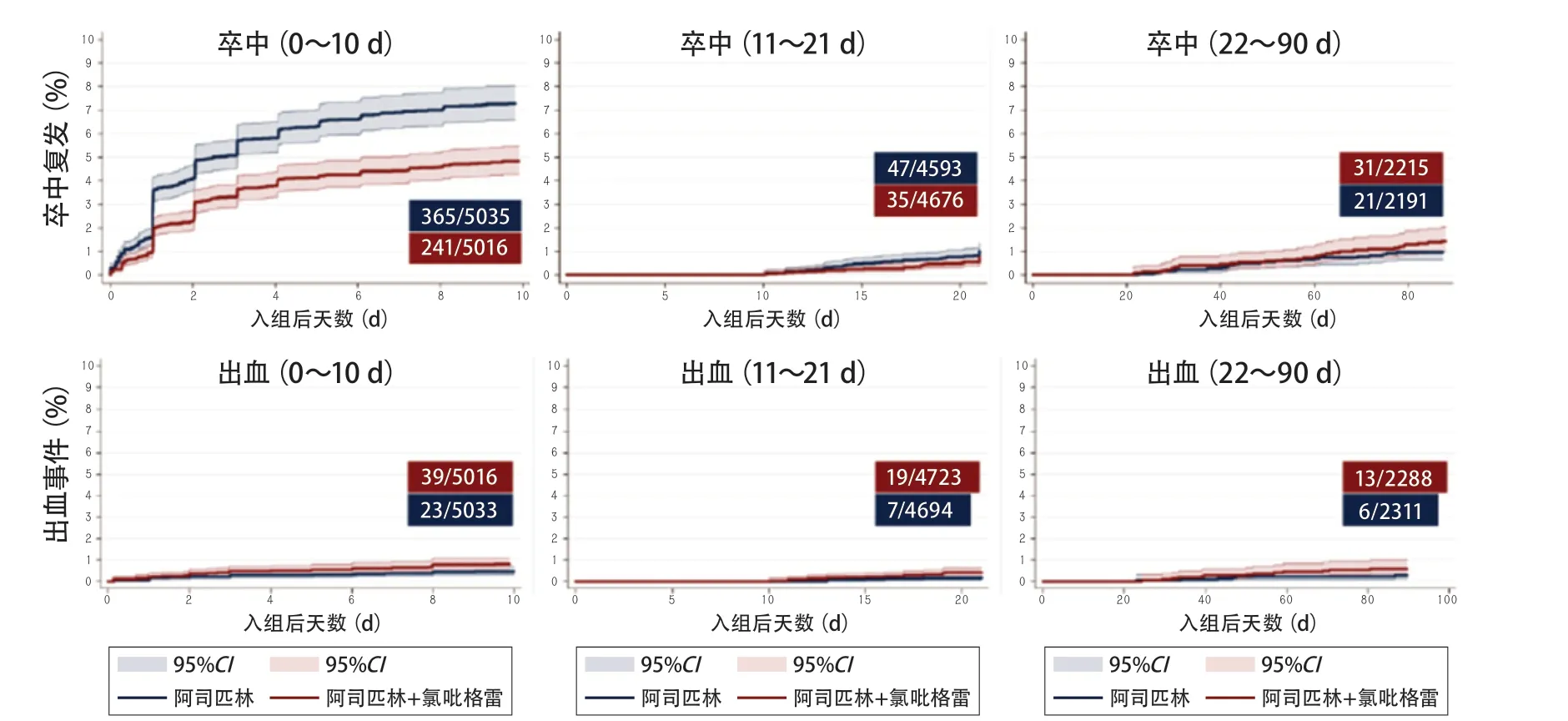
图6 缺血性卒中/主要出血事件在双重抗血小板治疗和阿司匹林治疗时间-事件曲线[24]

表3 氯吡格雷联合阿司匹林对比阿司匹林单药的疗效预后
7 原因不明的栓塞性卒中:机制和治疗难以确定
原因不明的栓塞性卒中(embolic strokes of undetermined source,ESUS),这一新概念在2014年由Robert G.Hart教授等首次提出。诊断标准为:经CT或MRI发现的非腔隙性卒中(腔隙性卒中定义为皮层下位于小、穿支动脉供血区的梗死,梗死灶最大直径≤1.5 cm,或MRI的PWI上≤2.0 cm,CT上梗死灶的出现需要在发病24~48 h后);无梗死区域责任动脉(颅内/颅外)≥50%管腔狭窄;无心源性栓塞高危因素(永久性或阵发性心房颤动、持续性心房扑动、心脏内血栓、人工心脏瓣膜、心房黏液瘤或其他心脏肿瘤、二尖瓣狭窄、4周内心肌梗死,左心室射血分数<30%、瓣膜赘生物或感染性心内膜炎);无其他能引起卒中的情况(动脉炎、动脉夹层、偏头痛/血管痉挛、药物错用)[27]。栓子来源可能是源自低危/隐匿心脏来源,静脉来源的反常性栓塞或主动脉弓、颈动脉、脑动脉的非闭塞性斑块。提出在原因不明的栓塞性卒中二级预防中抗凝治疗可能优于抗血小板治疗的假设。基于这一假设,多项抗凝治疗试验开始实施。
2018年6月,Robert G.Hart教授在NEJM上发表了Xa因子抑制剂利伐沙班与阿司匹林预防不明栓子来源的栓塞性卒中国际试验(New Approach Rivaroxaban Inhibition of Factor Xa in a Global Trial versus ASA to Prevent Embolism in Embolic Stroke of Undetermined Source,NEVIGATE ESUS)结果。NEVIGATE ESUS是一项事件驱动,Ⅲ期临床随机对照研究,在31个国家共459个分中心纳入了7213例患者,随机分入利伐沙班组(利伐沙班15 mg 1次/日,联合阿司匹林安慰剂1次/日)或阿司匹林组(阿司匹林100 mg 1次/日,联合利伐沙班安慰剂1次/日),分别在第1个月、第6个月、第12个月门诊访视,随后每6个月随访一次[28]。研究纳入发病7 d~6个月的影像证实为非腔隙性缺血性卒中患者,并且无责任动脉来源的颅外动脉>50%的狭窄,无心源性栓塞危险因素或其他原因。发病年龄需>49岁,发病年龄在50~59岁者需合并至少一个血管危险因素。筛选过程要求至少20 h心电监测以除外6 min或时间更长的心房颤动;要求行经胸或经食道超声除外心脏内血栓。PFO计划做封堵治疗者需排除在外。主要有效性终点为首次复发性缺血性/出血性卒中或全身栓塞。主要安全性终点为严重出血。既往研究显示利伐沙班(包括当前研究中使用的15 mg/d剂量)可以有效预防心房颤动患者的卒中复发,而当前试验并未观察到利伐沙班可以降低缺血性卒中复发率/全身性栓塞发生率(HR1.07,95%CI0.87~1.33),提示未检测到的阵发性心房颤动可能不是复发性卒中的主要原因。
在534例超声心动图诊断的PFO患者NE VIGATE ESUS亚组分析中,发现抗凝治疗可以减少一半患者卒中的复发。结合既往两项试验[PFO与隐源性卒中(PFO in Cryptogenic Stroke Study,PICSS)和PFO封堵术与抗凝治疗预防卒中复发(Patent Foramen Ovale Closure or Anticoagulants versus Antiplatelet Therapy to Prevent Stroke Recurrence,CLOSE)]的系统分析,缺血性卒中预防复发倾向于抗凝治疗(OR0.48,95%CI0.24~0.96,P=0.04)。需要进一步评价对于原因不明栓塞性卒中后发现合并PFO的患者到底是抗凝、抗血小板治疗或是PFO封堵治疗最能获益[29](图7)。
8 脑出血的药物治疗:难以止住的终点
在所有类型的卒中中,自发性ICH比例高达20%,目前唯一能改善功能结局的干预措施是早期强化降压。在发病最初的几个小时内,1/3的ICH患者有血肿扩大,且与预后不良相关。影像学特点如CTA“点征”是预测血肿扩大的可能标志,大部分人认为应该药物止血,但既往研究发现止血药不仅不改善功能结局,还可能会增加患者下肢静脉血栓风险。
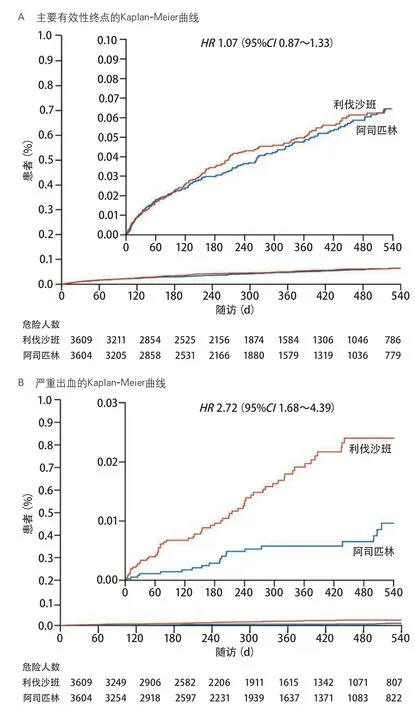
图7 主要有效性终点/严重出血在利伐沙班治疗和阿司匹林治疗的累计风险[29]
2018年在Lancet杂志上,英国Nikola Sprigg教授发表了关于超急性期颅内出血患者氨甲环酸治疗的研究结果(Tranexamic acid for hyperacute primary Intracerebral Haemorrhage,TICH-2)[30]。TICH-2是一项国际、多中心、随机、安慰剂对照的Ⅲ期优效试验,旨在探讨颅内出血患者超急性期氨甲环酸治疗能否降低血肿扩大风险及改善患者预后。研究共纳入发病8 h内的ICH患者2325例,其中氨甲环酸组1161例(静脉给予1 g氨甲环酸推注,随后8 h输注1 g氨甲环酸),安慰剂组1164例。尽管氨甲环酸降低了血肿扩大、早期死亡和严重不良事件,90 d功能状态在氨甲环酸和安慰剂组的患者中并没有显著性差异(图8)。事后亚组分析的结果提示,这可能是样本量和患者的选择造成的,仍需要进一步临床试验的探索。下一步的研究可以通过CT平扫“混杂征”、CTA“点征”等影像学手段筛选或人工智能预测可能发生血肿扩大的患者,提前给予氨甲环酸治疗。这三种方法都是下一个临床实验的起点,期待氨甲环酸这类价格低廉且相对安全的药物可以改写教科书,对ICH领域的治疗产生重要影响。
9 脑血管病康复治疗:聚焦药物
近年来,尽管在急性期血管再通治疗方面取得了巨大进展,仍有约50%的幸存者将终身残疾,给家庭和社会带来了沉重的负担,迫切需要可以减少神经损伤、改善功能预后的康复治疗。目前常用的康复手段主要是物理治疗和促康复药,其中,使用最广泛的是抗抑郁药。在临床试验中评价最多的是弗洛西汀,用于新发卒中的康复治疗。有一种观点认为,抗抑郁药也是促康复药。国际同步启动了3项临床试验,分别是英国进行的项弗洛西汀和安慰剂的随机对照试验(Fluoxetine Or Control Under Supervision,FOCUS),澳大利亚、新西兰和越南的弗洛西汀在卒中康复中的评估(Assessment of Fluoxetine in Stroke Recovery,AFFINITY)和瑞典的弗洛西汀对急性缺血性卒中的有效性和安全性[Establishing the Effect(s) and Safety of Fluoxetine Initiated in the Acute Phase of stroke,EFFECTS][31]。在这三项研究中,弗洛西汀的主要目的并不是用来治疗抑郁,而是促康复。每项试验都是独立进行的,最终将通过Meta分析得到最精确的总体结果估计。
其中,英国的FOCUS研究结果2018年发表在Lancet上,旨在探究卒中发作后2~15 d的患者,常规给予6个月的氟西汀(每日20 mg)治疗是否能够降低卒中后依赖、致残、促进患者康复及停药之后的临床改善(延长随访至12个月)[32]。这是一项双盲随机对照试验,共计划纳入3000例患者,实际纳入3152例患者,最终进入随机的有3127例。其中1564例患者服用氟西汀6个月治疗,1563例患者服用安慰剂。主要终点是阴性的(图9),只有精神健康问卷结果在两组间有统计学差异,说明氟西汀能够改善抑郁,但不能改善患者临床结局,且增加了骨折的发生风险。这个结果并不支持常规使用弗洛西汀治疗卒中后抑郁和促进功能恢复。但这并不是最终结果,在接下来AFFINITY,和EFFECTS及三项研究Meta分析的结果将提供更多关于这方面的证据。
10 脑血管病医疗质量改进:循证医学的胜利
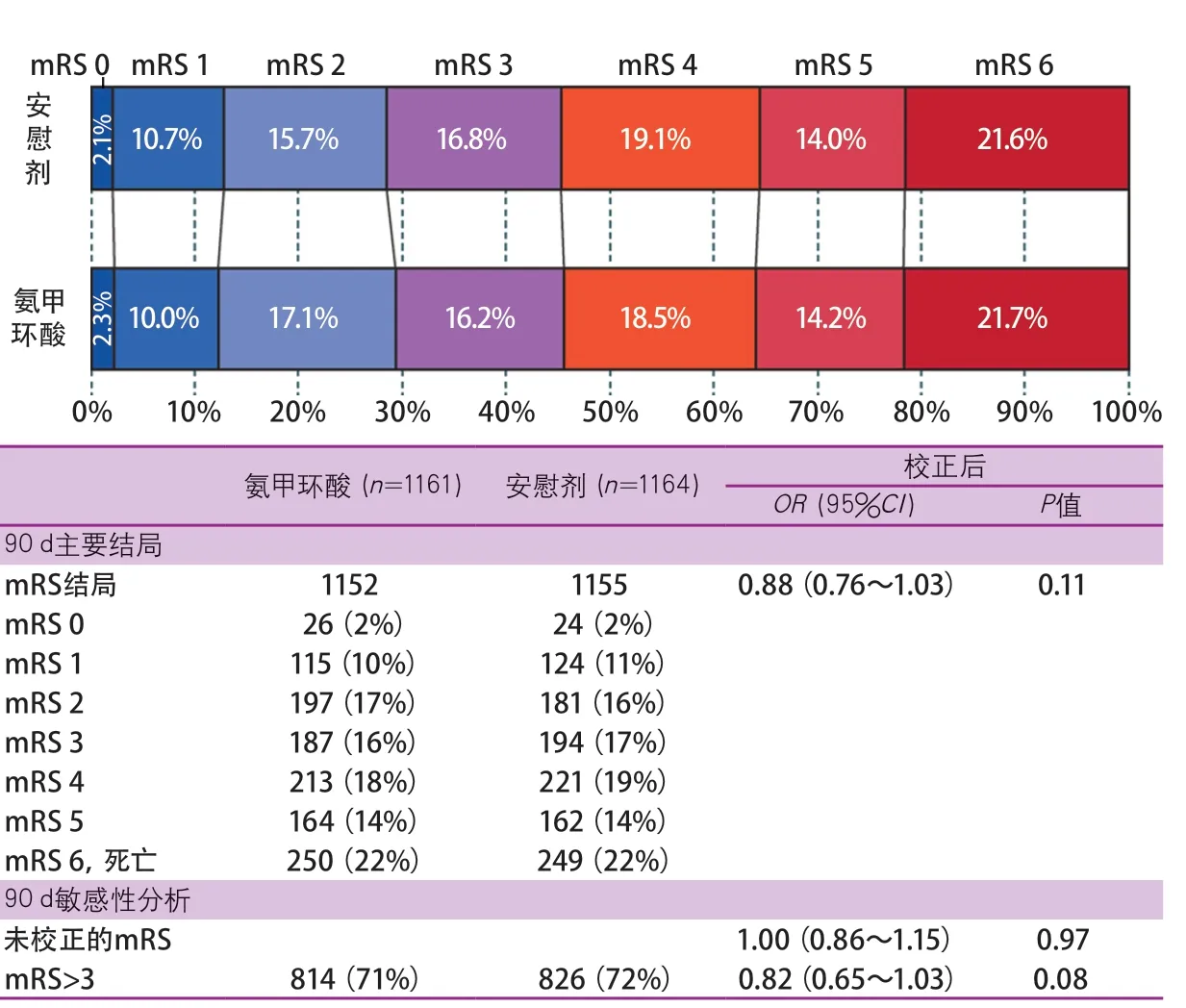
图8 TICH-2研究结果(主要终点事件)[30]
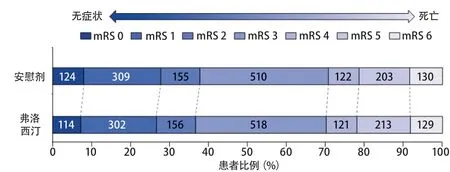
图9 FOCUS研究主要终点事件(90 d mRS评分)[32]
脑血管病领域的第十项进展,是脑血管病的医疗质量改进,医疗质量改进第一次有了循证医学的支持证据。2018年第一项医疗质量改进的数据是来自中国的研究,这是基于过去的十年,中国医疗质量整体的进步(图10,图11)。2018年发表了3项关于医疗质量的观察性研究数据。第一项是中国和美国医疗质量的比较,发表在JAHA杂志上[33];第二项是中国和印度医疗质量的比较[34];第三项是来自于中国国家卒中登记研究(The First China National Stroke Registry,CNSR)1和2的数据,发表在Circulation的分册上[35]。2018年2月,美国AHA/ASA发布了急性缺血性卒中患者早期管理指南,明确了美国指南对医疗质量的推荐。但证据级别是B-NR,也就是中等强度证据。说明证据来源于1个或多个设计比较好的非随机对照试验、观察试验或者注册试验,以及这些试验的Meta分析,但没有标准的RCT研究去支持医疗质量改进可以改善预后,国际上也一直在寻找这样的干预证据,直到2018年中国发表了第一项干预研究:金桥工程,发表在JAMA杂志上[36]。这是一项整群随机对照研究,旨在探究多重干预模式对遵从急性缺血性卒中医疗服务指标的影响,即对现有的指标的干预能否改善临床结局。

图10 中美医疗质量比较[33]

图11 中印医疗质量比较[34]
研究设计采用区组抽样RCT设计,是以医院为单位的抽样研究。从中国卒中研究网络的560家单位随机选取40家医院,其中20家接受多重干预措施,根据动态循环的管理模式,反复强化、持续改进这些指标。另外的20家医院,根据常规医疗手段进行并记录。入组患者在18岁以上,经影像学证实为发病7 d内的急性缺血性卒中,同时排除其他血管事件。提供4种干预措施:①提供临床路径;②提供医疗指标操作手册;③要求医院设专职的医疗质量协调员;④设置质量评价和反馈信息平台。每个月对干预的9项指标进行医疗质量反馈,其中包括有4项急性期指标(3 h内静脉rt-PA溶栓、入院48 h内抗栓药物治疗、入院48 h内深静脉血栓预防、住院期间吞咽功能评价),5项出院指标(出院时抗栓药物治疗、心房颤动患者出院时抗凝治疗、出院时他汀药物治疗、高血压患者控制血压、糖尿病患者出院时降糖药物治疗),都是指南中推荐的二级预防方式。主要终点是依从性,次要终点是血管事件、致残和全因死亡。研究结果显示,与对照组医院相比,干预组医院卒中复发率降低26%,致残率降低28%,但是死亡率没有改善(表4)。采用医疗质量改进的多重干预模式(临床路径、标准操作流程、专职质量控制人员和医疗质量持续反馈),可提高基于循证医学证据的缺血性卒中医疗质量服务的复合指标,进一步降低患者1年的新发血管事件发生率和致残率,从而改善患者预后。
这是全球第一篇脑血管病医疗质量改进的随机对照试验。JAMA杂志同期发表了两页述评(图12),评价该研究是基于循证医学证据的医疗质量改进模式的最佳代表,架起了卒中医疗证据与临床实践之间的桥梁。
2018年,人类防治脑血管病的征程在这些研究的推动下大幅前进。我们有理由期待更为辉煌的下一个年度。

表4 金桥工程干预组和对照组缺血性卒中临床结局事件比较[36]

图12 JAMA杂志:金桥工程架起了卒中医疗证据与临床实践之间的桥梁

