埃克替尼联合化疗在有EGFR敏感突变的初治非小细胞肺癌患者中的回顾性分析
周 欣, 朱红革, 范志勤
(新疆医科大学第三临床医学院1肺内科二病区, 2胸外科, 乌鲁木齐 830011)
肺癌是全球癌症死亡率的主要原因,其中80%~85%患者为非小细胞肺癌(NSCLC)[1]。大多数非小细胞肺癌患者在诊断时都为晚期(IIIB或IV期),因此不适合手术。对这些患者来说,全身化疗仍然是标准的治疗方案,但效果有限,而其副作用会严重影响患者的生活质量。表皮生长因子受体(EGFR)途径在非小细胞肺癌增殖中起重要作用,它在超过半数的非小细胞肺癌小分子表皮因子受体酪氨酸激酶抑制剂(EGFR-TKIs)中被激活[2],可以阻断依赖EGFR的途径,这些EGFR-TKIs靶向药物的发展为晚期非小细胞肺癌患者提供了新的治疗方案,为他们提供了新的希望。EGFR-TKIs药物目前有三代,第一代药物如吉非替尼、厄洛替尼、埃克替尼,第二代药物如阿法替尼,第三代药物如奥希替尼。EGFR突变型非小细胞肺癌患者对EGFR-TKIs敏感,对EGFR-TKIs的疗效达到70%~80%,中位存活时间达到20~30个月,与化疗患者相比,接受EGFR-TKIs的患者生活质量明显提高[3]。因此,EGFR-TKIs在美国国立综合癌症网络(NCCN)和中国抗癌协会临床肿瘤学协作专业委员会(CSCO)指南中被推荐为一线治疗方案,通常用于有EGFR敏感突变的晚期非小细胞肺癌患者。某些非小细胞肺癌患者的亚组(如女性、亚裔、不吸烟者和腺癌)EGFR敏感突变(外显子19的缺失和外显子21的L858R突变)更常见[4]。
尽管EGFR-TKIs治疗有很高的缓解率和治愈率,但它仍将不可避免地产生药物的耐药性[5]。EGFR外显子20 T790M突变是第一代EGFR-TKIs最常见的耐药机制,约占耐药病例的50%~60%。第三代EGFR-TKIs,如奥希替尼和(CO-1686),已经成为阻止(EGFRT790M)突变阳性肿瘤生长的潜在药物[6]。最近,为了延缓药物耐药性的发展,提高EGFR-TKIs作为一线治疗的疗效,将EGFR-TKIs联合化疗作为EGFR突变型晚期非小细胞肺癌的一线治疗方法[7],给予了密切关注。鉴于其不同的作用机制,EGFR-TKI联合化疗可能会改善预后。然而,一些先前的随机对照试验的结果,包括(INTACT-1)、(INTACT-2)、(TRIBUTE)和(TALENT),表明这种组合并不比单纯的化疗更有益[8]。未能取得阳性结果可能是没有通过EGFR敏感突变来选择患者。一线治疗使用EGFR-TKIs联合化疗提高生存的有效性仍存在争议。
埃克替尼(杭州贝达药业股份有限公司)是一代口服的、可逆的小分子EGFR-TKIs。与同为一代EGFR-TKIs的吉非替尼和厄洛替尼相比,埃克替尼表现出了相同的疗效,较轻的不良反应,较好的耐受性和较低的价格[8]。最常见的不良事件包括皮疹和腹泻,没有间质性肺病的报道。在以往的研究中,大多数联合治疗主要集中在吉非替尼或厄洛替尼上,因此埃克替尼联合化疗的疗效和安全性尚不清楚。为改善埃克替尼一线治疗的效果,并提供EGFR-TKIs联合化疗使用的临床依据, 本研究进行了回顾性分析,全面观察埃克替尼联合化疗一线治疗有EGFR突变晚期非小细胞肺癌患者在未设对照的总体疗效和安全性。此外,有研究报道,晚期非小细胞肺癌 EGFR 外显子19缺失的患者相比于L858R突变的患者在EGFR-TKIs治疗后,可能会有更长的PFS或OS[9]。因此,在本研究中,我们还分析了不同治疗对不同基因突变的疗效(EGFR 外显子 19缺失或L858R突变),现报道如下。
1 资料与方法
1.1一般资料在2015年1月-2017年12月,对191名符合纳入标准的患者进行回顾性分析。在分析之前,患者的记录被匿名化和去识别。本研究经新疆医科大学附属第三临床医学院伦理委员会批准。参与研究的患者均签署了书面知情同意书。研究对象包括92名男性(48.2%)和99名女性(51.8%)。中位年龄为60.8岁(范围为39~80岁)。
1.2纳入及排除标准纳入标准:(1)年龄≥18岁;(2)东部合作肿瘤组体能状态评分(ECOG PS)≤2分;(3)病理诊断晚期非小细胞肺癌(分期IIIB或IV期);(4)有EGFR突变(主要是外显子 21 L858R点突变或外显子19缺失);(5)有可测量或可评价的病灶;(6)没有其他癌症;(7)一线治疗以埃克替尼 (125 mg, tid)+化疗或埃克替尼单独(125 mg, tid)或单独化疗。排除标准:晚期非小细胞肺癌患者接受了任何先前或同时的抗癌治疗。
1.3方法
1.3.1 资料收集 统计整理患者的年龄、性别、吸烟史、EGFR突变类型、最佳疗效、毒性和生存数据。
1.3.2 疗效评价和不良事件 应用实体肿瘤的疗效评价标准(RECIST1.1)来评价肿瘤的疗效。缓解标准:完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。主要终点是无进展生存期(PFS),为从最初使用埃克替尼或化疗到肿瘤进展,及任何原因引起的死亡,或最后的随访。次要终点包括总生存期(OS)、客观反应率(ORR)、疾病控制率(DCR)和毒性。OS为埃克替尼或化疗开始使用和死亡日期或随访截止日期之间的间隔。ORR为CR+PR。DCR为CR+PR+SD。不良事件根据美国国家癌症研究所(3.0版)不良事件的常用标准评估。
1.4统计学处理采用SPSS22.0软件进行统计学分析,用χ2检验比较ORR和DCR,组间的显著性水平5% (α=0.05,双侧)。利用Kaplan-Meier方法获得PFS和OS,用对数秩检验来比较组间的差异性,采用多元Cox回归模型计算风险比,以P<0.05为差异有统计学意义。
2 结果
2.1总体患者
2.1.1 患者特点 在191例患者中,59例接受埃克替尼+化疗(A组),75例单独接受埃克替尼 (B组),57例单独接受化疗(C组),患者基线特征(年龄、性别、吸烟史、ECOG PS评分、EGFR突变)见表1。所有患者均经病理证实为肺腺癌。大多数患者为非吸烟者,有良好的美国东部合作肿瘤组体能状态评分(ECOG PS) 0~1分。102例患者(53.4%)有EGFR 外显子 19缺失,而89例(46.6%)有EGFR外显子21 L858R点突变。A组患者的化疗方案包含培美曲塞+顺铂/卡铂(20, 33.9%),紫杉醇+顺铂/卡铂(39, 66.1%)。C组的化疗方案包含培美曲塞+顺铂/卡铂(25, 43.9%),紫杉醇+顺铂/卡铂(32, 56.1%)。
2.1.2 短期疗效 A组的ORR高于B组(64.4%、46.7%,P<0.05)。B组的ORR优于C组(46.7%、26.3%,P<0.05)。A组、B组、C组的DCR分别为94.9%、92.0%和70.2%;A组与B组差异无统计学意义(P>0.05),均优于C组(P<0.05),见表2。
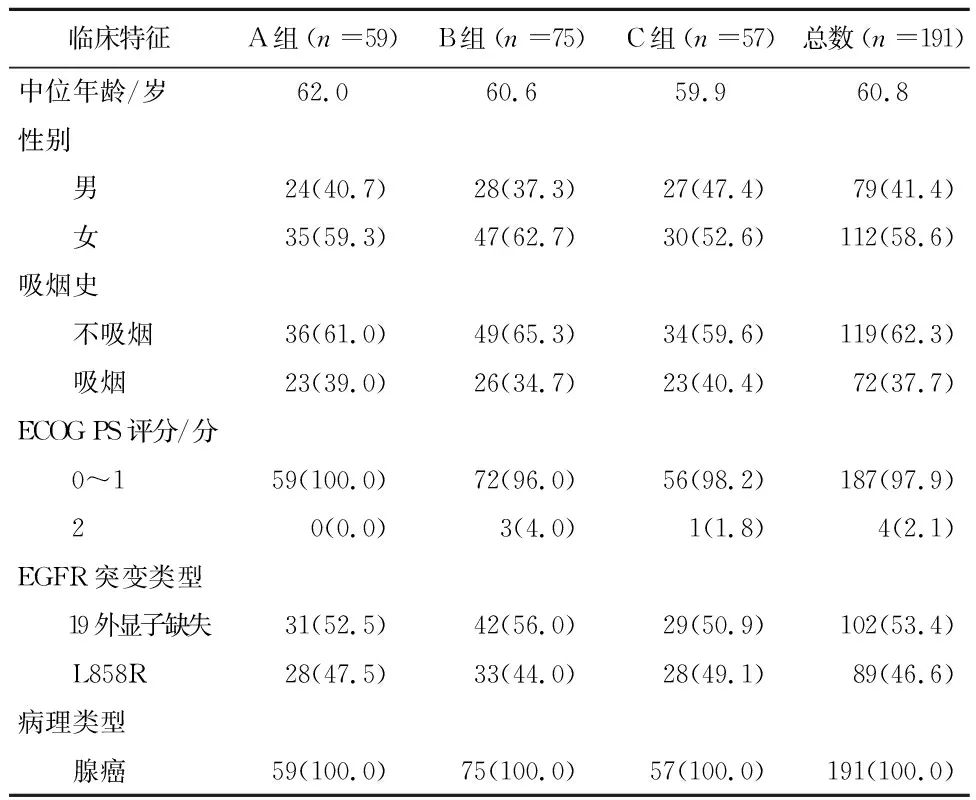
表1 总体患者的临床特点/例(%)
注: ECOG PS评分:美国东部肿瘤协作组体能状态评分。
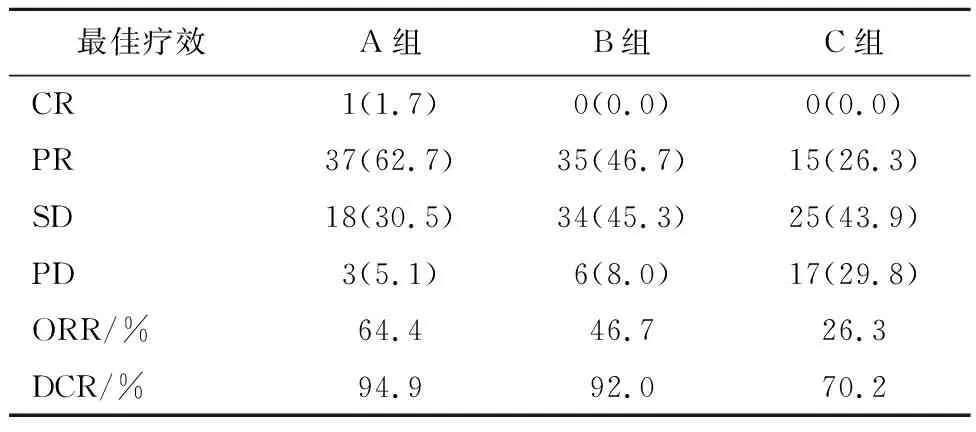
表2 总体患者的短期疗效/例(%)
注: CR:完全缓解; PR:部分缓解; SD:疾病稳定;PD:疾病进展; ORR:客观缓解率; DCR:疾病控制率。
2.1.3 生存分析 截至2017年12月,188例患者(98.4%)已达到疾病进展或死亡的终点。A组、B组和C组患者中位无进展生存期 (mPFS)分别为11.569个月(95%CI: 10.347~12.764)、8.607个月(95%CI: 7.806~9.407)和6.544个月(95%CI: 5.634~7.453)。结果显示,与单独使用埃克替尼的患者相比,使用埃克替尼+化疗的患者PFS有延长的趋势(P<0.001,图1A)。此外,单独使用埃克替尼的患者与单独化疗的患者相比PFS明显延长(P<0.05,图1A)。最后随访时,38.7%(74例)患者仍存活(A组24例、B组31例、C组19例)。中位OS为24.379个月(95%CI:21.125~27.632),A组20.244个月(95%CI:18.493~21.995), B组20.633个月(95%CI:18.148~23.117),C组OS数据不成熟。A组OS比 B组更好(P<0.05,图1B),B组与C组OS比较无统计学意义(P>0.05,图1B)。
2.1.4 不良反应 A组最常见的不良事件是血液毒性(中性粒细胞减少50.8%,贫血40.7%,血小板减少18.6%,白细胞减少22.0%),胃肠道反应(恶心39.0%,呕吐39.0%,腹泻33.9%,便秘11.9%),皮肤反应(皮疹52.5%),肝功能受损[天冬氨酸转氨酶(AST)/丙氨酸转氨酶(ALT)升高37.3%]。其他常见的不良反应包括口炎(22.0%)、疲劳(25.4%)和脱发(16.9%)。B组最常见的不良反应为皮疹(30.7%)、腹泻(21.3%)、AST/ALT升高(12.0%)。C组最常见的不良反应为血液病毒性(中性粒细胞减少, 42.1%,贫血50.9%,血小板减少22.8%,白细胞减少22.8%),胃肠道反应(恶心40.4%,呕吐40.4%,腹泻21.0%,便秘21.0%),皮肤反应(皮疹14.0%),肝功能受损(AST/ALT升高24.6%)。其他常见的不良反应包括口炎(5.3%)、疲劳(24.6%)和脱发(22.8%)。A、C组发生的血液学不良事件和胃肠道反应发生率相近,与化疗毒副反应一致。埃克替尼似乎没有加重这些毒性。与埃克替尼相关的不良事件为皮肤和胃肠道反应,大部分为轻度。3级或4级的不良事件多发生在联合治疗和化疗中。未发现与药物有关的肺间质疾病或与药物有关的死亡,见表3。
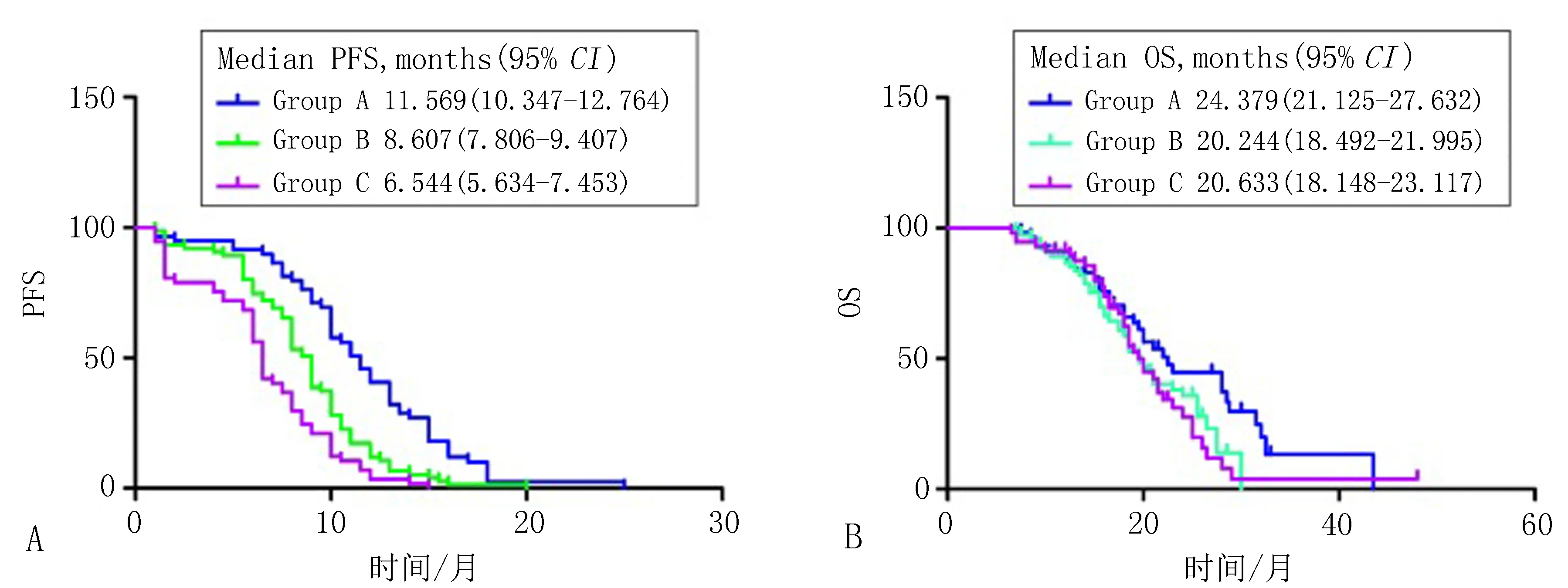
注: PFS:无疾病进展生存时间; OS:总生存时间
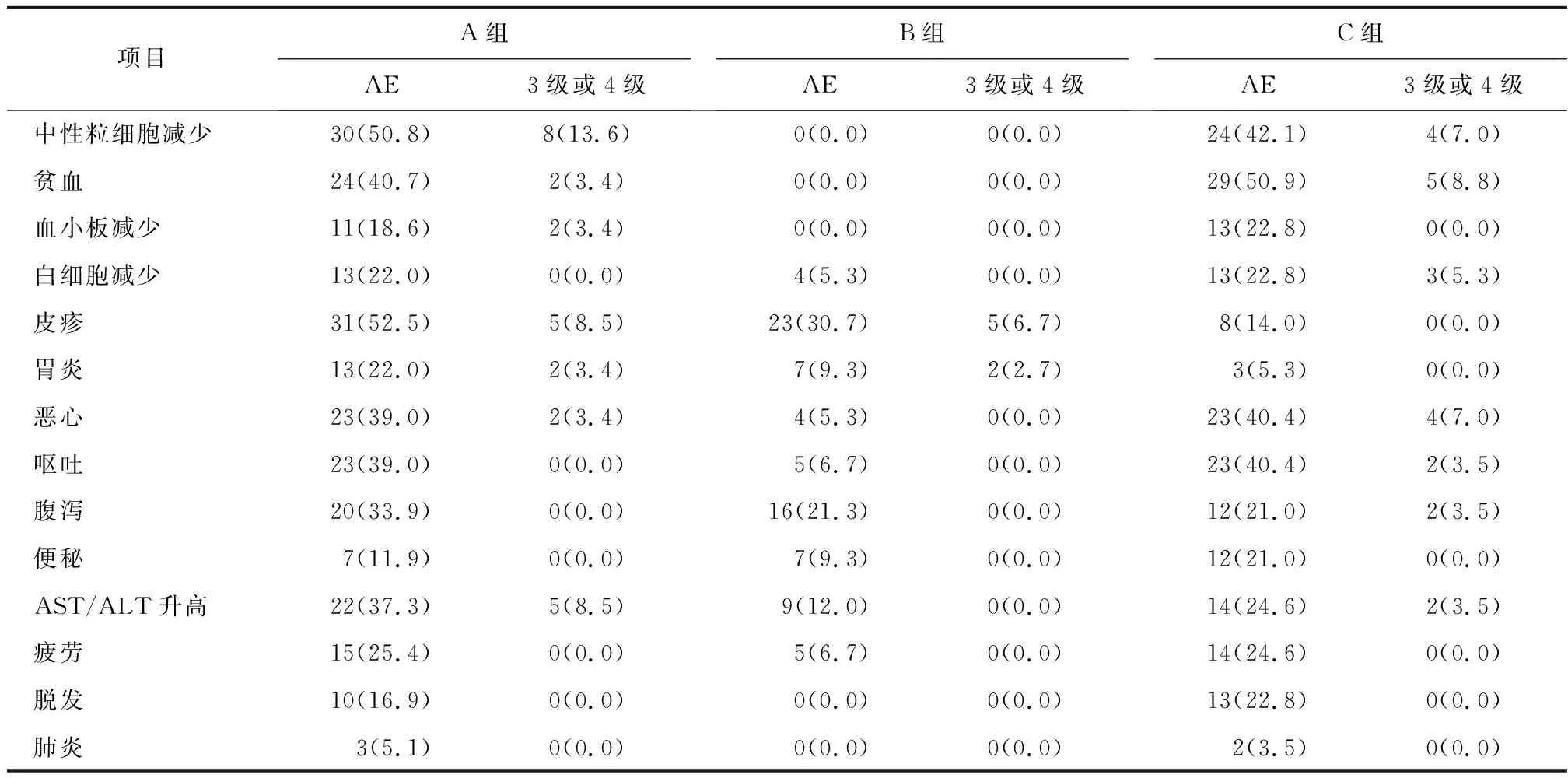
表3 不良事件
注:AE:不良事件; ALT: 丙氨酸氨基转移酶; AST: 天冬氨酸氨基转移酶。
2.2EGFR外显子19缺失患者
2.2.1 患者特点 共有102例患者存在EGFR 外显子19缺失。其中31例患者使用埃克替尼+化疗(A1组),42例患者单独使用埃克替尼 (B1组),29例患者单独使用化疗(C1组)。患者的基线特征(年龄、性别、吸烟史、ECOG PS)见表4。
2.2.2 短期疗效 A1组ORR高于B1组(74.2%,50%,P<0.05), B1组ORR优于C1 组(50%,24.1%,P<0.05)。A1组与B1组的DCR差异无统计学意义(96.8% ,92.9%,P>0.05);B1组的DCR优于C1组(92.9% ,69%,P<0.05),见表5。
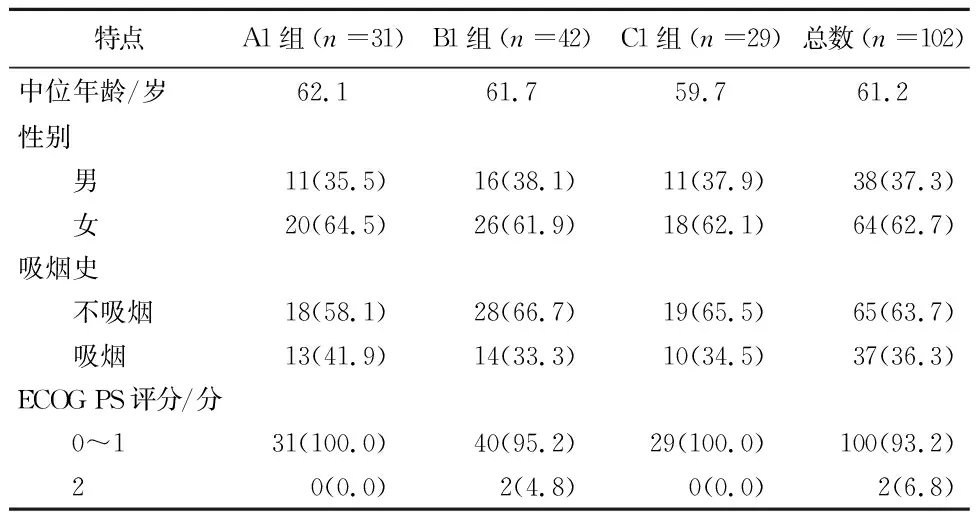
表4 EGFR外显子19缺失患者的特点/例(%)
注: ECOG PS评分:美国东部肿瘤协作组体能状态评分。
2.2.3 生存分析 A1组、B1组和C1组的mPFS分别为13.391个月(95%CI: 11.636~15.146)、9.202个月(95%CI: 8.122~10.283)和5.655个月(95%CI: 4.395~6.915)。埃克替尼+化疗患者的PFS较单独埃克替尼治疗的患者长。此外,单独使用埃克替尼患者的PFS明显比单独化疗患者长(P<0.001,图2A)。A1组的OS中位数为26.096个月(95%CI为21.533~30.660),B1组为20.470个月(95%CI为18.018~22.923),C1组为20.618个月(95%CI为16.987~24.248)。A1组OS优于B1组(P<0.05,图2B)。B组与C组OS比较无差异(P>0.05,图2B)。
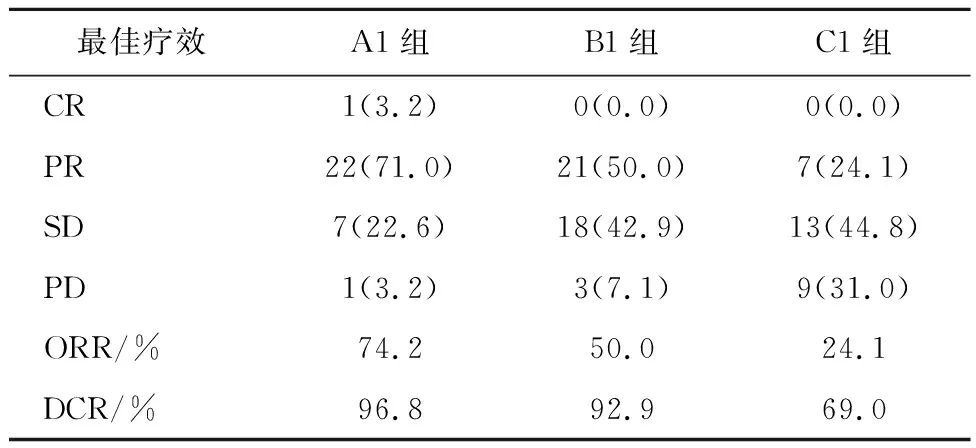
表5 EGFR外显子19缺失患者的短期疗效/例(%)
注: CR:完全缓解; PR:部分缓解; SD:疾病稳定;PD:疾病进展; ORR:客观缓解率; DCR:疾病控制率。
2.3EGFR外显子21L858R突变患者
2.3.1 患者特点 共有89例患者存在EGFR外显子 21 L858R突变。其中28例患者使用埃克替尼+化疗(A2组),33例患者单独使用埃克替尼 (B2组),28例患者单独使用化疗(C2组)。患者的基线特征(年龄、性别、吸烟史、ECOG PS),见表6。
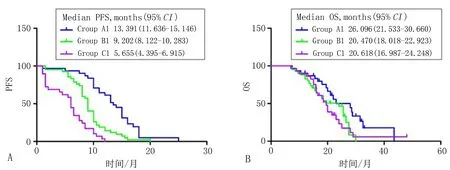
注: PFS:无疾病进展生存时间;OS:总生存时间。
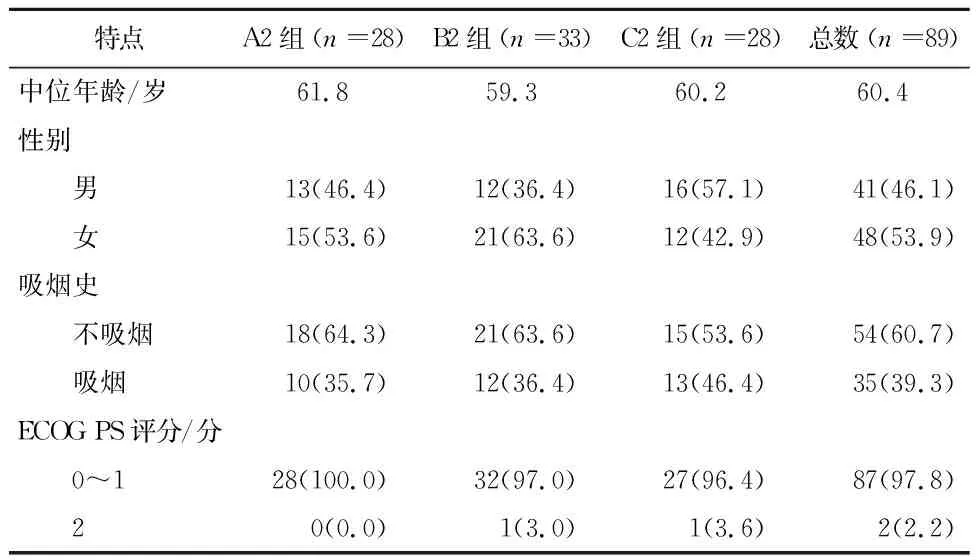
表6 EGFR L858R突变患者的特点/例(%)
注: ECOG PS评分:美国东部肿瘤协作组体能状态评分。
2.3.2 短期疗效 A2组与B2组间ORR差异无统计学意义(53.6%,42.4%,P>0.05)。虽然B2组的ORR高于C2组,但2组间差异无统计学意义(42.4%,28.6%,P>0.05)。A2组、B2组和C2组间DCR差异无统计学意义(92.9%,90.9%,71.4%,P>0.05),见表7。

表7 EGFR L858R突变患者的短期疗效/例(%)
注: CR:完全缓解; PR:部分缓解; SD:疾病稳定;PD:疾病进展; ORR:客观缓解率; DCR:疾病控制率。
2.3.3 生存分析 A2组、B2组和C2组的中位PFS为9.571个月(95%CI: 8.29~10.853)、7.848个月(95%CI: 6.92~9.005)、7.464个月(95%CI: 6.219~8.709)。在A2组中,中值OS为21.587个月(95%CI: 18.251~24.922), B2组为19.822个月(95%CI: 17.343~22.302), C2组为20.125个月(95%CI: 17.847~22.404)。埃克替尼+化疗患者与单独使用埃克替尼患者相比,PFS有较长的趋势(P<0.05,图3A),而A2组和C2组的PFS无差异(P>0.05,图3A)。虽然A2组的OS比B2组长3个月,但2组差异无统计学意义(P>0.05,图3B)。B2组和C2组的OS比较无差异(P>0.05,图3B)。

注: PFS:无疾病进展生存时间;OS:总生存时间。
3 讨论
大型临床试验显示,非小细胞肺癌存在EGFR突变的首选治疗方法是EGFR-TKIs[10-11]。然而,耐药性严重降低了EGFR-TKIs的疗效。为延缓耐药性的发展,并改善远处转移,EGFR-TKIs联合化疗与单用EGFR-TKIs的临床试验正在变得越来越流行。本研究进行的这项回顾性分析,研究了单独使用埃克替尼或联合化疗作为非小细胞肺癌患者EGFR突变一线治疗的整体疗效。
共有191名患者参加了本项研究,本研究选择5个变量(年龄、性别、吸烟史、ECOG评分和EGFR突变类型)。从统计学上看,调整化疗的各种类型和化疗药物的使用周期是很复杂的。因此,本研究的主要终点是PFS而不是OS。对于所有患者,我们发现3组患者的PFS差异有统计学意义,提示埃克替尼+化疗的疗效优于单独使用埃克替尼或单独化疗,单独使用埃克替尼的疗效优于单独化疗。本研究结果也提示埃克替尼联合化疗作为一线治疗晚期非小细胞肺癌EGFR突变有更好的ORR。虽然OS数据不成熟,但与单独使用埃克替尼或单独化疗组相比,在联合组中观察到更好的OS,而单独使用埃克替尼和单独化疗的患者OS没有差异,这可能与后续治疗有关。鉴于本研究具有回顾性,毒性资料并不是非常完整的。本组资料显示,在埃克替尼+化疗和化疗组中,不良事件更频繁。虽然有些患者在联合组中经历了3级或4级不良事件,但这些事件是可预测的和可管理的。在本组中没有发生肺间质性疾病的事件。所有的药物都耐受良好,没有与治疗相关的死亡。
本研究还观察了不同治疗对不同EGFR突变患者的疗效。结果显示,EGFR 外显子 19缺失患者埃克替尼联合化疗组比单独埃克替尼组或单独化疗组明显延长PFS,也明显延长了OS。然而,对于EGFR外显子21 L858R突变的患者,虽然埃克替尼和化疗的结合延长了PFS,但它并没有明显延长OS。先前的研究发现,晚期非小细胞肺癌患使用EGFR-TKIs治疗时,EGFR外显子 19缺失比L858R突变的患者可能会有更好的疗效。本研究还发现,与L858R突变型患者相比,EGFR 外显子19缺失的患者在使用埃克替尼联合化疗或单独埃克替尼治疗时,有更大的生存获益。
本研究存在包括小样本量、回顾性的性质和治疗方案的异质性的局限性。虽然3个组之间的基线特征有5个重要的基线变量,但化疗方案和治疗的数量各不相同,可能带来潜在的偏倚,影响研究结果。此外,由于患者人数较少,分析的能力有限,无法提供更好的治疗。此外,由于回顾性的性质,其他未测量的混杂因素可能被引入治疗组。然而,研究数据确实反映了当时的临床实践,提供了有价值的真实证据。
本研究结果与之前对厄洛替尼或吉非替尼的研究结果一致,强调EGFR突变的晚期非小细胞肺癌患者如果使用埃克替尼+化疗联合治疗,与单独埃克替尼或单独化疗相比,可以获得更好的治疗效果,特别是对于那些有EGFR外显子19缺失的患者,其毒性的适度增加在临床上是可以控制的[12-13]。这些结果表明,存在EGFR突变非小细胞肺癌患者可能会从化疗联合EGFR-TKIs出现临床获益。如果化疗联合EGFR-TKIs作为一线治疗,第三代EGFR-TKIs可以在患者被确诊有 T790M突变后继续使用。除一线治疗外,其余化疗药物仍可在进展后使用。化疗联合EGFR-TKIs可能是EGFR突变阳性非小细胞肺癌患者的一种新的治疗方案,与目前的治疗标准相比它可以改善临床结果。由于本研究是基于一小部分患者的临床数据,并考虑到在埃克替尼联合化疗的患者中出现更长的PFS或OS的趋势,应该进行更大型的前瞻性研究来确定这些治疗的真正疗效和毒性,及证实本研究的发现。此外,化疗联合EGFR-TKIs使得疗效更佳是哪些化疗药物类型,及EGFR-TKIs联合其他药物(如血管生成抑制剂或免疫抑制剂)的疗效,是未来很有前景的研究。

