白色萎缩26例临床及组织病理分析
梁晓冬,田 歆,邓 婕,叶瑞贤,陈慧姮,薛如君,梁景耀,张锡宝
白色萎缩,又名青斑样血管病变、透明性节段性血管炎,是一种好发于小腿、踝部和足背的慢性、复发性血管闭塞性疾病,以红斑、紫癜、疼痛性溃疡,愈合后遗留象牙白色瘢痕、毛细血管扩张和色素沉着为特征[1]。临床上白色萎缩并不少见,为了解其临床及组织病理特征,本文回顾性分析了广州医科大学皮肤病研究所2013 年5 月—2017年12 月诊治的26 例白色萎缩患者临床资料,现报告如下。
1 病例与方法
1.1 病例资料
所有被统计者均为广州医科大学皮肤病研究所2013 年5 月—2017 年12 月确诊为白色萎缩的患者。纳入标准:临床表现、体征、皮损组织病理检查结果符合白色萎缩诊断[1,2]。排除标准:①临床资料不全者;②有严重肝、肾功能损害者,孕期或哺乳期妇女;③组织病理诊断不明确者;④依从性差者。
1.2 方法
按照年份依次记录患者的性别、发病年龄、临床表现、既往史、既往诊断、检查结果等,组织病理重新阅片,并记录每例患者组织病理改变特征。通过电话或复诊方式对患者进行随访,了解治疗效果及复发情况。
1.3 统计学方法
采用Excel 表建立数据库,统计临床和组织病理资料。应用SPSS20.0 软件包进行数据处理。定量资料的描述采用均数±标准差,两组间显著差异分析采用Wilcoxon 检验,P<0.05 为差异有统计学意义。
2 结果
2.1 一般情况
26例白色萎缩患者中女15例,男11例,比例约1.36∶1;年龄14~81 岁,平均(29.96±18.71)岁;发病年龄9~81 岁,平均(27.19±19.39)岁;病程1 周~20年,平均(2.87±4.10)年。不同性别平均年龄、平均发病年龄、平均病程每两组间统计比较,差异无统计学意义(P均>0.05)。就诊例数在夏季最多(6~8 月,42.31%),其次为秋季(9~11 月,30.77%)、春季(3~5月,19.23%)、冬季(12 月~次年2 月,7.69%)。既往左下肢静脉栓塞史、痛风史1 例;高血压病、下肢静脉栓塞史1 例;足部外伤史3 例,包括刺伤1 例、踢伤2 例。对阿司匹林过敏1 例。亲属有类似症状1 例。
2.2 临床表现(图1)
患者皮损多位于小腿及其远端部位,其中皮损位于单侧下肢6 例,双侧下肢20 例。双侧中小腿、脚踝和足背10 例;小腿脚踝3 例;足背3 例;小腿2 例;脚踝足背2 例。早期所有患者均出现红斑、紫癜、瘀斑,在此基础上发生疼痛、大小不一的溃疡(25 例),部分患者还出现水疱(4 例)、轻中度水肿(8 例)、皮温升高(5例)。溃疡愈合后出现紫黑色、黄褐色色素沉着(26 例),点状、星状或不规则白色萎缩,肉眼毛细血管扩张(8 例)(图1)。有明显夏重冬轻发作规律6 例。
2.3 皮损组织病理改变
26 例患者均在我所行皮损组织病理检查,组织病理学示:表皮增生(主要为棘细胞层不规则增生、肥厚)13 例(50.5%),局灶表皮坏死6 例(23.1%),表皮部分缺失4 例(15.4%),表皮萎缩2 例(7.7%)。真皮内血管周围含铁血黄素沉积6 例(23.1%),真皮内见血管壁纤维蛋白样坏死22 例(84.6%),透明血栓23 例(88.5%),血管内皮细胞增生、管壁增厚4 例(15.4%),少量或大量红细胞外渗16 例(61.6%),毛细血管增生扩张,血管周围少量或大量淋巴细胞浸润,可见核尘11 例(42.3%),胶原增生7 例(26.9%)。组织病理表现为早期、急性期、晚期各为4 例、19 例、3 例(15.4%、73.1%、11.6%)(图2)。
2.4 实验室检查
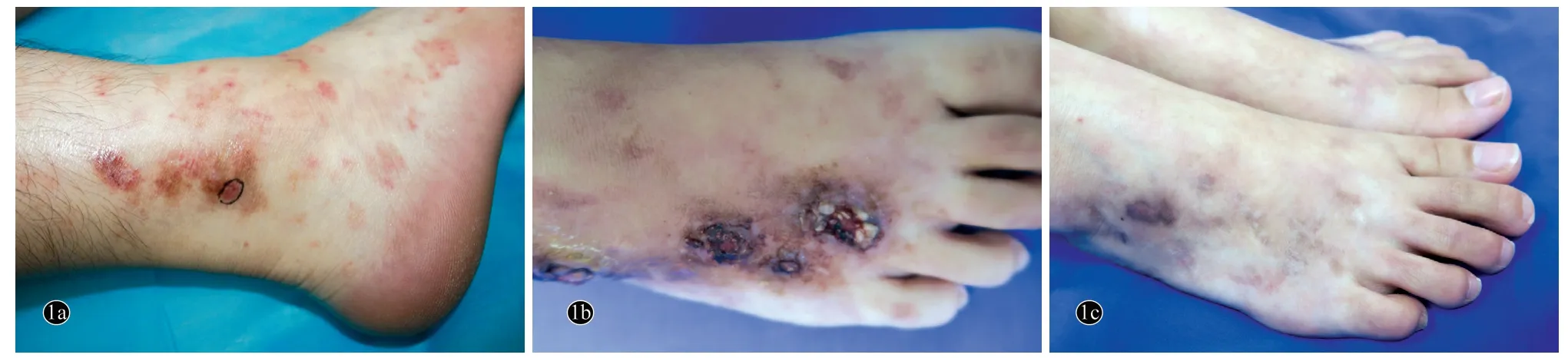
图1 白色萎缩患者小腿及足部皮损临床表现

图2 白色萎缩患者皮损组织病理(HE染色)
对26 患者进行一系列相关实验室检查,发现血常规异常11 例(42.3%),包括白细胞计数升高6 例,血小板计数升高3 例,红细胞计数并血红蛋白浓度升高1 例,红细胞沉降率升高2 例(7.7%);C 反应蛋白升高4 例(15.4%);尿常规异常6 例(23.1%),包括尿蛋白阳性2 例,尿白细胞异常4 例;凝血时间、风湿因子检查正常;肝、肾功能检查:尿酸升高3 例(11.6%);抗核抗体谱阳性、抗心磷脂抗体阳性各1 例(各占3.9%);免疫球蛋白及补体检查异常2 例(7.7%),包括C3 并IgE 升高、IgG 并C4 升高各1 例(各占3.9%)。5 例患者皮损部位真菌及细菌培养,见铜绿假单胞菌混合金黄色葡萄球菌生长1 例(20.0%)。5 例行双下肢动静脉超声检查,发现血管病变2例(40.0%)。
2.5 误诊
26 例患者中,6 例曾被诊断为变应性血管炎(23.1%)、3 例过敏性紫癜或紫癜样皮病(11.6%)、1 例淤积性皮炎(3.8%)、1 例麻风(3.8%)。
2.6 治疗与随访
除1 例患者药物过敏外,上述患者均予以阿司匹林100 mg、双嘧达莫 50 mg、维生素C 0.2 g 每日3 次口服。16 例(61.5%)口服醋酸泼尼松5~30 mg/d。6 例(23.1%)系统给予罗红霉素、阿奇霉素等抗炎治疗,1 例(3.8%)服用华法林抗凝。除系统治疗外,根据患者皮损表现予雷弗努尔、硼酸溶液湿敷创面,夫西地酸软膏、多磺酸黏多糖软膏外涂,He-Ne 激光或红蓝光照射治疗。大部分患者疼痛逐渐减轻,8~12 周明显缓解,12 周左右溃疡基本愈合。随访跟踪发现,18 例(69.2%)愈合后无复发,维持期5 个月~3 年;5 例(19.2%)病情仍反复发作,3 例(11.6%)已失访。
3 讨论
白色萎缩是一种慢性、复发性、疼痛性累及远端下肢的罕见皮肤病,于1929 年首次被Milian 等[3]描述,人群患病率约1/10 万,平均发病年龄为45 岁,男女比例约为1:3[4]。初起病一般表现为双小腿、踝部、足背对称性出现红斑、紫癜、斑疹,部分为结节、水疱,继而在其基础上发生尖锐性疼痛、溃疡、渗液、结痂,上述表现难以治愈且反复发作,夏重冬轻,长期复发遗留象牙白色或黄白色萎缩性瘢痕,呈星状、点状或不规则形,伴有毛细血管扩张和色素沉着[5]。
目前白色萎缩病因尚不明确,有学者认为与血液的高凝状态、蛋白C 蛋白S 功能缺失、高同型半胱氨酸血症、Leiden V 因子、凝血酶原基因突变、3 型粘滞性血小板综合征、血浆纤溶酶原激活物抑制因子增高等有关[6-8]。白色萎缩是一种纯粹的缺血、闭塞性皮肤病变,因此常无其余系统症状的发生,类似表现可见于某些自身免疫性疾病,如硬皮病或全身性红斑狼疮及肿瘤等,但发生机制和本质不同[9]。目前认为,直接引起血栓形成的3 个主要因素是:内皮损伤或改变、血流障碍和血液因子紊乱,从而导致高凝状态,血管梗死[10]。血栓形成源于内皮细胞纤维蛋白溶酶原缺陷、血小板功能障碍或纤维蛋白形成增强。纤维蛋白沉积、低组织灌注、循环不畅、温度变化导致伤口难以愈合,增强微生物感染几率,最终恶性循环、进一步发展成水肿和血栓形成[11]。
白色萎缩是长期血管病变的结果,因此随疾病发展阶段不同呈现不同的组织病理改变。从笔者统计的患者组织病理检查显示,早期真皮上部血管周围有稀疏淋巴细胞浸润,血管壁内纤维蛋白沉积,静脉管腔可见纤维蛋白血栓;发展期浅深层血管周围中等密度淋巴细胞浸润,真皮上部静脉壁见纤维蛋白、管腔血栓闭塞、红细胞外渗、真皮乳头水肿;终末期真皮上部稀疏淋巴细胞浸润、硬化,大量毛细血管扩张,表皮萎缩。中性粒细胞常在坏死溃疡情况下出现,通常是次要表现。该病必须行皮损组织病理检查,个别患者皮损表现特殊需进行多次或多点的取材,要求应包括溃疡基底与边缘的皮损,以提高临床组织病理检出效率。白色萎缩皮肤镜下特征与组织病理特征相关,中央象牙白色区域对应于血管炎性溃疡愈合后的真皮纤维化处;网状色素斑对应于表皮基底细胞色素沉着、真皮乳头内黑素增加;线型或球型血管对应上层真皮毛细血管扩张和增生[12]。直接免疫荧光检查显示血管壁可见均匀或颗粒状免疫复合物、纤维蛋白和补体沉积,主要由C3 和IgM 组成,这也是与其他疾病免疫复合物沉积区别的特征。最初,白色萎缩被认为是血管炎,缺血-血栓性改变是由于原发性炎症过程引起的。然而目前,许多学者认为其起初病理生理机制是由真皮内中、小口径血管血栓形成引起,而继发后期皮损的炎症反应[13]。血管炎属于异质性的临床疾病,其特征是在任何大小的动静脉管壁和任何器官中炎症发展过程,在皮肤病中非常常见。另一方面,血管病变指的是某些原因引起的血管和毛细血管非炎症性病变[14]。总之,白色萎缩为非炎症性的纤维蛋白样血管病变,区别于变应性血管炎等原发性炎症,继发性炎症往往轻微,在较多临床报告上也极易被误诊[15-18],所以尽早行组织病理检查显得尤为重要。
白色萎缩可分为特发性和继发性,一般根据确切的病史、典型发病过程、疼痛症状以及皮损组织病理检查进行诊断。另一方面,实验室检查不但可确定相关的风险因素,且可排除其他诊断[2]。临床上部分患者只表现部分的上述症状,但对其早期诊断的一个重要标志是相应部位发生溃疡前,烧灼、尖锐疼痛的出现,这种讯号是非常重要的,因为在这一阶段,皮肤缺血状态未成熟,瘢痕形成仍可预防[9]。有研究表明,皮肤血管炎分类复杂,临床表现各异,当临床诊断和组织病理诊断不一致时,应当以典型临床特征或特异性组织病理表现作为诊断依据[19]。鉴别诊断包括白细胞碎裂血管炎、结节性多动脉炎、抗磷脂综合征、高同型半胱氨酸血症、自身免疫性疾病、坏疽性脓皮病、人工性皮炎、慢性粒细胞性白血病等[20]。
白色萎缩的治疗尚无标准,主要基于现有的病例报告、系列研究和专家经验等,治疗旨在解除疼痛、预防萎缩性瘢痕的形成。迄今为止,白色萎缩的治疗主要有抗凝剂、抗血小板药、糖皮质激素、溶栓剂、静脉注射用免疫球蛋白、抗炎药、维生素、高压氧、紫外线光疗等[21]。抗凝剂如华法林是最常用的单一疗法,大部分患者对此反应良好,但由于对维生素K 依赖性因子的影响需监测国际标准化比率(维持2~3),以防出血风险[22]。利伐沙班作为新兴的直接X 因子抑制剂,一方面被报道适用于无明显凝血功能障碍患者[23,24],另一方面发现其长期维持治疗可有效预防白色萎缩的复发[25]。促性腺激素抑制剂如达那唑也较常用,有报道发现与脂蛋白a 水平升高相关的白色萎缩患者,达那唑不仅可减缓疼痛、促进伤口愈合,且可降低脂蛋白a 水平[26]。抗血小板药物通过血管舒张以及抑制环氧合酶而预防血栓形成发挥其作用[27]。对于传统治疗无效的患者可应用高压氧治疗,研究已证明高浓度纯氧能促进血管内皮细胞释放纤溶物质,伤口部位成纤维细胞、上皮细胞和新生血管的增殖,增加炎性细胞杀菌能力,增加红细胞活性,减少组织水肿以及保存细胞内能量的作用,促进伤口愈合[28,29]。此外,还有些对症支持治疗,包括止痛、使用弹力袜、抬高患肢、戒烟等措施。
本研究中大部分患者均有相似的临床特征和典型的组织病理变现,但初始误诊率仍较高,占42.31%(11/26)。阿司匹林、双嘧达莫对大多数患者有较好效果,并可作稳定病期的维持选择,在溃疡急性期,联合阿奇霉素或罗红霉素、泼尼松可使急性期溃疡疼痛较快得到控制,对于有明显季节性发作加重患者而言,按时复诊和药物维持,减少复发频率、降低症状严重程度、提高生活质量显得尤为重要。69.23%(18/26)患者经治疗后获得缓解或痊愈,但仍有部分患者疗效不佳或反复发作,病情未得到较好的控制。在临床工作中,仍需提高对白色萎缩的鉴别诊断,不断摸索最佳的治疗方案,提高诊疗效果。

