(-)-β-蒎烯对沙门氏菌的抑菌机制
何静如,刘 雪,陈文学*,陈卫军,陈海明
(海南大学食品学院,海南 海口 570228)
近年来,食源性疾病在人们的日常生活中受到越来越多的关注[1]。致病性细菌存在于各种食品中,例如,沙门氏菌、金黄色葡萄球菌和大肠杆菌等存在于鸡蛋、牛肉、鸡肉、猪肉、蔬菜、水果甚至饮用水中,严重威胁人体的健康状况[2-3]。为了抑制食品中的致病性细菌对人体的危害,食品防腐剂在食品工业中尤为重要,而常见的食品防腐剂多为一些可能对人体有副作用的化学物质;故寻找真正对人体安全、天然的抑菌物质至关重要[3]。精油是从不同植物的不同部位分离出来的一种混合物[4],它是由多种化学成分组成,其中较为重要的成分有萜烯类化合物、萜类化合物、芳香族和脂环族化合物,例如α-蒎烯、(-)-β-蒎烯、柠檬烯、C16和C29类的烷烃等[5-7]。据相关文献报道,精油不仅具有良好的抗氧化性、抗癌性以及抗过敏性,其对单核细胞增生李斯特菌、金黄色葡萄球菌、沙门氏菌都有很好的抑菌效果;且精油作为一种可预防食源性疾病的天然食品添加剂对人体健康几乎没有危害[3,8-9]。尽管已经有很多关于精油成分以及精油抑菌活性和机制的研究,如Cui Haiying等[10-11]的研究发现精油可以破坏细胞膜的完整性,使胞内物质如DNA、腺苷三磷酸(adenosine triphosphate,ATP)溢出等。但关于精油中究竟是哪种成分起主要作用仍不是十分明晰,也鲜有报道[8],因此后续对精油的深入研究空间较广。
Zou Lan等[12]研究了胡椒提取物对大肠杆菌和金黄色葡萄球菌的抑菌机制,结果表明胡椒提取物对细菌的细胞结构、ATP含量和三羧酸(tricarboxylic acid,TCA)循环中有机酸含量等有影响。而(-)-β-蒎烯存在于各种植物精油中,它也是胡椒提取物中的一种重要成分,更重要的是,有研究表明其具有抑菌、抗抑郁、抗病毒等功效[13]。因此,深入研究(-)-β-蒎烯的抑菌机制,可为其作为一种天然食品防腐剂提供理论依据。
沙门氏菌属于革兰氏阴性菌,除鸡白痢沙门氏菌和鸡伤寒沙门氏菌外,大多数沙门氏菌可以依靠周身鞭毛运动[14]。沙门氏菌感染可经鸡蛋、饮水、加工食品、环境等途径传播,不仅对家禽的生存造成威胁,而且被其感染的食品经消化道进入人体内,会对人体健康造成严重损害,已引起国际上越来越多的关注和重视[15-16]。因此,找到有效抑制沙门氏菌的天然食品添加剂对人类健康至关重要。
综上所述,本研究主要探究(-)-β-蒎烯对沙门氏菌的抑菌机制,通过测定最小抑菌浓度(minimum inhibition concentration,MIC)确定其抑菌活性,再通过扫描电子显微镜观察,并分析其对沙门氏菌的电导率、TCA循环中关键酶活力和ATP含量的变化趋势研究其抑菌机理。本研究为预防食源性致病菌对人体的危害提供了新思路和理论依据。
1 材料与方法
1.1 菌株、材料与试剂
实验菌种为沙门氏菌,由广东微生物菌种保藏中心提供。
(-)-β-蒎烯 阿拉丁试剂(上海)有限公司;营养肉汤、琼脂(均为生物试剂)、琥珀酸脱氢酶活力测定试剂盒、α-酮戊二酸脱氢酶活力测定试剂盒、ATP含量测定试剂盒 北京索莱宝科技有限公司;无水乙醇(分析纯) 广州化学试剂厂。
1.2 仪器与设备
TU1810紫外-可见分光光度计 北京普析通用仪器有限责任公司;ST16R高速冷冻离心机 美国Thermo公司;S-3000扫描式电子显微镜 日本日立公司;SPX-288生化培养箱 宁波江南仪器厂,SHA-2恒温振荡器 常州奥华仪器有限公司;JYD-650L超声波细胞粉碎机 上海之信仪器有限公司;DDS-307电导率仪 上海雷磁有限公司;TDZ5-WS多管架离心机上海卢湘仪离心机仪器有限公司;ALPHA 1-2型冷冻干燥机 北京五洲东方科技发展有限公司。
1.3 方法
1.3.1 MIC测定
采用肉汤稀释法进行MIC的测定[17]。用无菌生理盐水(NaCl质量分数0.9%)将培养24 h的沙门氏菌稀释至106~107CFU/mL。在无菌平板中添加2 mL(-)-β-蒎烯溶液(体积分数70%的乙醇溶液溶解),同时加入18 mL温度为40~60 ℃的固体培养基并迅速往复摇动,使(-)-β-蒎烯含量别为40、20、10、5、2.5、1.25、0.625 mL/L。以添加相同体积的无菌生理盐水和体积分数70%乙醇溶液分别作为空白对照组和阴性对照组。取200 μL上述菌悬液在各平板上涂布均匀,于37 ℃恒温培养箱中倒置培养24 h,以肉眼不见菌生长的(-)-β-蒎烯含量为MIC。
1.3.2 细胞形态的观察
采用扫描电子显微镜观察沙门氏菌细胞形态的变化[18-19]。向培养至对数期的目标菌悬液中加入(-)-β-蒎烯,使其含量分别为2 MIC、1 MIC、1/2 MIC,以不加(-)-β-蒎烯的作为空白对照组,以加入体积分数70%乙醇溶液的作为阴性对照组。将各组菌悬液置于37 ℃恒温摇床培养,取培养至8、16 h的菌悬液各50 mL,6 000 r/min低温离心10 min收集菌体。使用无菌磷酸盐缓冲液(pH 7.2)清洗菌体3 次,再用体积分数依次为20%、40%、60%、80%的乙醇溶液进行梯度脱水,每个含量均洗脱2 次,最后用无水乙醇洗脱3 次。将脱水后的样品在-20 ℃条件下预冻2 h后使用真空冷冻干燥机冷冻干燥12 h。取出完全干燥的样品,上样、镀金、扫描电子显微镜观察。
1.3.3 电导率测定
采用电导率仪进行测定[20]。将2%沙门氏菌菌悬液(106~107CFU/ mL)接种于150 mL营养肉汤培养基中,摇床振荡(130 r/min、37 ℃)培养至对数期,再向其中分别加入2 MIC、1 MIC和1/2 MIC的(-)-β-蒎烯溶液;以不加抑制物的为对照组,置于37 ℃摇床中继续振荡培养,并分别于0、2、4、6、8、10、12、14 h取出5 mL,4 000 r/min离心15 min,取上清液测其电导率。平行测定3 次。
1.3.4 样品制备
使用无菌生理盐水溶液对斜面传接至4 代的沙门氏菌进行洗脱,采用麦氏比浊管法配制浓度为106~107CFU/mL的菌悬液。分别取体积分数2%的菌悬液加入5 个装有250 mL营养肉汤培养基的锥形瓶中,置于37 ℃、130 r/min条件下摇床培养至对数期。再向其中添加(-)-β-蒎烯溶液,使其含量分别为2 MIC、1 MIC、1/2 MIC,以添加相应量的体积分数70%乙醇溶液作为阴性对照组,以不添加任何物质的作为空白对照组,继续摇床培养。培养过程中分别于0、3、6、9、12、24 h取10 mL菌液在4 ℃下11 000 r/min离心10 min,弃上清液,收集菌体,用无菌磷酸盐缓冲液清洗3 次并重新悬于缓冲液中。在冰浴条件下,使用超声细胞破碎仪对细菌悬浮液破碎6 min(550 W,间隔10 s),将破碎的悬浮液于4 ℃下11 000 r/min离心10 min,弃下层细胞残渣,将上清液保存于4 ℃冰箱中以备测定琥珀酸脱氢酶(succinic acid dehydrogenase,SDH)、α-酮戊二酸脱氢酶(α-ketoglutarate dehydrogenase,α-KGDH)活力和ATP含量。
1.3.5 SDH活力测定
SDH活力采用试剂盒进行测定[21]。向相应编号的试管中加入100 μL样品液,迅速加入2.6 mL工作液,立即混匀并计时,迅速倒入比色皿中,在可见分光光度计600 nm波长处比色,5 s时读取吸光度A1,在1 min5 s时再次测定吸光度A2,求出2 次吸光度差值ΔA(A1-A2)。样品蛋白质量浓度测定采用考马斯亮蓝法。并采用公式(1)进行SDH活力计算。

式中:t为反应时间(1 m i n);V为取样量(0.1 mL);ρpr为样本蛋白质量浓度/(mg/mL)。
1.3.6 α-KGDH活力测定
α-KGDH活力采用试剂盒进行测定。取1.3.4节中的样品液按照试剂盒说明书进行操作,立即记录340 nm波长处20 s时的吸光度A1和2 min 20 s时的吸光度A2,以上比色均采用蒸馏水调零;计算ΔA(A2-A1)。并采用公式(2)进行α-KGDH活力计算。

式中:V总为反应体系总体积/L;ε为NADH摩尔消光系数(6.22×103L/(mol·cm));d为比色皿光径/cm;V样为样本体积/mL;ρpr为样本蛋白质量浓度/(mg/mL);t为反应时间/min。
1.3.7 ATP含量的测定
细菌培养过程中ATP含量采用ATP含量测定试剂盒进行测定[22]。取1.3.4节中的样品液按照试剂盒说明书进行操作,最后在636 nm波长处,用光径0.5 cm比色皿,以双蒸水调零,测定各管吸光度。
1.4 数据处理
所有结果均使用DPS 6.5数据分析软件进行方差分析,结果以平均值±标准差表示。Origin 9.0软件制图。
2 结果与分析
2.1 (-)-β-蒎烯对沙门氏菌的MIC
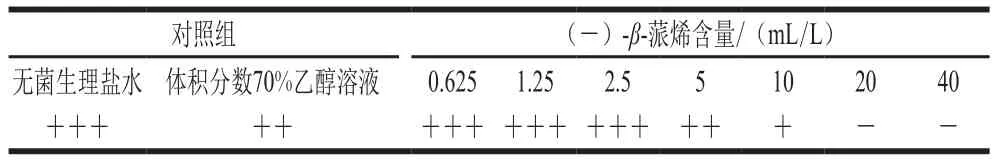
表1 沙门氏菌生长情况Table1 Growth status of Salmonella
从表1中可以看出,体积分数70%的乙醇溶液对沙门氏菌的生长并无明显影响,随着(-)-β-蒎烯溶液含量的逐渐增大,其对沙门氏菌生长的抑制作用也随之增大,当抑菌物质的含量达到20 mL/L时,没有菌体生长,即(-)-β-蒎烯对沙门氏菌的MIC为20 mL/L。
2.2 (-)-β-蒎烯对沙门氏菌细胞形态的影响

图1 (-)-β-蒎烯处理后沙门氏菌的细胞形态Fig.1 Effect of (-)-β-pinene on the morphology of Salmonella
如图1所示,空白对照组的沙门氏菌细胞呈现正常的杆状(图1a),阴性对照组的沙门氏菌细胞形态受到微小破坏,大部分仍呈现正常的短杆状(图1b),而(-)-β-蒎烯处理组的沙门氏菌的细胞形态则受到严重破坏(图1c~e)。(-)-β-蒎烯处理16 h后,细胞破裂、黏结在一起,界限模糊,细胞壁和细胞膜被破坏,细胞形态受到严重影响,且破坏程度依次为2 MIC>1 MIC>1/2 MIC(图1c~e)。因此,实验结果表明(-)-β-蒎烯可以破坏沙门氏菌的细胞壁和细胞膜,且含量越大,破坏作用越大。(-)-β-蒎烯造成沙门氏菌的细胞形态及结构的破坏可能会导致胞外的大分子物质可以进入细胞内,细胞内的一些物质也会溢出细胞外,同时细胞的正常代谢途径也会受到一定程度的影响[18],最终导致细菌死亡。
2.3 (-)-β-蒎烯对沙门氏菌细胞膜完整性和通透性的影响

图2 (-)-β-蒎烯对沙门氏菌电导率的影响Fig.2 Effect of (-)-β-pinene on the conductivity of Salmonella
电导率的变化是衡量细菌细胞结构变化的一个重要指标。从图2中可以看出,不加抑菌物质的沙门氏菌菌液电导率呈现微小上升的趋势,由0 h的9.88 mS/cm上升到14 h的10.11 mS/cm;而添加(-)-β-蒎烯的菌悬液电导率明显增大,如2 MIC的菌液电导率由0 h的9.90 mS/cm增加至14 h的11.80 mS/cm;1 MIC的菌液电导率由0 h的9.87 mS/cm增加到14 h的11.67 mS/cm;1/2 MIC的菌液电导率由0 h的9.91 mS/cm增加至14 h的11.21 mS/cm。整个实验过程中电导率基本为2 MIC>1 MIC>1/2 MIC>空白对照组,这表明(-)-β-蒎烯使沙门氏菌的细胞膜结构遭到一定程度的破坏,膜渗透性发生改变,胞内离子如K+、Ca2+、Mg2+外泄增加,从而导致菌液的电导率增大,且(-)-β-蒎烯的含量越大,对膜结构的破坏作用也就越大,离子泄漏也更加多,这与张赟彬等[23]研究的荷叶精油对沙门氏菌的菌液电导率影响结果相一致。另一方面,在8 h之后,添加抑菌物质的菌液电导率都有一定幅度的下降,这可能是因为此时(-)-β-蒎烯与外泄的离子产生了静电结合[24],从而导致离子浓度下降,使电导率降低。
综合2.2、2.3节中对沙门氏菌细胞形态的观察以及对菌液电导率变化的研究结果,表明(-)-β-蒎烯对沙门氏菌的细胞形态和结构都会产生一定的破坏作用,会导致细胞变短变粗、破裂、黏结、细胞膜的完整性和通透性发生改变,胞内物质外溢,从而使电导率增大,影响菌体的正常生长和代谢,最终导致死亡,且(-)-β-蒎烯的含量越大,破坏作用越大。
2.4 (-)-β-蒎烯对沙门氏菌TCA中关键酶活力的影响
2.4.1 对SDH活力的影响
SDH在TCA循环中主要起到了氧化脱氢的作用,其催化琥珀酸进行脱氢反应,黄素腺嘌呤二核苷酸是该反应的辅基,生成黄素腺嘌呤二核苷酸递氢体,为细菌细胞的代谢途径提供能量,从而使整个TCA循环具有可持续性[25-26]。

图3 (-)-β-蒎烯对沙门氏菌SDH活力的影响Fig.3 Effect of (-)-β-pinene on SDH activity in Salmonella
如图3所示,空白对照组和阴性对照组的SDH活力变化不明显;而在(-)-β-蒎烯作用下,实验组的SDH活力呈现先上升后下降再上升的趋势。在0~9 h,添加不同含量的(-)-β-蒎烯溶液的实验组波动不明显,SDH活力差异也较小;9 h之后,实验组的SDH活力均呈大幅度增加,且明显有2 MIC>1 MIC>1/2 MIC>对照组,结果说明随着培养时间的延长,(-)-β-蒎烯可使沙门氏菌的SDH活力增强,这可能是由于(-)-β-蒎烯作用于SDH活力部位,导致沙门氏菌对(-)-β-蒎烯产生了抵抗作用,从而使SDH活力增大,且(-)-β-蒎烯的含量越高,抵抗作用就越强,SDH活力就增大得越多。
2.4.2 对α-KGDH活力的影响
在TCA循环中α-KGDH酶系催化α-酮戊二酸生成琥珀酰CoA,并产生NADH,将电子提供给呼吸链[27]进而产生细菌生长繁殖所需要的能量。α-KGDH酶系包括α-KGDH、二氧硫辛酸琥珀酰转移酶和二氢硫辛酸脱氢酶3 种酶。

图1 (-)-β-蒎烯对沙门氏菌α-KGDH活力的影响Fig.1 Effect of (-)-β-pinene on α-KGDH activity in Salmonella
从图4中可以看出,空白对照组的α-KGDH活力呈波动趋势,但变化不大,阴性对照组的α-KGDH活力波动变化并最终下降至最低点,而添加(-)-β-蒎烯的实验组的α-KGDH活力在0~9 h内呈现波动趋势,在9 h后,则迅速增大,至24 h时增大至最高点,且2 MIC>1 MIC>1/2 MIC>空白对照组>阴性对照组,说明在(-)-β-蒎烯的作用下,随培养时间的延长,α-KGDH活力增大,这可能是由于(-)-β-蒎烯对沙门氏菌α-KGDH的基因表达产生影响,使其对抑制物的敏感性增强,从而使α-KGDH活力增大。同时,ATP为该酶的别构抑制剂,当ATP含量充足时,酶活力降低,而当ATP含量下降时,酶活力升高。通常,当细胞凋亡、坏死或在毒性物质作用下时,细胞的膜电位会下降,为了保持细胞的质子动势平衡,ATP的含量也会急剧下降[28]。因此,在(-)-β-蒎烯的作用下可能导致了α-KGDH活力的增强。
2.5 (-)-β-蒎烯对沙门氏菌细胞内ATP含量的影响
ATP是由一分子腺嘌呤、一分子核糖和三分子磷酸组成的不稳定化合物,其在细胞的各种生理、病理过程中起着十分重要的作用,并且直接为生物体生命活动提供能量。
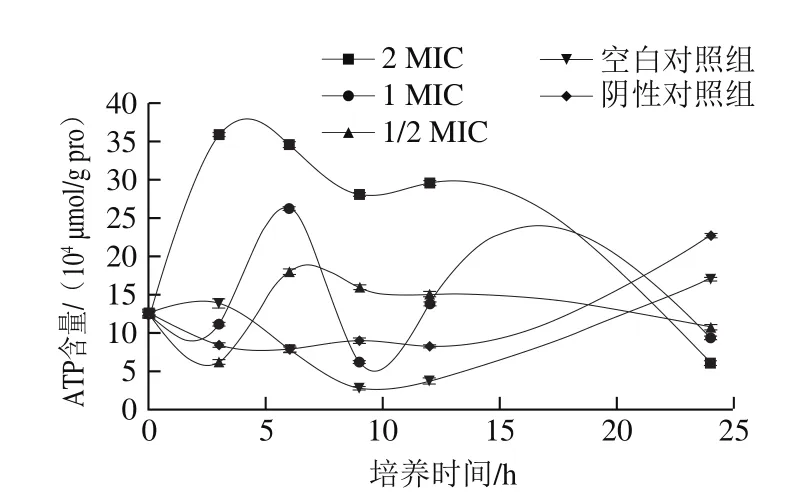
图5 (-)-β-蒎烯对沙门氏菌ATP含量的影响Fig.5 Effect of (-)-β-pinene on ATP level in Salmonella
从图5可以看出,空白对照组和阴性对照组的ATP含量在培养前期处于波动状态,在培养后期均呈现增大趋势;而添加(-)-β-蒎烯的实验组,在0~9 h均呈现先上升后下降的趋势,2 MIC组在3 h时ATP含量增大到最大值,为359 348.849 μmol/g pro;而1 MIC组和1/2 MIC组则在6 h时增大到最大值,分别为262 332.292 μmol/g pro和179 776.059 μmol/g pro;而在培养后期ATP含量急剧下降,在24 h时ATP含量降至最低,分别为60 975.982(2 MIC)、93 195.885(1 MIC)、107 400.849(1/2 MIC)μmol/g pro。结果表明(-)-β-蒎烯对沙门氏菌生长过程中ATP的形成存在一定程度的影响,会造成ATP含量的下降,这可能是因为在(-)-β-蒎烯的作用下,导致细胞质子动力的降低[29]或者膜电位的降低,阻碍了氢的传递与接收[30],从而使ATP的合成受到了抑制。同时,ATP水平的降低也可能是由于细胞过度凋亡和过度的ATP消耗造成的,因为细胞凋亡是一种依赖于ATP的过程[30]。总之,(-)-β-蒎烯会削弱沙门氏菌的产能能力。
3 结 论
综合以上(-)-β-蒎烯对沙门氏菌的抑菌机制研究结果,表明(-)-β-蒎烯主要是通过破坏其细胞形态和结构,导致离子的泄漏,增强TCA循环中SDH和α-KGDH的活力以及降低ATP含量来抑制沙门氏菌的正常生长。本研究为之后进一步探究(-)-β-蒎烯和精油中其他成分对食源性致病菌的抑菌机制提供理论支撑和新的思路。

