离子色谱-三重四极杆质谱联用法测定奶粉中氟乙酸钠
张秀尧,蔡欣欣,张晓艺,李瑞芬
(温州市疾病预防控制中心,浙江 温州 325001)
氟乙酸钠是有机氟类杀鼠剂,属A级剧毒物,大鼠口服半致死量为0.22 mg/(kg·bw), 人体口服半致死量为0.1~10 mg/(kg·bw)。由于氟乙酸钠对人和动物的毒性极强、起效快、致死率高,并容易引起二次中毒,我国于1982年就明令禁止其生产、销售和使用[1],但在新西兰、澳大利亚、以色列和美国仍允许使用[2]。
目前,氟乙酸钠的检测方法有气相色谱-质谱联用法[3]、离子色谱法[4]、液相色谱-串联质谱法[1, 5-6]等。其中,气相色谱-质谱联用法需要将样品衍生化后才能测定,操作较繁琐;离子色谱法灵敏度低,定性能力较弱,易出现假阳性结果;采用液相色谱-串联质谱法检测时,由于氟乙酸钠在反相色谱柱上保留较弱,易受基质成分干扰[1],若进行衍生化,产率受样品基质影响,且操作复杂耗时[5],也有采用反相和强阴离子交换固相萃取柱(PAX)进行净化的报道,但因柱容量有限,易被样品基质饱和而影响氟乙酸钠回收率[6]。奶粉中氟乙酸钠的测定方法主要有液相色谱-串联质谱法[7]和液相色谱-四极杆/静电场轨道阱高分辨质谱法[8]。前者将奶粉样品用丙酮溶液提取,再将提取液过自填的AG 1-X8强阴离子树脂固相萃取柱,用0.2 mol/L HCl溶液洗脱,用3-硝基苯胺衍生氟乙酸钠,衍生物经Oasis HLB固相萃取柱净化,样品前处理比较繁琐。后者先用正己烷脱脂,再用6 mol/L硫酸调节pH<1,用乙腈超声提取,NaCl和MgSO4盐析,氮吹浓缩,虽然步骤简化但净化效果不佳。
本研究拟建立离子色谱-三重四极杆质谱联用方法检测奶粉中氟乙酸钠。采用高氯酸沉淀去除样品中蛋白和脂肪等杂质,叔丁基甲醚萃取净化,借助于离子色谱分离,三重四极杆质谱检测,稳定同位素内标法定量分析,希望为检测奶粉中氟乙酸钠提供新途径。
1 实验部分
1.1 仪器与设备
离子色谱系统:美国Thermo Scientific公司产品,由Dionex ICS-1100离子色谱仪、淋洗液自动发生器(RFC-30)、电解再生抑制器(ASRS 500)和自动进样器(DV-AS)组成,由变色龙工作站(7.22版)控制;QTRAP 6500三重四极杆/复合线性离子阱串联质谱仪:美国AB SCIEX公司产品,由Analyst 1.6.2软件控制;Multi Reax数显型多管旋涡混合器:德国Heidolph公司产品;3-30K高速冷冻离心机:德国Sigma公司产品;N-EVAP氮吹仪(24孔):美国Organomation公司产品;2510超声波清洗机:美国Branson公司产品;Gradient A10 Mill-Q 超纯水器:法国Millipore公司产品。
1.2 材料与试剂
叔丁基甲醚、丙酮:均为HPLC级,德国Merck公司产品;高氯酸:上海桃浦化工厂产品;亲水性聚丙烯(GHP)滤膜针式过滤头(直径13 mm,孔径0.2 μm):美国Pall公司产品;氟乙酸钠标准物质(纯度97%):德国Dr. Ehrenstorfer公司产品;13C2-氟乙酸钠同位素标准物质:新西兰BDG Synthesis公司产品。分别用水溶解氟乙酸钠、13C2-氟乙酸钠标准物质并稀释,得到1.30 g/L氟乙酸钠标准贮备溶液和130 mg/L13C2-氟乙酸钠标准贮备溶液,使用时用水稀释至合适浓度的标准工作溶液。
1.3 实验条件
1.3.1样品前处理 称取0.50 g奶粉试样于15 mL塑料具塞离心管中,加入100 μL 1.3 mg/L13C2-氟乙酸钠同位素内标液和2.0 mL水,旋涡10 s,再加入4.0 mL 3%高氯酸,旋涡10 s,超声提取5 min,于6 ℃以10 000 r/min离心5 min,取约4 mL(pH 0.5~1.0)中间清液于15 mL具塞离心管中。向其中加入5.0 mL叔丁基甲醚,于多管旋涡混合器中旋涡3 min,以10 000 r/min离心2 min,移取上清液,用5.0 mL叔丁基甲醚重复提取残渣1次,合并2次提取液。向提取液中加入100 μL 1%氨水丙酮溶液,混匀,于45 ℃氮吹至近干,加入1.0 mL 0.1%氨水溶液,旋涡10 s,过0.2 μm有机滤膜,待测。
1.3.2色谱条件 IonPac AS 19 型色谱柱(2 mm×250 mm×7.5 μm),AG19保护柱(2 mm×50 mm);ASRS 500阴离子抑制器(2 mm,外接水模式);KOH淋洗液由RFC-30自动在线产生;梯度淋洗程序:0~7 min(5 mmol/L KOH),7~8 min(5~50 mmol/L KOH),8~14 min(50 mmol/L KOH),14~20 min(5 mmol/L KOH);淋洗液流速0.30 mL/min;柱温30 ℃;进样体积10 μL。
1.3.3质谱条件 电喷雾电离(ESI)负离子多反应监测模式;离子化电压(IS)-4 500 V;离子源温度650 ℃;气帘气压强277 kPa;喷雾气压强345 kPa;辅助加热气压强345 kPa;碰撞气设为Medium;氟乙酸钠定量离子对为m/z77.0>57.0,去簇电压-40 V,碰撞能量-15 eV;13C2-氟乙酸钠的定量离子对为m/z79.0>59.0,去簇电压-40 V,碰撞能量-15 eV;质谱峰驻留时间均为1 000 ms。
进样运行开始时,离子色谱柱流出液经六通切换阀切换至废液,5.50 min切换至离子源,质谱同时采集数据,直到8.00 min六通切换阀又将柱流出液切换至废液中。
2 结果与讨论
2.1 质谱条件优化
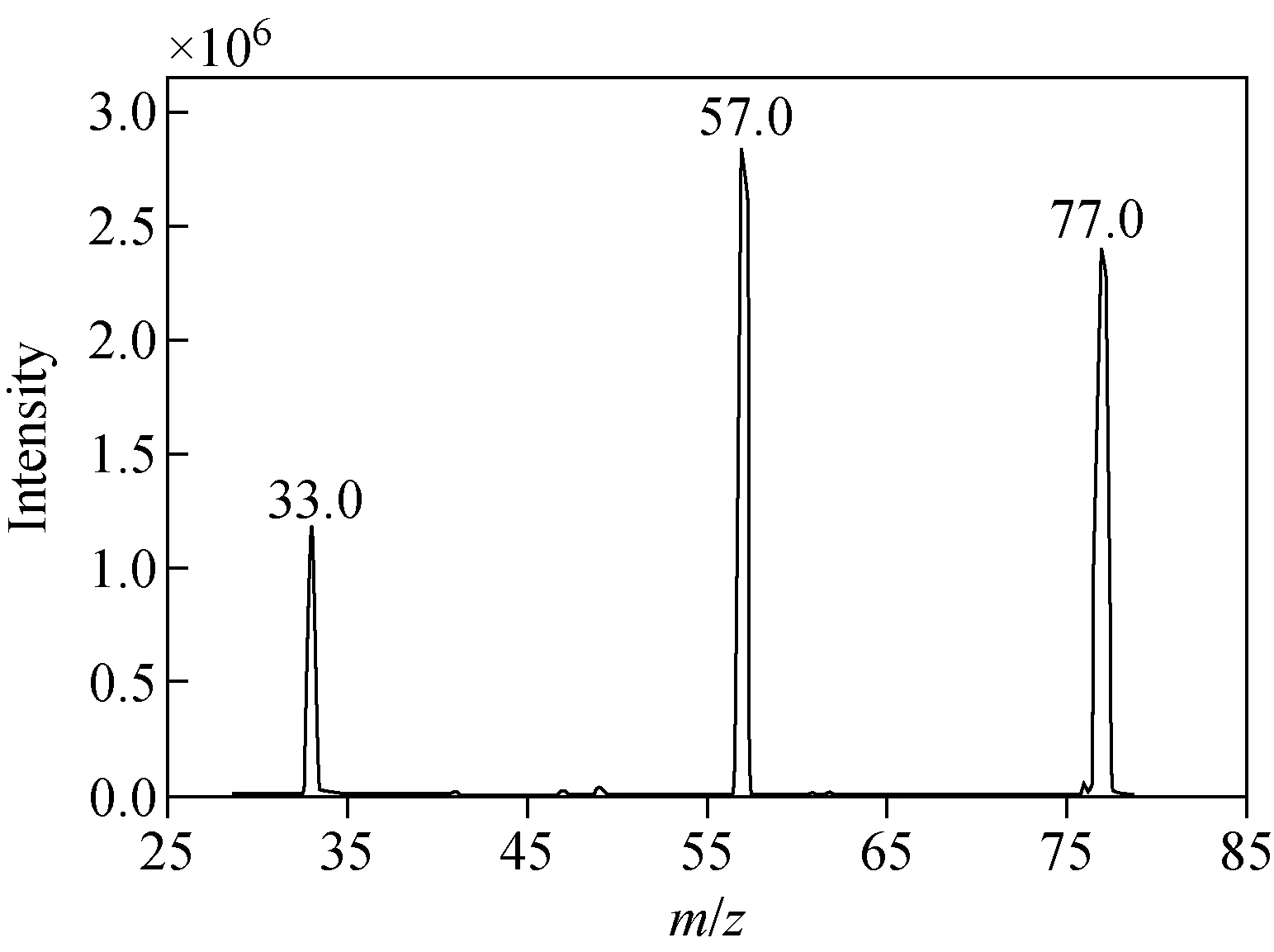
图1 氟乙酸钠子离子扫描谱图Fig.1 Product ion scan spectrum of sodium monofluoroacetate
在ESI-模式下,优化检测氟乙酸钠(M)的质谱条件,Q1扫描时出现[M-Na]-峰,以[M-Na]-为母离子进行碰撞解离,通过子离子扫描,得到碎片离子m/z57.0[M-Na-HF]-和m/z33.0[M-Na-COO]-,示于图1。然后,优化去簇电压、碰撞能量等参数,使子离子的信号达到最强,优化后的结果显示:m/z33.0碎片离子响应值较低,约为m/z57.0的10%,且基线较高,检测实际样品时干扰峰较多,因此,后续实验仅选择m/z77.0>57.0作为定量离子对。同时设定合适的峰驻留时间以确保色谱峰的采样点数在15~20之间,以得到较好的定量重复性。优化后的质谱条件见1.3.3节。
2.2 离子色谱条件优化
氟乙酸钠为弱酸盐,lgKow为-3.89,水溶性强,使用常规反相色谱柱不能保留,文献中有采用反相机理的Waters Aquity CSH Fluoro-Phenyl色谱柱进行分离[1],也有采用亲水相互作用色谱(Hilic)机理的Waters Atlantis Hilic色谱柱进行分离[7],但氟乙酸钠的保留均不理想,且易受样品基质影响,保留时间不稳定[9]。离子色谱适用于氟乙酸钠的分离[10-11],采用高容量AS19阴离子交换色谱柱,先用5 mmol/L KOH对样品中氟乙酸钠进行分离,然后用50 mmol/L KOH对色谱柱进行淋洗以去除强保留成分,色谱柱流出液经阴离子抑制器去除K+,流动相中KOH转化成水,直接进入质谱系统进行检测。采用0.5 mL带滤头的自动进样瓶,进样前先用1 mL水清洗进样管路,进样1 300 μg/L氟乙酸钠标准溶液后,再进一针空白,结果表明,无氟乙酸钠残留。优化后的色谱条件见1.3.2节。
2.3 样品前处理方法优化
2.3.1提取剂的选择 氟乙酸为弱酸性水溶化合物,pKa 2.73[8],在pH<2的酸性条件下可被乙酸乙酯萃取[12-13]。奶粉样品富含蛋白、乳糖、脂肪和矿物质等,选择3%高氯酸作为提取剂对奶粉进行超声提取,经低温高速离心后取中间层提取液,可去除大部分蛋白和脂肪等杂质,此时提取液的pH值为0.5~1.0;此条件下氟乙酸呈分子状态,易被有机溶剂萃取,在萃取液中加入100 μL 1%氨水丙酮溶液,使氟乙酸生成氟乙酸铵盐,避免其在氮气吹干过程中损失,再用0.1%氨水溶解残渣,经0.2 μm滤膜滤除脂溶性杂质。称取0.50 g奶粉样品,加标10 ng氟乙酸钠,测定氟乙酸钠的响应值,再与0.50 g奶粉样品处理液加标10 ng氟乙酸钠的响应值进行比较,计算出高氯酸作为提取剂的提取率约为86%。
2.3.2萃取剂的选择 称取0.50 g奶粉样品,加标10 ng氟乙酸钠,分别用5.0 mL叔丁基甲醚和乙酸乙酯萃取。结果表明,叔丁基甲醚作为萃取剂的氟乙酸钠响应值比乙酸乙酯作为萃取剂的响应值高20%,故选择叔丁基甲醚作为萃取剂。
2.3.3提取液pH值的优化 取7份奶粉的高氯酸提取液,用高氯酸或氨水调pH值分别为0.5、1.0、1.5、2.0、3.0、4.0和5.0,再加入20 ng氟乙酸钠标准溶液,用5.0 mL叔丁基甲醚萃取2次后测定,绘制pH值-氟乙酸钠响应曲线,示于图2。结果表明,在pH 0.5~1.0范围内,氟乙酸钠的响应值最高,故选择提取液pH值范围为0.5~1.0。
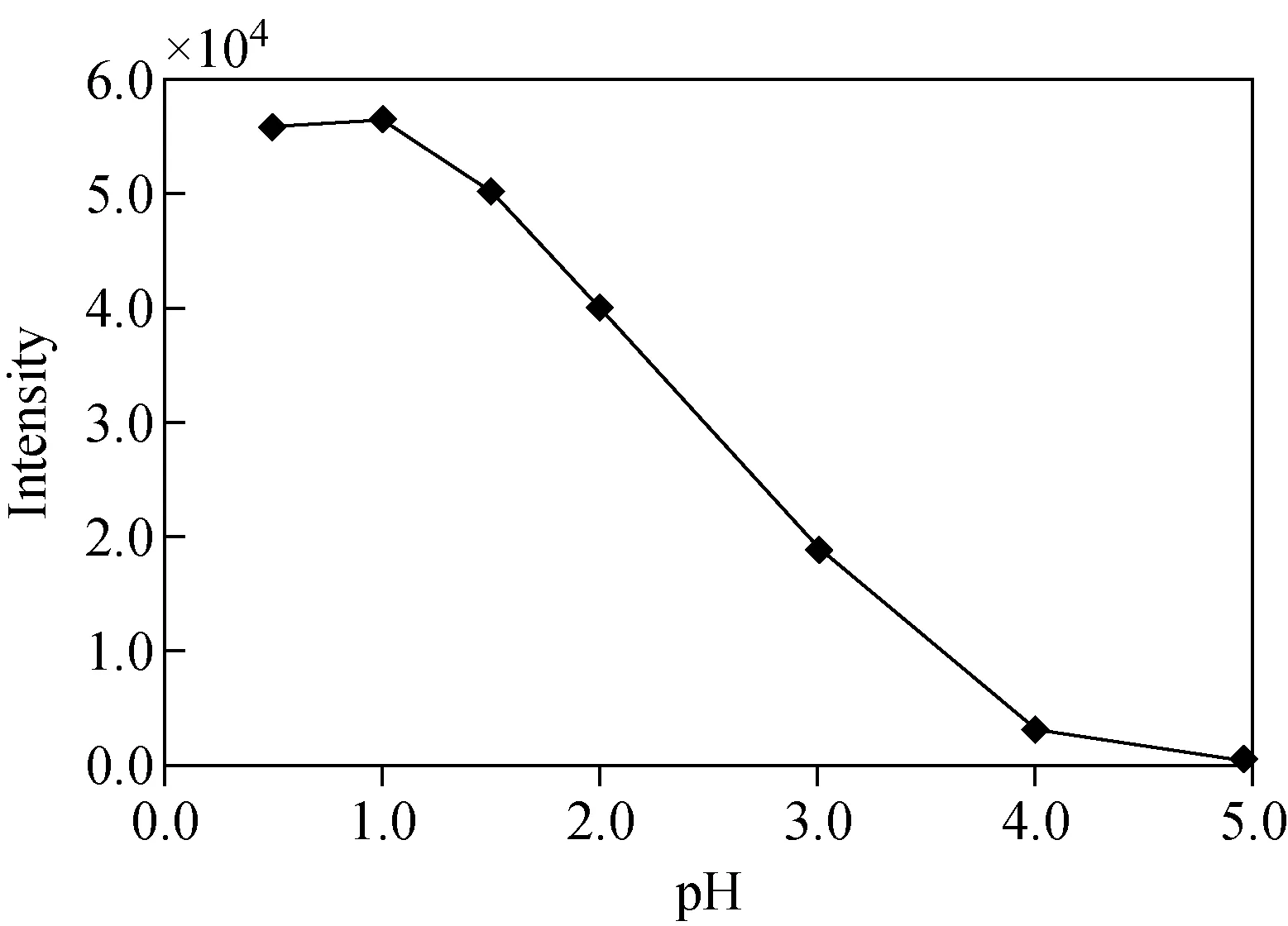
图2 pH值对叔丁基甲醚萃取氟乙酸钠的影响Fig.2 Effect of pH on sodium monofluoroacetate extracted by methyl tert-butyl ether
2.3.4萃取次数的选择 将处于pH 0.5~1.0的高氯酸提取液加标10 ng氟乙酸钠标准溶液,用5.0 mL叔丁基甲醚萃取3次,测定每次氟乙酸钠的萃取量,通过除以3次萃取总量计算每次的萃取率。第1次叔丁基甲醚的萃取率约为60%,第2次约为30%,两次的总萃取率约为90%,最终选择采用5.0 mL叔丁基甲醚萃取2次。
2.3.5盐析效应 本实验考察了盐析效应对氟乙酸钠萃取率的影响,在高氯酸提取液中加标10 ng氟乙酸钠标准溶液,再加入2.0 g氯化钠后测定,并与不加氯化钠的结果比较,发现盐析效应对氟乙酸钠的萃取率无明显影响,故实际样品萃取时无需加入氯化钠进行盐析。
2.3.6基质效应 本实验采用稳定同位素内标法进行定量分析,可有效校正样品中的基质效应。取空白婴幼儿配方奶粉得到空白处理液,加入氟乙酸钠标准溶液制成基质标准溶液(10 μg/L),与溶剂标准溶液(10 μg/L)相比评估基质效应[14],婴幼儿配方奶粉中氟乙酸钠的基质抑制效应约为33%。
2.4 方法的线性范围、检出限和定量限
将氟乙酸钠标准溶液稀释成浓度分别为0.3、1.0、5.0、50.0、100、600、1 300 μg/L的系列标准溶液(含130 μg/L13C2-氟乙酸钠同位素标准溶液),采用MultiQuant定量软件进行数据处理,以定量离子对与内标物的峰面积比值(y)对标准系列浓度(x,μg/L)进行线性回归(权重取1/x),回归方程为y=0.016 7x+0.002 55,相关系数为0.999 8,线性关系良好、线性范围较宽。
向空白奶粉中加入低浓度氟乙酸钠溶液,以分子离子对信噪比S/N≥3的样品浓度作为检出限(LOD),以S/N≥10的样品浓度作为定量限(LOQ),测得方法的检出限和定量限分别为0.2、0.6 μg/kg,测定上限为2.6 mg/kg。空白和加标氟乙酸钠婴幼儿配方奶粉的IC-MS/MS色谱图示于图3。
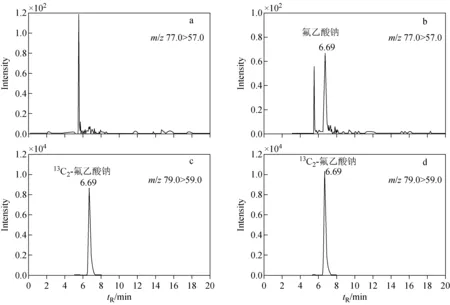
图3 空白婴幼儿配方奶粉(a,c)和0.6 μg/kg加标水平婴幼儿配方奶粉加标样品(b,d)的IC-MS/MS色谱图Fig.3 IC-MS/MS chromatograms of blank infant formula (a,c) and infant formula added with sodium monofluoroacetate at 0.6 μg/kg (b,d)
2.5 加标回收率和精密度
向空白婴儿配方奶粉和全脂奶粉样品中添加不同浓度的氟乙酸钠标准溶液,混匀,放置1 h,使待测成分与样品基体成分相互作用达到平衡,再按1.3.1节方法处理样品,其回收率和精密度结果列于表1。结果表明:氟乙酸钠的加标回收率在89.7%~104%之间,相对标准偏差在0.50%~11%范围内,符合痕量分析的要求。
2.6 实际样品的测定
采用该方法检测了5种进口婴幼儿配方奶粉和3种全脂奶粉,均未检出氟乙酸钠。
3 结论
本研究采用离子色谱-三重四极杆质谱法测定奶粉中氟乙酸钠。通过优化样品的前处理过程,达到了较好的样品净化效果,降低了基质效应;通过优化离子色谱和质谱条件,得到了较好的分离效果和检测灵敏度;采用稳定同位素稀释内标法定量分析,结果准确、重现性好。本方法操作简单、灵敏度高、线性范围宽,可用于奶粉中氟乙酸钠的日常检测,也可应用于相似基质食品中氟乙酸钠的测定。
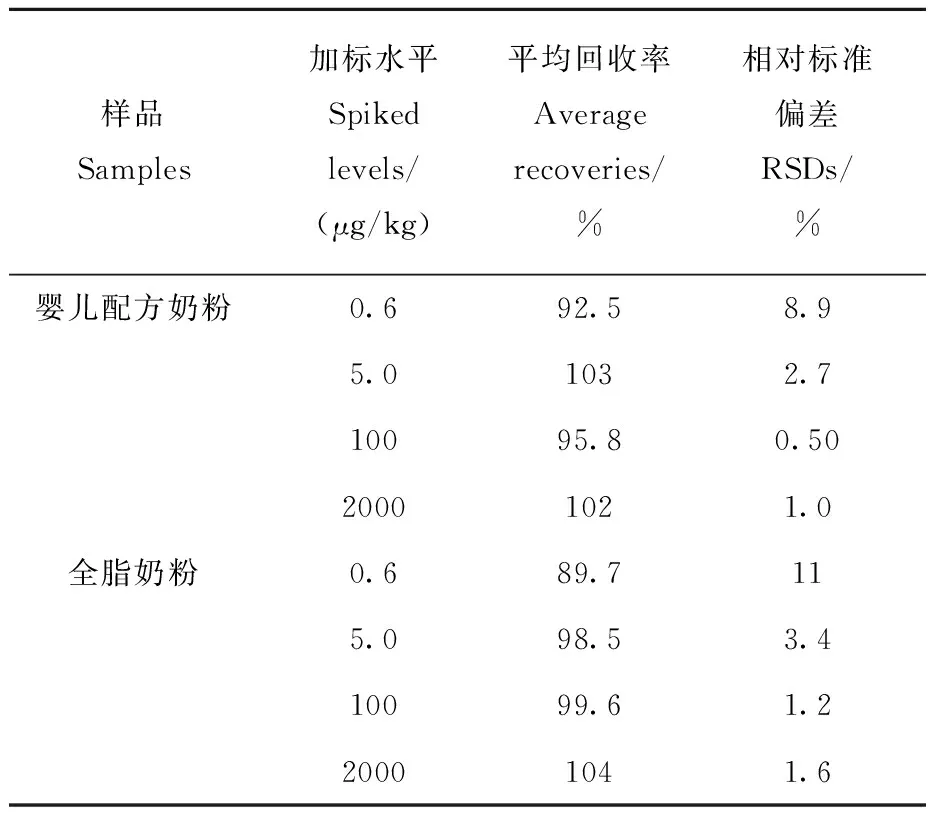
表1 在不同添加水平下,奶粉中氟乙酸钠的回收率和精密度(n=6)Table 1 Recoveries and RSDs of sodium monofluoroacetate at different spiked levels in dairy powders samples (n=6)

