基于超分子溶剂分散液液微萃取技术测定食品接触材料中8种邻苯二甲酸酯的迁移量
王 春,翟俊峰,黄雪梅,,连显会,4,王长海,雷海民,白 桦,马 强
(1.中国检验检疫科学研究院,北京 100176;2.南京农业大学资源与环境科学学院,江苏 南京 210095;3.北京中医药大学中药学院,北京 102488;4.大连理工大学生命与医药学院,辽宁 盘锦 124221)
食品安全不仅限于食材本身的安全,食品接触材料的安全性也是食品安全的重要组成部分。为了追求更好的包装性能,食品接触材料中会加入种类繁多、功能各异的添加剂、加工助剂等化学成分,这些化学物质在一定的介质环境和温度条件下会溶出和释放,并通过或透过食品接触材料迁移到食品中而被人体摄入,从而对消费者的身体健康造成危害。邻苯二甲酸酯(phthalic acid esters, PAEs)是工程塑料行业中普遍使用的增塑剂,已被广泛应用于食品接触材料、玩具、化妆品、涂料、医疗器械等产品中[1]。有研究表明,邻苯二甲酸酯属于环境雌激素类物质,具有生殖毒性及致癌作用,会造成人体内分泌失调、生殖系统病变和致畸致癌等不良后果[2-4]。世界各国都强化了对于邻苯二甲酸酯的安全使用与管理,并颁布了一系列有关限制增塑剂使用的政策和法规。
研究和控制食品接触材料中所含化学危害物质的迁移行为,对于保护消费者的健康安全具有重要意义。为了测试和评估食品接触材料的安全性,通常采用迁移实验,即通过食品模拟物在一定的实验条件下与材料接触,模拟实际使用时材料与食品接触的过程,然后对食品模拟物进行分析以确定其中化学迁移物的含量水平是否符合安全限量的要求。目前,关于食品接触材料中邻苯二甲酸酯类增塑剂迁移量的测定方法主要有气相色谱(GC)法[5]、气相色谱-质谱(GC-MS)法[6-11]、高效液相色谱(HPLC)法[12-14]和高效液相色谱-串联质谱(HPLC-MS/MS)法[15]等。
在食品接触材料迁移实验中,往往会涉及到大体积食品模拟物试液,特别是水性模拟物试液。由于微量目标组分在迁移溶液中的含量较低,需要采用前处理技术对样品溶液进行浓缩富集,以提高检测灵敏度。目前常用的前处理方法有液-液萃取法[16-18]、固相萃取法[19-22]等。液-液萃取法操作繁琐,耗时,需要使用大量挥发性有机溶剂;而固相萃取法成本较高,且在目标化合物的回收率和精密度方面存在不足。
超分子溶剂(supramolecular solvents, SUPRASs)是指由两亲性化合物通过两相或分子间有序自组装过程形成的一种具有纳米结构的胶束聚集体[23]。超分子溶剂萃取是一种以超分子溶剂作为萃取剂的新型萃取技术,多用烷基醇或酸与四氢呋喃和水混合,形成不溶于水的反相胶束,适用于天然水、地下水、废水、红酒、啤酒、牛奶、尿液等液体样品中多环芳烃、农药、内分泌干扰物、酚类化合物等不同极性范围分析物的萃取,具有成本低廉、操作简单、绿色环保等优势,可替代传统萃取过程中使用的挥发性强、毒性较大的有机溶剂[24-26]。
本研究拟采用超分子溶剂分散液液微萃取技术,对食品接触材料迁移溶液中的8种邻苯二甲酸酯类增塑剂进行富集,并对烷基醇的种类与用量、四氢呋喃用量、涡旋时间等条件进行优化。采用超高效液相色谱-串联质谱结合同位素稀释技术,测定食品接触材料中邻苯二甲酸酯类增塑剂的迁移量。
1 实验部分
1.1 仪器与试剂
Acquity超高效液相色谱仪、XEVO TQ三重四极杆质谱仪:美国Waters公司产品,配有MassLynx数据处理系统;MS-H-Pro数显型磁力搅拌器:北京大龙兴创实验仪器有限公司产品;Milli-Q 超纯水器:美国Millipore公司产品;AB204-S型电子天平:瑞士Mettler Toledo公司产品;CR 21N型高速冷冻离心机:日本Hitachi公司产品;MS3型涡旋振荡器:德国IKA公司产品。
甲醇、乙腈、四氢呋喃:均为色谱纯,美国Fisher公司产品;正己醇、正辛醇、正癸醇、正十一醇和正十二醇:百灵威科技有限公司产品;正庚醇和正壬醇:日本TCI 公司产品;邻苯二甲酸二甲酯(dimethyl phthalate, DMP)、邻苯二甲酸二乙酯(diethyl phthalate, DEP)、邻苯二甲酸二戊酯(dipentyl phthalate, DPP)、邻苯二甲酸丁苄酯(benzyl butyl phthalate, BBP)、邻苯二甲酸二环己酯(dicyclohexyl phthalate, DCHP)、邻苯二甲酸二己酯(dihexyl phthalate, DHP)、邻苯二甲酸二(2-乙基)己酯(bis(2-ethylhexyl) phthalate, DEHP)、邻苯二甲酸二壬酯(dinonyl phthalate, DNP)及其对应的氘代同位素内标等标准品:均为德国Dr. Ehrenstorfer公司产品。8种邻苯二甲酸酯及其同位素内标的基本信息列于表1。
1.2 标准储备溶液及标准工作溶液的配制
分别准确称取10 mg(精确至0.1 mg)8种邻苯二甲酸酯及其对应的内标标准品至10 mL容量瓶,用甲醇溶解并定容至10 mL,配制成1 000 mg/L标准储备溶液,于4 ℃保存。使用时,用甲醇逐级稀释成系列质量浓度的标准工作溶液,现用现配。

表1 8种邻苯二甲酸酯及其同位素内标的基本信息Table 1 Basic information of the eight PAEs and their isotopic internal standards
1.3 超分子溶剂的制备
准确量取1.5 mL正辛醇和4 mL四氢呋喃,迅速注入50 mL玻璃离心管中,加入34.5 mL超纯水,磁力搅拌5 min后,以3 000 r/min离心10 min。用玻璃注射器移取上层有机相于玻璃瓶中,于4 ℃下密封保存。
1.4 迁移实验
将食品接触材料试样剪碎至5 mm×5 mm以下,按照食品安全国家标准GB 5009.156—2016和GB 31604.1—2015的要求进行迁移实验。向水、10%乙醇溶液(体积百分含量,下同)、20%乙醇溶液和4%乙酸溶液4种水性食品模拟物试液中分别加入0.5 g食品接触材料试样。于70 ℃恒温水浴中浸泡12 h后,移取5 mL迁移液至15 mL具塞玻璃离心管中,向离心管中加入400 μL超分子溶剂,涡旋振荡提取3 min后,以3 000 r/min离心10 min,移取150 μL上层液体,用甲醇稀释至0.5 mL,供超高效液相色谱-串联质谱测定。
1.5 分析条件
1.5.1色谱条件 色谱柱:Acquity UPLC BEH C18柱(2.1 mm×50 mm×1.7 μm);流速:0.3 mL/min;流动相:A为水, B为甲醇;梯度洗脱程序:0~1.0 min(35%B),1.0~2.0 min(35%~95%B),2.0~4.0 min(95%B);4.0~4.5 min(95%~35%B),4.5~6.0 min(35%B);柱温:30 ℃;进样量:2 μL。
1.5.2质谱条件 电喷雾离子源,正离子扫描模式;毛细管电压:4.0 kV;射频透镜电压:0.5 V;离子源温度:120 ℃;脱溶剂气温度:350 ℃;脱溶剂气流量:800 L/h;锥孔气流量:50 L/h;碰撞气:氩气;碰撞压强:0.32 Pa;数据采集模式:多反应监测(multiple reaction monitoring, MRM)。8种邻苯二甲酸酯及其对应内标的质谱分析参数列于表2,多反应监测色谱图示于图1。

表2 8种邻苯二甲酸酯及其同位素内标的质谱分析参数Table 2 Mass spectrometric parameters of the eight PAEs and their isotopic internal standards

图1 8种邻苯二甲酸酯标准溶液的多反应监测色谱图Fig.1 MRM chromatograms of the eight PAE standard solutions
2 结果与讨论
2.1 烷基醇种类的选择
选择具有两亲性质的四氢呋喃,分别与一系列不同碳原子数的烷基醇(正己醇、正庚醇、正辛醇、正壬醇、正癸醇、正十一醇和正十二醇)组合形成超分子溶剂,对邻苯二甲酸酯进行萃取,结果示于图2a。超分子溶剂的萃取作用力主要体现在烷基链提供的疏水相互作用和亲水基提供的氢键作用。正辛醇-四氢呋喃-水超分子溶剂体系对8种邻苯二甲酸酯的萃取回收率为96.5%~116.4%,且回收稳定;其他烷基醇,如庚醇等,虽然对邻苯二甲酸酯的萃取效果较好,但萃取回收率波动较大。因此,本实验选择正辛醇-四氢呋喃-水体系作为超分子溶剂。
2.2 烷基醇用量的优化
烷基醇与四氢呋喃组合形成的超分子溶剂属于反相胶束类型超分子溶剂。实验考察了正辛醇用量分别为0.5、1、1.5、2、2.5和3 mL(保持超分子溶剂总体积为40 mL)时样品的回收率,结果示于图2b。随着正辛醇用量的增加,回收率呈先上升后下降的趋势,当正辛醇用量大于或等于1.5 mL时,样品回收率较高且稳定。因此,选择正辛醇的用量为1.5 mL。

图2 萃取溶剂(a)、烷基醇用量(b)、四氢呋喃用量(c)和涡旋时间(d)对萃取效率的影响(n=3)Fig.2 Effect of extraction solvents (a), amounts of alkyl alcohol (b), amounts of tetrahydrofuran (c) and vortex time (d) on the extraction efficiencies (n=3)
2.3 四氢呋喃用量的优化
作为超分子溶剂的重要成分,四氢呋喃是该体系中影响萃取效率的重要因素。实验考察了四氢呋喃用量分别为2、4、6、8、10和12 mL(保持超分子溶剂总体积为40 mL)时样品的回收率,结果示于图2c。当四氢呋喃用量为4 mL时,各样品回收率均接近100%,且回收率稳定;当四氢呋喃用量小于4 mL时,样品的回收率偏低且波动较大;而当四氢呋喃用量大于4 mL时,虽然样品的回收率有所提高,但呈现出偏高的趋势。与此同时,随着四氢呋喃用量的增加,会出现超分子溶剂与样品互溶的现象,使上清液体积变少,甚至达不到检测所需的体积。因此,本实验选择四氢呋喃的用量为4 mL。
2.4 涡旋时间的优化
在超分子溶剂分散液液微萃取中,分析物通过萃取剂和样品溶液之间的充分接触可迅速达到分配平衡,引入涡旋振荡可以促进超分子溶剂与食品模拟物中目标物的充分混合,以形成良好的乳浊液状态,促进传质过程。实验考察了涡旋时间分别为1、3、5、7、9、11 min时样品的回收率,结果示于图2d。随着涡旋时间的增加,回收率呈先上升后稳定的趋势,当涡旋时间大于或等于3 min时,样品的回收率较高且趋于平稳。因此,选择涡旋时间为3 min。
2.5 方法学考察
2.5.1线性范围、检出限及定量限 在优化的实验条件下,测定一系列不同加标水平的样品,以logy(目标物峰面积/对应同位素内标峰面积)对x(目标物质量浓度)进行线性回归,绘制8种邻苯二甲酸酯的标准工作曲线。结果表明,8种邻苯二甲酸酯在各自的浓度范围内线性关系良好,线性相关系数r2>0.99。分别以3倍和10倍信噪比计算方法的检出限和定量限,结果列于表3。
2.5.2回收率与精密度 以经测定不含待测物的饮料瓶样品为空白基质,分别在2~200 μg/L 范围内添加低、中、高三个水平的混合标准溶液,按照上述优化的方法进行分析测定,每个添加水平平行操作6次,计算加标回收率。结果表明,8种邻苯二甲酸酯的平均回收率为84.8%~117.5%,相对标准偏差为2.1%~18.7%,详细结果列于表4。
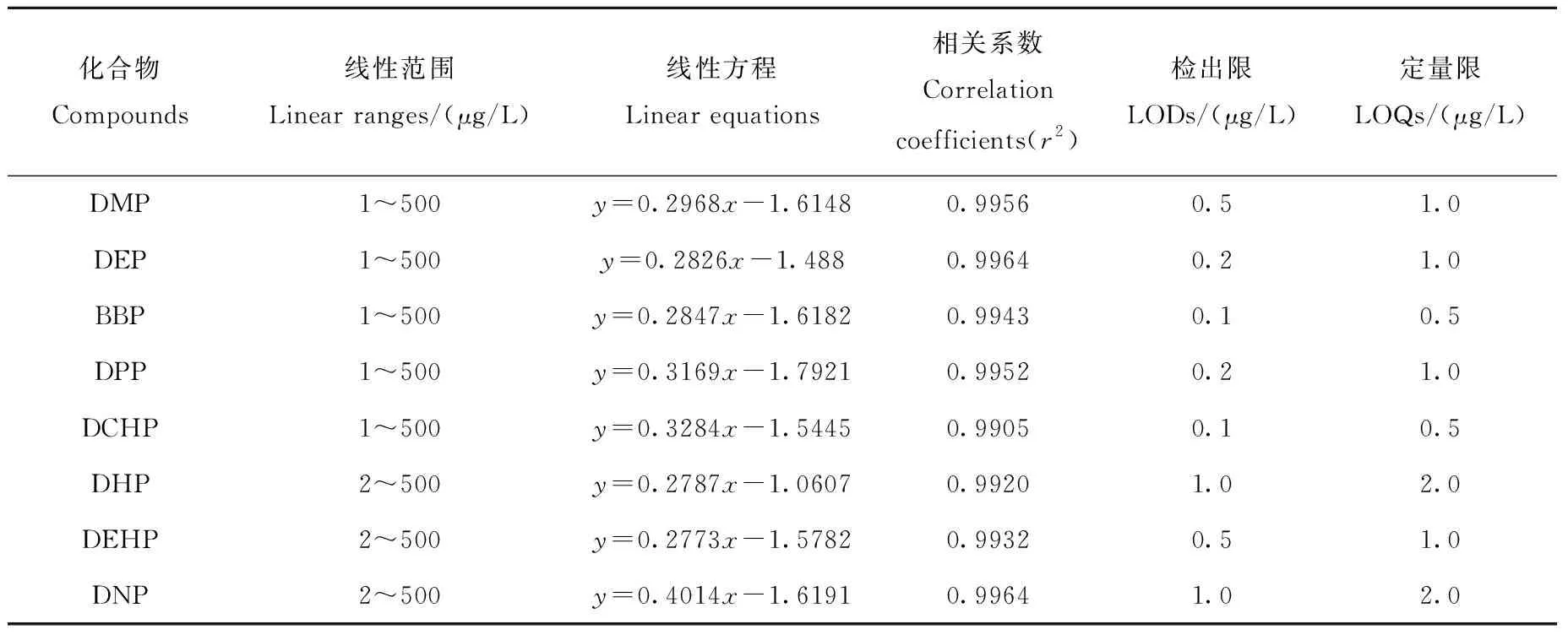
表3 8种邻苯二甲酸酯的线性范围、线性方程、检出限及定量限Table 3 Linear ranges, linear equations, limits of detection (LODs) and limits of quantitation (LOQs) of the eight PAEs

表4 8种邻苯二甲酸酯的加标回收率和相对标准偏差(n=6)Table 4 Recoveries and relative standard deviations (RSDs) of the eight PAEs (n=6)

续表4
2.6 实际样品分析
选取市场销售的一次性纸杯、饮料瓶、酸奶瓶等3类共10件食品接触材料样品进行测定。结果发现,1件食品接触材料样品在水、10%乙醇水溶液和20%乙醇水溶液模拟物中检测出邻苯二甲酸二环己酯,其迁移量分别为76.63、89.91、108.03 μg/L;1件食品接触材料在20%乙醇水溶液模拟物中检测出邻苯二甲酸二(2-乙基)己酯,其迁移量为191.67 μg/L;2件食品接触材料在水模拟物中检测出邻苯二甲酸二戊酯,其迁移量分别为17.23、11.95 μg/L。其余食品接触材料的迁移液中均未检出邻苯二甲酸酯类增塑剂。
3 结论
本研究建立了超分子溶剂分散液液微萃取,结合同位素稀释-超高效液相色谱-串联质谱测定食品接触材料中邻苯二甲酸酯迁移量的分析方法。实验分别对烷基醇的种类与用量、四氢呋喃用量、涡旋时间等因素进行了优化考察。在优化的实验条件下,8种邻苯二甲酸酯在各自的浓度范围内线性关系良好,线性相关系数r2>0.99,检出限为 0.1~1.0 μg/L,定量限为0.5~2.0 μg/L。在低、中、高3个添加水平下,8种邻苯二甲酸酯类增塑剂的平均回收率为84.8%~117.5%,相对标准偏差为2.1%~18.7%(n=6)。通过检测市场销售的实际样品,证明该方法准确可靠、操作简便、有机溶剂消耗量少,适用于测定食品接触材料中邻苯二甲酸酯类增塑剂的迁移量。

