颈外侧区良恶性病变MSCT诊断、鉴别诊断及病理分析
广西壮族自治区北海市人民医院放射科 (广西 北海 536000)
陈更瑞
颈外侧区是由颈动脉鞘及外围的脂肪组织组成,又称为颈动脉间隙,位于颈部脏器区和后区之间,内主要有颈动脉、颈内静脉、第IX~XII对脑神经、交感神经链及颈内静脉链淋巴结[1-2]。发生于该区域病变种类较多,极容易误诊。多层螺旋CT(MSCT)作为影像学最常用的检查手段之一,可以清楚地显示颈部病灶数目、边界、多发病灶是否融合、强化方式及血供情况,作者收集了经病理证实69例颈外侧区病变的MSCT影像学资料,进行回顾性分析,旨在提高对良、恶性病变的诊断及鉴别诊断。
1 资料与方法
1.1 一般资料搜集2014年3月~2017年8月69例患者临床及影像资料,男42例,女27例,最小年龄3岁,最大年龄75岁,平均年龄55岁。临床症状主要为颈部肿物。全部患者均经手术切除或穿刺活检,得出病理结果。
1.2 检查方法采用Philips Brilliance64多排螺旋CT扫描仪,扫描范围从主动脉弓水平至颅底,主要参数:管电压120KV,管电流100mA/s,扫描层厚0.9mm,重建间隔0.9mm,用高压注射器经肘静脉注入50ml非离子型对比剂,注射速率为5.0ml/s,先平扫后增强扫描,动脉期选取主动脉弓层面为监测平面,自动触发启动扫描,完成后再进行静脉期扫描,将原始图像传输至后处理工作站,重建方法包括最大密度投影、多平面重建、容积再现和曲面重建。
1.3 图像分析根据病灶数目、边界、多发病灶是否融合、是否有环状强化及血供情况等方面,进行影像图像分析。病灶强化分级:强化程度以增加扫描后CT值的增加值评估,轻度强化:增加值<20HU;中等强化:增加值20~40HU;明显强化:增加值≥40HU[3]。以中等强化及明显强化提示为血供丰富。
1.4 统计学方法采用SPSSl9.0统计软件对数据进行分析,采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 病理结果69例,恶性44例:淋巴结转移性癌32例(9例来源于鼻咽癌,9例来源于下咽癌及喉癌,3例来源于肺癌,3例分别来源于食道癌、鼻腔神经内分泌癌及小圆细胞恶性肿瘤,8例找不到原发病灶)(图1),淋巴瘤10例(非霍奇金淋巴瘤3例,间变性大细胞淋巴瘤及弥漫大B细胞淋巴瘤各1例,5例无分类)(图2),恶性孤立性纤维性肿瘤1例(图3),颌下腺多形性腺瘤恶变1例;良性25例:炎性病变16例(颈部脓肿2例,化脓性炎症3例,炎性肉芽肿2例,淋巴结反应性增生4例,慢性淋巴结炎3例,结核病2例)(图4-6),良性肿瘤5例(神经鞘瘤2例,神经纤维瘤、淋巴管瘤、海绵状血管瘤各1例)(图7-8),囊肿3例(腮裂囊肿2例,表皮囊肿1例),脂膜炎1例(图9)。恶性病变占63.7%(44/69),恶性病变中淋巴结转移性癌占72.7%(32/44),病灶多发52例(恶性39例,良性13例),单发17例(恶性5,良性12例)。
2.2 颈部良恶性病变影像征象见表1。其中恶性病变表现为边界不清所占比例最高,90.9%,病灶融合占81.8%,与良性病变所占比例差异显著(P<0.005)。
3 讨 论
3.1 颈外侧区良恶性病变的CT表现淋巴结转移性癌是颈部最常见恶性肿瘤,其原发病灶85%来源于头颈部,15%来自于躯干和四肢体[1],本组病例占72.7%(32/44),原发病灶主要来源于鼻咽癌、下咽癌及喉癌,占56.2%(18/32),结果一致,CT表现:平扫呈单发或多发肿大淋巴结,小病灶为结节状,边缘可以清晰,明显肿大病灶多融合成团块,边界不清,形态不规则或呈分叶状,增强扫描呈轻中度不均匀强化,部分为边缘环状强化,中心呈低密度坏死。文献[2]提出,边缘不规则强化伴中央坏死为鳞癌转移淋巴结的特征性影像表现,尤其以喉癌及下咽癌多见。本组病例,9例喉癌及下咽癌均为鳞癌,6例转移癌表现为边缘不规则强化伴中央坏死,3例表现为多发结节状强化,有2例鼻咽鳞癌及1例鼻腔神经内分泌癌淋巴结转移癌亦表现为边缘不规则强化伴中央坏死,1例食道鳞癌及2例未发现原发病灶的颈部淋巴结转移性鳞癌CT表现为多发结节状强化;7例鼻咽非角化性癌,其中3例具有边缘不规则强化伴中央坏死表现,4例为多发结节状强化。所以颈部淋巴结转移性鳞癌主要表现为边缘不规则强化伴中央坏死,但并非特征性表现。颈部淋巴瘤CT表现:多发大小不等结节,部分边缘可清晰,部分融合呈肿块,边缘不清,增强呈轻度不均匀强化,部分呈环状强化(分为边缘薄环状及不规则环状),中央可见囊变。而郭媛[4]等研究一组病例,以单侧颈部结节为主的淋巴瘤,容易误诊,本组病例均为双侧颈部多发病变。
良性病变主要有炎性病变,良性肿瘤及囊肿,在单发病灶中,良性病变占70.6%(12/17),其中良性肿瘤及囊肿单发常见,而良性病变中,炎性病变占60.0%(15/25)。颈部淋巴结炎症有多种多样,大多数无特征性影像学表现,典型化脓性淋巴结炎可表现为边缘不规则环状强化,内部坏死,多发病灶可融合呈团,边缘模糊,而陈荣华等[5]认为:淋巴结炎表现为淋巴结直径常小于1.0cm,呈卵圆形,界限清、无融合是其特点。颈部淋巴结结核,CT表现为多发结节,部分融合呈团块,边界不清,呈结节状或环状强化,团块病灶内见分隔及多发低密度区,形成“花环状”改变,具有特征性,本组1例具有分隔状强化,1例表现为多发结节,边缘尚清晰,呈轻度强化,部分有融合趋势,另见1例淋巴组织化脓性炎症,则表现为花环状强化。反应性淋巴结增生,CT表现:多发结节,大小多小于3.0cm,边界清晰,无融合趋势,部分可呈“串珠样”分布,轻度强化,很少见病灶内坏死,与文献[6]报道相吻合。神经源性肿瘤,在颈部病变中也较常见,具有特定解剖位置,大多位于颈动脉间隙的后、内侧,将颈动脉向前或外侧方推移,而迷走神经肿瘤则可以使颈动、静脉分离。神经鞘瘤多为单发,有包膜,边缘清晰,神经纤维瘤边界清晰,但缺乏包膜,两者主要鉴别:有低密度区环绕岛状或云雾状高密度区者,神经鞘瘤可能性大;而表现为实性或有大的囊变者,则以神经纤维瘤可能性大[2]。本组1例神经纤维瘤,病灶多发,以囊性为主,强化不明显,其内为片状稍高密度,边缘清晰,表现较为典型,与文献[7]报道:神经纤维瘤多呈均匀软组织密度,也可见出血和囊变,不相符合。
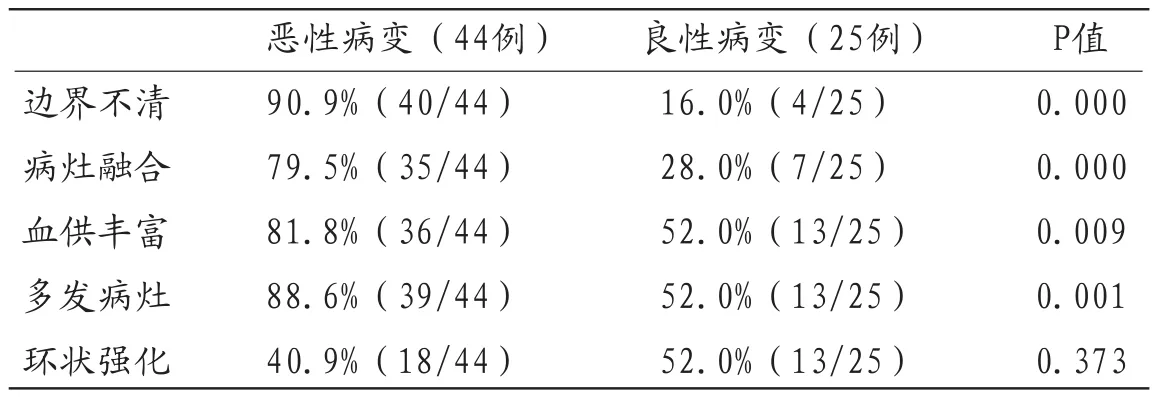
表1 颈部良恶性病变影像征象

图1 淋巴结转移性癌。图2 弥漫大B细胞淋巴瘤。图3 恶性孤立性纤维性肿瘤。图4 淋巴结化脓性炎症。图5 淋巴结反应性增生。图6淋巴结结核。图7 神经鞘瘤。图8 淋巴管瘤。图9 脂膜炎。
淋巴管瘤:为淋巴系统的先天畸形,最常见病理类型为囊性水瘤,CT表现为单房或多房囊性肿物,壁薄均匀,边界清晰,水样密度,无强化或轻度强化,合并感染时,壁可强化,边缘模糊;本组病例,诊断医师提出与神经源性肿瘤相鉴别,分析原因:可能是由于病变位于右侧颈动脉间隙后外侧方,颈动脉受压向前内侧推移缘故,却忽略神经性肿瘤内部往往可见稍高密度影,而淋巴管瘤内部呈均匀水样密度,文献[8]提出颈部囊性淋巴管瘤需与神经鞘瘤囊变区别,淋巴管瘤为囊性,囊内无强化,而神经鞘瘤常位于血管鞘内,实质部分可强化。刘勃等[9]认为:淋巴管瘤主要发生于儿童,80%~90%在2岁前被发现,以颈部最为常见,而本病例为成年男性。海绵状血管瘤,是血管瘤中一种病理亚型,CT最具有特征性表现:增强扫描呈“渐进性强化”,亦可呈迂曲血管状或多灶结节状明显强化。本例CT表现为椭圆形稍低密度影,密度均匀,边缘清晰,增强扫描呈中心部斑片状明显强化,误诊为神经纤维瘤,分析原因:首先是影像表现认识不足,神经纤维瘤强化程度不如海绵状血管瘤明显,其次没有行增强延时扫描,未能显示海绵状血管瘤特征性强化。文献[5]报道:海绵状血管瘤为血供丰富的肿瘤,呈团簇状、分叶状不均匀密度影,位置多表浅或靠颈动脉鞘后方,范围广,界限不清。本例位于颈后棘突左旁,位置较表浅,但与周围分界清晰。
腮裂囊肿:是由未完全退化的腮裂组织发育而形成的先天性囊肿,主要病变部位为腮腺区,CT表现为圆形或类圆形囊性病变,边界清晰,密度均匀,病灶内部无强化,边缘可轻度强化,合并感染时内部密度可不均匀,边缘模糊。本组1例位于颈动脉间隙,壁菲薄,无强化,边界清晰,需与位于颈动脉间隙淋巴管瘤鉴别,文献[10-11]提出:淋巴管瘤常具有浸润性,与邻近筋膜边界不清,可作为淋巴管瘤与其他囊肿相鉴别。表皮样囊肿:是胚胎性残余上皮发生而形成的囊肿,其CT表现与囊内成分有关:可表现为水样密度,若囊内含角蛋白和胆固醇,则呈稍高密度或混合密度,边缘清晰,很少见钙化,增强扫描无强化,本组1例密度呈均匀稍高,无强化,边缘光整,无钙化,考虑囊内主要成分为角蛋白,呈典型表现。
恶性孤立性纤维性肿瘤:丁汉军[12]研究所见:孤立性纤维性肿瘤较大时呈不均匀强化,出现“地图样”改变或坏死区,肿瘤内部周围可见紊乱迂曲血管影;考虑影像表现与组织病理学特点有关:由于肿瘤细胞及间质排列方式致密,又具有丰富的间质血管,有关细胞密集区和稀疏区强化程度不等,多种区域混杂则形成“地图样”强化,而肿瘤较大时中心供血不足形成坏死区。本例为恶性,位于左侧咽旁间隙,类圆形较大孤立肿块,边缘不清,呈边缘不规则环状强化,中心部密度较低,内可见较多紊乱迂曲血管显示,相邻上颌骨骨质破坏。与报道相符。另有文献[13]提出:孤立性纤维性肿瘤是一种少见的梭形细胞软组织肿瘤,其影像学表现具有一定特征性:CT增强扫描呈较明显强化,内可见多发迂曲肿瘤血管;MRI的T2WI呈低信号及增强后明显强化,但最终诊断有赖于组织病理学检查。
脂膜炎1例,男,29岁,CT表现:两侧颈部、胸部锁骨上及纵隔、肺门多发淋巴结肿大,其中右上纵隔病灶较大,融合成肿块,增强扫描呈轻度不均匀强化,内部见偏心性低密度无强化坏死灶,边缘不清晰,包绕头臂静脉及上腔静脉,脾脏亦见多发低密度灶,肝门区见多发肿大淋巴结,影像诊断考虑淋巴瘤。病理结果:颈部小块活检脂肪组织,混合性T、B淋巴细胞及组织细胞浸润,符合脂膜炎。IHC:CD43/CD3/CD20/PAX-5显示T细胞优势,CD68见较多组织细胞,KI-67:15-20%,TIA-1部分细胞(+),CD56(-),GB(-),Lyclin-D1(-),S-100,CK(-),结合形态学不支持淋巴瘤。分析误诊原因:主要是本病例为多部位多发淋巴结肿大,多发病变,部分融合呈肿块,边缘不清晰,内见坏死区,边缘不规则环状强化,肿大淋巴结轻度不均匀强化,部分包绕血管,影像上具有淋巴瘤表现,确实难以鉴别;其次是脂膜炎没有影像学特征,只能靠病理组织学诊断。而舒向芳等[14]提出:与皮下脂膜炎样T细胞淋巴瘤(SPTCL)不同的是,良性脂膜炎存在CD20(+)的B细胞聚集,混合有相近比例的 CIM(+)和CD8(+)的T细胞,TIA-1(+)的细胞偶尔可见。亦即从免疫组化鉴别。
3.2 颈外侧区良恶性病变的鉴别诊断及病理分析由表1可以看出,良恶性病变影像上增强扫描均可以表现为环状强化,两者所占比例差异没有统计学意义(P>0.05)。赵燕风等[15]研究结果:边缘环形强化、中心低密度是颈部病变中一类较为特殊的征象,在良、恶性病变中差异无统计学意义,主要是因为淋巴结结核和良性囊肿病变伴感染亦会有此表现。而本组病例,淋巴结转移性癌(13例)、淋巴瘤(5例)、化脓性炎症(7例)及淋巴结结核(2例)CT上表现为环状强化,伴中央坏死,但环壁厚薄、形态及边缘各有不同,考虑由于病理基础不同所决定:淋巴结转移性癌,环壁不规则、厚薄不均匀,部分看见囊壁结节,边缘不清,其病理为淋巴结边缘皮质网状窦首先被肿瘤细胞侵入,随后髓质和漏斗部被侵犯,导致回流障碍、组织坏死。淋巴瘤,呈融合肿块状,环壁较厚,边缘不清;其病理改变为淋巴窦受侵犯导致回流障碍,淋巴门受侵犯与压迫导致双重循环阻断,可出现淋巴结中央坏死。淋巴结结核环壁可厚薄不均匀,部分看见分隔,病理主要为中央发生干酪样坏死及周围结核性肉芽肿形成,当同一个淋巴结内同时出现多发肉芽肿伴中心坏死或多个淋巴结干酪增殖融合时,CT表现为多发坏死低密度区周围环状强化及多个分隔,形成具有特征性“花环状”改变。化脓性炎症,由于组织细胞受破坏,内部发生坏死或脓腔形成,CT则表现为厚薄均匀环壁强化,内壁光滑,边缘模糊。
恶性病变CT表现上在边界不清、病灶融合、血供丰富及多发病灶方面所出现几率均明显高于良性病变,P<0.05,具有统计学差异,可作为良恶性病变鉴别诊断的参考依据,其中边界不清及病灶融合更是具有显著差异(P<0.005)。与韦树华等[16]研究结果:恶性病变边界多不清晰,部分融合状,高度一致。本组恶性病变40例边缘不清晰,病理主要为肿瘤细胞具有侵袭性生长特点,沿各方向生长差异较大,当突破包膜及侵犯相邻组织时,在形态上多呈不规则或分叶状,边界不清。CT上表现为肿块边缘呈分叶状,淋巴结外侵犯则周围脂肪间隙消失;而4例良性病变亦表现为边缘不清晰,其中淋巴结结核1例,病理基础包括渗出、干酪样坏死、淋巴结周围炎、融合破溃等,CT显示为边界模糊;化脓性炎症3例,病理为细胞发生水肿、坏死及渗出,周围看见炎性水肿及粘连,CT表现为片状边缘模糊影。但对于以单发结节病灶或多发结节无融合病灶为主的恶性病变,边缘可表现为清晰,则与未发生干酪坏死的淋巴结结核及淋巴结反应性增生难鉴别,需结合临床其他资料综合考虑。郭媛等[4]研究也发现部分淋巴瘤容易误诊为淋巴结结核。
病灶融合是恶性肿瘤较常见的影像征象,其可能病理基础,是由于正常结构被肿瘤细胞所取代及破坏,而肿瘤细胞侵犯包膜或周围组织时,多发病灶相互相连融合而形成不规则肿块。本组35例恶性肿瘤均见病灶融合,7例良性病变亦见病灶融合,均为炎性病变:颈部脓肿1例,化脓性炎症3例,炎性肉芽肿1例,结核病2例,病理上多发淋巴结病灶发生干酪样坏死或液化坏死,周围肉芽组织结构生成,相互粘连、融合成团片状。良恶性融合病灶强化方式及程度可作为鉴别诊断依据,恶性病灶由肿瘤血管供血,强化明显,而炎性病变大多由纤维结缔组织或肉芽肿组织所形成新生血管供血,以边缘或分隔明显强化为主,若影像上难以鉴别,可结合临床资料,有红肿、发热、白细胞及血沉增高等,首先考虑炎性病变。本研究显示:颈部恶性肿瘤血供丰富为主,只有部分淋巴瘤呈轻度强化,提示为乏血供改变,有研究[15]提出:恶性病变多表现为密度不均明显强化,甚至出现中心坏死;而良性病变相对密度均匀,强化不明显,但良性病变中颈动脉体瘤与巨大淋巴结增生明显强化.故而用明显强化作为良恶性诊断标准不能获得满意的结果。与本组结果有差异,原因是本组病例中没有收集到颈动脉体瘤与巨大淋巴结增生等血供丰富的良性病变。
综上所述,颈外侧区病变类型多,MSCT表现复杂多样,综合应用各种诊断征象、结合临床资料,可明确部分诊断,但部分病例最终仍需依靠病理学检查和免疫组化确诊。

