多孔TS-1沸石的合成、表征及其对棕榈酸的加氢脱氧性能
朱超杰, 傅雯倩, 张 磊, 唐天地
(常州大学 石油化工学院, 江苏 常州, 213164)
1983年意大利Taramass首次用水热合成法合成了拓扑结构为MFI型的钛硅分子筛TS-1[1]。由于TS-1沸石骨架中含钛原子,使其具有良好的催化氧化性能,广泛应用于精细化学品的合成中[2-3]。另外,TS-1沸石自身的稳定性好,不容易发生热分解或化学破坏,被一致认为是环境友好、环保绿色的催化材料。但是由于其双十元环孔道的微孔结构无法实现大分子反应物的扩散,使得反应只能发生在TS-1沸石晶粒的表面,不利于反应的进行[4-5]。另外,即便对于小分子反应,也由于反应物分子在微孔孔道内过长的扩散时间而导致目标产物选择性变差[6]。在TS-1沸石晶体内引入介孔结构将有利于改善反应物分子的扩散限制和催化性能,并可以实现大分子反应物的催化转化。
加氢脱氧是生物柴油制备过程中的重要反应[7]。目前的研究工作大多以金属氧化物、酸性沸石为载体制备催化剂[8-11]。由于金属氧化物载体较低的比表面积,导致金属分散度不高,反应活性较低[12-13]。沸石分子筛具有高的比表面积,有利于其负载金属的分散[14]。特别是酸性硅铝沸石分子筛负载的金属催化剂具有更高的活性。但是,由于硅铝沸石分子筛较强的酸性导致反应产物进一步发生裂化,降低了目标产物的收率[15-17]。TS-1沸石分子筛呈现极弱的酸性,高的比表面积,但其微孔性质不利于其负载金属催化剂用于大分子反应物的加氢脱氧反应。因此,本研究首先合成具有介孔结构的TS-1沸石分子筛,并用于负载金属Ni催化剂(Ni/TS-1-M),研究其对大分子棕榈酸的加氢脱氧反应性能。
1 实验部分
1.1 原料和试剂
四丙基氢氧化铵(TPAOH),浙江肯特化工有限公司产品;正硅酸乙酯(TEOS)和钛酸四丁酯(TBOT),上海凌峰化学试剂有限公司产品;异丙醇,广东光华科技股份有限公司产品;六水硝酸镍(Ni(NO3)2·6H2O),国药集团化学试剂有限公司产品;有机硅季铵盐([(C2H5O)3SiC3H6N(CH3)2C18H37]Br,TPOAB),广东德美精细化工集团股份有限公司产品。
1.2 多孔TS-1沸石的合成
多孔TS-1沸石是以有机硅季铵盐TPOAB([(C2H5O)3SiC3H6N(CH3)2C18H37]Br)为介孔模板剂在水热条件下合成。合成步骤如下:向放有磁子的烧杯中加入0.3 g TBOT和10 mL TEOS,充分搅拌,使其混合均匀,记为溶液A。向另一烧杯中加入8 mL TPAOH、6 mL异丙醇和3.5 mL水,同样搅拌充分,记为溶液B。将溶液B缓慢滴加到溶液A中,然后80℃恒温水浴除醇3 h。降至 25℃后滴加3 mL TPOAB并搅拌1 h,将获得的凝胶装入聚四氟为内衬的水热反应釜中,在180℃晶化72 h。然后经过滤、洗涤、干燥、高温煅烧,获得的白色粉末即为TS-1-M沸石。在反应体系中不加入TPOAB,按照相同的制备方法可获得微孔TS-1沸石。
1.3 催化剂制备
用等体积浸渍方法制备催化剂,具体如下:将1.485 g 六水硝酸镍溶于5.5 g 蒸馏水,得到透明的浸渍溶液,将硝酸镍水溶液浸渍到5 g TS-1-M沸石上,于 25℃干燥10 h,100℃干燥12 h,然后将干燥的粉末样品置于瓷舟,于马福炉中在空气氛围中以3℃/min升至500℃,并在500℃煅烧3 h,煅烧结束降至室温,然后在H2氛围中以3℃/min升至400℃,在400℃还原4 h,H2的流速为100 mL/min。获得的催化剂样品标记为Ni/TS-1-M,其中Ni的负载量为6%(质量分数)。采用相同的方法制备6%Ni/TS-1催化剂。
1.4 催化剂表征
采用日本Rigaku公司生产的D′max 2500 PC型衍射仪进行X射线粉末衍射分析,CuKα射线,管电压40 kV,管电流100 mA,2θ扫描范围5°~50°,步进0.02°。
采用美国Micromeritics公司生产的ASAP 2020M 型自动吸附仪进行N2吸附-脱附实验,测试前样品经200℃脱气处理。用BJH模型获得样品的织构性质,包括比表面积、孔体积和孔径分布等。
采用德国蔡司公司生产的型号为SUPRA 55 SAPPHIRE的场发射电子显微镜进行扫描电镜(SEM)分析,加速电压为5 kV。
采用日本电子株式会社生产的JEM-2100型高分辨透射电子显微镜获得透射电镜(TEM)照片,分辨率为0.14 nm,操作电压200 kV。
上述表征全部在常州大学石油化工学院分析检测中心完成。
1.5 催化剂评价
采用美国 Parr 公司生产的 4566 型 300 mL 加压反应釜进行加氢脱氧反应实验。首先,将0.5 g 煅烧后的催化剂放在石英管中,以 2℃/min升温速率由室温升至 400℃,在 400℃、100 mL/min 的H2气流中还原 4 h,降至 25℃后,在H2气流中转移到装有 100 mL 十氢萘的反应釜中。然后加入 1 g 棕榈酸,装入反应釜。用 N2置换反应釜中空气,之后开始升温。反应条件:反应温度260℃,H2压力 4 MPa,搅拌速率 300 r/m。反应过程每隔 1 h 取样1次。采用安捷伦 7890B 型气相色谱仪进行样品分析,FID 检测器,HP-5 毛细色谱柱。采用内标法计算样品的组分含量。按照式(1)、(2)计算反应转化率(x)和产物选择性(s)。
(1)
(2)
式(1)、(2)中,m0、mt分别为反应物初始质量和t时刻反应物质量,g ;ni、n0分别为产物i的物质的量和反应物初始物质的量,mol。式(1)、(2)中涉及到的质量和物质的量都是用内标法根据物质峰面积计算得到的[18]。
2 结果与讨论
2.1 沸石载体和催化剂的表征结果
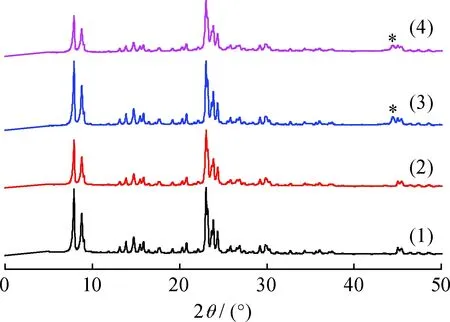
图1 合成的沸石样品及催化剂的XRD谱图Fig.1 XRD pattern of the synthesized zeolite samples and the catalysts(1)TS-1;(2)TS-1-M;(3)Ni/TS-1;(4)Ni/TS-1-M* The peak of nickel particles
图1为合成的TS-1-M、TS-1沸石和Ni/TS-1-M、Ni/TS-1催化剂的XRD谱。可以看出,TS-1-M和TS-1样品的XRD谱在2θ为 7.8°、8.8°、23.2°、23.8°和24.3°出现了5个典型的MFI特征衍射峰。负载 Ni催化剂经煅烧、还原后,上述5个特征衍射峰仍然存在,但强度略微减弱。其中,44.5°处出现的较弱的衍射峰为Ni金属颗粒的特征峰,通过布拉格方程计算,在Ni/TS-1-M和Ni/TS-1 2种催化剂上Ni颗粒的尺寸分别为9.8 nm和15.4 nm。这说明TS-1-M的高外表面积有利于金属的分散。
以合成的TS-1沸石为基准,按照下式计算得出TS-1-M的结晶度为81.3%。
相对结晶度=
图2为TS-1-M沸石样品的N2吸附-脱附等温线和孔径分布曲线。从图2(a)可见,TS-1-M沸石样品的吸附-脱附等温线在相对压力p/p0为0.40~0.95的范围内形成1个滞后环,表明样品中存在介孔结构。从图2(b)可以得知,样品的介孔孔径尺寸主要集中在3.5 nm。表1给出了沸石样品TS-1-M、TS-1和催化剂Ni/TS-1-M、Ni/TS-1的织构参数。从表1可知,合成的TS-1-M沸石有较大的比表面积、外表面积和介孔孔体积。负载金属Ni之后,催化剂Ni/TS-1-M的各参数均略微降低。值得注意的是,沸石载体的介孔表面积和介孔孔体积分别为210 m2/g和0.25 cm3/g,负载金属后分别降至174 m2/g和0.18 cm3/g,而微孔孔体积变化不大,说明金属物种主要分布在TS-1-M的介孔孔道的内表面和沸石颗粒的外表面上。
图3为TS-1-M沸石样品的SEM和TEM照片。从SEM照片可知,合成的样品晶粒呈现椭圆形形貌,尺寸较均一,约为300~400 nm(见图3(a)和图3(b))。从图3(c)和图3(d)的TEM图片可以看出,图像上存在亮的沟渠状结构,说明存在介孔孔道。

图2 TS-1-M沸石的N2吸附-脱附等温线和孔径分布图Fig.2 N2 adsorption-desorption isotherms and pore distribution curve of TS-1-M zeolite(a) N2 adsorption-desorption isotherms of TS-1-M zeolite; (b) Pore distribution curve of TS-1-M zeolite

SampleSBET/(m2·g-1)Sext/(m2·g-1)Vmic/(cm3·g-1)Vmes/(cm3·g-1)TS-1-M5362100.130.25TS-14771340.140.09Ni/TS-1-M4461740.120.18Ni/TS-1352810.110.07
SBET—BET surface area;Sext—External surface area obtained from thet-plot method;Vmic—External surface area obtained from thet-plot method;Vmes—Mesoporous pore volume obtained from thet-plot method

图3 合成TS-1-M沸石样品的SEM和TEM照片Fig.3 SEM and TEM images of the TS-1-M zeolite samples(a),(b) SEM images;(c),(d) TEM images
2.2 Ni/TS-1-M和Ni/TS-1催化剂催化棕榈酸加氢脱氧性能
在Ni/TS-1-M催化剂上考察了H2分压(pH2)和反应温度(T)对反应活性和产物分布的影响,结果分别列于表2和表3。
由表2 可知,当反应温度为260℃和反应时间为6h时,在不同H2分压下,棕榈酸的转化率均为100%。当H2分压为4 MPa时,棕榈酸全部转化为正构十五烷(92.0%)和正构十六烷(8.0%)。当H2分压降低至3 MPa 时,棕榈酸转化生成了大量的中间产物十六酸十六酯和十六醇。这说明H2分压强烈影响着产物分布。值得注意的是,随着H2分压进一步降低,中间产物十六酸十六酯的选择性几乎不发生变化,而十六醇逐渐减少,十五烷逐渐增多,这可能因为在较低的H2分压下,十六醇更容易生成十六醛,十六醛进一步转化为正构十五烷[19]。
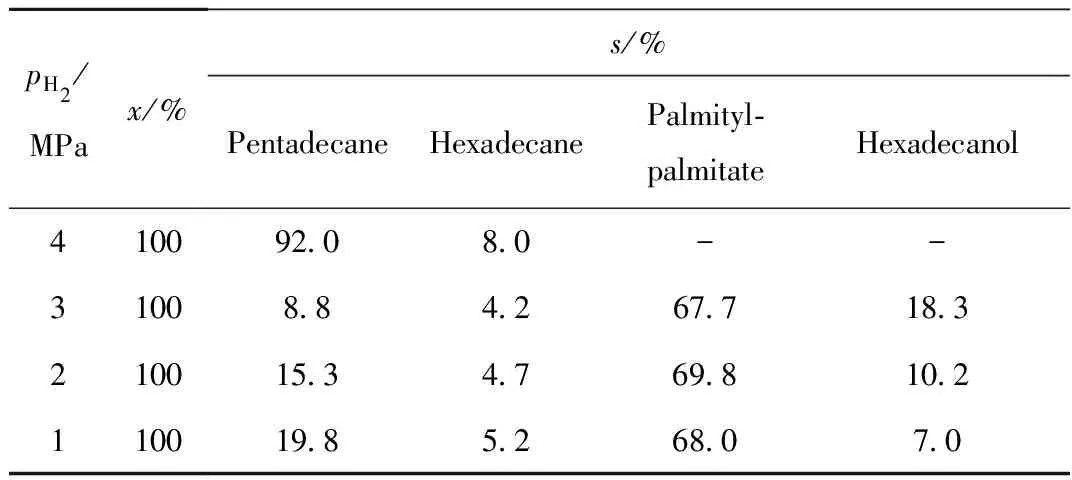
表2 在Ni/TS-1-M催化剂上H2分压(pH2)对产物选择性(s)的影响
Experimental conditions:m(Palmitic acid) = 1 g,V(Decalin)=100 mL,m(Ni/TS-1-M)=0.5 g,T= 260℃, Stirring speed 300 r/min,t=6 h

表3 在Ni/TS-1-M催化剂上反应温度(T)对产物选择性(s)的影响Table 3 Influence of reaction temperature (T) on selectivity (s) to products over Ni/TS-1-M catalyst
Experimental conditions:m(Palmitic acid)=1 g,V(decalin)=100 mL,m(Ni/TS-1-M)=0.5 g,pH2=4 MPa, Stirring speed 300 r/min,t=6 h
由表3 可知,其他反应条件保持不变,当反应温度为260℃时,棕榈酸全部转化生成目的产物正构十五烷和正构十六烷;但温度降低到240℃时,生成大量的中间产物十六酸十六酯和十六醇,仅有少量的正构十五烷;继续降低反应温度到 220℃,87.2% 的棕榈酸转化生成了中间产物十六酸十六酯和十六醇,这些结果说明反应温度也是影响该反应的重要因素。
综上所述,H2分压和反应温度均强烈影响棕榈酸的转化及其产物分布,当反应温度为260℃和H2分压为4 MPa 时,最有利于反应物的转化和目标产物的生成,故在此条件下,进一步探索了Ni/TS-1和Ni/TS-1-M催化剂催化棕榈酸加氢脱氧反应的性能。
图4为Ni/TS-1-M和Ni/TS-1催化剂催化棕榈酸加氢脱氧反应的转化率随反应时间的变化。由图4可知,在Ni/TS-1催化剂上反应5 h时的转化率只有47%,继续延长反应时间反应物不再转化。而在Ni/TS-1-M催化剂上反应1 h时棕榈酸的转化率即可达到97%,反应2 h时棕榈酸全部转化。
图5为Ni/TS-1和Ni/TS-1-M催化剂催化棕榈酸加氢脱氧反应的产物选择性随反应时间的变化。由图5(b)可知,在Ni/TS-1-M催化剂上,反应主要生成正构十五烷和正构十六烷,以反应物棕榈酸的摩尔量为基准,计算得到的正构十五烷和正构十六烷选择性分别为92%和8%。实际上,该反应的中间产物为十六醇和十六酸十六酯,它们在反应初期体系中含量较高。

图4 Ni/TS-1-M和Ni/TS-1催化棕榈酸加氢脱氧反应的转化率(x)随反应时间(t)的变化Fig.4 Conversion (x) of palmitic acid vs. reaction time(t)m(Palmitic acid) = 1 g, T=260℃, V(Decalin)=100 mL, pH2=4 MPa, Stirring speed= 300 r/min(1) 6.0% Ni/TS-1-M ; (2) 6.0% Ni/TS-1

图5 Ni/TS-1-M和Ni/TS-1催化棕榈酸加氢脱氧反应的产物选择性(s)随反应时间(t)的变化Fig.5 Selectivity (s) of products vs. reaction time (t)m(Palmitic acid) = 1 g, T=260℃, V(Decalin)=100 mL, pH2=4 MPa, Stirring speed= 300 r/min(a) 6.0% Ni/TS-1; (b) 6.0% Ni/TS-1-M
图6为Ni/TS-1-M催化剂催化棕榈酸加氢脱氧反应中不同反应时间产物分布的气相色谱。由图6可知,在Ni/TS-1-M催化剂上反应1 h,棕榈酸转化可以生成大量的十六醇和十六酸十六酯,选择性分别为28%、29%,并可以生成少量的正构十五烷和正构十六烷。随着反应的进行,十六酸十六酯可进一步转化为十六醇[20]。十六醇通过脱水反应生成少量的正十六烷,而十六醇通过脱羰反应可生成大量的正十五烷。另一方面,反应过程中也可能生成十六醛,该中间产物在反应条件下极易被还原生成十六醇,通过色谱分析手段很难检测到。PENG等[21]在研究以Ni/ZrO2为催化剂的棕榈酸加氢脱氧反应过程中,通过原位红外(IR)检测手段监测到了反应体系十六醛的存在。
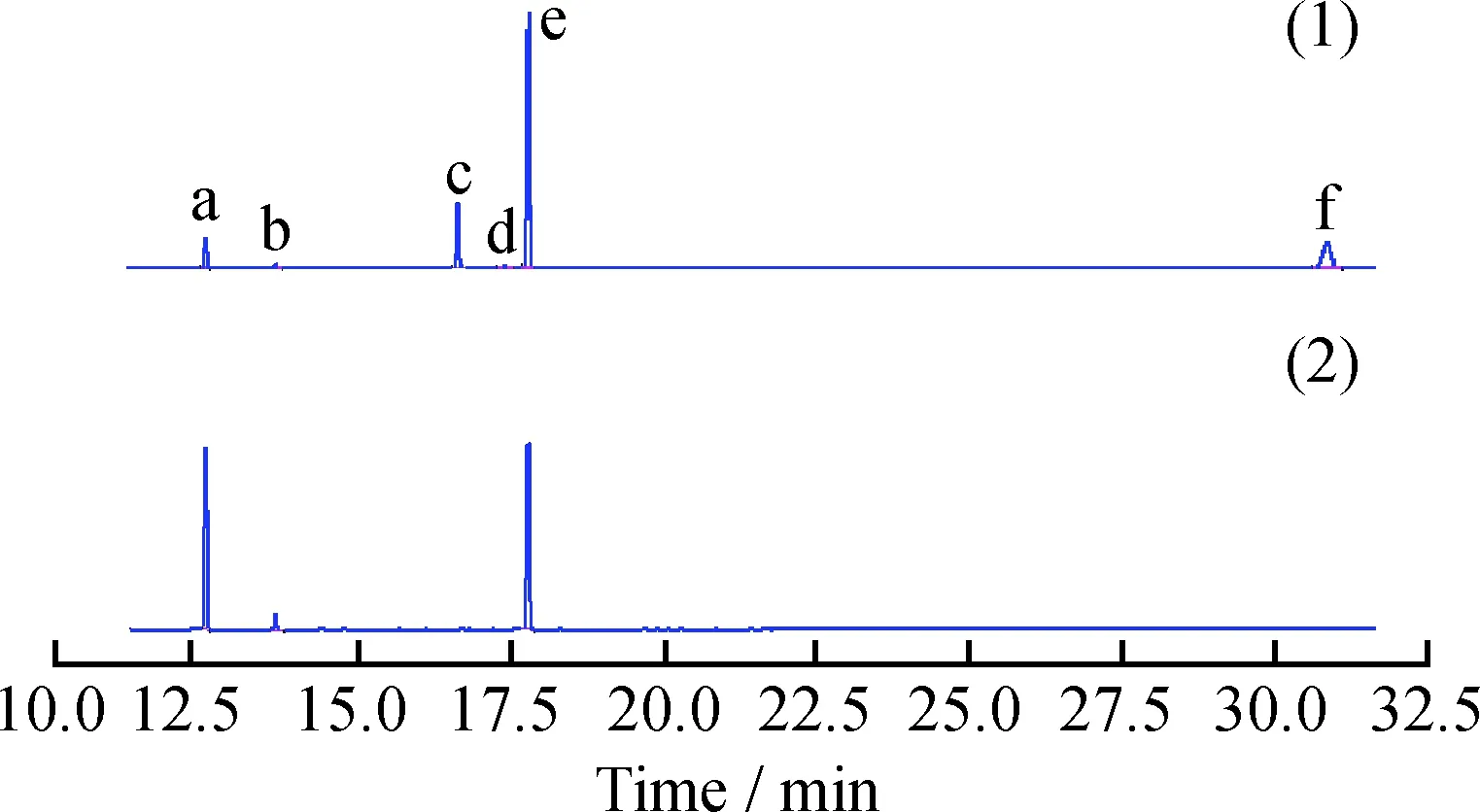
图6 Ni/TS-1-M催化剂上不同反应时间(t)产物分布气相色谱Fig.6 Gas chromatogram of products distribution at different reaction time (t) in Ni/TS-1-M catalysta—Pentadecane; b—Hexadecane; c—Hexadecanol; d—Palmic acid; e—Eicosane; f—Palmityl-palmitatet /h :(1) 1; (2) 6
与Ni/TS-1-M催化剂相比,Ni/TS-1催化剂催化棕榈酸加氢脱氧反应的中间产物类似,但是产物选择性差别较大。在反应时间5 h时,棕榈酸转化率为47%条件下,生成的中间产物十六醇、十六酸十六酯在Ni/TS-1催化剂上很难进一步转化,它们的选择性分别为5% 和21%,目的产物正构十五烷和正构十六烷的选择性较低,分别是48%和5%。
3 结 论
(1)以有机硅季铵盐 TPOAB为模板剂合成的TS-1-M沸石晶粒小,堆积形成大量的堆积介孔,具有较大的外表面积。以其为载体制备Ni催化剂,金属Ni的分散度高,Ni/TS-1-M催化剂中介孔结构的存在有利于反应物的扩散。
(2)Ni/TS-1-M在棕榈酸的加氢脱氧反应中具有很高的催化活性和目标产物选择性。在反应温度260℃、H2分压4 MPa、搅拌速率300 r/min的条件下,反应5 h时,与传统的TS-1沸石负载的Ni催化剂相比(反应物转化率为53%,十五烷和十六烷选择性分别为48%和5%),介孔TS-1-M负载的Ni催化剂上反应物转化率为100%,目标产物十五烷和十六烷选择性分别为92%和8%。

