血清标志物方程估算血液透析患者残肾功能及其临床应用价值
刘进,侯静,张帆,陈昕,王玉洁,秦建华,钟华
(1.西南医科大学附属医院 肾内科,四川 泸州 646000;2.四川大学华西医院,四川 成都 610041)
血液透析(hemodialysis,HD)的多数患者都有不同程度的残肾功能(residual kidney function,RKF)[1],其通常用残肾尿素清除率(residual kidney urea clearance,KRU)、残肾肌酐清除率或残肾尿素及肌酐清除率的均值表示[2]。取平均值与肾小管重吸收和分泌有关,因单尿素清除率会使肾小球滤过率(glomerular filtration rate, GFR)低估,而单用肌酐清除率会使GFR高估,临床常用两者均值表示RKF。RKF检测极为重要,因其与HD患者的生存和生活质量改善密切相关。其测量方法多[3],但不能用测量非HD患者的肾功能方法来定量RKF,因HD患者多有合并症干扰,且RKF水平很低[4]。传统用采集24 h或HD间期尿测量RKF,但该方法易出错。目前已有不需采集尿的方法问世[2,5],由血清标志物β-微量蛋白(β-trace protein, β-TP)和β2-微球蛋白(β2-microglobulin,β2-M)构成的估算RKF新预测方程[2],仅取HD前1次血标本,即能得出结果。鉴于该法简单、快速及准确,笔者使用尿常规方法作为金标准,利用新预测方法测量和估算42例终末期肾病需转入HD的新患者RKF,评价KRU预测方程检出KRU值>2.00 ml/(min·1.73 m2)的患者准确性,并将其应用于HD的处方中[2],现报道如下。
1 资料与方法
1.1 研究对象
选取2014年1月—2016年12月西南医科大学附属医院门诊和住院收治的终末期肾病需转入HD的42例新患者。其中,男性28例,女性14例;年龄44~73岁,平均(56±7.7岁);平均24 h尿量670 ml。纳入标准:年龄≥18岁;尿量≥200 ml/24 h;首次HD,并拟做动静脉内瘘者。排除标准:肾移植和肝炎。本研究通过医院伦理委员会批准,患者均签署知情同意书。见表1。
1.2 标志物检测
在首次HD当周的第1次HD前取血。用BN-II特种蛋白分析仪及其配套试剂(德国西门子公司),用散射免疫比浊法检测血清β-TP和β2-M水平,用全自动生化分析仪检测血清β-TP和β2-M、尿素氮及肌酐水平。
1.3 新预测方程和相关公式
1.3.1 常规方法HD间期尿测量RKF 开始HD第1次透析结束和在第2次HD之前取血,在2次取血之间的整个HD间期同步收集尿液用公式计算尿素和肌酐清除率[5]。清除率(ml/min)=尿浓度×尿量÷平均血清浓度(HD前后2值的平均值)÷尿采集时间长度。HD间期>3 d,可采用常规方法24 h尿法测量RKF[3]。
1.3.2 HD单室Kt/V(spKt/V) 使用第二代Daugirdas对数公式计算[6]:SpKt/V=-Ln(co/c1-0.008t)+(4.0-3.5×c1/co)xuf/w。t为HD时间长度(min),uf为超滤量(l),w为HD后体重(kg),co和c1分别为HD前后血尿素氮(mmol/L)。
1.3.3 smye公式纠正HD后测量血清尿素的反弹[7-8]尿素反弹=(ct-c1)/c1,ct=c15或c30。c15或c30分别为HD后15或30 min。
1.3.4 尿素分布容积(v) 采用 Watson 公式[6]。
1.3.5 KRU预测方程 ①KRU(ml/min)=69×β-TP-2.144( 女 ),KRU(ml/min)=69.000×β-TP-2.144×1.677(男);② KRU(ml/min)=1771.000×β2-M-2.328(女),KRU(ml/min)=1771.000×β2-M-2.328×1.610(男);③KRU(ml/min)=385×β-TP-1.450×β2-M-0.965( 女 ),KRU(ml/min)=385.000×β-TP-1.450×β2-M-0.965×1.694(男)。KRU单位(ml/min)便于并入Kt/Vurea,用Dubois公式计算体表面积[2],按体表面积转变成ml/(min·1.73 m2)。
1.3.6 GRF预测方程 ①GFR[ml/(min·1.73 m2)]=95×β-TP-2.16( 女 ),GFR[ml/(min·1.73 m2)]=95.000×β-TP-2.16×1.652(男);② GFR[ml/(min·1.73 m2)]=2 852×β2-M-2.417(女),GFR[ml/(min·1.73 m2)]=2 852.000×β2-M-2.417×1.592( 男 );③ GRT[ml/(min·1.73 m2)]=673.000×β-TP-1.406×β2-M-1.096( 女 ),GRT[ml/(min·1.73 m2)]=673.000×β-TP-1.406×β2-M-1.096×1.670(男)。
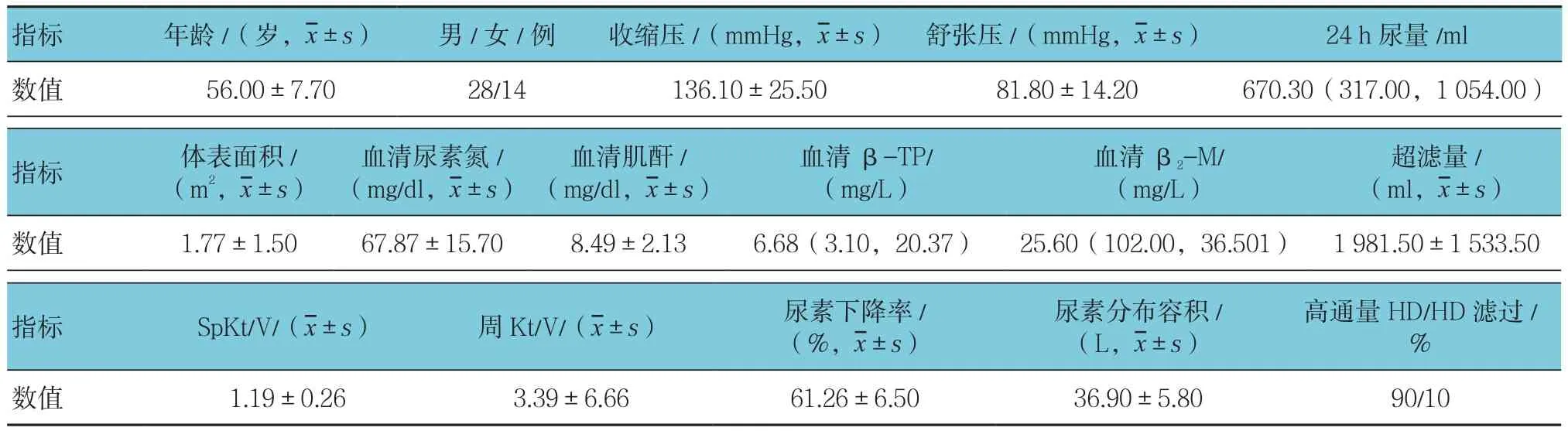
表1 HD一般资料 (n =42)
1.4 统计学方法
数据分析采用SPSS 18.0统计软件,计量资料以均数±标准差(±s)表示;计量资料非正态分布以中位数四分位间距[M(P25,P75)]表示,采用配对t检验,受试者工作特征曲线(receiver operating characteristic curve, ROC)下面积评价预测方程估算值对KRU的诊断效能,P<0.05为差异有统计学意义。
2 结果
2.1 KRU预测方程对KRU的诊断效能
KRU常规方法实测值和预测方程估算值之间的中位数偏离值为 0.30 ml/(min·1.73 m2)(P>0.05)。ROC分析显示,用方程估算KRU值>2.00 ml/(min·1.73 m2)来检出实测KRU值 >2.00 ml/(min·1.73 m2)的患者有高度诊断准确性,其ROC下面积0.88~0.91。例如用(β-TP+β2-M)的KRU预测方程估算KRU值>2.00 ml/(min·1.73 m2)作为截断值来检出实测KRU值>2.00 ml/(min·1.73 m2)的患者就给予ROC下面积0.91,其敏感性和特异性分别为71%和96%。见表2、3。
2.2 KRU预测方程应用的安全性
笔者按肾脏病生存质量指南(kidney disease outcomes quality initiative,KDOQI)所提出的最低Kt/V靶用KRU预测方程测定所能安全降低的患者比例。若以KRU值>2.00 ml/(min·1.73 m2)方程估算值为截断值可准确检出此截断值上下的患者,其符合率达82.1%。另有13.6%的患者KRU估算值<2.00 ml/(min·1.73 m2)(假阴性),还有 4.3% 的患者估算值 >2 ml/(min·1.73 m2)(假阳性)。在假阳性患者中,实测值和截断值之间平均低估值为0.74 ml/(min·1.73 m2),范围 0.05 ~ 2.00 ml/(min·1.73 m2)。按指南,如将该类患者单室Kt/V靶从1.2降低到0.9,这将导致低HD,相当于平均低0.10单室Kt/V单位(范围0.02~0.29),但还有95.7%患者接受靶值以上的HD剂量。
2.3 KRU预测方程用于开始HD处方
自报尿量>200 ml/d 42例患者中,KRU值>2.00 ml/(min·1.73 m2)的患者15例,KRU 值 >3 ml/(min·1.73 m2)的患者5例(见表4)。按指南,前者HD剂量可下调20%,后者1周1~2次HD。其余KRU值<2.00 ml/(min·1.73 m2)患者仍以常规方法3次/周HD,随后用KRU预测方程或GFR预测方程进行定期(>1~3个月)连续监测。
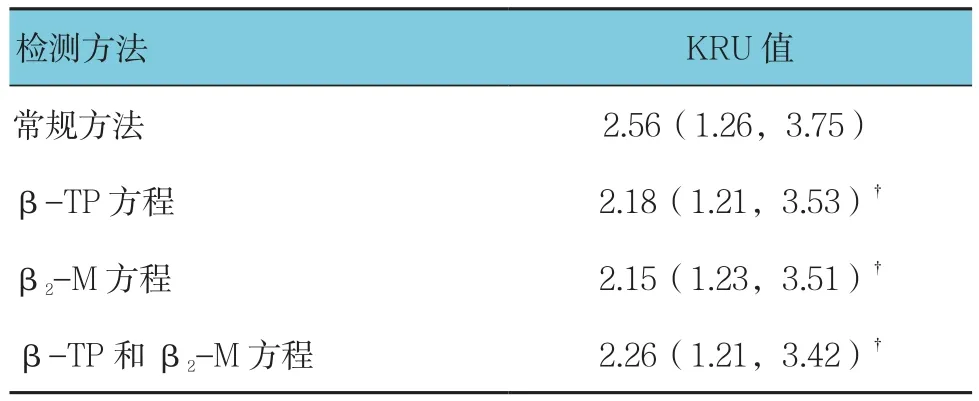
表2 KRU预测方程估算值与常规方法实测KRU值比较[n =42,ml/(min·1.73 m2)]
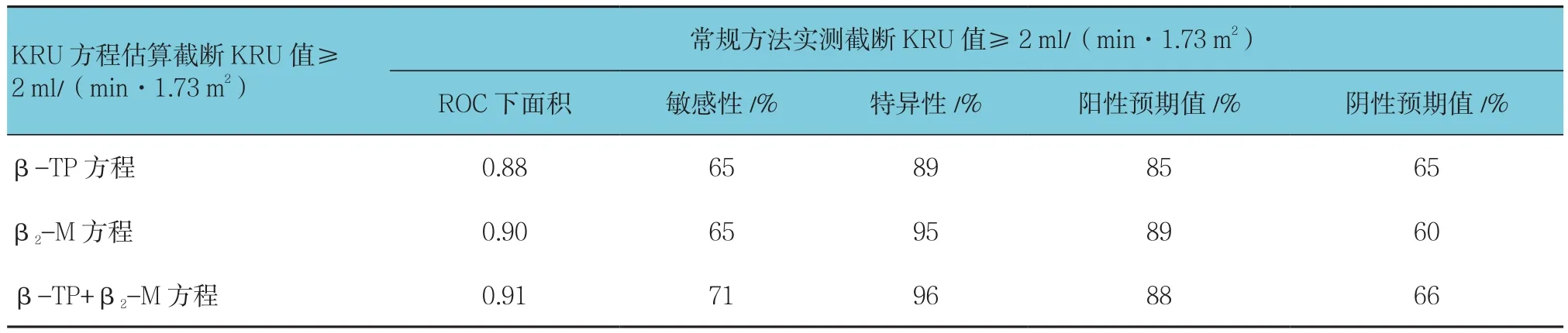
表3 3种KRU预测方程诊断RKF的效能比较 (n =42)
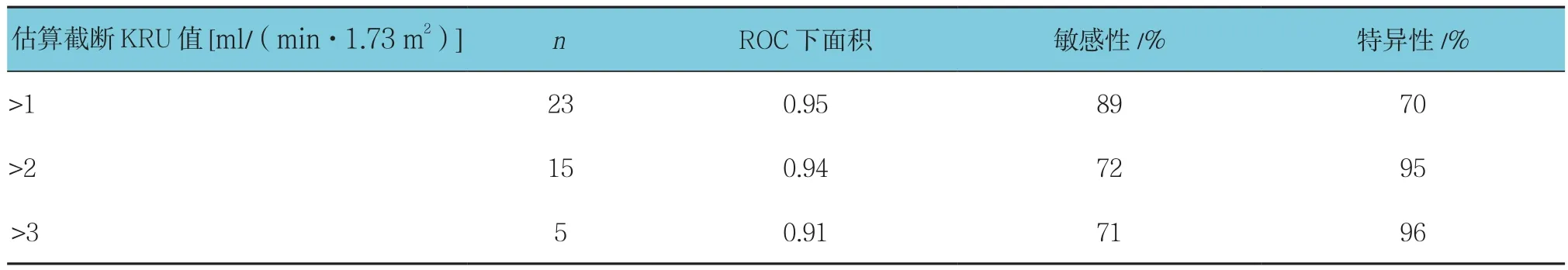
表4 KRU预测方程检出常规方法实测截断KRU值的患者ROC分析 (n =42)
3 讨论
研究证实,用β-TP和β2-M方程能准确检出KRU值≥2.00 ml/(min·1.73 m2)的患者,其符合率达82.3%,仅错误估算4.2%的患者。提示如按KDOQI算法用KRU估算值来调整最低透析Kt/V靶,那么只有小比例的患者接受低HD。KRU的优势在于:其可简单并入HD患者的处方;二是因尿素在肾小管重吸收导致KRU低估,在开始HD处方时使患者得到保护[3],从而降低HD风险。然而多数HD单位并未开展开始HD处方,如美国大多数患者均以3次/周开始,很少或根本未检测RKF以指导开始HD剂量,甚至有RKF患者(尿量/d>500 ml)也是如此[3]。因该群体2次/周HD可保留其RKF和改善生活质量[7],低频率的HD也可延长其动静脉内瘘寿命,降低经济成本。据报道,目前我国和西班牙已有半数患者2次/周做HD,但未有一个研究使用血清标志物做HD处方。据笔者所知,该法是最早应用于临床研究之一。
忽视RKF和其他患者因素做个体化处方的原因,可能与HD患者不能准确采集HD期间的尿液有关。因此,只有<5%的HD患者测量RKF。长期以来,认为HD患者RKF比腹膜透析下降快。尽管有45%的患者在开始HD时GFR值>10.00 ml/(min·1.73 m2),常规方法3次/周HD第1年的死亡率很高[7],使对HD患者保留RKF产生怀疑,因而把这种情况归咎于HD内低血压和间断性突然容量滞留;其次,忽视HD对肾可引起的与急性肾损伤相似的周期性缺血损害,如此反复缺血的累积效应可促使其RKF下降,这个假设与最近频繁的夜间HD结果一致[7]。强化的HD治疗也可移去剩余的肾小球单元高功能化的刺激,这与“完整肾小球单元”的假设一致。
最近指南推荐渐进性HD[单室Kt/V(SpKt/V)>1.2,周Kt/V>2.2,HD时间≤4 h[3]],开始HD时给予最小有效剂量、随着RKF减退逐渐增加剂量。在这情况下自然肾清除率的连续监测很重要,因要避免在此段时间RKF下降而引起的HD低处方。如用常规方法测量KRU比较麻烦,而监测总尿量与其他充分性标志物(如贫血和体液增加)的联合法适用,其任何1个充分性参数在临床有恶化都可指导HD频数的改变,即从2次/周改变为3次/周HD。但笔者和其他作者[2]的结果表明,新KRU预测方程+自报尿量>200 ml/d做渐进性HD处方,特别是做开始HD处方既简单又准确。
新方程血清标志物β-TP和β2-M。β-TP是23 kD糖蛋白在许多器官表达(包括脑、视网膜、睾丸、心脏及肾脏)。单由肾排泄其浓度在男性较高,而类固醇治疗和其他免疫抑制均可降低,但β-TP在其他炎症疾病,如红斑狼疮和恶病质者则增加。β2-M的分子量为11.8 kD,其血清水平在急/慢性炎症中,特别是在丙型肝炎和恶性疾病都可增加。可造成其预测方程估算值和实测值之间或个体间的差异[1]。相对而言,使用含2个血清标志物的方程可减少这一差异。
综上所述,β-TP+β2-M预测方程对KRU具有良好的诊断效能和准确性。对自报尿量≥200 ml和常规方法高通量(非对流)HD患者很有效,且比传统常规方法简单。不过该试验用于单个患者需谨慎,因在RKF低水平时,其敏感性有限。但当方程估算KRU值>2.00 ml/(min·1.73 m2)时,在临床检出有RKF 患者 [KRU 值 >2.00 ml/(min·1.73 m2)]则有效,尤其是做开始HD处方患者。

