应用XAFS研究十二指肠中锌的相对浓度和状态
■隋美霞 海 风 王宗伟 王汉海
(1.潍坊学院山东省生物化学与分子生物学重点实验室,山东潍坊261061;2.沈阳鸟岛管理有限公司,辽宁沈阳110000;3.山东省寿光市畜牧兽医管理局,山东寿光262700)
Zn元素因具有广泛的生理生化功能而被称为机体的“生命元素”,同时也是必需的微量元素之一。然而,不同状态锌源锌在机体内的生物利用率有显著差异。目前,生物制品中的Zn大多停留在应用原子吸收光谱进行锌的含量研究[1],并未涉及到其结构,X射线吸收精细结构(X-ray absorption fine structure,XAFS)技术不只是局限于结晶物质结构和物质电子结构的研究,还可研究吸收原子的几何结构和化合态。此外,XAFS技术能检测出与该微量元素相临界元素的氧化状态。目前,对Zn元素的研究主要集于饲养试验,大多数是对日粮中添加不同状态锌源的效果进行了报道,但对其在反刍动物十二指肠内的吸收特点及消化机理研究甚少,主要原因是缺乏有效的测定方法。本试验目的是应用XAFS探讨外翻肠囊试验条件下,不同状态的锌源锌经绵羊十二指肠肠囊吸收后浓度及状态变化。探索XAFS技术在动物营养研究中Zn的应用,并为反刍动物不同状态锌源的合理应用提供依据。
1 材料与方法
1.1 试验材料
不同状态锌源锌标准品:氧化锌,ZnO含量≥95.00%,Zn含量76.75%;硫酸锌,ZnSO4含量≥97.00%,Zn含量35.55%;蛋氨酸锌,ZnMet含量≥81.50%,Zn含量18.97%;赖氨酸锌,ZnLys含量≥28.00%,Zn含量5.31%。
在上海光源XAFS试验站进行Zn元素的XAFS谱测定,其中,电子能量为800 MeV,平均电流强度为105.6 mA。
1.2 试验设计
选取体格健壮、体重相近的18头绵羊作为十二指肠的供体动物,禁食12 h,屠宰,立即分离出10 cm长的十二指肠中段,用39~40℃的生理盐水冲洗,参照Seal等[2]所述方法,制成外翻肠囊,立即投入盛有20 ml按试验处理安排配制的不同形态锌培养液的培养瓶中,向瓶内充入95%O2和5%CO2后,密闭条件下40℃水浴振荡培养(100 r/min)40 min[3],整个过程不应超过15 min(保证肠段具有正常的生理机能)。按等量锌在上述处理中加入6种不同锌源(ZnO、ZnSO4、ZnMet、ZnLys、ZnSO4+Met、ZnSO4+Lys)。培养结束后,肠段用生理盐水反复冲洗,65℃干燥24 h,待用。同步辐射装置上测定Zn的XAFS谱,同时测定锌源标准品(ZnO、ZnSO4、ZnMet、ZnLys)的XAFS谱。
1.3 数据处理
试验所得数据应用 origin(6.1)软件整理后,同时进行归一化分析。
2 结果与分析
2.1 不同锌源标准品的XAFS谱
饲料级标准品锌源的K边XAFS谱见图1。
在XAFS图谱中,Zn的K边吸收值为9 659 eV,总能量范围在100 eV内。通过图谱可以看出,四种锌源标准品的XAFS谱吸收值差距明显,两种无机锌较两种有机锌的K边吸收值显著增大。ZnO与另外三种锌源不同点主要表现为,其在主吸收峰的低结合能一侧有肩峰,表明样品中饲料级ZnO中的Zn可能存在两种或两种以上的不同化学状态,但其主化学状态为ZnO;此外,局域结构也有所不同,这可能是锌周围氧原子数目不同导致形成的。其它三种锌源谱线表明基本只有一种化学状态。由以上谱线显示的能量和局域结构可以看出,Zn在这四种标准品中的结构存在显著差异。

图1 四种标准品锌的K边XAFS谱线
2.2 十二指肠肠囊中不同锌源的浓度和结构变化
十二指肠肠囊中四种锌源(ZnO、ZnSO4、ZnMet、ZnLys)的K边XAFS谱线见图2。

图2 十二指肠肠囊中不同锌源的K边XAFS谱线
由图2可以看出,经过密闭震荡培养40 min后,ZnO、ZnSO4、ZnMet、ZnLys四种锌源的谱线基本相同,但有机锌组(ZnMet、ZnLys)相对浓度明显优于无机锌组(ZnO、ZnSO4),ZnMet突变最大,ZnO突变最小,即十二指肠壁中ZnMet组锌浓度最高,ZnO组锌浓度最低,这说明在十二指肠体外培养过程中有机锌较易吸收。此外,从该图中也可以看出有机锌较无机锌K边吸收值较小,但四种锌源吸收峰后的曲线形状非常相似,说明经过体外培养十二指肠壁中Zn的化学状态相同。
十二指肠肠囊中不同锌源(ZnSO4、ZnMet、ZnLys、ZnSO4+Met、ZnSO4+Lys)的K边XAFS谱线见图3。
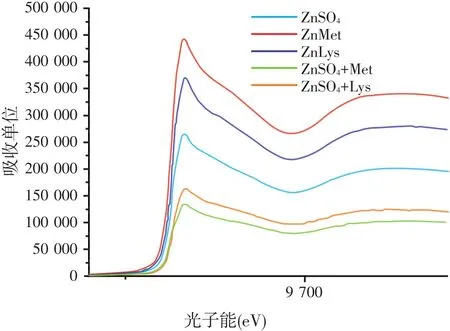
图3 十二指肠肠囊中不同锌源的K边XAFS谱线
由图3可以看出,经过密闭震荡培养40 min后,这5种锌源的谱线基本相同,吸收峰后的曲线形状非常相似,说明经过体外培养十二指肠肠囊中Zn的化学状态相同,但是其相对浓度却发生了明显变化,顺序 依 次 为 ZnSO4+Met<ZnSO4+Lys<ZnSO4<ZnLys<ZnMet。
ZnSO4、ZnSO4+Met、ZnSO4+Lys三种锌源来说,ZnSO4的突变最大,其相对浓度相对最高,而ZnSO4+Met、ZnSO4+Lys这两组差别不大,说明虽然在ZnSO4中添加了蛋氨酸和赖氨酸,但在吸收过程中,这两种游离氨基酸并未促进锌元素的吸收,反而抑制其吸收。
对于 ZnSO4、ZnMet、ZnSO4+Met三种锌源来说,ZnMet的突变最大,其相对浓度相对最高,其次是Zn-SO4,最后是ZnSO4+Met,说明有机锌较易被吸收,添加蛋氨酸抑制锌元素的吸收,但是其结构均相同。Zn-SO4、ZnLys、ZnSO4+Lys三种锌源的吸收情况与ZnSO4、ZnMet、ZnSO4+Met的相似。
3 讨论
3.1 XAFS技术测定元素的优越性
同步辐射XAFS技术除了能够定性定量检测大多数的微量元素,且能研究吸收原子的几何结构和化合态,鉴于此,XAFS技术将是生命科学研究的重要手段[4]。但目前XAFS技术在生物样品中的应用较少,仅有少量研究报道了应用Synchrotron radiation评定饲料中的微量元素[5],但试验结果显示,XAFS谱峰值对不同元素的价态均极为敏感,不同价态微量元素的XAFS谱可以很好被分开。
3.2 外翻肠囊技术在动物试验中的优越性
外翻肠囊技术即从屠宰的动物活体立即取出小肠后分割,将各片段外翻结扎,向囊状物中注入特定的培养液(不含待测物质),立即将其放入特定的含有待检测物质的培养液中,通过检测肠囊中待检测物质的含量及状态变化,从而明确元素吸收情况[6]。Evans[7]采用该方法研究了大鼠整段小肠Zn元素的最佳吸收部位,认为外翻肠囊法是目前有效的研究微量元素吸收的方法。
3.3 十二指肠肠囊Zn的相对浓度和状态变化
该试验结果可看出,在外翻肠囊试验条件下,十二指肠中有机锌较无机锌更容易被吸收。Ashmead等[8]的研究结果显示,大鼠分离不同肠段对有机铜的吸收率是无机铜的4倍,这与本试验所得结果一致。但是Hill等[9]利用大鼠十二指肠外翻肠囊技术结果显示,三种锌源(氯化锌、蛋氨酸锌、赖氨酸锌)中Zn元素在培养后液体中的出现率并无显著差异,表明有机锌和无机锌的生物学活性相似。这与本试验结果有较大差异,出现上述结果不一致的原因可能与试验方法、所用试验动物的种类、所处的生理状态不同有关。
本试验在无机锌中添加游离氨基酸,非但没有促进锌元素的吸收,反而抑制其吸收。计峰[10]通过外翻肠囊方法研究结果表明,无机锰与两种氨基酸(甘氨酸、蛋氨酸)混合物的吸收率都比单一无机锰的吸收率要小,这与本试验结果一致。Wapnir等[11]研究结果表明,较小分子量配体从某种程度上可以络合Zn,从而达到防止Zn元素在生理pH值条件下生成沉淀的效果,因而可促进Zn元素的吸收,且当配体与锌的比例小于或等于3∶1时作用最有效,此结论被过量组氨酸可竞争性抑制组氨酸锌的吸收所证实。Bonewitz[12]认为,小分子量配体的作用是使饲粮中的锌更易吸收,而不是锌转运体系中不可缺少的组成成分。本试验中添加蛋氨酸及赖氨酸,可能是由于添加过量,过量的蛋氨酸及赖氨酸竞争性地抑制了锌元素的吸收,所以锌的吸收相对减少。
国内外学者研究结果显示,大鼠肠道对Zn元素的吸收包含两个基本过程,即饱和载体调节及非饱和扩散[13-16]。Hempe等[17]认为,这种现象表明Zn元素在机体肠道内的吸收可分为跨细胞吸收和细胞间扩散两大类。本试验通过外翻肠囊技术研究绵羊十二指肠对不同状态Zn的吸收,其中四种标准品中Zn的状态不相同,所处环境亦不同,但经过绵羊十二指肠吸收后,四种结构状态反而相差不大,极为相似,这说明有机锌的吸收途径可能与无机锌的相似,即从吸收机理而言,有机锌与无机锌一样,即通过不依赖于载体调节的非饱和扩散形式被机体吸收的,有机锌首先解离成离子,然后通过无机锌的吸收途径被机体肠道所吸收。于昱[18]通过试验结果提出了有机锌与无机锌的吸收途径相似的假设,本试验结果确定了于昱提出的有机锌的吸收假说,本试验采用XAFS技术检测十二指肠肠囊锌元素的吸收状态,较于昱方法更为成熟,样品处理更简便,而且试验误差很小。
4 结论
本试验应用先进的XAFS技术,样品制备过程简易,测定结果更为准确,但影响因素相对较少。此外,通过外翻肠囊技术研究机体肠段对不同状态Zn的吸收,试验结果显示有机锌优于无机锌,有机锌更易被吸收,确定十二指肠肠道中有机锌的吸收机理与无机锌的相同。此外,本试验结果显示,无机锌与配体蛋氨酸及赖氨酸的结合反而抑制了锌元素的吸收,这可能与无机锌与配体比例有关,有必要开展进一步研究。但本试验是在外翻肠囊的试验条件下测定的,有必要进一步开展体内试验加以验证,在既不影响动物营养需要,又能提高锌的吸收及利用率的前提下,应用适宜廉价的锌添加剂,从而降低饲养成本。

