海藻酸钙包覆聚苯乙烯磺酸钠软胶囊去除废水中Cu2+和Cd2+
崔龙哲,万 思,刘 瑾,林晓宇
(中南民族大学 资源与环境学院,武汉430074)
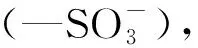
1 实验部分
1.1 试剂和仪器
聚苯乙烯磺酸钠(PSSA, Sigma-aldrich),Cu(NO3)2、Cd(NO3)2·4H2O、海藻酸钠、无水CaCl2、HNO3、NaOH(国药集团化学试剂),所有试剂均为分析纯.火焰原子吸收光谱仪(AAS,iCE3500型,赛默飞世尔科技);电子显微镜(Nikon SM2 1500,Dong Sung Medical. Co,Japan);傅立叶红外光谱仪(FT-IR,Spectrum GX,PERKIN-Elmer,USA).
1.2 PSSA@Alg软胶囊的制备
将2.0%CaCl2和12.5%PSSA混合溶液逐滴加至0.6%海藻酸钠溶液中,液滴中的Ca2+迅速迁移至液滴表面与海藻酸钠(SA)反应生成海藻酸钙固态壳,将PSSA液滴包裹,形成PSSA@Alg软胶囊,将胶囊置于2.0%CaCl2溶液中再次固化30 min,用蒸馏水洗涤至中性,4 ℃下储存(制备过程见图1).为便于比较,将0.6%海藻酸钠溶液逐滴加至2.0%CaCl2溶液中,海藻酸钠与CaCl2快速反应形成微球状海藻酸钙凝胶,继续缓慢搅拌30 min使之进一步固化,制得海藻酸钙微球于4 ℃下储存备用.
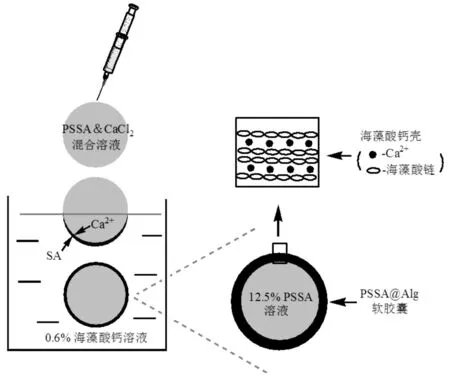
图1 PSSA@Alg软胶囊的制备过程Fig.1 Preparation process of PSSA@Alg soft capsule
1.3 静态吸附
分别制备1 g·L-1的Cu(II)和Cd(II)储备溶液,进一步稀释得到一定浓度的重金属溶液,量取50 mL重金属溶液置于250 mL锥形瓶中,加入一定质量的吸附剂,将锥形瓶置于恒温振荡箱内振荡吸附,使用火焰原子吸收光谱仪测定吸附前后溶液中金属离子浓度,吸附量由式(1)计算:
(1)
式中:Ci和Cf分别为初始和吸附后的金属浓度, mg·L-1;Vi和Vf分别为初始和吸附后的溶液体积,L;M为吸附剂的干重,g.
2 结果与讨论
2.1 PSSA@Alg性能表征
PSSA@Alg软胶囊外观如图2所示.由图2可见:所制备的PSSA@Alg软胶囊大小较均匀,呈6~7 mm椭圆球状,壳体厚度约125~140 μm,呈透明状,内包乳白色溶液.
因吸附实验中所取用的吸附剂均为未经烘干的Alg微球和PSSA@Alg软胶囊,为了方便计算吸附量,将一定湿重的吸附剂于80 ℃条件下烘干48 h,称量其干重[7],用式(2)计算干湿比.

(2)
干湿比的计算结果如表1所示,分析数据可知,Alg微球和PSSA@Alg软胶囊的干湿比分别为(3.99±0.04)%,(5.06±0.07)%,说明采用吸附材料干重计算吸附量可行.

图2 PSSA@Alg软胶囊的电镜图Fig.2 SEM figure of PSSA@Alg soft capsule
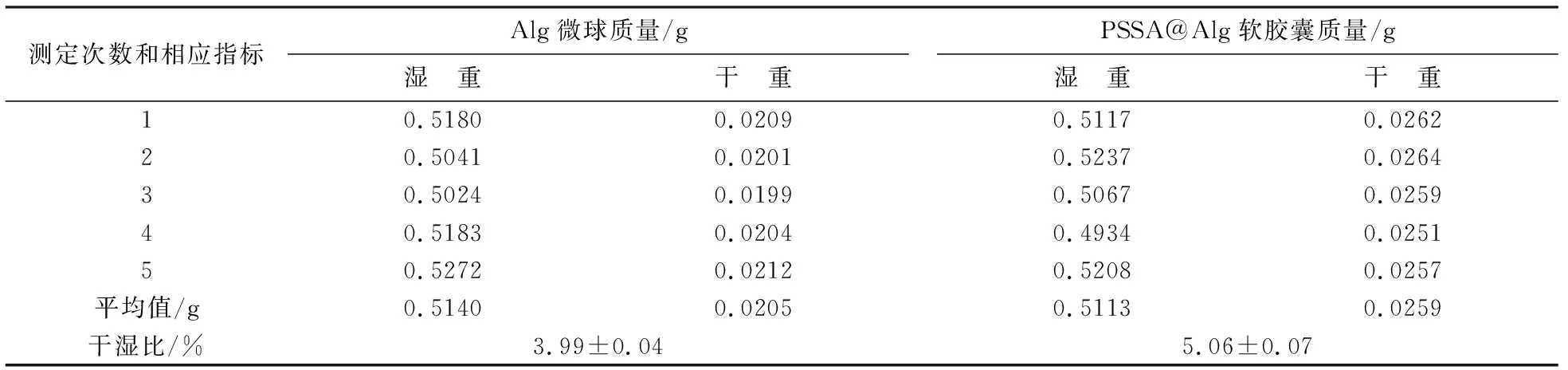
测定次数和相应指标Alg微球质量/g湿 重干 重PSSA@Alg软胶囊质量/g湿 重干 重10.51800.02090.51170.026220.50410.02010.52370.026430.50240.01990.50670.025940.51830.02040.49340.025150.52720.02120.52080.0257平均值/g0.51400.02050.51130.0259干湿比/%3.99±0.045.06±0.07
2.2 溶液pH对吸附的影响
溶液pH 对PSSA@Alg软胶囊吸附Cu(II)和Cd(II)的影响,及与Alg微球的吸附性能的比较结果如图3所示.由图3可见:PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附量均随着pH值的升高而增大.因为在pH较低时,溶液中H+浓度较大,与金属离子竞争吸附位点,使金属离子的吸附量偏低;随着pH值增大,H+浓度降低,吸附材料对铜离子、镉离子吸附量增大.Alg微球对Cu(II)和Cd(II)亦有一定的吸附作用,溶液pH对Alg微球吸附重金属离子的影响趋势与PSSA相同.比较两种材料的吸附量可知:PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附量均约为Alg微球的2倍,可见固态的海藻酸钙壳体和内包的PSSA溶液均对重金属离子Cd(II)和Cu(II)的吸附起作用.
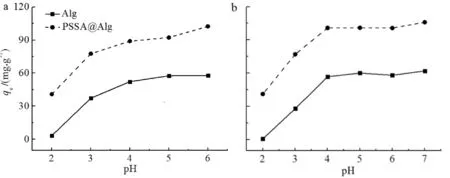
a)Cu(II); b)Cd(II)图3 pH对Cu(II)和Cd(II)吸附的影响Fig.3 Effect of pH on adsorption of Cu(II) and Cd(II)
2.3 吸附动力学
PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附量随吸附时间的变化结果见图4.由图4a可知:初始阶段PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附速率较快,吸附量随吸附时间的延长而快速增大,随着吸附时间的持续延长,溶液中重金属离子浓度逐渐降低,吸附速率变缓,最终达到吸附平衡,Cu(II)和Cd(II)达到吸附平衡的时间分别约需240,360 min.为进一步评价吸附动力学特征,用公式(3)~(5)的拟一级、拟二级动力学模型和颗粒内扩散模型[8]对图4a中的实验数据进行拟合,相关参数见表2和表3.
拟一级动力学:ln(qe-qt)=lnqe-K1t,
(3)
(4)
颗粒内扩散:qt=kit0.5+Ci,
(5)
式中:qt为时间t时金属离子吸附量,mg·g-1;qe为吸附平衡时金属离子的吸附量,mg·g-1;K1为拟一级平衡速率常数,min-1;K2为拟二级平衡速率常数,g·(mg·min)-1;ki为粒内扩散速率常数,mg·(g·min1/2)-1;Ci为颗粒内扩散常数,mg·L-1.
拟合结果见图4b~4d所示.由图4b,4c及表2可知:拟二级动力学的R2值高于拟一级动力学模型,表明吸附过程更加符合拟二级动力学.由图4d可知:PSSA@Alg软胶囊吸附Cu(II)和Cd(II)的颗粒内扩散曲线在达到吸附平衡之前均可拟合为两段直线,且直线都不经过原点,说明内扩散不是控制吸附过程的唯一步骤;图中4条直线拟合的相关系数R2均大于0.96,说明吸附过程包括吸附剂表面吸附和固态海藻酸钙壳内缓慢扩散2个过程.由表2可知:k1>k2,说明PSSA@Alg软胶囊对Cu(II)和Cd(II)吸附均大约90 min后较慢的吸附过程(固态海藻酸钙壳内缓慢扩散)占优势[6].
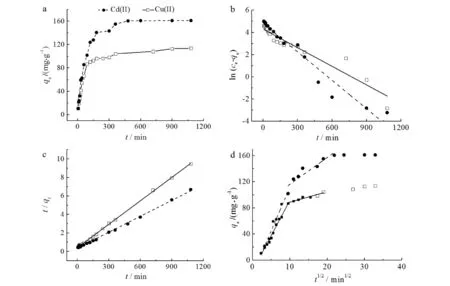
a)接触时间对吸附量的影响; b)拟一级动力学; c)拟二级动力学; d)颗粒内扩散图4 动力学特征及拟合曲线Fig.4 Kinetic characteristics and fitting curves

不同离子拟一级动力学模型qe/(mg·g-1)K1/min-1R2拟二级动力学模型qe/(mg·g-1)K1/min-1R2Cu(II)73.610.00560.9290118.480.00020.9991Cd(II)121.680.00850.9516174.220.00010.9973
表3 PSSA@Alg软胶囊对吸附铜(II)和镉(II)的颗粒内扩散模型的参数
Tab.3 Parameters of the particle diffusion model of adsorption of Cu(II) and Cd(II) by PSSA @ Alg soft capsule

不同离子不同参数k1R2k2R2Cu(II)10.7920.9941.6060.967Cd(II)13.3280.9933.2450.963
2.4 等温吸附
在25 ℃下考察了PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附量与溶液中重金属离子平衡浓度之间的关系,并用下式(6),(7)的Langmuir和Freundlich等温模型对实验数据进行了线性拟合.
(6)
(7)
式中:qe为吸附平衡时的吸附量, mg·g-1;qm为最大吸附量,mg·g-1;b为Langmuir平衡常数,L·mg-1;Ce为吸附平衡时金属溶液的浓度,mg·L-1;k为Freundlich常数,mg1-1/n·L1/n·g-1;n为Freundlich指数.
拟合结果见图5和表4.由图表可知:PSSA@Alg软胶囊对Cu(II)和Cd(II)的等温吸附数据用Langmuir模型拟合的相关系数(R2)均大于Freundlich模型,说明吸附过程更符合Langmuir模型,表明吸附剂的活性位点较为均匀,PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附以单层吸附为主,倾向于化学吸附.25 ℃下,PSSA@Alg软胶囊对Cu(II)和Cd(II)的最大吸附量分别为143.92,193.64 mg·g-1,对应的摩尔吸附量分别为2.265,1.723 mmol·g-1.PSSA@Alg软胶囊对Cu(II)的摩尔吸附量大于Cd(II),原因是铜离子半径比镉离子小,有利于铜离子传输至吸附剂内部与聚苯乙烯磺酸钠发生反应.
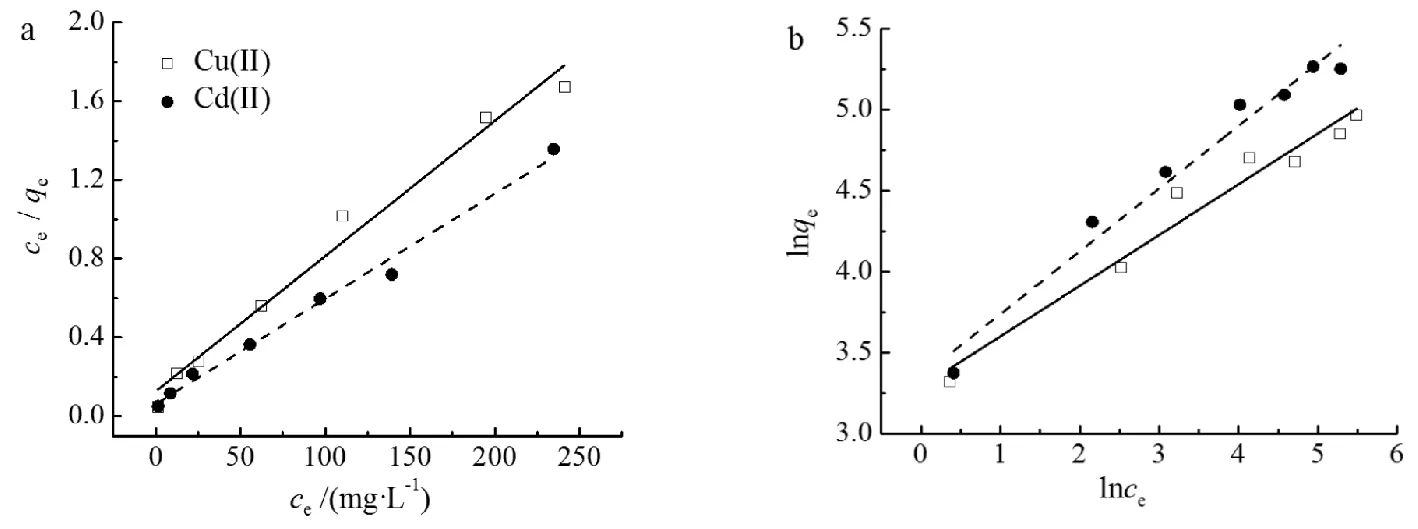
a)Langmuir等温吸附; b)Freundlich等温吸附图5 不同等温吸附方程的拟合曲线Fig.5 Fitting curve of different isothermal adsorption equations
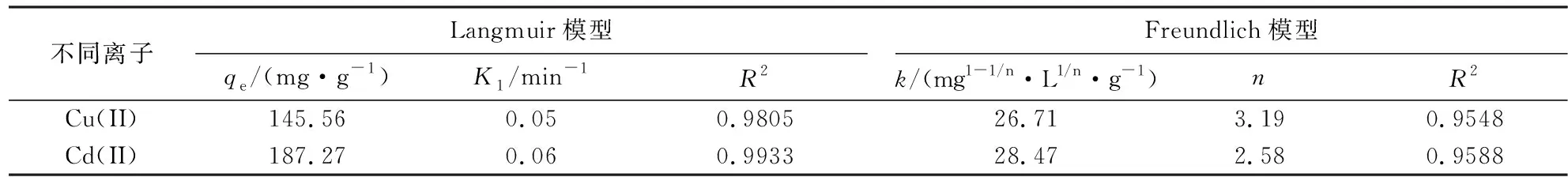
不同离子Langmuir模型qe/(mg·g-1)K1/min-1R2Freundlich模型k/(mg1-1/n·L1/n·g-1 )nR2Cu(II)145.560.050.980526.713.190.9548Cd(II)187.270.060.993328.472.580.9588
表5列出了已报道文献中的其他吸附剂对Cu(II)和Cd(II)吸附,与大多数吸附剂相比,PSSA@Alg软胶囊显示出更好的吸附能力.

表5 PSSA@Alg软胶囊与其他吸附剂吸附Cu(II)和Cd(II)的比较Tab.5 Comparison of adsorption of Cu(II) and Cd(II) by PSSA @ Alg soft capsule and other adsorbents
2.5 吸附机理分析
Alg微球和PSSA@Alg软胶囊对Cu(II)和Cd(II)均有一定的吸附作用,PSSA@Alg软胶囊对Cu(II)和Cd(II)的吸附量约为Alg微球的2倍,说明固态的海藻酸钙壳体和内包的PSSA溶液能吸附重金属离子Cd(II)和Cu(II).吸附Cu(II)和Cd(II)后的PSSA@Alg软胶囊与吸附前对比,海藻酸钙壳体厚度无变化,表明PSSA@Alg软胶囊很稳定.吸附Cu(II)后的海藻酸钙壳体和内包的PSSA溶液为淡蓝色,也证明了吸附作用.
吸附重金属前、后的PSSA@Alg软胶囊的傅里叶红外(FTIR)分析结果见图6.由图6可见:1171,1127, 1036 cm-1为SO的伸缩振动峰[15],1598 cm-1为COO-的不对称伸缩振动峰[16]PSSA@Alg软胶囊吸附Cu(II)和Cd(II)后SO和COO-的红外特征峰均发生了偏移,说明海藻酸钙上的羧基和PSSA上的磺酸基团在PSSA@Alg软胶囊吸附重金属离子的过程中起重要作用[17].
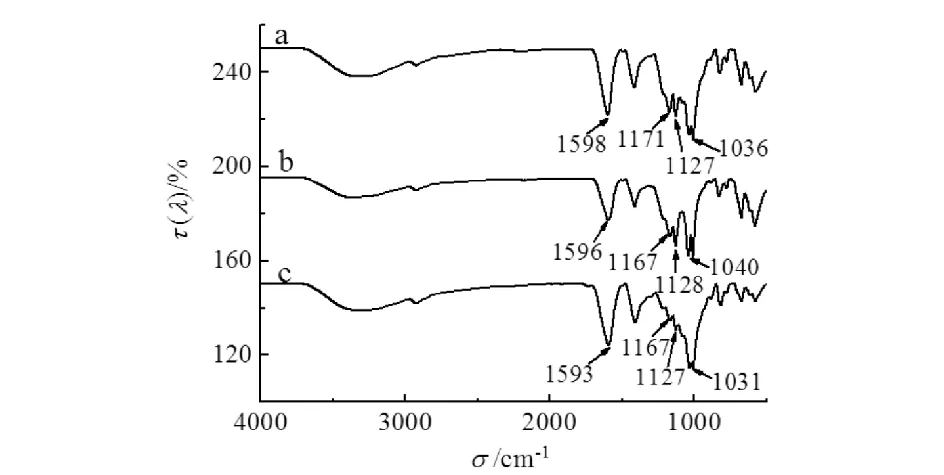
a)吸附前; b)吸附Cd; c)吸附Cu图6 PSSA@Alg软胶囊吸附前后的红外光谱图Fig.6 Infrared spectra of PSSA @ Alg soft capsule before and after adsorption
PSSA@Alg软胶囊对重金属Cu(II)和Cd(II)的吸附过程主要分两步(见图7):(1)固态的海藻酸钙壳体中的羧基与Cu(II)和Cd(II)之间的静电吸附;(2)内包的PSSA溶液中的磺酸基团与Cu(II)和Cd(II)通过螯合作用而产生吸附.

图7 PSSA@Alg软胶囊与重金属反应机理Fig.7 Reaction mechanism of PSSA@Alg soft capsule and heavy metal
3 结论
(1)溶液pH对吸附有较大的影响,PSSA@Alg软胶囊对溶液中Cu(II)和Cd(II)的吸附量随溶液pH升高而增大.
(2)PSSA@Alg软胶囊对溶液中Cu(II)和Cd(II)的吸附分为吸附剂表面吸附和固态海藻酸钙壳内缓慢扩散两个过程,吸附过程符合拟二级动力学模型,分别约240 min,320 min达到吸附平衡.
(3)等温吸附数据符合Langmuir模型,25 ℃下,PSSA@Alg软胶囊对Cu(II)和Cd(II)的最大吸附量分别为143.92,193.64 mg·g-1.
(4)海藻酸钙上的羧基和PSSA上的磺酸基团在PSSA@Alg软胶囊吸附重金属离子的过程中起重要作用.

