含洛匹那韦/利托那韦二线方案抗HIV病毒治疗失败基因型耐药情况分析
刘家法,张 米,李健健,杨壁珲,邓雪媚,雷素云
(云南省传染病专科医院/艾滋病关爱中心,昆明 650301)
云南省是我国人类免疫缺陷病毒(HIV)/艾滋病(AIDS)的传播、流行和危害最为严重的地区之一,目前治疗人数较多,基因型较为复杂,已成为云南省的重大公共卫生问题和社会问题之一,引起社会各界的高度重视。据云南省防治艾滋病局的报道,截至2016 年12 月,全省存活HIV感染者92 957例,累计治疗患者88 549例,正在治疗70 317例,其中因耐药发生治疗失败总人数9 344例,累计治疗总人数中耐药发生率为10.55%。对于治疗失败的患者不得不更换治疗方案,使用二线治疗方案,提高治疗效果。本文对云南省更换含洛匹那韦/利托那韦(LPV/r)二线抗病毒治疗方案治疗失败的患者进行基因型耐药检测,以便了解目前云南省二线治疗方案的耐药情况。
1 资料与方法
1.1 一般资料
收集2014年1月1日至2016年12月31日来自云南省传染病专科医院接受免费抗病毒治疗的患者治疗信息,筛选出更换含LPV/r治疗方案且治疗时间大于6个月、检测病毒载量大于1 000 copy/mL的血浆标本共计162份。同时收集这部分患者的人口学、临床及实验室资料。
1.2 方法
1.2.1HIV-1病毒载量检测 参照《HIV-1病毒载量测定及质量保证指南》(2013版)。采用罗氏公司的HIV病毒载量检测仪,以及其配套试剂COBAS TaqMan HIV-1 Test v2.0定量检测HIV-1病毒载量,具体检测方法参见仪器说明书及试剂盒说明书。
1.2.2血浆RNA提取 采用美国雅培公司m2000sp全自动核酸提取仪及配套试剂从待检血浆中提取病毒RNA,具体提取方法参见仪器说明书及试剂盒说明书。
1.2.3基因型耐药性检测 采用自建基因型耐药检测方法进行逆转录扩增,并参照《HIV-1基因型耐药检测及质量保证指南》(2013版),通过套式聚合酶链反应扩增覆盖蛋白酶基因全序列和反转录酶1~300位密码子序列,扩增产物送北京诺赛基因有限公司进行纯化和序列测定。扩增及测序引物参照文献[1]。
1.2.4序列拼接与分析 耐药分析应用Contig Express 软件拼接原始核苷酸序列,用BioEdit 软件对拼接后的序列校对、整理和比对分析,整理后序列提交美国斯坦福大学HIV耐药基因型检测数据分析和解释系统(http://hivdb.stanford.edu)进行耐药突变位点的分析和解释耐药变异情况。
2 结 果
2.1 人口学特征
筛选云南省抗病毒治疗数据库,筛选出符合条件样本162份,其病毒载量均值为40 951 copy/mL,CD4+T淋巴细胞计数均值为249个/μL,平均治疗时间为42.3个月。这部分患者中男96例,女66例,男女比率为1.45∶1.00;年龄4~81岁,平均年龄为43岁。患者具体信息见表1。
2.2 耐药基因扩增和测序结果
162例样本经自建基因型耐药检测方法RT-PCR扩增阳性,将扩增出来的片段进行基因序列测序,共获得162份完整基因序列。
2.3 耐药情况
以出现任意1种药物耐药突变(低、中、高度耐药)统计为耐药,将162例完整基因序列,上传美国斯坦福大学HIV-1耐药基因型检测数据分析和解释系统结果显示,65(40.1%)例对核苷类逆转录酶抑制剂(NRTIs)、非核苷类逆转录酶抑制剂(NNRTIs)以蛋白酶抑制剂 (PIs)有不同程度耐药;其中对NRTIs和NNRTIs的耐药分别有34例(21.0%)和54例(33.3%),对PIs耐药5例(3.1%)。在已检出具有不同程度耐药的65例患者中,有3例(1.9%)出现对3类药同时耐药的患者;有28例(17.3%)的患者对NRTIs及NNRTIs两种药物同时出现耐药。在使用过的药物中,对NVP、EFV、3TC、FTC高度耐药的情况分别是45例(27.8%)、35例(21.6%)、26例(16.0%)、26例(16.0%),对PIs有2例患者出现高度耐药的情况。具体对每种药物的耐药情况见表2。

表1 162例患者的临床资料
EFV:依非韦伦;NVP:奈韦拉平;3TC:拉米夫定;AZT:齐多夫定;D4T:司他夫定;TDF:替诺福韦;ABC:阿巴卡韦
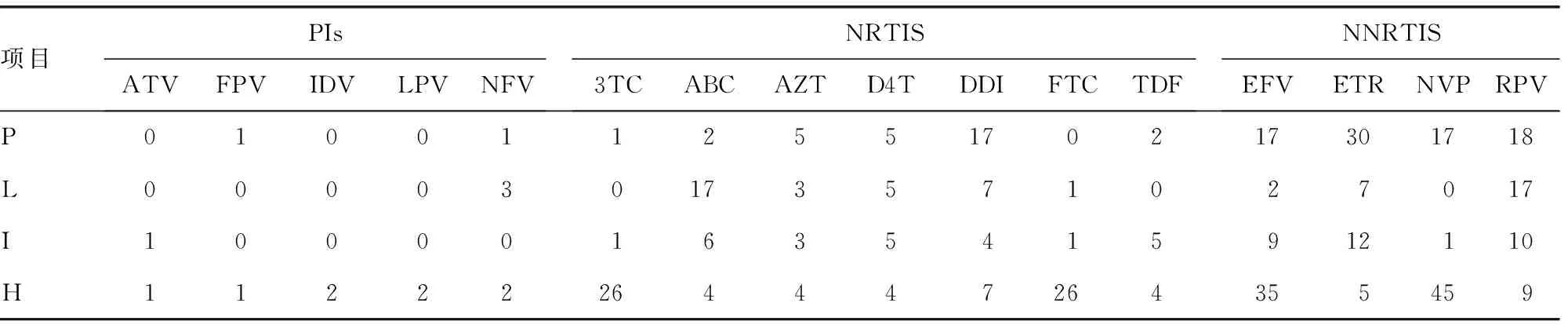
表2 3类药物的耐药数量及耐药水平
P:代表潜在耐药;L:低度耐药;I:代表中度耐药;H:高度耐药
2.4 基因型耐药突变位点情况
162例患者的检测结果中,与PIs相关的主要耐药基因突变位点有M46I、V82A、L76V、I84V和I54V各1例。与NRTIs相关的突变中,突变位点发生频率前3位的是M184V/I、T69N/D和K70R,分别为16.0%(26/162)、8.0%(13/162)和4.3%(7/162)。与NNRTIs的突变中,突变位点发生频率前3位的是K103N/E、V179D/E/T和V90I,分别为15.4%(25/162)、14.2%(23/162)和8.6%(14/162)。具体耐药位点情况见表3。
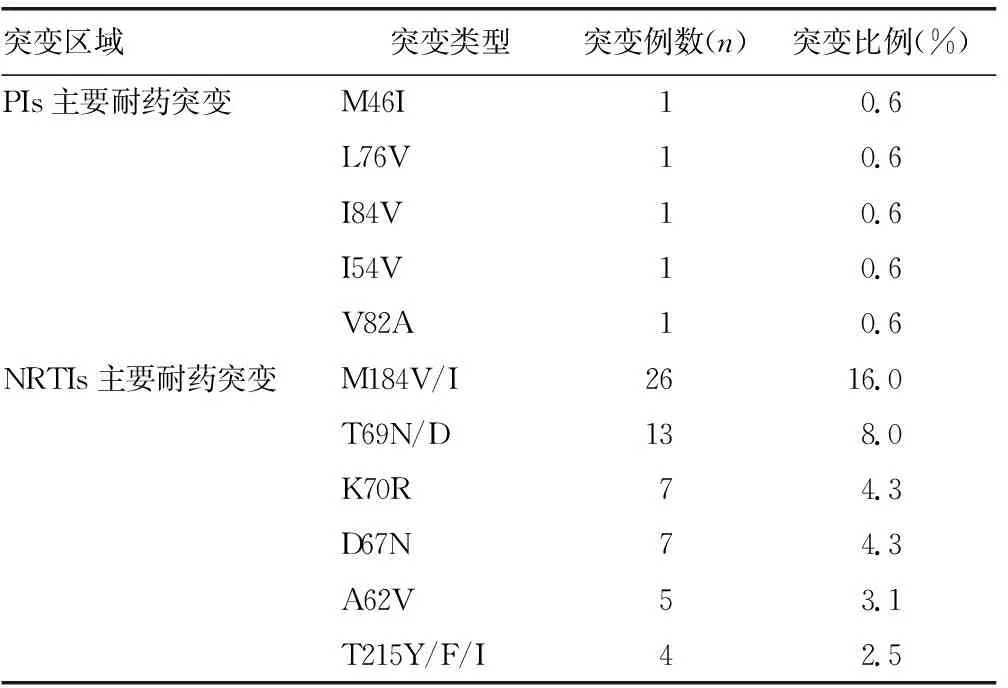
表3 常见耐药突变类型及比例
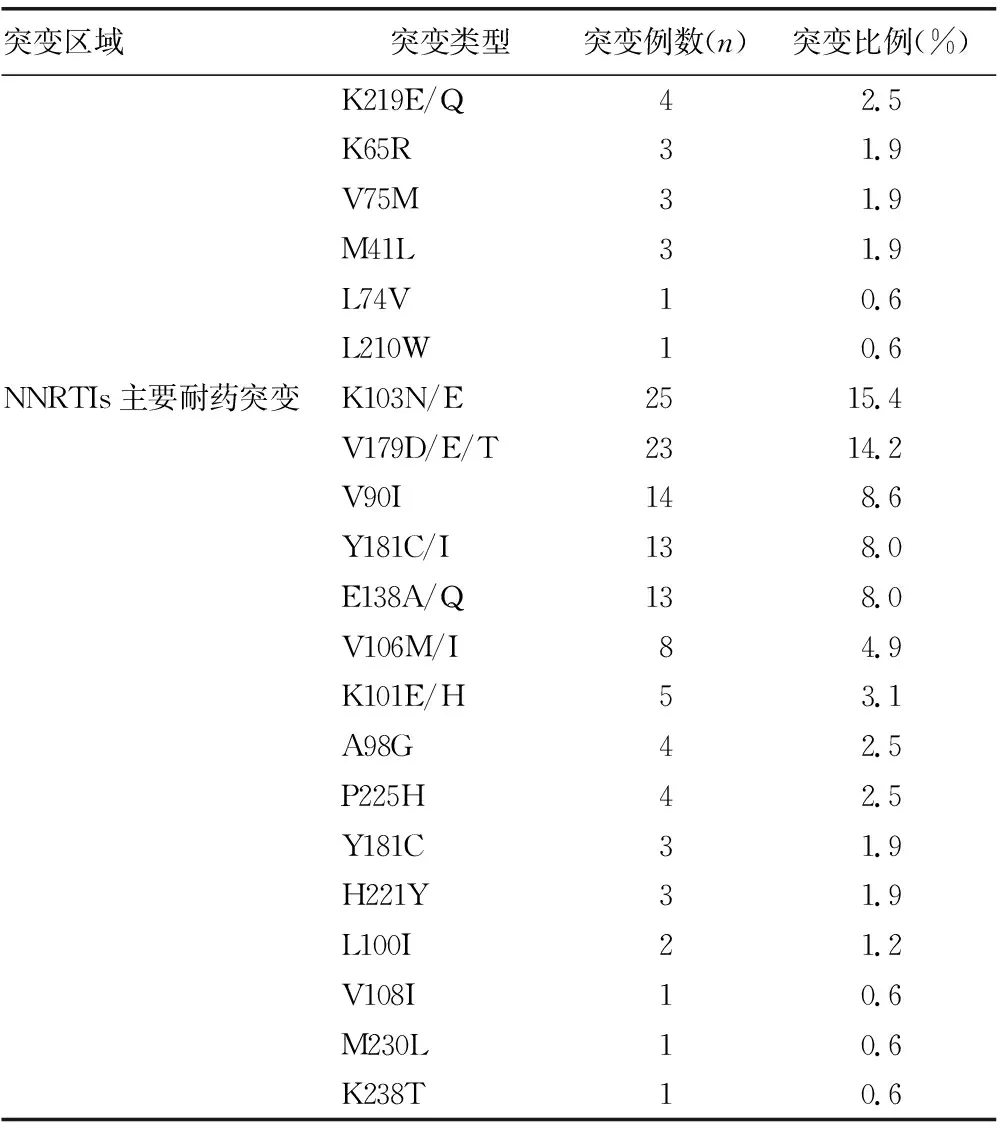
续表3 常见耐药突变类型及比例
2.5 基因型耐药突变位点情况
不同感染方式中的基因型分布见表4。

表4 不同感染方式中HIV-1基因型分布[n(%)]

表5 针对不同治疗方案耐药发生情况及耐药比例
2.6 不同抗病毒治疗方案耐药发生情况
对不同治疗方案的耐药情况见表5。
3 讨 论
为了有效控制AIDs疫情的蔓延,我国从2002年开始试行AIDs免费抗病毒治疗项目,自2003年起全面开展落实国家“四免一关怀”政策[2-3]。经过10多年来各级政府逐步落实AIDs患者免费抗病毒治疗的政策,建立起了免费AIDs抗病毒治疗的各级保障机制,符合治疗标准且接受抗病毒治疗的患者比例逐年增多。随着抗病毒治疗时间延长,治疗失败的患者逐年增多。对于治疗失败的患者,需要选择更换为二线治疗方案。在我国,主要的二线治疗方案为两种NRTIs加一种PI共同治疗[4]。目前国内免费使用的PIs主要是LPV/r,对于更换含LPV/r二线治疗方案治疗失败的患者,将面临无免费抗病毒药可用的情况。
HIV属于反转录病毒,病毒在复制过程中伴随着高度变异性。经过长时间的治疗,在抗病毒药物的选择压力下,HIV基因易发生突变而对多种药物的产生耐药[5]。在本研究中,65(40.1%)例对NRTIs、NNRTIs和PIs有不同程度耐药;其中对NRTIs和NNRTIs的耐药分别有34例(21.0%)和54例(33.3%),对PIs耐药5例(3.1%)。在已检出具有不同程度耐药的65例患者中,有3例(1.9%)出现对3类药同时耐药的患者;有28例(17.3%)的患者对NRTIs及NNRTIs两类药物同时出现耐药。云南省2012年所有治疗失败人群的耐药率为58.9%[1],2008-2012年所有治疗失败人群的耐药率为53.8%[6],本研究耐药率低于之前的研究。究其原因一方面是这些更换二线治疗方案的患者可能仅有少数是因为耐药更换治疗方案,还有一部分是因为免疫重建不良、药物不良反应及怀孕等原因更换,其患者对药物本身并不耐药。另一方面可能是由于PIs比NNRTIs有更高的耐药屏障,不易产生耐药。
在使用过的药物中,耐药率较高的几种药仍然是NVP、EFV、3TC、FTC,耐药率低于其他研究[1,6-7]。对PIs有5例患者出现耐药的情况,其中2例患者对LPV/r产生高水平耐药。本次研究中有3例患者对PIs、NRTIs和NNRTIs这3类药均出现耐药,这3例患者均是通过性传播方式感染的男性患者,出现多重耐药的原因可能跟性传播导致交叉感染有关。本研究中,PIs的主要突变位点M46I、I54V、L76V、I84V和V82A各出现1次。M46I为辅助突变,当与其他PIs突变同时出现时,可降低PIs敏感性;I54V与其他PIs突变同时出现时,会增加PIs的耐药性;V82A是PIs较常出现的耐药突变,通常在PIs治疗失败早期出现;I84V常出现在PIs持续治疗无效时,可使全部PIs的敏感性降低[8]。在本研究中与NRTIs和NNRTIs相关的耐药突变中,排名前3位的耐药突变分别是M184、T69、K70和K103、V179、V90,这与云南省杨绍敏等[6]的研究结果不一致。其主要原因一方面是云南省处于边境地区,人员流动性大,导致HIV毒株在不停地变化,重组毒株在不断增加,而耐药突变与HIV-1基因亚型相关[9],导致耐药位点也在不停地变化。另一方面是本次研究的患者都是先使用一线治疗方案后再改为含LPV/r的二线治疗方案,在不同的药物作用下,导致耐药位点发生改变。
在更换的二线治疗方案中,主要使用的是3TC+TDF+LPV/r和3TC+AZT+LPV/r两种治疗方案,两种方案的耐药率分别为35.5%(36/102)和21.4%(12/56),使用3TC+TDF+LPV/r的耐药率高于使用3TC+AZT+LPV/r方案的患者,其主要原因可能为TDF易出现胃肠道不良反应和肾毒性[10],从而影响药物的吸收有关。
随着抗病毒治疗时间的延长,因为一线药物耐药屏障低,同时不良反应大,在药物压力作用下治疗失败的患者会越来越多,未来会有更多的患者使用二线治疗方案,而我国目前可供免费使用的二线药物有限。因此,在治疗过程中应加强对患者依从性教育,同时加强监测检测,减少对二线药物耐药的产生,同时减少耐药毒株的传播,是以后抗病毒治疗的重点工作。

