响应面法优化类水滑石吸附F-条件
秦宝丽,许昶雯,2,王国英,刘吉明
(1.太原理工大学环境科学与工程系,太原 030024;2.滁州学院地理信息与旅游学院,安徽 滁州 239000)
在地表水和地下水中有大量的氟化物存在,氟是人体内必不可少的微量元素,饮用水中加入少量氟可以预防龋齿。但是在我国多数地区的地下水中,氟离子超标导致水体污染。长期饮用高氟水,轻者使牙齿产生斑釉,关节疼痛,重者会影响骨骼发育,致使丧失劳动力[1]。因此,采取有效方法去除水中氟离子已是当前关注的热点。
目前常用的去除水中氟离子的方法有:吸附法、电凝聚法、反渗透法、离子交换法、化学沉淀法和混凝沉降法等[2],其中类水滑石作为一种典型的阴离子吸附剂,制备方便,操作简单,吸附效果好[3],为了提高吸附效果,本文在之前课题组实验的基础上[4],利用Mg/Al/Fe类水滑石(MLT)吸附水中氟离子,通过响应面法优化MLT对氟离子的吸附条件。
响应面法(response surface methodology,RSM)是数学方法和统计方法结合的产物,是用来对所感兴趣的响应受多个变量影响的问题进行建模和分析的,其最终目的是优化该响应值[5]。如果有许多因子,首先需要进行Plackett-Burman试验设计实现筛选以剔除不重要的因子,然后利用二阶模型Box-Behnken实验设计逼近响应面值,最后确定最优点的位置。
1 实验部分
1.1 仪器与试剂
主要仪器:电子天平(FA1004型,上海舜宇恒平科学仪器有限公司),恒温磁力加热搅拌器(HJ-3型,天津滨海新区大港红杉实验设备厂),数显鼓风干燥箱(GZX-9076,上海市博迅实业有限公司),循环水真空泵(SHZ-Ⅲ型,上海知信实验仪器技术有限公司),马弗炉(SX2-4-10型,天津市中环实验电炉有限公司),恒温振荡器(THZ-C型,太仓市实验设备厂),氟离子选择电极(PF-1C型,上海越磁电子科技有限公司),pH计(pHS-3C型,上海市精密科学仪器有限公司)。
主要试剂:碳酸镁,硝酸铝,硝酸铁,氢氧化钠,碳酸钠,氟化钠,冰乙酸,氯化钠,环己二胺四乙酸,乙二胺四乙酸二钠,均为分析纯。
1.2 实验方法
根据课题组已有方法制备MLT[4],并去除水中F-,研究不同条件对F-去除率的影响。将MLT在不同温度下进行焙烧,取50 mL含F-浓度为10 mg/L溶液置于250 mL锥形瓶中,投加一定量的MLT,调节溶液pH,将瓶口用橡胶塞塞紧后置于恒温振荡器中在一定温度和转速下反应。反应结束后过滤,用氟离子选择电极法测定溶液中F-浓度,计算去除率Y。
去除率Y用式(1)计算:
(1)
式中:Ce为吸附平衡时溶液中剩余F-浓度,mg/L;C0为F-初始浓度,mg/L。
(1)Plackett-Burman实验设计。以F-去除率为响应值,利用Plackett-Burman试验对影响F-吸附去除率的5个因素进行研究,通过实验设计及方差分析筛选出对F-去除率有显著影响的因素。其中5个因素分别为焙烧温度(A)、MLT投加量(B)、反应时间(C)、pH(D)、反应温度(E)。实验设计水平如表1所示。
(2)Box-Behnken实验设计。根据Plackett-Burman试验的结果,对筛选出的因素进行Box-Behnken实验设计,通过方程拟合预测响应值及因素方差分析最终得出MLT去除F-的最佳吸附条件。
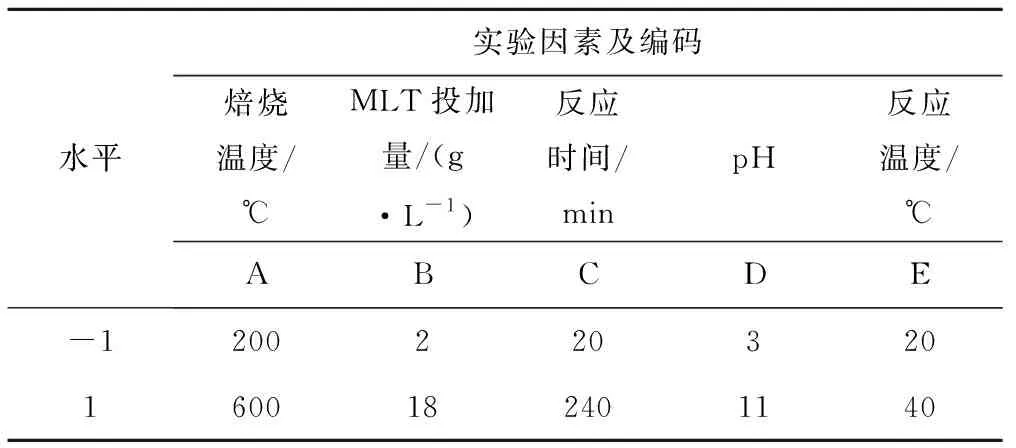
表1 Plackett-Burman 实验设计的因素与水平Tab.1 Factors and level of Plackett-Burman design
(3)分析方法。试样经0.45 μm的滤膜过滤后,F-浓度用氟离子选择电极法测定。
1.3 吸附动力学试验
动力学实验是将50 mL F-浓度为10 mg/L的溶液移入到250 mL的锥形瓶中,再加入MLT,放入20±1 ℃的恒温振荡器进行吸附,每隔一定时间测定滤液中残留的氟离子的浓度,从而得出不同时段的氟离子的吸附量。吸附剂对氟离子的吸附量qt用式(2)计算:
(2)
式中:qt为不同时间MLT对氟离子的吸附量,mg/g;Ct为不同时间溶液中残留的氟离子浓度,mg/L。
2 结果与讨论
2.1 Plackett-Burman实验结果
根据表2设计进行实验,3次试验取平均值,将实验结果去除率记录在表2中。
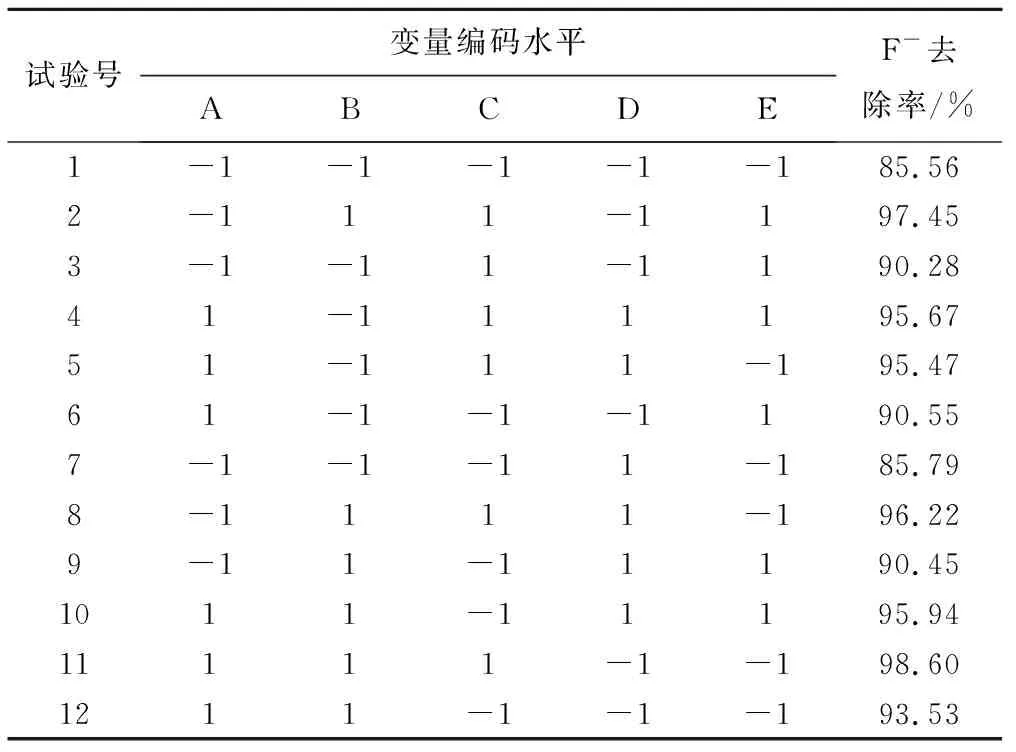
表2 Plackett-Burman实验设计结果Tab.2 Plackett-Burman design and experimental results
注:A~E分别表示焙烧温度(℃)、MLT投加量(g/L)、反应时间(min)、pH及反应温度(℃)。
预测F-去除率的Plackett-Burman实验方差分析结果如表3所示,该模型的P值为0.000 1,且回归模型的相关系数达到97.4%,表明利用该模型可以准确预测F-去除率。根据表3数据显示,可知焙烧温度、MLT投加量和反应时间对F-去除率有显著影响,pH和反应温度P值均大于0.05,对实验结果没有显著影响。原因是MLT经焙烧后层状结构消失,其焙烧产物拥有“记忆效应”,在水中和水中阴离子会重新构建原本结构,在此过程中会释放出一定量的OH-,增大了碱性,起到了缓冲作用,因此pH值影响不大[6];而反应温度只影响整个反应过程的吸附速率,对最终结果影响不大。因此,选择焙烧温度、MLT投加量和反应时间这3个因素为影响F-去除率的显著因素进行后续Box-Behnken实验。

表3 预测F-去除率的Plackett-Burman实验方差分析结果Tab.3 ANOVA of Plackett-Burman experimental for the prediction of F- removal efficiency
注:P<0.05为*,显著;P<0.01为**,非常显著;A~E含义同表2。
2.2 Box-Behnken实验结果
Box-Behnken实验设计的因素编码水平如表4所示,并根据表5进行三因素三水平实验设计,实验结果3次取平均,依次记录在表5中。

表4 Box-Behnken实验设计的因素与水平Tab.4 Factors and level of Box-Behnken design

表5 Box-Behnken 实验设计及结果Tab.5 Box-Behnken design and experimental results
2.2.1 方差分析
应用Design Expert软件对实验结果进行二次多项回归拟合后,编码方程模型如式(3)所示:
Y=92.66+1.97A+2.18B+3.69C-0.33AB+0.55AC-
0.085BC-2.17A2+1.66B2-0.48C2
(3)
对拟合方程进行方差分析,结果如表6所示。

表6 预测F-去除率的Box-Behnken实验模型方差分析Tab.6 ANOVA of Box-Behnken experimental model for the prediction of F- removal efficiency
注:P<0.05为*,显著;P<0.01为**,非常显著。
由表6可知,模型P值<0.01,表明该模型的回归方程非常显著;失拟值的P值为0.091 0>0.05,不显著,表明实验中误差不大;变异系数C.V.%为1.04%<10%,表明实验结果稳定性较好;模型的相关系数为0.970 1,校正系数为0.931 7,说明模型拟合效果好,可以利用本模型进行F-去除率的分析预测。
由表6可知,A、B、C、A2、B2对响应值有非常显著的影响,AB、AC、BC、C2对响应值影响不显著。通过比较三个影响因素的均方值可得到因素对F-去除率影响的显著关系:C>B>A。
2.2.2 因素交互影响
3D响应面图中,响应面越陡表明因素影响越大[7];等高线图中,图形越圆,表明因素的交互影响越不显著[8]。由图1所示,可看出F-去除率随MLT投加量和反应时间的增大而增大直至平衡;随着焙烧温度的增加F-去除率逐渐增大,之后呈下降趋势。出现上述情况的原因如下:随着MLT投加量的增大,吸附剂与F-的接触面积增大,更多的吸附位点被F-占用,导致F-去除率增大直至达到饱和状态;随着反应时间的增加,F-与吸附剂活性位点反应机会增多,因此去除率逐渐增大;随着焙烧温度的增加,焙烧水滑石的“记忆效应”越来越明显,F-在水中进入水滑石层间恢复层状结构而被去除,F-去除率增大,直至500℃左右达到顶峰,之后随着焙烧温度的增加,水滑石逐渐形成尖晶石而失去“记忆效应”[9],因此去除率呈下降趋势。
2.2.3 模型验证分析
经响应面分析,模型给出的最佳吸附条件如下:焙烧温度542.22 ℃,MLT投加量17.11 g/L,反应时间235.11 min,在此最佳条件下,模型预测的F-去除率为99.39%。为了验证模型的可行性,在最佳条件下进行实验,3次实验最终结果取平均得到F-去除率为99.25%,与预测的相差0.14%,表明模型可以较为准确地预测各因素对F-去除率,并具有一定的实用性。
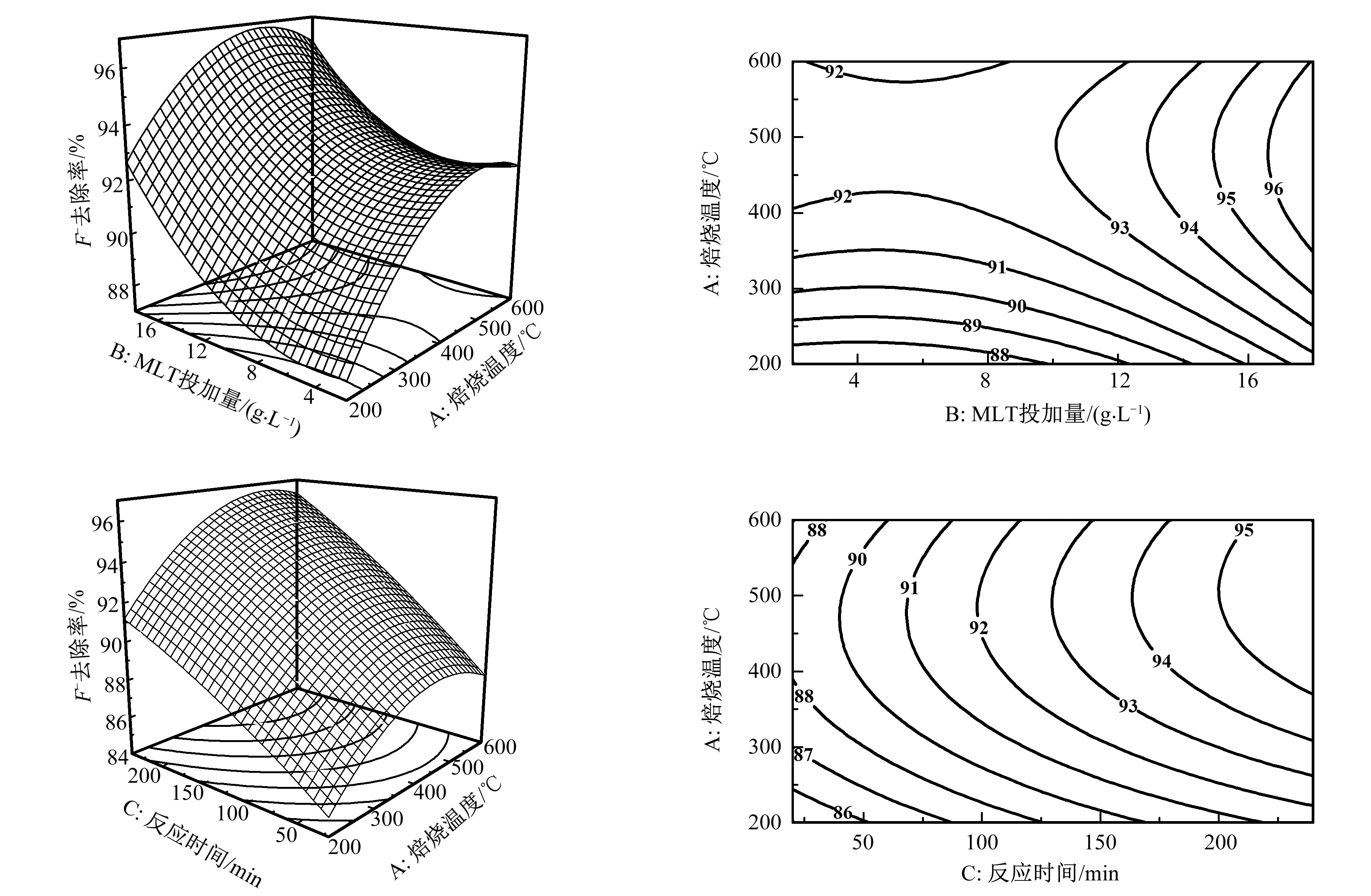

图1 不同因素交互影响的响应面分析Fig.1 Response surface analysis of interaction of different factors
2.2.4 MLT对原水中F-的去除效果
含高浓度氟离子天然水来自山西省闻喜县地下水,原水水质见表7。

表7 天然水水质指标Tab.7 Chemical composition and characteristics of the natural water samples
根据地下水水质标准(GB/T 14848-2017),原水中F-浓度远远超过地下水Ⅲ类标准值1.0 mg/L,为了验证实验的可实践性,在最佳条件下进行实验,3次实验最终结果取平均得到F-=0.31 mg/L≤1.0 mg/L,达到地下水水质Ⅲ类标准。
2.3 吸附动力学
吸附动力学可以反映吸附效率。常用的动力学模型为拟一级(4)[10]、拟二级(5)[11]和粒内扩散模型(6)[12]。
ln(qe-qt)=ln(qe)-k1t
(4)
式中:k1为吸附速率常数,min-1。
(5)
qt=KFt1/2+C
(6)
式中:k2为拟二级吸附速率常数,g/(mg·min);KF为粒内扩散速率常数,mg/(g·min0.5)。
动力学拟合氟离子模型见图2,动力学拟合参数见表9。可以看出相对于拟一级动力学,拟二级动力学拟合相关系数更高,RMSE值更低。k2值较低,表明反应速率很快。
不同温度下拟二级反应速率常数见表10。可以通过对活化能的计算确定吸附试验的吸附机理[13]。活化能计算可利用阿伦尼乌斯公式(Arrhenius equation)(7)求得:
k=Ae-Ea/RT
(7)

图2 吸附氟离子动力学Fig.2 Kinetics of fluoride adsorption on the MLT from
式中:k为拟二级反应速率常数,g/(mg·min);Ea为活化能,kJ/mol。
通过计算得到活化能为19.65 kJ/mol。活化能Ea值低于20 kJ/mol是内扩散控制过程[14],对应着快速脱氟阶段是由扩散控制,即由MLT吸附氟离子和MLT的反应为内扩散控制。

表9 MLT吸附氟离子动力学模型及参数Tab.9 Kinetic models for fluoride adsorption on MLT and the calculated constants
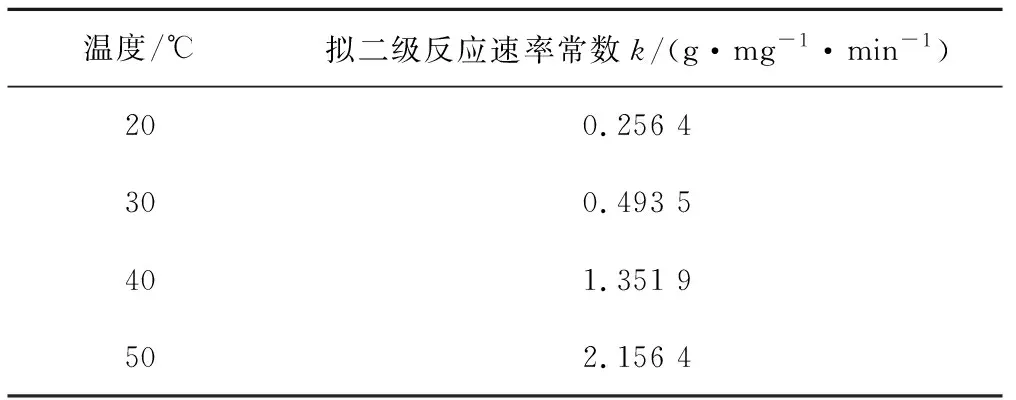
表10 不同温度下拟二级反应速率常数Tab.10 The k value under different temperature
3 结 语
(1)以F-去除率为响应值,利用Plackett-Burman试验对影响F-吸附去除率的5个因素进行研究,得出对F-去除率有显著影响的因素分别为焙烧温度、MLT投加量和反应时间。
(2)根据Plackett-Burman试验筛选出的因素进行Box-Behnken实验设计,通过方差分析,表明利用该模型能有效地预测MLT对F-去除率。其中,3个因素均对响应值有非常显著的影响,且三个影响因素对F-去除率影响的显著关系为反应时间>MLT投加量>焙烧温度。
(3)通过模型得出的最佳吸附条件如下:焙烧温度542.22 ℃,MLT投加量17.11 g/L,反应时间235.11 min,在此条件下F-去除率为99.39%,通过验证,实验值和预测值仅相差0.14%,表明该模型的实用性。
(4)经过实验验证MLT处理F-超标的原水,可使 F-浓度达到地下水水质标准,在实际中具有很大的实践意义。
(5)根据吸附动力学研究表明,MLT对F-的吸附满足拟二级动力学模型,该吸附反应非常迅速,且受内扩散控制的影响。
□

