15-脱氧-Δ12,14-前列腺素J2对大鼠酸性胃内容物吸入性肺损伤的保护作用
施劲东, 隆 玄, 符翠萍, 李建楠, 谢 娟, 施天昀, 梅周芳, 揭志军, 李善群*
1. 复旦大学附属上海市第五人民医院呼吸科,上海 2002402. 复旦大学附属中山医院呼吸与危重症医学科,上海 200032
吸入性肺损伤是危重病患者的常见并发症之一,可迅速进展为急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)。临床上常见的吸入性肺损伤主要由胃酸、食物颗粒等胃内容物反流误吸所致,目前尚缺少有效的治疗方法,导致其发病率和死亡率居高不下。胃酸及胃内颗粒物是胃内容物的主要成分,吸入后导致双相肺损伤,早期主要为由酸介导的化学损伤,后期主要为由炎症细胞、炎症因子介导的炎症级联反应[1-2]。因此,降低或阻断酸性胃内容物吸入性肺损伤时的炎症级联反应可能是提高该病抢救成功率的关键。
研究[3]表明,前列腺素类化合物15-脱氧-Δ12,14-前列腺素J2(15 -deoxy-Δ12,14-prostaglandin J2,15d-PGJ2)能抑制机体的炎症及氧化应激损伤。在内毒素和博来霉素诱导的ARDS和感染性休克动物模型中,15d-PGJ2能够通过激活过氧化物酶体增殖物激活受体-γ(peroxisome proliferator-activated receptor-γ,PPAR-γ)或抑制核转录因子-κB(NF-κB)、转录因子-1(AP-1)等途径,发挥肺保护作用[4-7]。本研通过建立酸性胃内容物所致大鼠肺损伤模型,进一步探讨15d-PGJ2能否减轻肺损伤程度。
1 材料与方法
1.1 实验动物 雄性SPF级Sprague-Dawley(SD)大鼠25只,体质量200~250 g,购自复旦大学上海医学院动物房。动物由复旦大学附属中山医院实验动物中心于SPF级条件下饲养,自由摄水、饮食。
1.2 酸性胃内容物悬液制备 酸性胃内容物颗粒悬液(combined acid and gastric particles,CAGP)的制备方法参照文献[8]:将用于提取胃内容物的5只SPF级雄性SD大鼠经腹腔注射20%乌拉坦麻醉(7.5 mL/kg),待大鼠安静后将其仰卧置于手术台板上,固定头部与四肢;腹部备皮消毒,切开腹部皮肤,暴露大鼠胃并用手术剪切开,收集胃内容物;用0.9%氯化钠液冲洗胃内容物3次,然后外科纱布过滤,以去除胃内大分子颗粒、胆盐等;过滤液在高压蒸汽下消毒灭菌25 min,以800×g在室温下离心2 min;弃去上清液,进一步去除胃内胆盐等物质,收集离心所得沉淀物,称重,用pH 为1.25的盐酸溶液(经0.2 μm无菌一次性针头滤器过滤)重悬,制成浓度为20 mg/mL的酸性胃内容物悬液。
1.3 吸入性肺损伤模型的建立及干预治疗 将20只SPF级雄性SD大鼠随机分为对照组和治疗组,每组10只。所有大鼠经腹腔注射10%水合氯醛按4 mL/kg进行麻醉,待大鼠安静后将其仰卧置于无菌手术台板上,固定头部与四肢,使台板倾斜30°。颈部备皮消毒,于中线做约8 mm小切口,分开筋膜后,游离甲状腺并用血管钳分开颈前肌,暴露气管。将14G静脉套管针插入气管至隆突上0.5~1 cm,拔出针心,套管针连接于1 mL注射器,向气管内缓慢滴注制备好的CAGP (1.5 mL/kg)。滴注后取下套管针,保持台板倾斜的同时轻轻转动大鼠,使注射的酸性胃内容物悬液均匀分布至大鼠双侧肺。滴注CAGP后即刻,治疗组腹腔注射15d-PGJ2(1 mg/kg),对照组腹腔注射相同体积的PBS。用缝线分别缝合气管与颈部切口,使大鼠正常呼吸,并在室温下自行苏醒。分别于滴注CAGP后4 h和12 h,每组各取5只大鼠终止实验,并采集标本。
1.4 标本采集和检测方法
1.4.1 血气分析 损伤后4 h和12 h,经腹腔注射20%乌拉坦麻醉大鼠。消毒后打开腹腔,将腹腔内肠管翻至一侧,暴露出腹主动脉。用事先肝素化的1 mL注射器抽取腹主动脉血0.5 mL后,立即用止血钳夹闭腹主动脉,以避免动脉血喷射。抽出的动脉血即刻用血气分析仪进行动脉血氧分压(arterial partial pressure of oxygen, PaO2)检测。
1.4.2 血清采集和肺湿重/干重比值(wet-to-dry weight ratios, W/D)测定 大鼠行血气分析后,剪开腹主动脉放血处死,采集腹腔内积血,分离血清冻存待检。放血后迅速打开胸腔,结扎右侧主支气管,取出右肺上叶,用吸水纸吸干其表面液体后,于电子天平秤上称其质量,记录为湿重。将称量好的右肺上叶置于60℃鼓风干燥箱内72 h以上,至其质量不再发生变化后,再次称重,记录为干重。计算前后两次的比,即W/D。
1.4.3 支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)的收集、蛋白测定、细胞计数 对大鼠左肺进行支气管肺泡灌洗。用16G插管针气管插管,用注射器取1.5 mL无菌冷PBS行支气管肺泡灌洗术3次。收集的BALF于4 ℃离心机250×g离心10 min,留取上清液于-20 ℃冻存。用BCA法(试剂盒购自碧云天公司)测定大鼠BALF上清液中总蛋白浓度,以观察大鼠肺泡内蛋白渗出情况。操作方法严格按照说明书进行。
细胞沉淀用0.5 mL PBS重悬,吸取20 μL用细胞计数板计数细胞总数。余悬液在TXT3细胞涂片上于离心机中250×g离心10 min,使细胞均匀平铺于载玻片上,晾干后,用瑞-姬氏染液进行快速染色,在高倍镜下计数200个细胞,进行中性粒细胞计数。
1.4.4 肺组织病理学检测 将大鼠左肺用4 % 多聚甲醛充盈,结扎左侧主支气管后放入4 ℃的4 % 多聚甲醛中固定,3 d后进行包埋、切片和苏木精-伊红(H-E)染色,在200倍视野下观察、拍照。由未参与实验的病理科医师分别在低倍和高倍视野下进行观察和炎症程度评分,参考文献[9-10]。
1.4.5 BALF和血清肿瘤坏死因子-α(tumor necrosis factor -α, TNF-α)浓度测定 采用ELISA法检测BALF上清液和血清中的TNF-α浓度,试剂盒购自上海森雄科技实业有限公司。
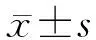
2 结 果
2.1 肺部H-E染色和PaO2结果(图1、表1)表明:与对照组相比,损伤后4 h和12 h,治疗组炎症程度明显下降,PaO2明显改善,差异均有统计学意义(P<0.05)。
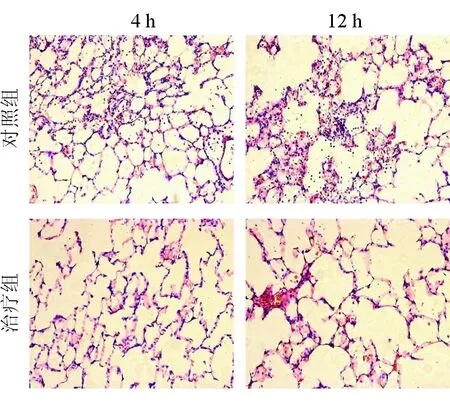
图1 两组大鼠肺组织H-E染色结果比较
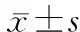
表1 两组大鼠炎症和肺功能相关指标比较n=5,
PaO2:动脉血氧分压;W/D:肺组织湿重/干重比值;BALF:支气管肺泡灌洗液;TNF-α:肿瘤坏死因子-α.*P<0.05与对照组同时间点相比
2.2 肺损伤程度 结果(表1)表明:损伤后4 h、12 h,治疗组肺部渗出(W/D)与蛋白渗漏(总蛋白)均较对照组减少,差异均有统计学意义(P<0.05)。
2.3 BALF中白细胞总数和中性粒细胞数 结果(表1)表明:损伤后4 h、12 h,治疗组BALF中白细胞总数和中性粒细胞数均较对照组减少,差异均有统计学意义(P<0.05)。
2.4 BALF和血清中TNF-α浓度 结果(表1)表明:损伤后4 h、12 h,治疗组BALF和血清中TNF-α浓度均较对照组下降,差异均有统计学意义(P<0.05)。
3 讨 论
胃内容物误吸是ARDS的主要病因之一。在年老体弱、酗酒、颅脑创伤、神经系统疾病、肿瘤等危重患者中,吸入性肺损伤发生率更高[11-12]。与其他因素所致的ARDS不同,酸性胃内容物吸入性肺损伤是一个双相过程:早期主要为酸液介导的化学性损伤,一般发生于损伤后3 h之内;后期为吸入的胃内容物引发由炎症细胞和炎症因子介导的炎症级联反应,此阶段的损伤程度更为剧烈,损伤后4~6 h达高峰,15 h后逐渐出现修复反应[13]。目前,临床对于酸性胃内容物吸入性肺损伤的治疗仅限于对症及支持治疗,如气管插管或气管镜下清除吸入物质、机械通气、抗生素治疗、糖皮质激素抗炎治疗等。然而,这些治疗方法均未能取得令人满意的效果。因此,寻找有效控制吸入性肺损伤的治疗方法成为了该领域的研究热点之一。
近年研究[14]表明,15d-PGJ2是组织炎症及氧化应激损伤时释放的内源性物质,对机体的炎症及氧化应激损伤起着重要的抑制作用。15d-PGJ2由前列腺素D2(prost aglandin D2, PGD2)自发脱水形成,是PPAR-γ的天然配体及强激动剂之一。Genovese等[6]在博来霉素诱导肺损伤小鼠模型中发现,给予PPAR-γ的两个激动剂,即罗格列酮和15d-PGJ2,能够减轻肺水肿,减轻炎症细胞浸润和肺部炎症程度,降低小鼠死亡率。Wang等[7]研究表明,在内毒素诱导的急性肺损伤小鼠模型中,PPAR-γ激活后能通过抑制高迁移率族蛋白B1(high mobility group box 1,HMGB1)-晚期糖基化终产物受体(receptor for advanced glycation endproducts,RAGE)水平发挥肺保护作用。因此,本研究在大鼠发生酸性胃内容物吸入性肺损伤后,给予外源性15d-PGJ2,观察其能否发挥抗炎、免疫调节及抗氧化应激的作用,从而产生肺保护作用。
本研究结果显示,大鼠发生吸入性肺损伤后,与对照组比较,治疗组损伤后4 h和12 h肺组织炎症评分、BALF中的白细胞总数和中性粒细胞数均下降(P<0.05),提示15d-PGJ2能减轻吸入性肺损伤大鼠肺部炎症;治疗组BALF中总蛋白减少、W/D比值下降(P<0.05),提示给予15d-PGJ2治疗能减少急性肺损伤过程中肺泡内富含蛋白液体的渗出,进而保护肺功能。Lu 等[5]的研究也发现,在内毒素诱发的急性肺损伤大鼠模型中,通过静脉注射15d-PGJ2能减轻肺部炎症和蛋白渗漏。 Zingarelli等[15]发现,15d-PGJ2能改善脓毒血症大鼠的血流动力学,降低其血浆TNF-α等细胞因子的浓度,减轻肺组织中性粒细胞浸润,并抑制肺组织中NF-κB和AP-1的活性。此外,本研究还发现,15d-PGJ2能降低BALF和血清中TNF-α的浓度,且能改善PaO2(P<0.05),纠正急性肺损伤所诱发的低氧血症。
综上所述,在酸性胃内容物吸入性肺损伤大鼠模型中,腹腔注射15d-PGJ2能减轻其肺部损伤和肺部炎症水平,改善PaO2。本研究的局限性在于:(1)未设置吸入0.9%氯化钠液的正常对照组,因此不利于评估15d-PGJ2是否对其他吸入性肺损伤发挥作用;(2)观察时间较短,难以明确15d-PGJ2治疗对大鼠预后的影响;(3)没有阐明15d-PGJ2通过PPAR-γ调控肺脏炎症的具体分子机制。今后将补充上述实验,进一步验证15d-PGJ2对肺损伤的保护作用。随着对急性肺损伤发病机制研究的不断深入,15d-PGJ2有望取代糖皮质激素成为吸入性肺损伤的有效治疗药物。

