从碳到氢能源:昨天、今天、明天
BASHIR Sajid,甄强,李榕,李翠霞,刘静波④†
①美国德克萨斯农工大学-金斯威尔校区, 金斯威尔, 德克萨斯州 78363-8202;②上海大学 纳米科学与技术研究中心/先进功能材料实验室,上海 200444;③兰州理工大学 材料科学与工程学院, 兰州 730050;④美国德克萨斯农工大学, 大学城, 德克萨斯州 77845
在近十年内,作为美国化学学会会议的主持人,我们注意到可再生能源日益受到重视并得到推广使用,以提高能源的有效利用并减少温室气体(COx、NOx和SOx)的排放。从热力学的观点来看,能量或熵是生命的核心,因此随着人口接近70亿,便携式设备达到68亿,人类对能源的需求必然成指数增加[1-5]。目前的化石燃料储量将不足以满足人类需求并最终枯竭,而氢气作为天然替代物,通过对现有设施进行改善,可以在降低费用的条件下被有效利用[6-10]。在氢气的使用过程中,除了被视为空气清洁剂的氢氧自由基外无副产品产生,从而可以避免对环境造成负担[11-15]。
根据哈伯特建模数据可知,美国的石油产量在1965—1970年达到峰值,之后下降。1860—1970年,近250亿桶的石油被提炼出来,用量加速[16-20]。页岩、焦油砂等新发现的能源也具有广阔应用前景,但碳排放问题依然无法根治[21-25]。目前的电力需求约为20 000 TW,预计到2030年将增加20 000 TW以上。目前约1/3的能源来源于石油,假设能源消耗量为12 000万t标准煤,则产生近7万t CO2,其中大部分资源是电力或热量,到2050年预计排放量增加到14万t。由于供能系统效率低下,约10 %的能源在传输过程中损失[26-30]。据美国能源信息署估计,煤炭、天然气储量将满足美国261年和原油储量满足其84年的需求,因此氢基燃料有望满足预期的电力需求。氢气和其他燃料的一些物理特性总结在表1中[31-35]。
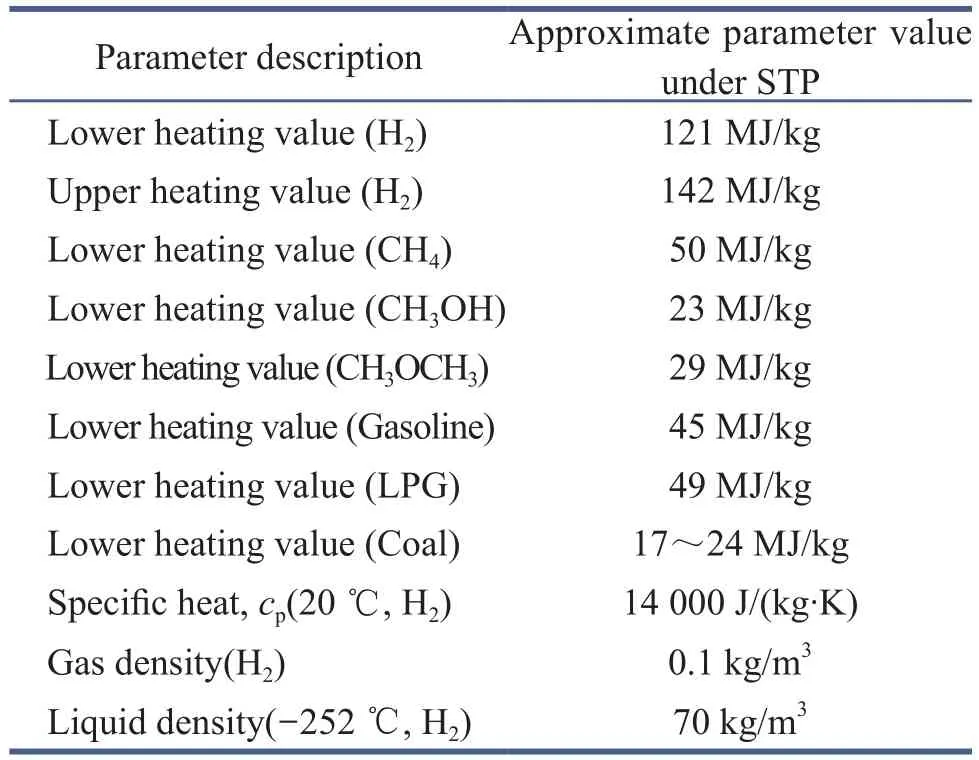
表1 主要能源性能一览表
表1表明,如果20 %的运输能源改用氢气或相关燃料(如生物甲醇、生物乙醇或生物柴油),温室气体的排放量将直接或间接减少。然而,氢气必须储存在高压、低温、微孔颗粒内,因此对产品的开发技术要求更高。下文将就产氢、储氢及使用氢三方面进行论述(图1)[36-40]。
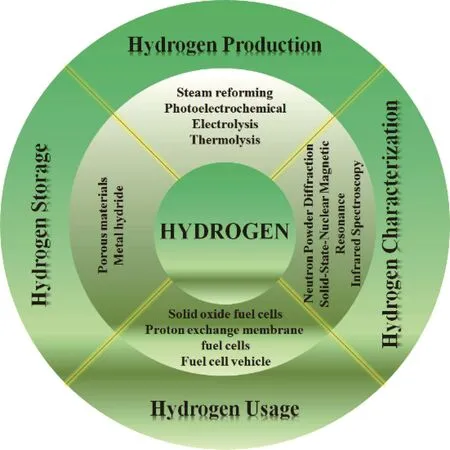
图1 氢气的产生、储存及使用
1 氢气的产生
1.1 蒸汽甲烷重整制氢
水蒸气甲烷重整是目前工业上较成熟且最简单、经济的制氢工艺(化学反应式见式(1)和式(2))。在生产氨水、甲醇以及其他化工产品过程中,所需要的氢即通过水蒸气重整制得。Ni/Al2O3是该工艺中最常用的催化剂之一,在它催化下甲烷转化率高达 90 %~92 % ,但是催化剂表面容易出现碳沉积,因此需要加入助剂来抑制[41-45]。

式(2)中产生的二氧化碳可以通过加压降温过程(>5.1 atm,216.15 K)在三相点附近将其以液态方式分离出来,并进一步储存在深海或湖中(>3 000 m)。该过程每生产1 kg H2将附加产生14 kg CO2。甲烷水蒸气重制氢气产生的CO2是传统煤气化制氢气产生的CO2量的一半。研究结果表明,纳米催化剂的加入可提高氢气产量。图2为蒸汽甲烷重整制氢示意图[46-50]。
1.2 甲烷热解制氢
天然气中的甲烷热解制备氢气并无CO2产生,反应方程式如式(3):
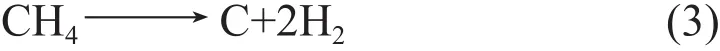
由于C—H键能约为440 kJ/mol,1 000 °C 下ΔH°≈75 kJ/mol。此方法焓变约为40 kJ/mol,而蒸汽重整制氢的焓变接近65 kJ/mol。
通过加入非均相金属催化剂可以降低甲烷热解制氢的反应温度。常用的催化剂有金属镍、铁、第五周期过渡金属,以及碳纳米管、线或无定形碳。由于天然气含硫,金属催化剂易中毒失活。碳基催化剂即使失活,也会由于水蒸气和CO2的存在而再生,因此被广泛应用于工业化甲烷热解制氢[51-55]。
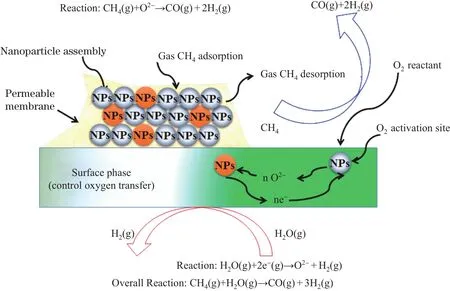
图2 蒸汽甲烷重整制氢示意图
1.3 光催化水解制氢
迄今为止,太阳能被视为最经济、最充足的可再生资源。然而,鉴于太阳光照的间歇性,将其作为主要能源必须进行转换和储存。以化学键的形式存储太阳能是有效可行的方法,即通过太阳能光解水制备氢气和氧气。该反应在热力学上为非自发的吸热过程,因此必须加入催化剂有效降低活化能,来提高反应速率。研究表明,对金属氧化物进行改性并调节能带宽度,可大幅度改善光解水的效率(图3)[56-60]。
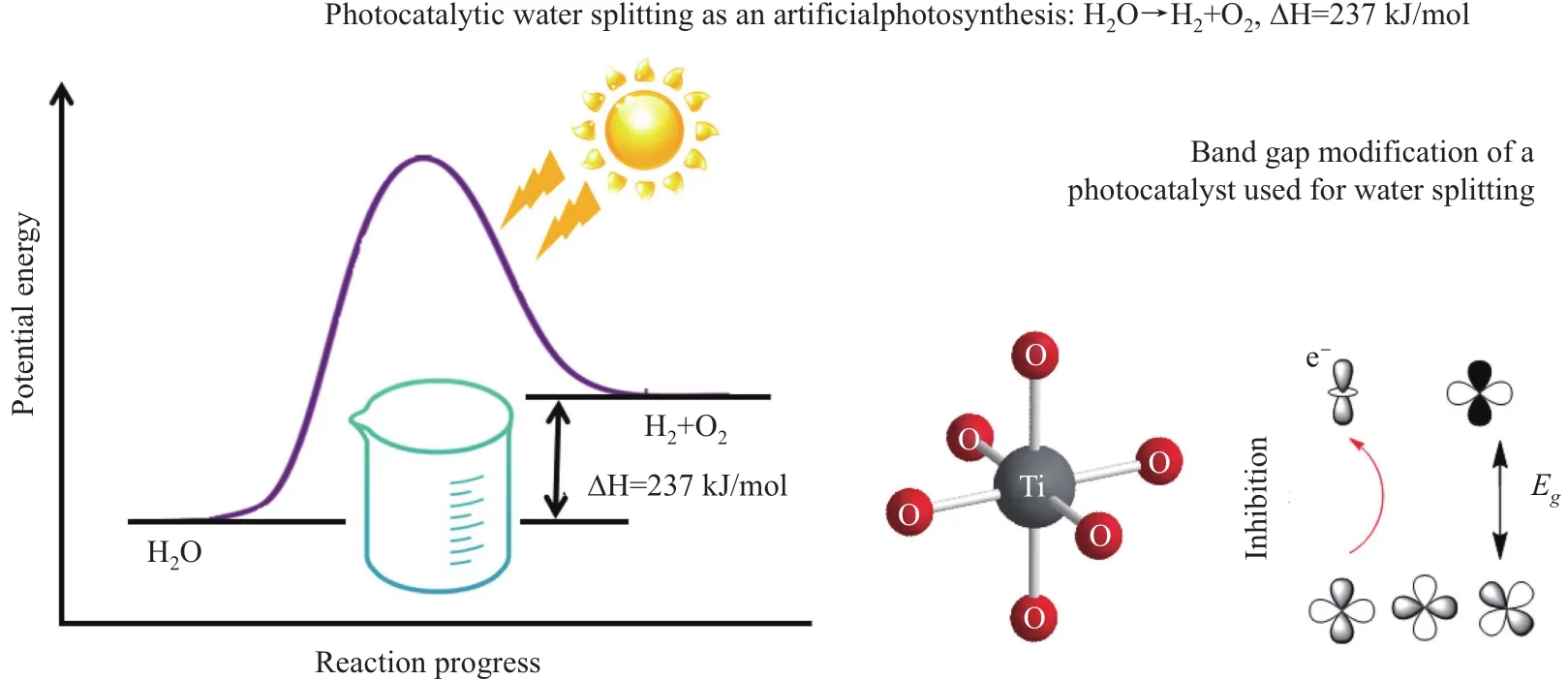
图3 光催化水解制氢示意图
1.4 电解水制氢
在阳极水被氧化产生氧气,其标准还原电位E°=0.82 V,反应式如下:
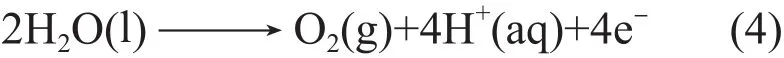
在阴极,水被还原产生氢气,其标准还原电位E°=-0.41 V,反应式如下:
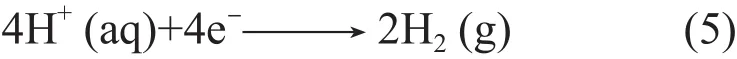
根据上述氧化还原反应可以得出,4 mol电子将产生2 mol H2和1 mol O2。也就是说,每库仑电量约产生5 µmol H2和2.5 µmol O2。若按60 %的效率计算,产生1 m3H2实际电能消耗约为5 kWh(图4)。 电解水所需电压可按能斯特方程进行计算:
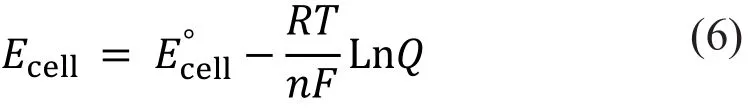
其中Ecell代表蓄电池电位;代表蓄电池标准电位;R代表理想气体常数(8.314 J•mol-1•K-1);F为法拉第常数(96 485 C•mol-1);n为氧化还原反应过程中电子转移数;Q为化学熵,视氧化还原反应进程而定,为无量纲的自然数,和温度、气体浓度及分压有关[61-65]。
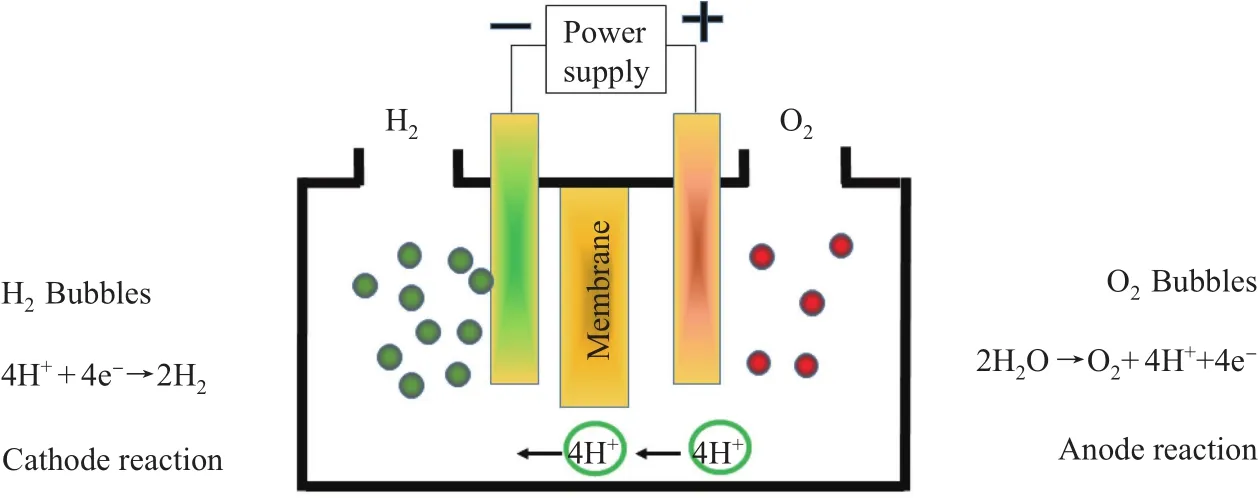
图4 电解水制氢示意图
1.5 微生物酶催化制氢
生物质制氢不但减少二氧化碳的排放,而且可以使用可持续的生物质材料。特别是将农作物副产品的生物能转化为氢气,可增加农产品的使用价值。但是,其操作成本很高、腐蚀性强、氢气产率低等缺点限制了生物质制氢的推广应用。通过氢化酶催化藻类和蓝菌,在光照条件下将水转化为氢气,主要的氧化还原反应如下[66-70]:

在乏氧条件下,糖类可以被转化为酸类,进而产生氢气,化学反应式如下:

图5为微生物酶催化制氢示意图。微生物酶(藻类和蓝菌)能够催化糖类等生物质产生氢气,其催化过程是通过将电子转移给还原态的铁氧还蛋白,然后在氢化酶的作用下被重新氧化成氧化态的铁氧还蛋白。生物质光能转化为化学能储存在三磷酸腺苷中。在氢化酶的作用下,氧化还原反应传输4个电子,通过生物光解产生氢气及二磷酸腺苷(ADP)。另外,氢化酶生物光解也可以在厌氧发酵的情况下发生,将有机产物转化为氢气[71-75]。
2 氢气的储存
氢气的质量能量密度(120 MJ/kg)约为汽油(44 MJ/kg)的3倍,但液氢的体积能量密度(8 MJ/L)远小于汽油的密度(32 MJ/L)。如表1所示,氢气必须储存在高压、低温或微孔颗粒内。储氢容量为5~13 kg可以满足轻型车辆的行驶。美国能源部的初始目标是质量分数为11 % 的氢气的续航里程达到400 km。为了满足短期和长期的储氢目标,美国能源部制定相应的储氢路线。根据上述的储氢蓝图,常见的储氢办法(如化学法、物理法等)总结如图6[76-80]。

图5 微生物酶催化制氢示意图
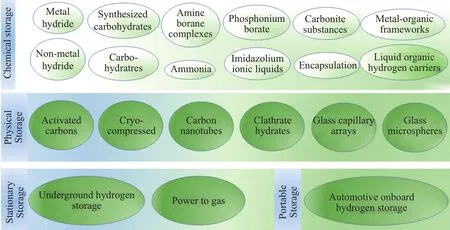
图6 常见的储氢办法
3 氢气的使用
氢气在石油炼制、清洁能源、玻璃净化、半导体制造、航空航天、肥料生产等领域得到广泛应用。作为汽油替代品,氢气将成为重要的能源载体,为终端用户提供能源需求,特别是为交通运输提供燃料。但是,氢燃料电池汽车(FCV)目前正处于开发前期生产阶段,氢燃料的基础设施尚不完善。美国能源部氢能和燃料电池项目也处于研发阶段。刘静波课题组近年来集中研发由氢气燃料电池驱动的模型车(图7),以改进其续航能力。研发的关键点为:①研制系列纳米催化剂取代铂,以减少贵金属的用量及中毒;②组装燃料电池器件,为模型车提供电力来源;③利用光催化进行水的电解,实现区域化供氢。研究结果表明,与传统催化剂相比,课题组研制的纳米结构使得燃料电池的功率密度提高了一个数量级,模型车辆的行驶速度提高了32.4 %,行驶距离增加了47.6 %,水解速度提高了61.2 %。数据还表明,使用非铂(Pt)系材料可以防止催化剂降解以延长其使用寿命。通过光催化水解,体系能够在很大程度上实现燃料的自我循环供应,降低能耗。由于燃料电池无碳排放的忧虑,提升了模型车的性能,为绿色能源汽车的实现提供了科学依据。

图7 氢气的产生及燃料电池驱动的模型车
4 总结
18世纪以来由于重工业的快速发展,大量污染物排放到环境中,造成严重污染并影响人类健康。2016年55个温室气体排放国签署“巴黎协议”,以期降低温室气体的排放,将气温升幅控制在1.5 ℃以内,因此,对无碳能源的开发尤其重要。从碳燃料过渡到氢能源,需要实现技术突破以应对预期的能源需求。《联合国气候变化框架公约》指出,氢能源驱动的汽车预计将在2050—2100年得到大幅度开发,以减少CO2的排放。
致谢作者一并感谢上海大学“高端外专”项目以及中国国家留学基金委(201608625038)、德克萨斯农工大学-金斯威尔校区的资助。
(2018年7月6日收稿)■

