铂基金属-氧化物纳米催化剂研究进展
李榜全,卢玉和,陈爱军
(山西大同大学物理与电子科学学院,山西大同037009)
随着煤、石油、天然气等非再生能源日渐枯竭,清洁能源和可再生能源材料在解决能源短缺和环境污染问题方面具有很大的应用前景。在世界范围内,纳米科学和纳米技术在清洁能源技术方面已取得了迅速进展,这对能源产生和储存有着深远影响。由于纳米材料具有不寻常的催化、磁学、电学和光学性质,近年来引起了极大的关注,利用先进纳米技术和纳米材料作为解决能源问题与环境挑战的有效途径。因此,在过去的几十年,纳米技术的研究与发展是热门的研究领域之一。
用氢或有机小分子供给的燃料电池在交通运输和能源方面显示出巨大的发展前景,它具有高能量转换效率、可持续的燃料来源和低的有害气体排放的特点[1-2]。直接乙醇燃料电池(DEFC)具有无毒,低成本和易操作等优点,被认为是最有前景的能源之一。相对于氢气和甲醇,乙醇作为一种常见的液体燃料,易被控制、储存和运输,具有高能量密度(8 kWh∙kg-1,6.32 kWh∙L-1)和较低的毒性。在技术上,它的生产来源广泛,可以是各种农产品,既方便又经济[3]。在实际应用中,乙醇氧化反应在电解质-电极界面上的反应非常复杂,Pt基催化剂材料在乙醇氧化反应中广泛使用,近年来关于其制备和性质改进吸引了大量的研究和关注。乙醇是含有C-C、C-H、C-O和O-H键的简单分子,这些键的选择性断裂决定了反应途径和最终产物。例如,通过C-C键-裂解途径的EOR,乙醇的完全氧化产生CO2,同时产生12电子转移,而C-H、O-H或CO键的裂解导致乙醇不完全氧化而生成乙醛的(2e转移)或者乙酸(4e转移)[4]。在这些路线,乙醇完全氧化为CO2是首选,因为它提供了最高的法拉第效率。但在负载纯Pt催化剂的阳极中,电流密度过低,电荷主要从不完全氧化反应产生(通常为90%)[5]。在纯Pt表面上动力学缓慢;中间体的碳(如CO、CHX等)的产生,即使少量,也会严重阻碍Pt催化剂的活性位点,阻碍乙醇的解离吸附。探究铂基纳米材料的可控制备方法,形成机制及其物理化学性质,有助于理解材料的结构-性能关系,获得具有优异性能的铂基纳米材料,对于促进相关技术的实际应用具有重要的意义。
1 Pt及Pt合金催化剂
不同晶面结构、尺寸的催化剂在乙醇燃料电池中的催化效果有很大不同,在不使用有机添加剂的情况下,直接在碳载体上制备具有(100)择优取向的立方Pt纳米粒子,与负载型多晶铂纳米颗粒相比,碳为DEFC提供了优异的功率密度和CO2选择性[6]。采用恒电位法,直接在碳布上电沉积制备多孔Pt纳米材料在DEFC的乙醇氧化反应中表现出催化性能随着温度的升高而提高,与商业化Pt样品相比,多孔样品在表现出更好催化性能[7]。采用化学气相沉积法在多壁碳纳米管(MWCNTs)上沉积铂胶体纳米颗粒,极化曲线结果显示Pt/MWCNTs比商业Pt/C更高的电活性[8]。
纯Pt吸附在C等表面,可以作为直接乙醇燃料电池的催化剂。乙醇氧化反应活性和Pt颗粒以及Pt的多孔性等有关。但是单纯Pt并不是理想催化材料,由于Pt吸附CO导致Pt中毒,降低Pt的反应活性。通过合金化方法,既可以降低贵金属Pt的用量,也可以提高催化剂的活性,例如Sn、Ru、Pd、Ir、Co、Ni等金属,可以增强反应活性。在Pt表面的金属的Sn可以让CO氧化成CO2更容易进行[9];金属Ru可以有效解决Pt中毒问题,并且两者结合后使C-C键的断裂所需电势更小,并且Ru可以有效修复中毒的Pt-CO,重新活化Pt[10]。PtCo[11]和Ni及其化合物已被证明能显著促进Pt催化剂在CO氧化和甲醇氧化反应中的催化活性。近年来,发现八面体Pt-Ni/C合金催化剂比Pt-Ni/C和Pt/C显示出更高EOR电流密度[12]。如图1所示,相比于Pt-Sn催化剂,Mo的加入更增强了乙醇氧化反应的活性[13]。若仅仅将Pt和金属Sn以一定比例混合作为催化剂时,主要产物是醋酸,并没有有效地断裂C-C键,因此第三种过渡金属元素Rh的加入,可以有效增强C—C键的断裂,从而提高了CO2的选择性[14]。
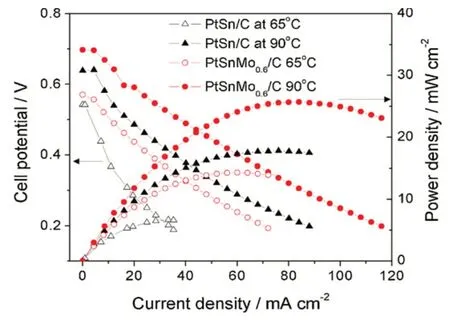
图1 PtSn/C和PtSnMo0.6/C的DEFC性能比较
2 Pt-氧化物催化剂
除了Pt以外的金属,例如锡,在反应中以氧化物的形式存在,在反应动力学方面,Pt(111)-SnOx[15]、Pt-SnO2[16-17],Pt与金属氧化物结合产生协同效应,氧化物在其中可以通过双功能机制降低Pt吸收CO并将其氧化所需要的电势,可以提高乙醇氧化反应活性以及电荷转移率。Ni@NiO/Pt催化剂:以金属Ni的导电核心表面作为支撑,Pt分布在NiO分布的细孔中,形成一维均匀纳米结构,合适的纳米结构间距有利于乙醇的吸附解吸,从而加快反应速率。乙醇氧化反应电化学活性的增强是因为在一维金属Ni外Pt和NiO壳两者结合的协同作用。Pt-TiO2含Pt和Ti的催化剂在不同的原子配比下显示出Pt-TiO2(2:1)/C具有较高的ORR活性。以Pt-TiO2(2:1)/C为阴极催化剂的DEFC比以Pt/C为阴极催化剂的DEFC具有更好的性能[18]。花状CeO2的Pt-CeO2/C催化剂的催化性能,稳定性和抗中毒能力比传统的Pt/C更优秀。随着碳球载体粒径的减小,催化剂的催化性能,稳定性及抗中毒能力随之增强[19]。Pt/C-In2O3的催化性能比Pt/C高,这表明In2O3的积极参与显著提高了Pt/C在乙醇氧化过程中的催化活性。因此,在直接乙醇燃料电池中,用PBI膜组装的In2O3负载Pt/C可作为乙醇高温氧化的有效复合电催化剂[20]。
如图2所示,低倍和高倍放大TEM图显示具有连接的砌块多孔纳米多晶结构,NiOx物种与相互连接的Pt纳米晶体均匀混合。通过构建Pt-NiOx[21]的3D模型多孔纳米结构,是由互连的Pt纳米晶体和无定形NiOx物种组成,Pt-NiOx/C在0.45 V(vs.SCE)下具有比Pt/C催化剂高得多的电流和更好的稳定性,表面氧化物显著提高了Pt基纳米材料的电催化活性,构建的3D多孔结构将使催化剂具有良好的稳定性。
3 Pt基金属-氧化物催化剂
PtRhOx-SnO2[22-23]结构被发现能有效提高C-C裂解率,并能提高氧化电流密度。相对Pt/SnO2/C电极,Pt/Rh/SnO2电极的活性更高,并且氧化电流密度衰减更慢,具有高的耐久性。与Pt、Rh和氧组分的特定排列有关的协同效应对乙醇的C-C裂解起重要作用。共存的金属和氧化的Pt和Rh可能对C-C裂解具有特殊作用,金属和氧化Pt和Rh在表面的共存有助于CO2的形成,而金属相通过C-C裂解提供了大量可用的乙醇解离吸附位点,氧化Pt和Rh相提供了用于氧化反应的可移动的O原子。
如图3所示,在PtSn-SnO2催化剂中,由于Pt-Sn合金协同效应,减弱O的化学吸附,以及SnO2使附着在Pt上类似于CO有毒物种转化为CO2,乙醇氧化反应活性的提高主要是得益其有效解决CO中毒问题[24]。

图3 Pt-Pt-Sn/SnO2循环伏安曲线图
Pt-Ir-SnO2/C三元催化剂用于乙醇氧化时,Pt可以吸附乙醇分子到催化剂表面,并解离出氢,Ir辅助Pt催化裂解乙醇的C-C键,SnO2在较低的电位下解离水分子,提供OH基团,使乙醇氧化的中间产物进一步氧化,Ir和Sn的协同作用可以降低Pt-Ir-SnO2催化剂对乙醇氧化反应的活化能,有效地提高乙醇电催化活性[25]。由于氢的溢出效应、耐酸性和金属催化剂电子作用,与贵金属可以可以作为催化剂的负载,Pt-Sn-SiO2复合催化剂中,SiO2嵌入纳米纤维(SECNF)增加其导电性,分别将SECNF和纳米纤维(CNF)作为负载时,Pt3Sn1/SECNF对乙醇电氧化的活性是Pt3Sn1/CNF的1.3倍,是商业Pt/C的3.7倍。Pt3Sn1/SECNF最大功率密度是商业Pt/C的3.5倍。Pt3Sn1/SECNF的高活性可能与Pt-Sn-SiO2的氢溢出、Sn的OH供给和配体效应等相互作用有关。这种作用能促进乙醇的电氧化[26]。电化学测试实验表明,PtSnRh/CSb2O5·SnO2(90:05:05)和PtSnRh/C-Sb2O5·SnO2(70:25:05)电催化剂 比PtSnRh/C电催化剂具有更高的乙醇氧化性能,PtSnRh/C-Sb2O5·SnO2电催化剂的高催化活性可归因于催化剂组分(金属Pt和Rh、SnO2和Sb2O5·SnO2)之间的协同作用,其中SnO2或Sb2O5·SnO2强烈吸附水,阻止Pt和Rh位点发生反应。H2O形成M-OH,使Pt和Rh位点可用于乙醇电氧化[27]。
4 结论与展望
直接乙醇燃料电池利用液态乙醇电氧化发电的技术,具有广泛的应用前景。研究乙醇氧化过程,主要解决如何提高铂基纳米材料催化活性并减少铂的用量,进而降低催化剂成本的问题。许多研究通过构建三维互连结构,避免超小纳米粒子聚集。催化剂表面的氧化物种起着至关重要的作用,金属氧化物在比较低的电势下活化水分子产生羟基自由基,羟基自由基再和CO结合避免Pt中毒;在反应热力学方面,可以增强电催化稳定性,通过元素间的协同效应,提高催化性能。因此,氧化物的加入大大提高乙醇燃料电池氧化生成CO2的效率。发展多元Pt纳米催化剂将提高催化剂的催化活性和稳定性,最终提高DEFC的性能效率。

