提速中的中国药品审评审批—药审中心化药各审评序列排队时长分析
文/李天泉 曾亚 曹洁
2015年8月18日在国务院新闻办新闻发布厅举行新闻发布会上,国家食品药品监督管理部门相关负责人在介绍药品医疗器械审评审批制度改革的有关情况中提到,到2015年止,我国出现过三次药品审评积压的高峰:2005年积压达17 000件;2007、2008年第二次高峰积压达27 000件,2008年采取集中审评,解决了审评的积压问题;2011年以后,又出现新的积压,2015年8月积压数量为21 000件。根据相关数据统计,从2011起,药品审评中心(以下简称CDE)每年承办新的药品申请(以受理号计)突破了7000个,2014、2015年连续两年均在8000件以上。
超负荷的审评工作量导致我国药品审评完成的速度和程度大打折扣,最为严重的结果即审评排队时间过长。同时,每年化药的申报量占总数的85%以上,审评积压的现象集中体现于化药,因此本文选取化药审评排队时长作为分析重点,反映提速中的中国药品审评审批情况。
本文分析图表分为箱形图和折线图,其中箱形图六个数据节点的解释如下:
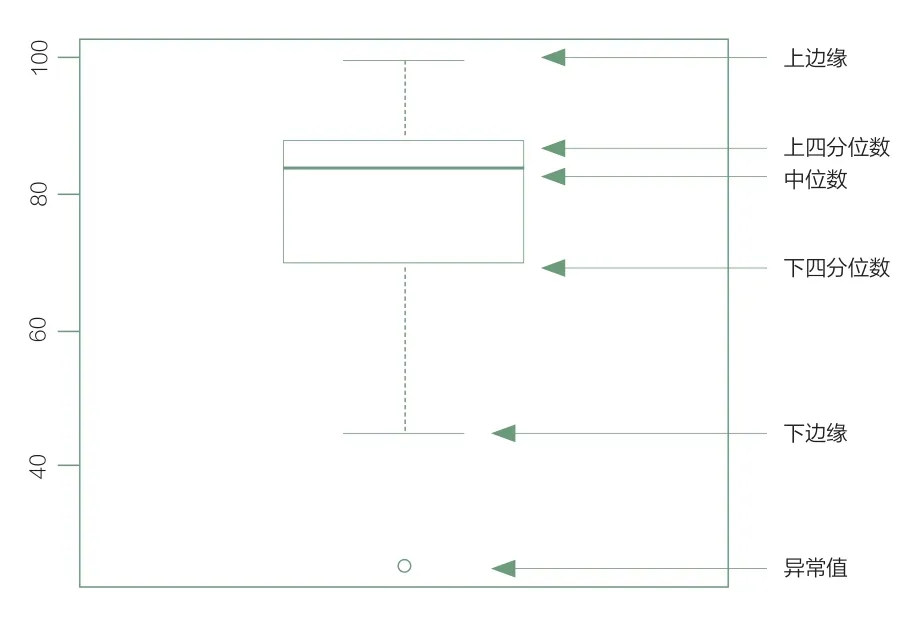
根据CDE网站新报任务公示—化药审评序列公示中,化药审评任务分类共分为6类:新药临床试验申报(IND)、新药上市申请(NDA)、简略新药申请(ANDA)、验证性临床、补充申请(包含临床补充申请和药学补充申请)、进口再注册,以下将根据相关数据库所采集的从2013年1月~2017年9月的历史数据对这6类的排队时长做详细分析。排队时长表示从进入CDE到审评启动之间的时长,我们选取中位数作为折线图分析数据。
1.化药IND审评序列排队时长分析
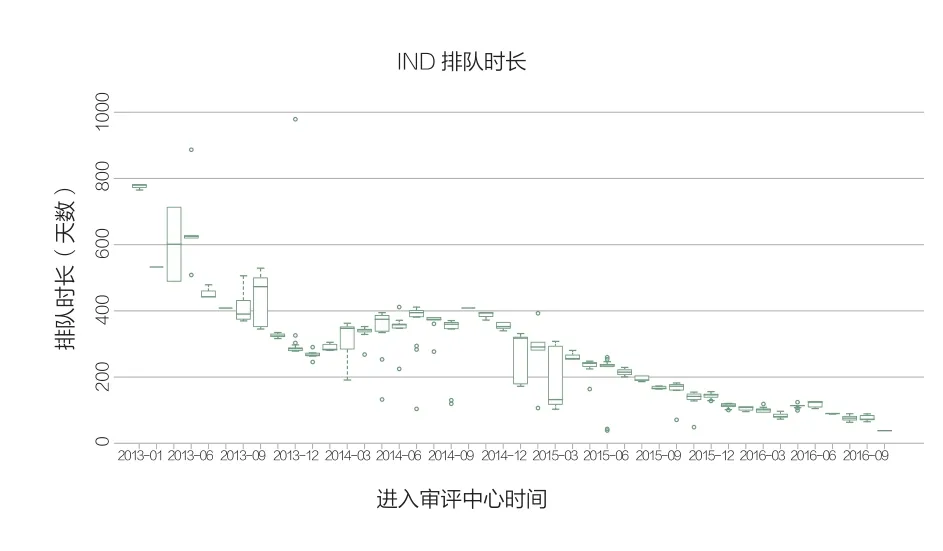
从箱型图中可知,横轴表示进入CDE时间,即通常所说的承办日期,纵轴为排队时长(按天计),整体来说,同一时间进入IND审评序列的药品排队时间差异不大,排队时长也逐渐呈现下降趋势,且相比其他审评序列,IND序列排队时长相对较短,受审评积压影响程度比较小。
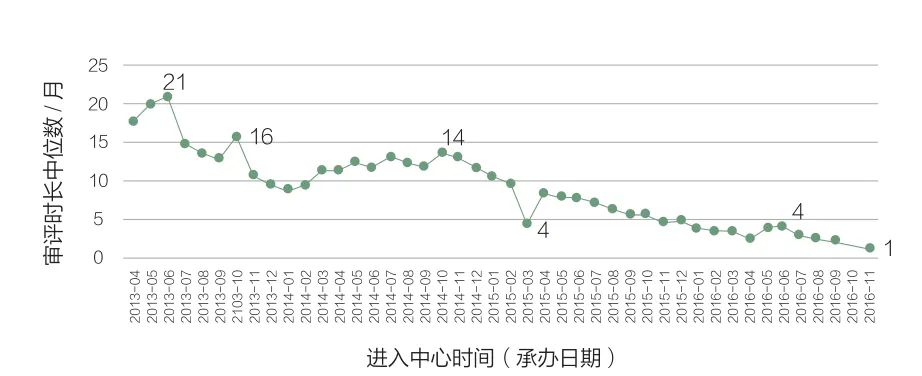
图1 IND审评序列排队时长(月)
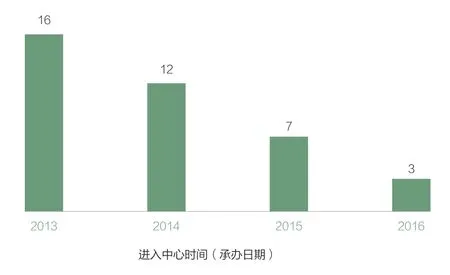
图2 2013~2016年IND审评序列平均排队时长(月)
从中位数图图1分析,IND审评序列2013年6月出现年最大值,平均排队时长达21个月,2014年初至2015年初,又出现一个小高峰,从2015年4月之后保持平稳下降趋势,到2016年11月出现排队时长仅1个月的情况。从图2更能清晰可见,从2013年起平均排队时长下降非常明显, 2016年平均排队时长仅为2013年的18.75%。
2.化药NDA审评序列排队时长分析
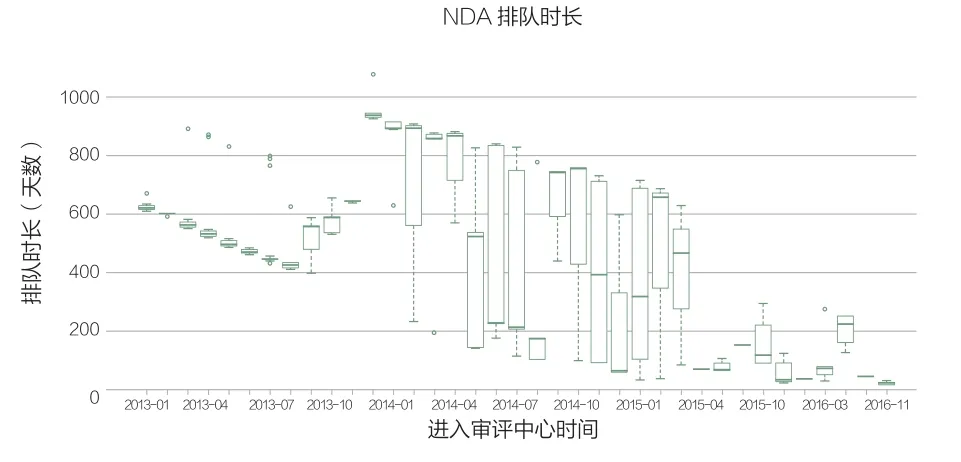
NDA审评序列排队时长相对比较无序。2013年1月~8月均保持排队时长下降状态,但从2014初至2015初,出现了排队时长阶段性增加,同一时间进入CDE的药品排队时间最大值与最小值差距比较大。
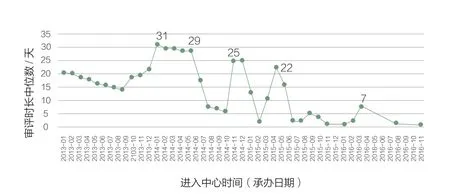
图3 NDA审评序列排队时长(月)
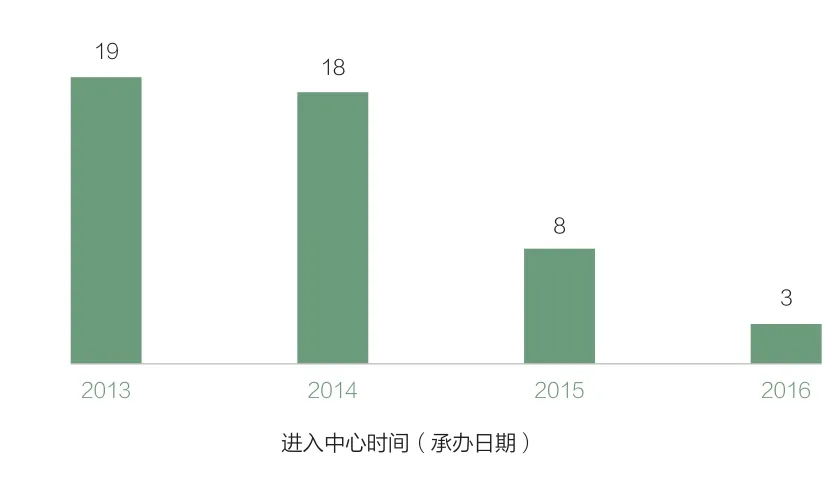
图4 2013~2016年NDA审评序列平均排队时长(月)
从图3来看,排队时间的异常变化更加明显,这可能与2015年前后药品审评严重积压有关,导致2013末至2015年进入中心待审评的药品排队时间大幅增加,即2014年进入CDE的药品,要平均等待18个月才开始审评,这一情况直到2015年3月左右才得到缓解,2016年平均排队时长下降到3个月。
3.化药ANDA审评序列排队时长分析
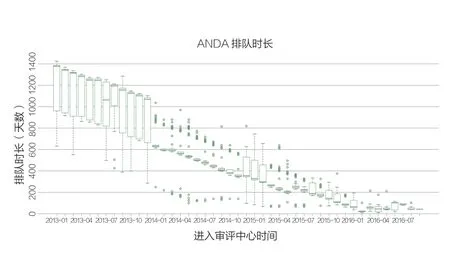
2013年进入审评中心ANDA序列的药品排队时长上下四分位数差值较大,说明该时间段内,同一时间进入序列的药品排队时间差异很大,而且总体来说排队时间偏长。2014年初起,同一时间进入ANDA审评序列的药品排队时长差异减小,并且等待时间迅速缩短,保持平稳下降。
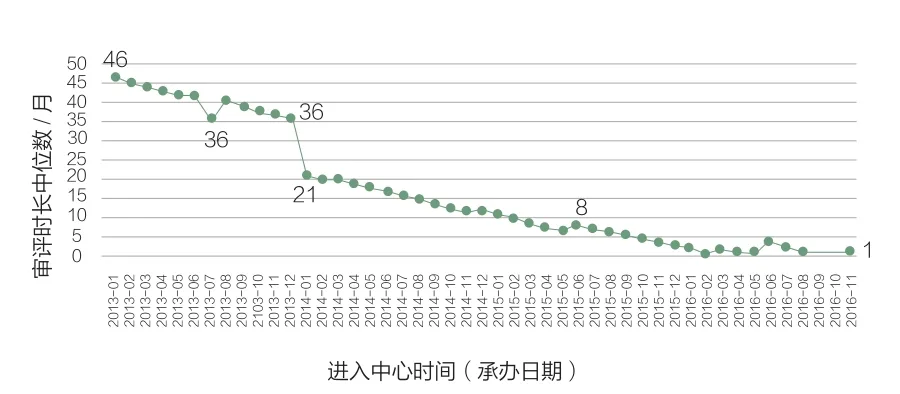
图5 ANDA审评序列排队时长(月)
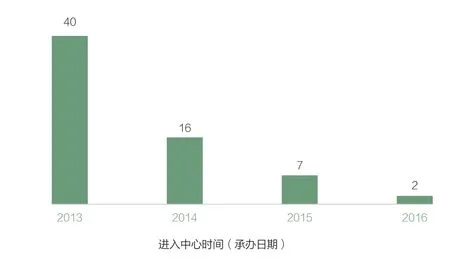
图6 2013~2016年ANDA审评序列平均排队时长(月)
图5可知,2013年12月,排队时长断崖式下降,至2016年初左右,排队时间锐减。图6可视,至2014年ANDA审评序列平均排队时长缩短至16个月,到2016年缩短到2个月。
2013年ANDA序列排队时长过长的情况非常严重,由于我国药品研发情形的特殊性,大部分以仿制药为主,并且低水平的仿制现象较为突出,这就导致了ANDA序列过度积压。根据相关数据统计,2015年左右ANDA序列排队序列号最高值曾达到了令人吃惊的8000件以上,而目前维持在1000件以下。
值得注意的是,化药注册分类实行改革后现在的化药3类划分为仿制药,其审评序列为ANDA,相当于原3类新药审评序列由验证性临床变更为ANDA。但是由于到目前为止按新3类申报的仿制药数量有限,因而需纳入本次统计范畴的受理号数量更少,因此也未对整体的排队时长情况造成影响。
4.化药验证性临床审评序列排队时长分析
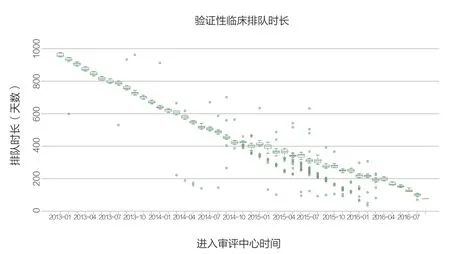
2013年起,验证性临床审评排队时长保持平稳下降,同一时间进入中心的药品排队时间差异不大。从上图来看,2015年出现排队时长异常值的情况比较多见,尤其是出现极小异常值的情形,可考虑为集中审评的原因。
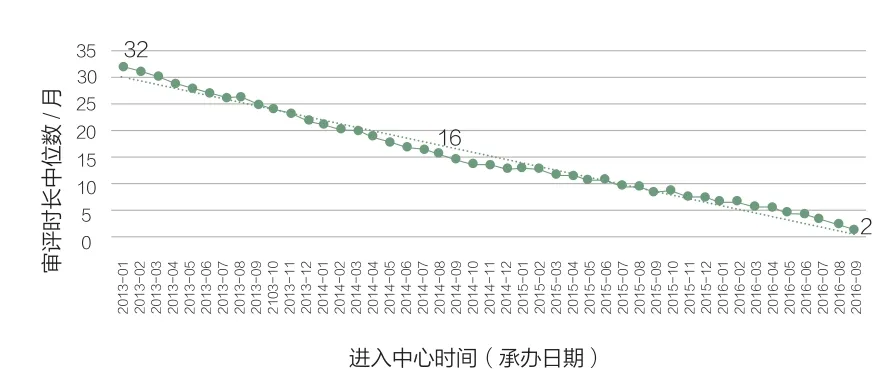
图7 验证性临床审评序列排队时长(月)
图8 2013~2016年验证性临床审评序列平均排队时长(月)
化药注册分类改革前,化药3类新药一度是药企争先申报的宠儿。根据数据统计,承办日期从2010年1月1日~2016年12月31日,中心共受理化药新药10452件,其中化药3类新药(按照旧注册分类)8201件,占比78.5%,2015年更是达到了2248件。
从图7来看,2013年验证性临床排队时长最大值达到了32个月,但总体情况相对乐观,进入验证性临床序列的数量在增加,从图7、图8能清楚看到排队时长整体呈线性下降趋势。其原因是,一方面随着化药分类的推进,进入验证性临床序列的药品数量大幅减少;另一方面审评的提速,验证性临床的审评压力得到了极大的缓解。
5.化药补充申请审评序列排队时长分析

补充申请每年申报数量非常庞大,大约每年占比1/4~1/3。就2014年来说,其是近年来药品申报高峰年,中心共受理化药7817件,化药补充申报2445件,其比例为31.3%。由于数量多,在排队时长上差异较大。
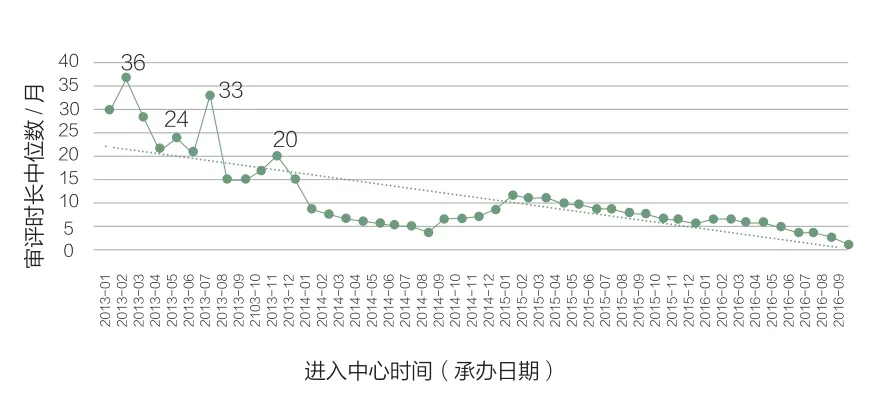
图9 补充申请审评序列排队时长(月)

图10 2013-2016年补充申请审评序列平均排队时长(月)
从排队时长中位数图9来分析,补充申请长则达36个月,短至1个月,但从2014年后时长明显缩短了。从图10来看,2015年平均排队时长略有上升,究其原因可能由于2014年出现药品申报高潮,导致药品审评堆积,而2016年补充申请审评序列数量开始稳步下降了。
6.化药进口再注册审评序列排队时长分析

图11 补充申请审评序列排队时长(月)
图12 进口再注册审评序列排队时长(月)
相比其他的审评序列,进口再注册由于其申报数量少,受到审评积压的影响最轻,2014年2月以后排队时间保持相对较短的水平。
总体来说,各审评序列由于审评积压等客观因素导致排队时间大幅增加的情况在2013年前后进入审评中心的药品,药品积压是一个相对缓慢的过程,该时间段申报的药品,平均排队时间在2年左右(不同的审评序列略有不同),意味着需要等到2015年甚至更晚的时间才能开始审评,而新申报药品的数量不断增加,新旧冲击导致在2015年部分序列品种产生新的积压高潮。
IND、NDA序列排队时长相比其他审评序列,从数字上来看相对乐观。IND序列2013年平均排队时长16个月,NDA序列2013年平均排队时长19个月,但与美国FDA等发达国家相比,排队时间仍然过长,这对我国创新药研发非常不利。与新药相比,仿制药的审评时间更长。其中ANDA序列,即仿制药的申报受到积压影响最大,2013年申报的药品平均排队时长达到了40个月,这意味着申报一个仿制药仅在排队待审评上所花费的时间就超过3年。
可喜的是,经过国家食药监管部门近几年多管齐下的政策改革,随着审评人员的增多、以及提高申报品种含金量,化药总体申报数量正在大幅下降,审评积压的情况得到缓解。2016年新申报的药品排队时间大幅缩短,基本实现了到年底前消化完积压存量的目标。2017年以来审评排队时长趋于平稳,并达到相对合理的审评时限(含排队时间)。相信随着审评时间的加快,医药新政的实施,我国新药研发将进入又一个高锋期。
(本文数据来源:药智网注册与受理数据库)

