连续流动分析法测定水中总氰化物的研究
(北京市环境保护监测中心,北京100048)
氰化物是一种剧毒物质,受氰化物污染的水体可引起水生生物、家畜乃至人类发生急性中毒。因此,氰化物的测定是环境监测领域的重要项目之一。水中的氰化物以简单氰化物和络合氰化物的形式存在[1]。氰化物的常用分析方法有滴定法、电极法和比色法等[2]。目前手工法测定氰化物的国家标准是《水质 氰化物的测定 容量法和分光光度法》(HJ 484—2009)。手工法测定水中氰化物时,水样所需量较大、需要蒸馏,显色时间较长并且在操作过程中会释放出氢氰酸,易对人体产生危害[3-9],尤其在处理大批量样品时,该方法的应用受到了一定的限制[10]。使用连续流动分析仪可以自动测定水中的总氰化物,样品不需复杂的前处理,避免了人为误差的影响[4,11-13]。因此,本实验就连续流动分析仪测定水中总氰化物的方法进行了研究。实验结果优于现行国家分析标准,准确度与精密度均能满足测试要求。
1 实验部分
1.1 仪器与试剂
1.1.1 仪器
AutoAnalyzer3全自动连续流动分析仪(德国Seal公司);AD-2100F型连续pH测定仪(上海仪乐);ME2002E电子天平(梅特勒-托利多仪器(上海)有限公司)。
1.1.2 试剂
实验所用的试剂均为优级纯,对空白测试无干扰。
①蒸馏试剂:溶解1.6 g氢氧化钠在300 mL去离子水中,加入20.0 g柠檬酸,用去离子水稀释至1000 mL,搅拌至完全溶解。
②(水+ Brij-35)溶液:量取5.0 mL聚氧乙烯月桂醚(Brij-35)溶液(20%)于500 mL去离子水中。
③缓冲溶液:溶解2.3 g氢氧化钠在300 mL去离子水中,加入20.5 g邻苯二甲酸氢钾,用去离子水稀释至1000 mL,搅拌至完全溶解,然后再加入Brij-35溶液(20%)1.0 mL。
④显色剂:溶解3.5 g氢氧化钠在300 mL去离子水中,加入8.4 g 1,3-二甲基巴比妥酸和6.8 g异烟酸,用去离子水稀释到500 mL,搅拌至完全溶解,然后再加入Brij-35溶液(20%)1.0 mL。
⑤氯胺-T溶液:称取2.0 g氯胺T溶于1000 mL去离子水中。
⑥水中氰成分分析标准溶液:50 mg/L(GBW(E)080115),购买自中国计量科学研究院。
⑦1.0 mol/L氢氧化钠溶液:称取40.0 g氢氧化钠溶解于700 mL去离子水中,冷却至室温,并用去离子水稀释至1000 mL,混匀。
⑧0.01 mol/L氢氧化钠溶液:称取0.4 g氢氧化钠溶解于700 mL去离子水中,冷却至室温,并用去离子水稀释至1000 mL,混匀。
⑨1.0 mol/L稀盐酸溶液:量取85.0 mL浓盐酸(37%)于700 mL去离子水中,冷却至室温,并用去离子水稀释至1000 mL,混匀。
1.2 实验原理
水样中加入0.32 mL/min的蒸馏试剂,在pH=3.8条件下,经过紫外消解、120℃蒸馏,蒸馏后的氰化物中依次加入0.05 mL/min的(水+ Brij-35)溶液、0.42 mL/min的缓冲溶液、0.42 mL/min的氯胺T溶液和0.42 mL/min的显色剂溶液,氰化物和氯胺T反应生成氯化氰,然后与异烟酸及1,3-二甲基巴比妥酸在37℃时反应生成红色络合物,该络合物在600 nm波长处有最大吸收,根据朗伯-比尔定律进行比色定量测定。工作流程图见图1。
2 结果与讨论
2.1 方法性能指标
移取不同体积的氰化物标准溶液,用0.01 mol/L氢氧化钠溶液稀释[14,15],配制成浓度分别为:0、2、5、10、20、50、80和100 μg/L的总氰化物标准系列。以总氰化物标准溶液浓度为横坐标,峰高为纵坐标,计算得到的标准曲线和相关系数如表1所示。实验结果表明,使用异烟酸-巴比妥酸连续流动法测定总氰化物具有较好的线性关系,其相关系数r2为1.0000。

表1 异烟酸-巴比妥酸连续流动法测定总氰化物的标准曲线方程与相关系数
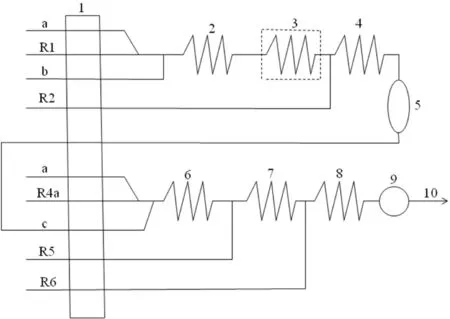
图1 连续流动测定总氰化物工作流程图R1.蒸馏试剂; R2.清洗水;R4a.缓冲溶液;R5. 氯胺T;R6. 显色剂;1. 蠕动泵;2、4、6、7 .混合反应圈;3.紫外消解器;5.蒸馏单元;8加热; 9.流动检测池;10.废液;a.空气;b.样品;c.蒸馏后的样品
按照HJ 168—2010的要求,按照样品分析的全部步骤,平行测定0.5 μg/L总氰化物标准溶液7次,根据实验结果计算方法的检出限,结果如表2所示。方法的检出限为0.169 μg/L,低于《水质 氰化物的测定 容量法和分光光度法》(HJ 484—2009,方法3异烟酸-巴比妥酸分光光度法)的检出限。

表2 方法的检出限
对标准值为(14.6±1.3)μg/L和(68.8±6.4)μg/L的总氰化物标准样品平行测定6次,计算相对标准偏差,结果见表3。结果表明,不同浓度的总氰化物测定的相对标准偏差为0.6%~1.2%,实验数据平行性较好,本方法具有良好的精密度。
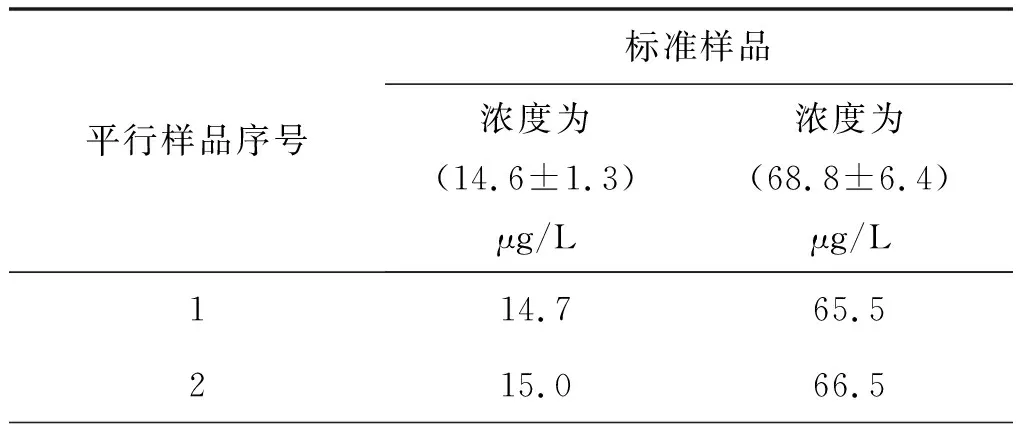
表3 方法精密度
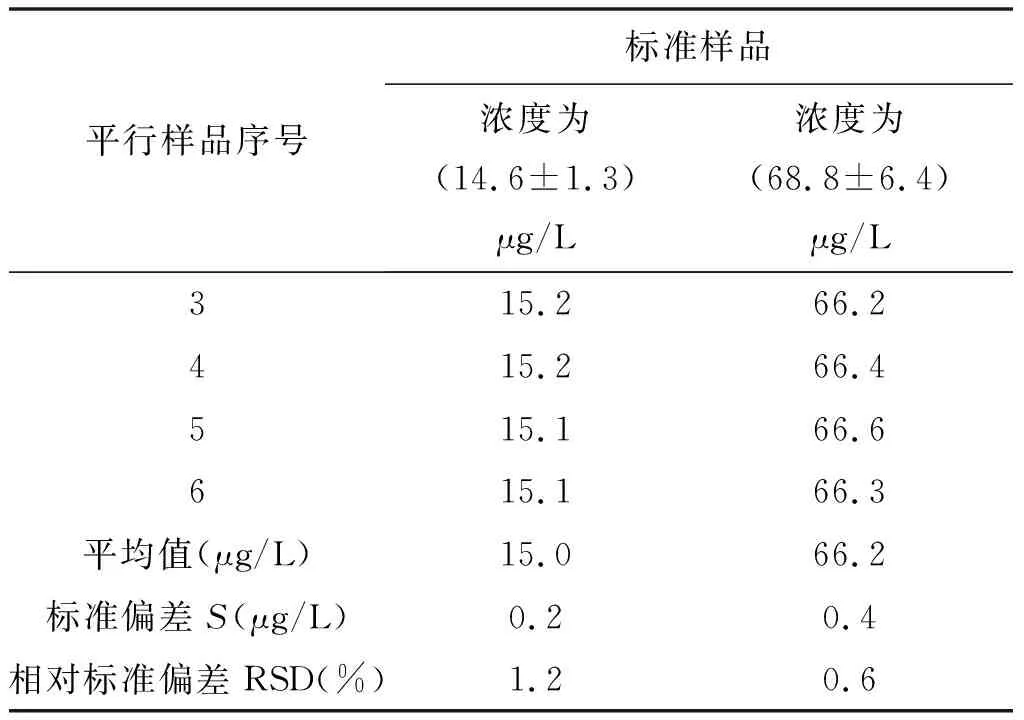
续表3
分别用去离子水、地下水和地表水进行不同水质的加标回收实验,重复测定6次,计算样品的平均浓度和加标回收率,结果如表4。可见,不同浓度的样品加标回收率为94.3%~101.2%。该方法适用于地下水和地表水中总氰化物的测定。
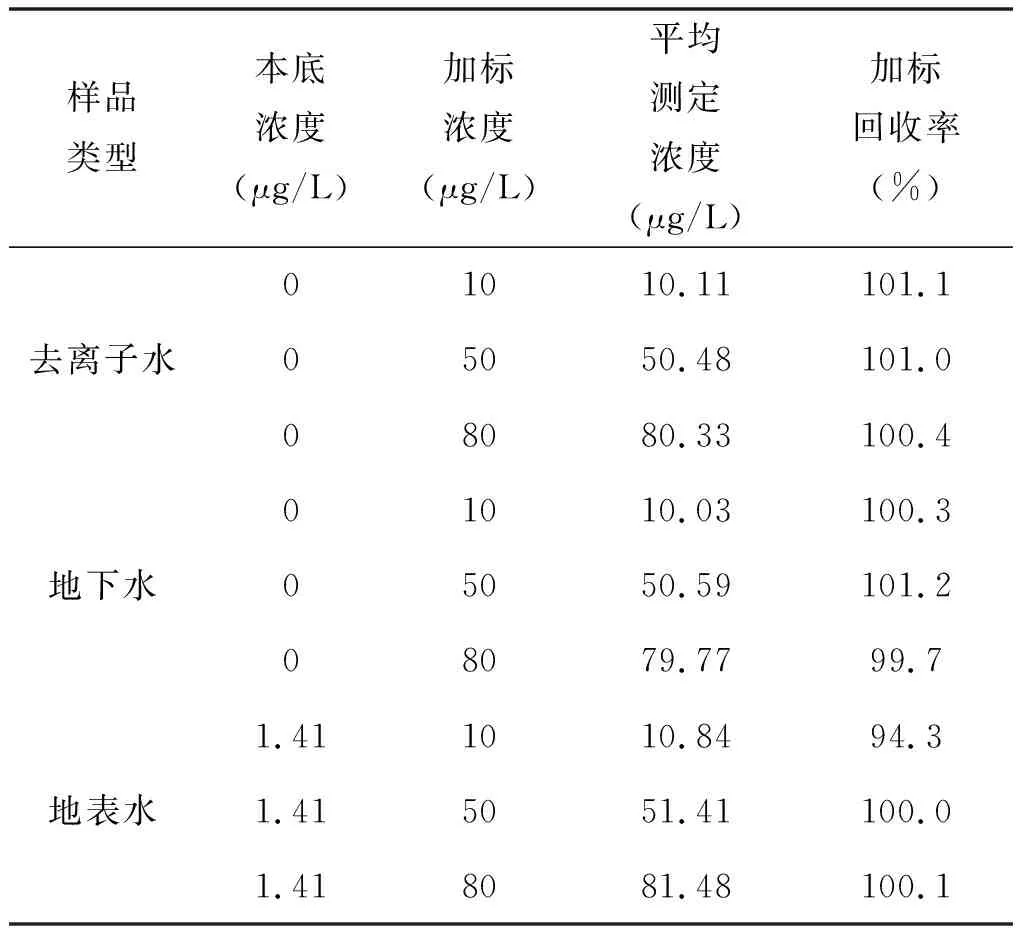
表4 加标回收率实验结果表
2.2 蒸馏温度对实验结果的影响
考察不同的蒸馏温度对样品中总氰化物吸光度值的影响,分别在110、115、120、125、130和140℃的蒸馏温度下,对浓度为(68.8±6.4)μg/L的标准样品平行测定6次,计算其平均吸光度值,并作图2不同蒸馏温度对标准样品的平均吸光度值的影响。由图2可见,在110℃~120℃之间,随着蒸馏温度的升高,标准样品的吸光度值也随之升高;当蒸馏温度高于120℃时,随着温度的升高,标准样品的吸光度值下降。当蒸馏温度为120℃时,标准样品的吸光度值最大;当蒸馏温度为140℃时,标准样品的吸光度值仅为120℃时的一半。因此,测定水样中总氰化物最佳的蒸馏温度为120℃。
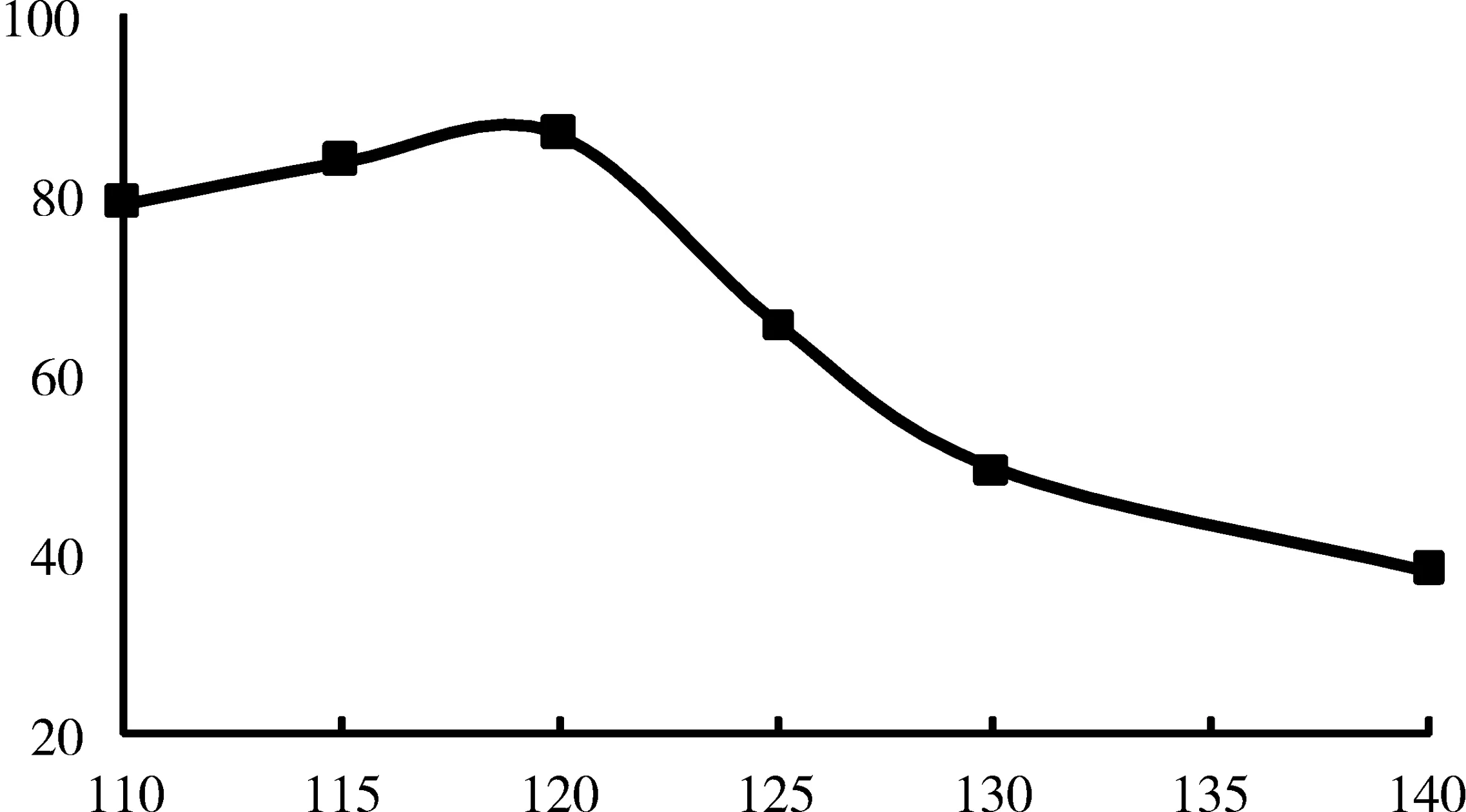
图2 不同蒸馏温度对标准样品吸光度值的影响
2.3 不同pH值的试剂对反应的影响
在1.1.2配制的试剂基础上,分别通过加入1.0 mol/L氢氧化钠溶液和1.0 mol/L稀盐酸调节缓冲溶液、蒸馏试剂和显色剂的pH值,并对浓度为(68.8±6.4)μg/L的标准样品平行测定6次,计算标准样品的平均测定浓度和相对误差,如表5~7所示。实验结果表明:当缓冲溶液pH值≤2.7时,蒸馏试剂pH值≤1.2时,显色剂pH值≤2.8时,影响反应进行,试验结果偏低。
2.3.1 不同pH值的缓冲溶液对反应的影响
根据表5,当蒸馏试剂pH=3.8,显色剂的pH=5.2时,发现缓冲溶液的pH值在5.2~7.0之间,标准样品的测定值均在标准样品不确定度范围内,相对误差为-2.5%~-3.8%;当缓冲溶液的pH值为2.7时,标准样品测定值未检出。结果表明:当缓冲溶液pH值≤2.7时,影响实验反应进行,试验结果偏低。
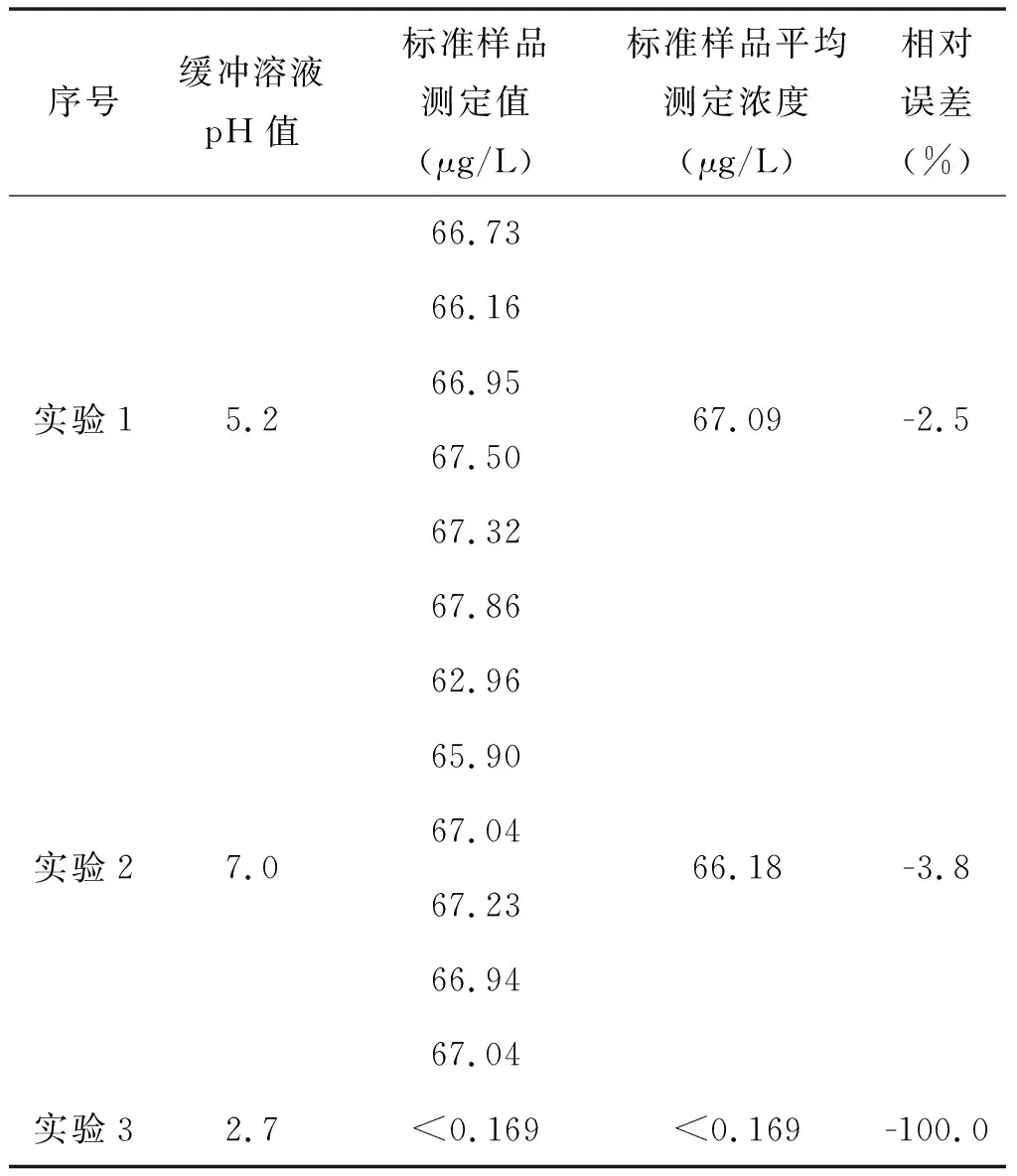
表5 不同pH值的缓冲溶液下标准样品(68.8±6.4)μg/L的测定结果
2.3.2 不同pH值的蒸馏试剂对反应的影响
根据表6,当缓冲溶液pH=5.2,显色剂pH=5.2时,发现蒸馏试剂的pH值在3.8~5.4之间,标准样品的测定值均在标准样品不确定度范围内,相对误差为-2.5%~2.6%;但当蒸馏试剂的pH值减小至1.2时,标准样品的平均测定浓度下降至49.48 μg/L,试验结果偏低。实验结果表明:当蒸馏试剂pH值≤1.2时,影响实验反应进行,试验结果偏低。
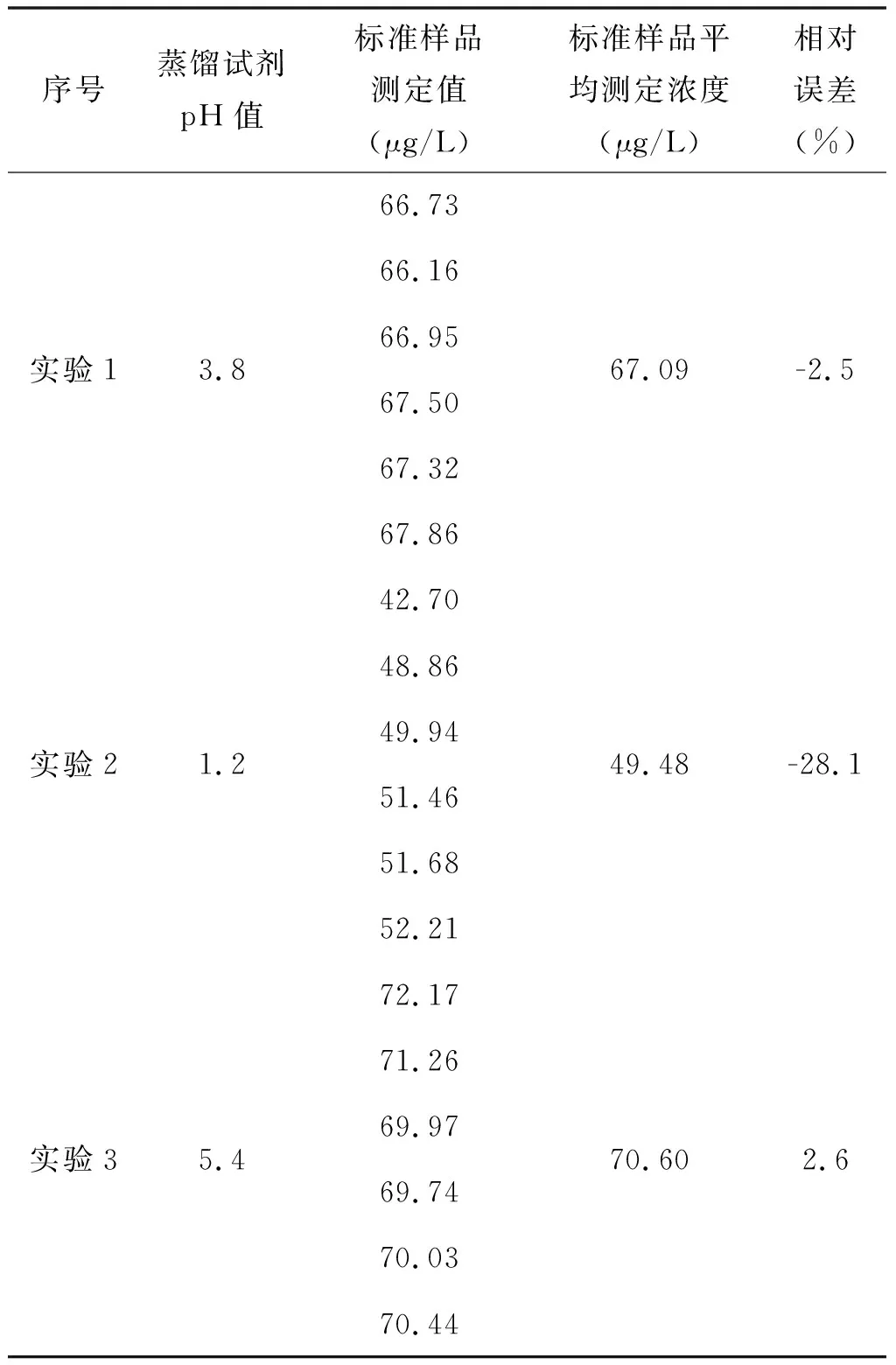
表6 不同pH值的蒸馏试剂下标准样品(68.8±6.4)μg/L的测定结果
2.3.3 不同pH值的显色剂对反应的影响
根据表7,当缓冲溶液pH=5.2,蒸馏试剂pH=3.8时,发现显色剂的pH值在5.2~7.6之间,标准样品的测定值均在标准样品不确定度范围内,相对误差为-2.5%~-6.2%;当显色剂的pH值为2.8时,标准样品测定值未检出。结果表明:当显色剂pH值≤2.8时,影响实验反应进行,试验结果偏低。
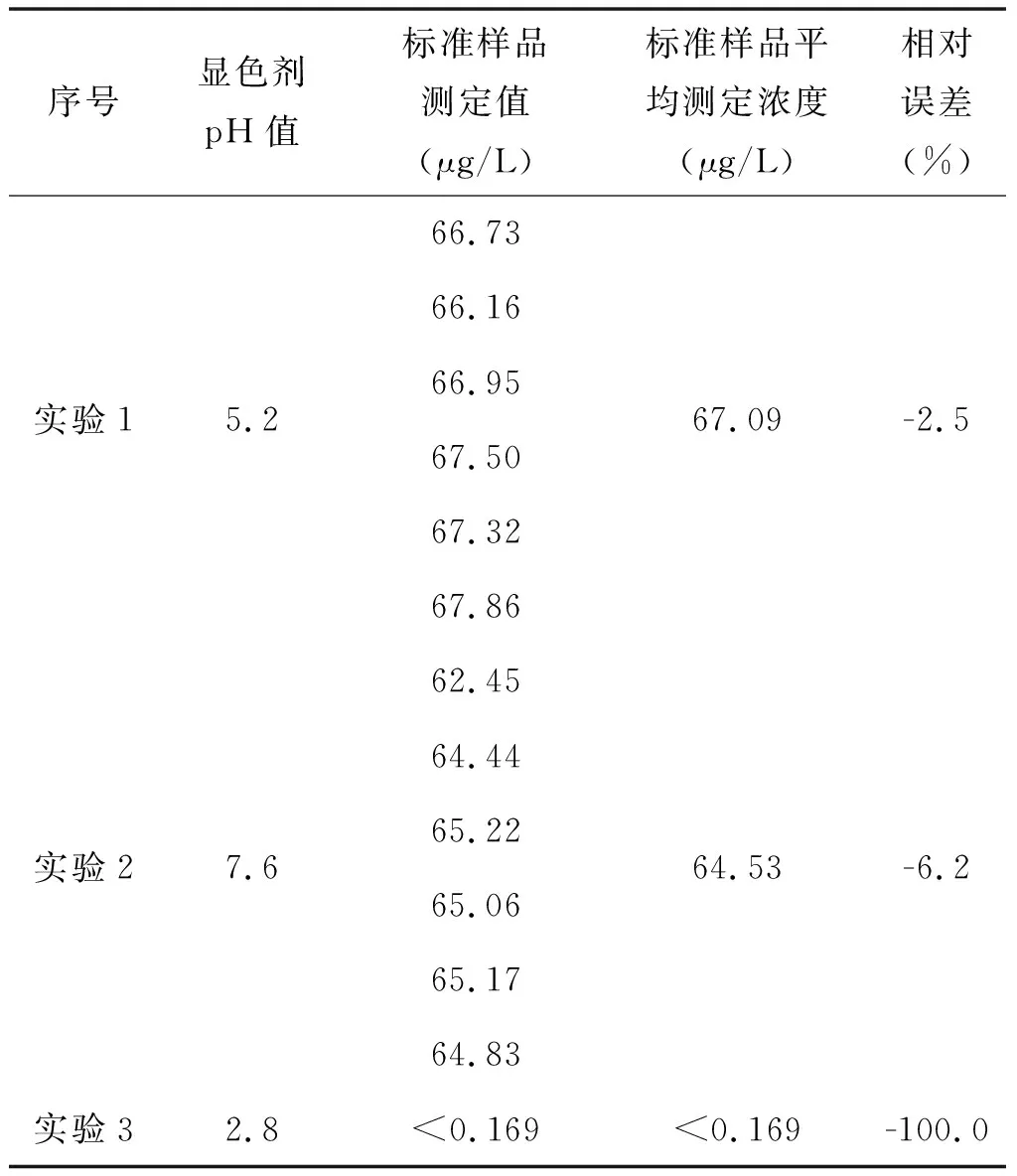
表7 不同pH值的显色剂下标准样品(68.8±6.4)μg/L的测定结果
2.4 干扰物的测定
参照《水质 氰化物的测定 容量法和分光光度法》(HJ 484—2009)对水样中的干扰物进行讨论,分析不同浓度的亚硝酸钠和硫化钠两种干扰物,对测定总氰化物结果的影响。分别配制0.2、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0、10.0 mg/L的亚硝酸钠溶液和1.0、5.0、10.0、50.0、100.0 mg/L的硫化钠溶液,然后使用本方法测定其总氰化物的含量,测定结果如图3和图4所示。由图3可知,随着亚硝酸钠浓度的升高,其总氰化物的浓度逐渐升高。当亚硝酸钠浓度为1.5 mg/L时,总氰化物的浓度为1.18 μg/L,超出了《水质 氰化物的测定 容量法和分光光度法》(HJ 484—2009)(方法3异烟酸-巴比妥酸分光光度法)的检出限1 μg/L。当亚硝酸钠浓度为10 mg/L时,总氰化物的浓度达到了52.48 μg/L。当样品中亚硝酸钠的浓度小于1.5 mg/L时,对样品总氰化物的测定结果影响较小;当亚硝酸钠浓度较高时,在蒸馏前可加入氨基磺酸(NH2SO2OH)去除。由图4可知,硫化钠的浓度小于100 mg/L时,其总氰化物的浓度均在0.3 μg/L以下,低于《水质 氰化物的测定 容量法和分光光度法》(HJ 484-2009)(方法3异烟酸-巴比妥酸分光光度法)的检出限。由此说明,当样品中硫化钠的浓度小于100 mg/L时,对样品总氰化物的测定结果影响较小。
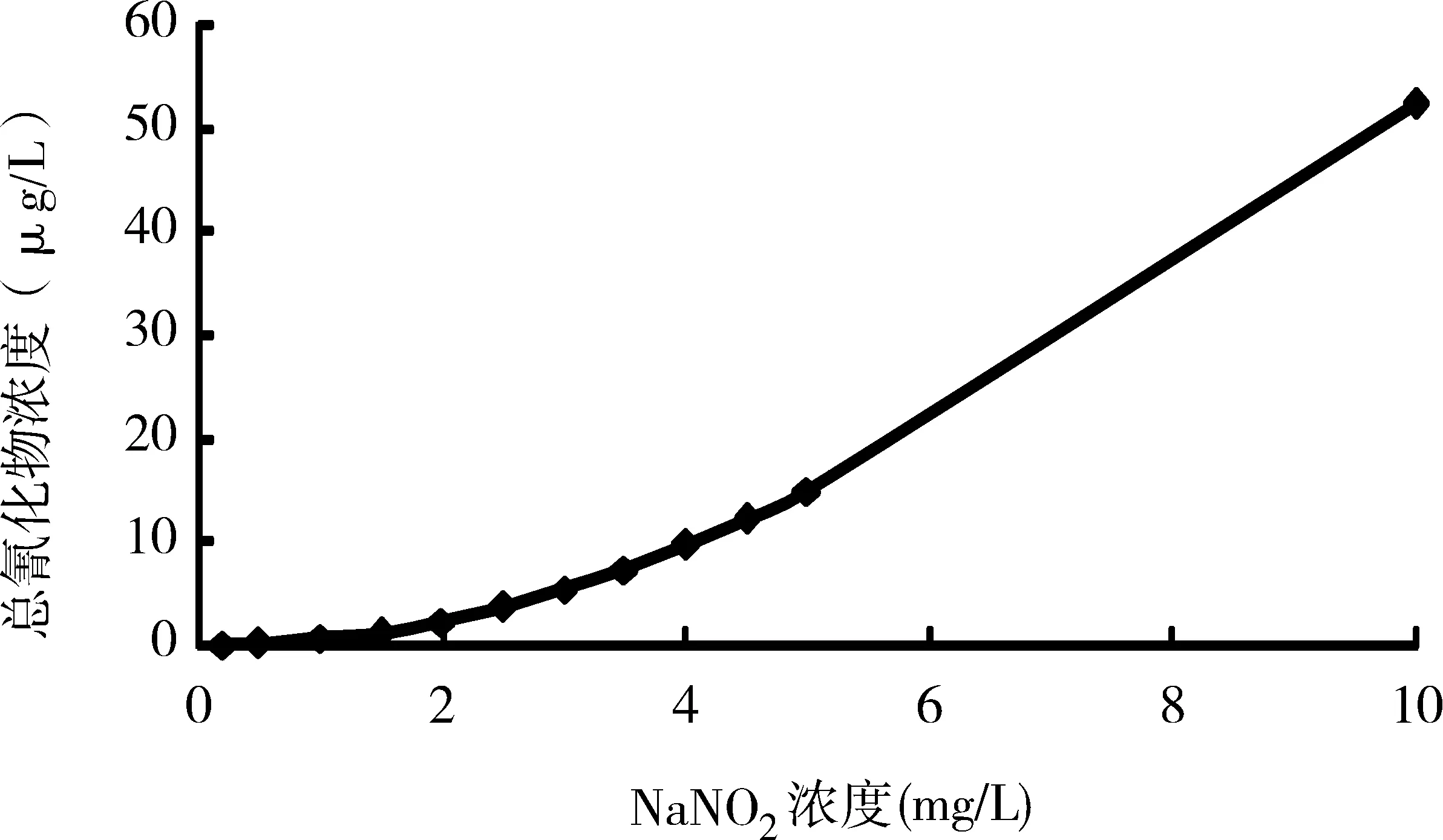
图3 不同浓度的亚硝酸钠中总氰化物的含量
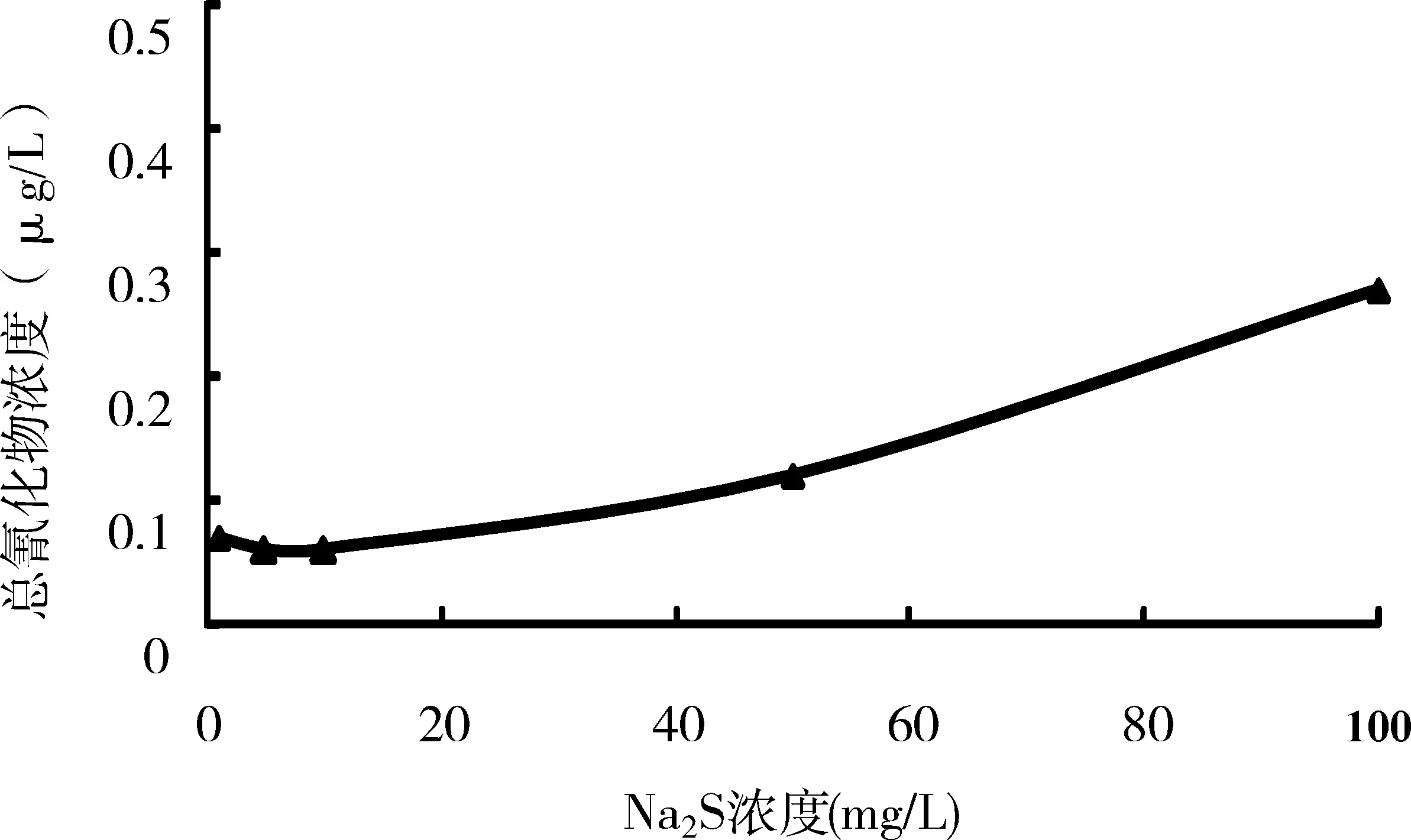
图4 不同浓度的硫化钠中总氰化物的含量
2.5 氰化钠、铁氰化钾、六氰基钴酸钾的测定
选取氰化钠、铁氰化钾、六氰基钴酸钾3种氰化物,分别配制5、10、50、100 μg/L的氰化物溶液,并用总氰化物的标准曲线分别平行测定这3种氰化物溶液6次,计算平均测定浓度和回收率。
氰化钠、铁氰化钾、六氰基钴酸钾的回收率如表8所示。从表8中,可以看出5~100 μg/L的氰化钠标准溶液的回收率为100.7%~104.2%,铁氰化钾标准溶液的回收率为94.8%~111.8%,均满足《水质 氰化物的测定 容量法和分光光度法》(HJ 484-2009)的测定要求,5~100 μg/L的六氰基钴酸钾溶液的回收率较低,为13.4%~20.4%。这可能是由于Co金属性较强,比较稳定,Co3+与-C≡N之间的键能较强,在进行蒸馏和紫外消解时,Co3+与-C≡N之间的键不能完全断裂,只有部分CN-参与反应,使得回收率较低。
2.6 水样保存实验
取4份500 mL去离子水,其中两份pH值为7.41,添加氰化物标准溶液50 μg/L,将试样瓶摇匀、密封,分别放置于室温和4℃冷藏保存;另外两份均用1.0 mol/L的氢氧化钠溶液调节其pH值为12.24,添加氰化物标准溶液50 μg/L,将试样瓶摇匀、密封,分别放置于室温和4℃冷藏保存。在不同的保存时间下,各取出10.0 mL水样平行测定6次,计算试样的加标回收率,结果如表9所示。
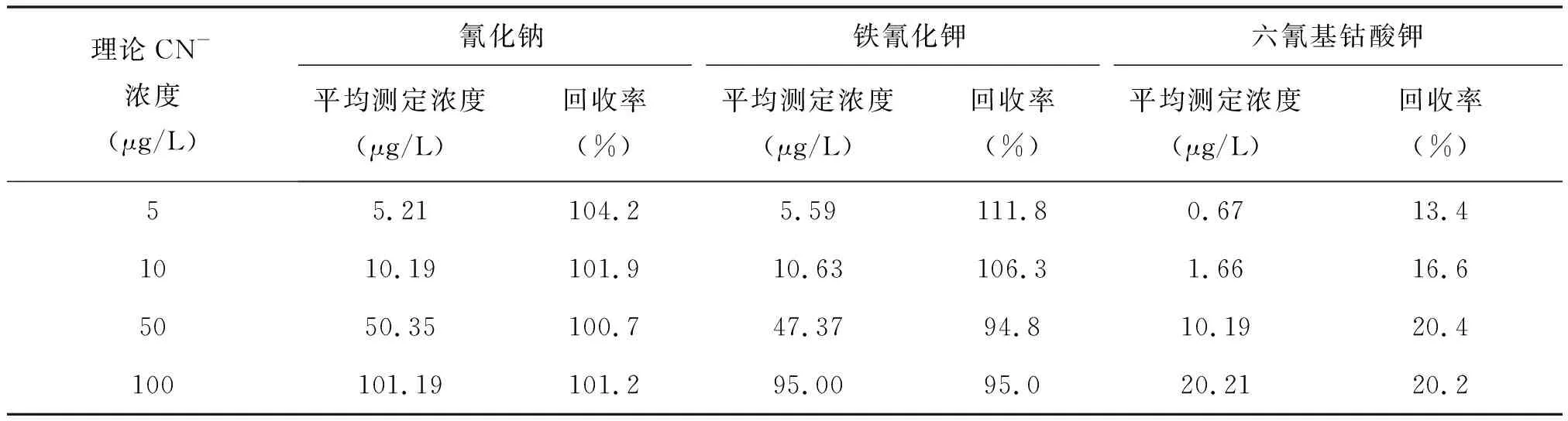
表8 3种氰化物中总氰化物的含量测定结果
从表9中,可以看出pH值为7.41的样品(即:不添加固定剂氢氧化钠),随着保存时间的增加,样品的加标回收率呈下降趋势;经过16天后,在25℃室温保存条件下,样品的加标回收率从89.3%下降至7.5%;在4℃冷藏保存条件下,样品的加标回收率从89.5%下降至68.6%。当用1.0 mol/L的氢氧化钠溶液调节样品的pH值为12.24时,经过16天后,在25℃室温保存条件下,样品的加标回收率从99.8%仅下降至94.2%;在4℃冷藏保存条件下,经过16天,样品的加标回收率为97.7%~99.8%。在相同保存时间下,4℃冷藏比25℃室温保存条件下的样品加标回收率高。因此,通过加入氢氧化钠调节样品pH≥12,在4℃冷藏,可使样品保存的时间较长;当保存时间为16天时,样品的加标回收率仍保持在97%以上。
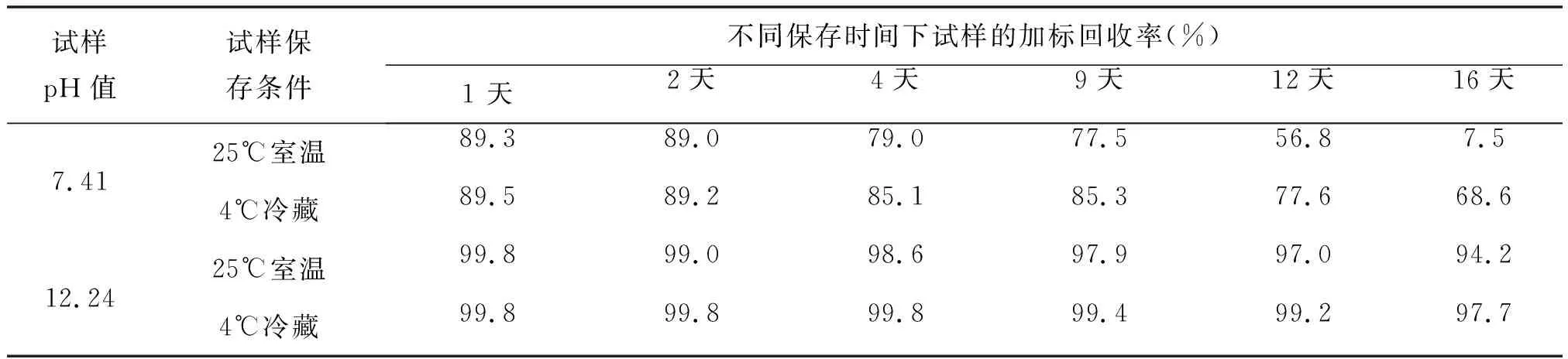
表9 不同保存条件下及不同保存时间下试样的加标回收率
3 结论
使用连续流动分析仪测定水样中总氰化物,曲线相关系数r2为1.0000,检出限为0.169 μg/L,具有良好的精密度和较高的准确度,样品测定的相对标准偏差小于5%。最佳的蒸馏温度为120℃;加入氢氧化钠的使水样pH≥12,在4℃冷藏保存16天时,其加标回收率达97%以上。当样品中亚硝酸钠干扰物的浓度小于1.5 mg/L,硫化钠干扰物的浓度小于100 mg/L时,对样品总氰化物的测定结果影响较小。该方法操作简便快捷,适用于大批量样品的测定。

