含钾硝水盐体系降温过程研究*
严雪鸿,黄雪莉,刘侠侠,王雪莹
(新疆煤炭洁净转化与化工过程重点实验室,新疆大学化学化工学院,新疆乌鲁木齐830046)
盐湖、海水以及化工生产中一些副产盐水体系的相平衡关系受温度的影响很大。一般来说,常温下的水盐体系相图最复杂,可以存在多种复盐,例如在 25 ℃下含钾硫酸盐型卤水体系有6种复盐,含硝酸盐的水盐体系如有 2 种复盐;温度较高时含硝酸盐、氯化镁的复盐结晶区缩小甚至消失,如钠硝矾和光卤石;低温时硫酸盐型复盐也有类似变化,如钾芒硝、钾镁矾等结晶区缩小或消失;-15℃以下时上述两个体系的硫酸盐型复盐的结晶区全部消失[1-3]。目前针对一些典型卤水体系的低温相平衡研究已有报道,不过相图表达的是热力学稳定状态,需要结合动态的降温结晶过程进行工艺研究。张霞等[4]基于新疆硝酸盐型卤水水盐体系,研究了不同浓度特征的硝酸盐水盐体系自然降温过程中液相组成的变化,并与人工降温过程进行对比,获得了硝酸盐型盐湖水盐体系低温相变规律。谢绍雷等[5]模拟冬季卤水冷冻结晶行为,探究了青海大浪滩盐湖卤水低温冷冻时的析盐结晶规律。黄维农等[6]通过盐田现场卤水冬季日晒蒸发实验,对西藏扎布耶盐湖冬季盐田卤水的组成变化规律进行了探究。毕思峰等[7]选取不同浓度的一里坪盐湖晶间卤水,分别在不同冷冻温度下进行除硫酸根实验,得到了卤水冷冻除硫酸根的最佳条件。
笔者研究团队在前期工作中对新疆杂硝石矿加工以及钠硝石生产硝酸钾工艺中涉及到的水盐体系在 0、-15 ℃下的相平衡进行了研究[1-2]。在此基础上,笔者对 Na+,K+∥Cl-,体系中不同组成的溶液进行自然降温实验,并与人工降温实验对比,结合相图研究其降温过程中液相组成变化及析盐规律,为开发盐湖资源低温工艺提供理论支持。
1 实验部分
1.1 试剂和仪器
实验所用试剂均为分析纯和优级纯。实验仪器为XTL-1型体视显微镜、X射线衍射仪、冰箱等。
1.2 实验方法
1.2.1 配制卤水体系
表1列出了实际杂硝石矿物浸取液体系组成(T组数据)。为更全面地研究具有不同浓度特征的溶液在降温过程中液相组成的变化规律,笔者参考25 ℃时对 NaCl饱和的五元体系相图[8],配制了4组不同组成的实验体系溶液,组成点分别为p、m、q、g。实验体系数据见表1,对应相图上的位置见图1。

图1 实验体系的设置(均对NaCl饱和)
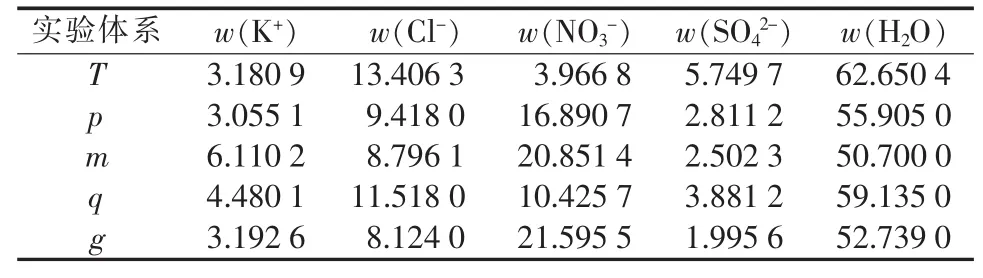
表1 卤水体系的组成 %
1.2.2 降温实验
1)自然降温:实验在1月份进行,气温为-10~-18℃,风力≤3级。根据表1中各实验体系的组成配制1 kg样品溶液,置于室外寒冷环境中进行自然降温。 当温度降至 5、0、-5、-10、-15 ℃左右时,取上层清液测定其组成,分离出固相进行物相鉴定。
2)人工降温:选取与自然降温相同的5组实验体系配制各样品溶液1 kg,置于-18℃左右的恒温冰箱中。同样,当温度降至 5、0、-5、-10、-15 ℃左右时,取样分析液相组成并鉴定析出的固相。
1.3 化学分析方法[9]
K+用四苯硼钾重量法测定;Cl-用硝酸银容量法测定用硫酸钡重量法或比浊法测定;用重铬酸钾氧化还原法测定;Na+用差减法计算;固相采用体视显微镜、X射线晶体衍射综合鉴定。

表2 自然降温与人工降温液相组成
2 结果与讨论
表2列出了各实验体系自然降温与人工降温液相组成(溶解度数据),同时列出了Janecke相图指数,并据此绘制出降温过程的液相组成变化走势(见图2)、各离子含量变化(见图3)。图4给出了典型会有钾芒硝析出,从而有助于钾的富集。

图 2 各实验体系降温过程中液相组成变化趋势

图3 各实验体系液相中各离子含量的变化
3)实验体系q与T不同,q处于25℃相图中NaCl和复盐Gla两盐共晶区。降温至5℃左右时,液相中K+和含量减少,结合固相鉴定结果表明减少的K+和以复盐Gla形式析出。由5℃降至-15℃的m点组成在-13.6℃下的固相XRD谱图。由表2、图2、图3并结合固相鉴定结果可以得出以下结论。
1)组成相同的实验体系自然降温与人工降温析盐规律基本相同,稍有差别,主要是因为自然降温过程降温速率较人工降温过程缓慢; 组成不同的实验体系其结晶路线不同。下面主要讨论自然降温情况。
2)从图2可知,实际杂硝矾浸取液组成T体系点处于NaCl和Na2SO4两盐共晶区。由表2可以看出,降温过程中液相组成中含量持续减少,其他离子含量基本不变。对应于相图上降温过程复盐Gla结晶区逐渐缩小至消失,Na2SO4·10H2O结晶区扩大,体系点一直处于Na2SO4·10H2O结晶区,不断析出Na2SO4·10H2O。针对析出的固相进行XRD鉴定,结果表明降温过程中只有Na2SO4·10H2O和氯化钠两种固相析出。因此,对于此类卤水降温过程中不的过程中,液相中含量大幅减少,此时减少的则是以Na2SO4·10H2O形式大量析出。由图2看出,体系点q自然降温与人工降温的路径稍有差别,但盐析规律相同。原因是自然降温前期室外气温的降温速率较缓,体系点在复盐Gla相区停留时间较长,析出Gla盐较多,带走液相中的K+较多,导致自然降温的结晶路线较人工降温偏右。对于此类卤水,快速降温使体系不在钾芒硝结晶区停留,可以减少钾随着氯化钠和芒硝析出,减少钾的损失。

图4 m实验体系-13.6℃下结晶固相XRD谱图
4)实验体系m降温初期的情况类似于q体系,有部分钾芒硝随着芒硝和氯化钠析出。由表2和图3可知,此阶段液相中K+和含量减少,以复盐Gla形式析出。5~-10℃的降温过程中,大幅减少,减少的以Na2SO4·10H2O形式析出。但降温至-10℃后,含量开始减少,结合固相XRD鉴定结果(见图4)可知,减少的以 KNO3形式析出。
5)实验体系 p处于 NaCl和 Na2SO4两盐共晶区,初期降温过程情况类似于实验体系T,先析出Na2SO4·10H2O和氯化钠,继续降至-10℃左右K+含量开始减少,结合固相鉴定结果表明减少的K+以KNO3形式析出。
6)实验体系g,由于处于25℃相图中复盐Dar和NaCl结晶区,前期降温过程中首先析出复盐Dar和氯化钠,但复盐Dar析出量很少,因为低温下复盐Dar结晶区缩小至消失,Na2SO4·10H2O结晶区扩大,体系点很快过渡到Na2SO4·10H2O结晶区,不再析出复盐Dar。5~-5℃的降温过程中,由表2和图3看出各离子含量基本不变,只有稍有减少,少量析出。继续降至-10℃时,含量开始大幅减少,Na2SO4·10H2O在此阶段大量析出。-10℃以后,K+和含量急剧减少,结合固相鉴定结果综合判定析出固相为KNO3。同样,为减少硝酸根的损失,对于此类卤水通过快速降温,使体系迅速进入到氯化钠和芒硝的结晶区,可以减少钠硝矾的析出。
3 结论
对于相同组成的卤水,降温速度在一定范围内对盐类结晶规律的影响不大;组成不同的卤水体系,降温过程中盐析规律表现不同;位于硫酸盐结晶区的卤水,快速降温能够避免或减少钾芒硝和钠硝矾复盐的析出,硫酸盐只以十水芒硝的形式结晶,实现钾和硝酸根的富集;硝酸盐含量偏高的卤水,过低的温度会导致硝酸钾或硝酸钠析出,不利于硝酸盐的富集。

