胶原/HA复合涂层多孔钛的细胞响应行为
李若琳,张云龙,寇宏超,李仁兴,卢雅琳
(1. 江苏理工学院材料工程学院,江苏 常州 213001)(2. 西北工业大学 凝固技术国家重点实验室,陕西 西安 710072)
1 前 言
医用钛合金材料已成为骨科、齿科和心血管等植介入物或器械用主要原材料,但要满足患者临床治疗的长效安全性和功能性,医用钛合金材料的生物及力学相容性仍有待提高[1]。钛合金植入人体后会产生应力屏蔽,在外力和体液的侵蚀下,表面的氧化物钝化膜有可能出现剥离和溶解,因此在使用过程中会有物质释放到组织中,在生物体内产生毒性、炎症、血栓等反应[2],这些缺点严重影响了钛合金人工关节的长期应用效果[3]。为解决以上问题,研究人员采用了在钛及钛合金中引入孔隙并对其进行表面改性的方法[4]。多孔结构可通过调控孔隙率使材料的弹性模量接近人骨而减少应力屏蔽[5, 6],且其独特的三维连通孔能使体液和营养物质在多孔植入体中传输,促进组织再生与重建,加快愈合过程。
人工植入材料的基本要求是不仅具有生物相容性,而且与相邻宿主骨间存在生物活性[7, 8]。羟基磷灰石(hydroxyapatite,HA)是人体硬组织的基本无机成分,具有良好的生物相容性及生物活性[9, 10],HA涂层的溶解刺激了骨组织的结合,它植入人体后能在短时间内与人体的软组织形成紧密结合[11]。在多孔钛表面涂覆HA活性涂层,可改变原多孔钛的表面形态,使其具有与人骨相近的钙磷比,有利于成骨细胞的粘附、增殖和分化[12]。另一方面,水溶性胶原蛋白是构成细胞外基质的骨架,并保留了自身生物活性,且胶原在细胞外基质中形成半晶体的纤维,给细胞提供抗张力和弹性,并在细胞的迁移和发育中起作用[13, 14]。综合以上研究结果,选取多孔钛作为基体,在其表面涂覆胶原/HA复合涂层,有望使植入多孔钛得到更好的细胞响应,促进骨组织长入并形成生物固定。本文研究胶原/HA复合涂层的表面形貌及化学成分,探讨复合涂层在多孔钛上的形成机理,进行体外细胞毒性实验并分析了多孔钛表面细胞响应行为。
2 实验方法
钛网层状压制烧结多孔钛样品[15]的直径为16 mm、高4 mm,钛网在使用前需在酒精、硝酸、氢氟酸体积比为1∶3∶7的混合溶液中浸泡以完成表面活化,然后在丙酮中超声波清洗20 min。清洗后的样品放入浓度为5.0 mol/L的NaOH溶液中,密封、60 ℃保温处理24 h。取出后用去离子水清洗,空气中干燥。处理后的样品在630 ℃进行热处理,热处理时升温速度为3 ℃/min,在630 ℃保温1 h,随炉冷却。然后对样品进行预钙化处理:将样品放入0.5 mol/L Na2HPO4溶液中24 h,再在饱和Ca(OH)2溶液中浸泡5 h。取出后用去离子水清洗,于36.5 ℃模拟体液(simulated body fluid,SBF,离子浓度见表1)中浸泡2周,取出后于空气中干燥,进行高压消毒灭菌(120 ℃、20 min),消毒完成后进行干燥,即制备了HA涂层多孔钛。将HA涂层多孔钛完全浸入浓度为7 g/L的水溶性胶原溶液中5 h,完成胶原/HA复合涂层制备。浸泡过程中每48 h更换一次SBF,以(CH2OH)3CNH2溶液作为缓冲液,调节pH到7.25。
进行体外细胞毒性实验时,选用小鼠前成骨细胞MC3T3-E1,采用直接接触方式,首先将胶原/HA复合涂层多孔钛在120 ℃、20 min高温灭菌。以2×104的细胞密度种植于24孔板,连续培养5 d后,部分进行噻唑蓝(MTT)比色法检测,其余用乙醇进行细胞固定,用以观察细胞响应行为。

表1 模拟体液(SBF)和人体血清离子浓度对照(mmol/L)Table 1 Ion concentrations of simulated body fluid (SBF) and human blood plasma
采用TESCAN VEGA3扫描电镜(SEM)及能谱分析仪(EDS)对胶原/HA复合涂层的表面形貌及化学成分进行分析,探讨了胶原/HA复合涂层的形成机理,对改性前后多孔钛表面的细胞响应行为进行观察。
3 结果与讨论
对胶原/HA复合涂层多孔钛表面进行打磨至其露出横截面,SEM照片如图1a所示,未打磨的样品纵向表面SEM照片如图1b所示,增大放大倍数至5000(图1c),观察打磨后横截面的胶原/HA复合涂层与多孔钛基体结合程度。对比图1a和1b可看到,打磨后的样品表面由内到外分为a、b、c、d 4层,表2为对这4个区域进行EDS测试后得到的各元素原子百分比,a层由内向外为纯钛纤维基体及表面活化纳米层,这种微孔结构便于HA的形核,并且所形成的HA层与基体的结合力很强;b层由于其表面含有大量钙元素及少量磷元素,推测b层为预钙化层,预钙化对HA有诱导沉积作用,进而可形成均匀涂层;c层钙磷原子比达到1.7,满足标准HA涂层钙磷原子比1.67的要求,c层为HA涂层,使材料表面具有与人骨相近的钙磷比,提高了材料的生物活性;d层含有大量的C,O元素,少量Ti元素,符合胶原蛋白组成,d层为胶原层,进一步提高了材料表面的生物活性;Ti元素的原子百分比由内到外依次递减。因此,多孔钛表面由内到外依次为:多孔钛基体及表面活化纳米层、预钙化层、HA层和胶原层,实现了预定的多孔钛表面功能化涂层的设计。
从图1c中可看出,胶原/HA复合涂层的厚度约为3~5 μm,与多孔钛基体结合良好。图1d为HA涂层缺损处,胶原直接附着在碱热处理形成的纳米孔上的形貌,说明了即使涂层存在表面微裂纹等缺陷,胶原也可以起到补充加强多孔钛生物相容性的作用。
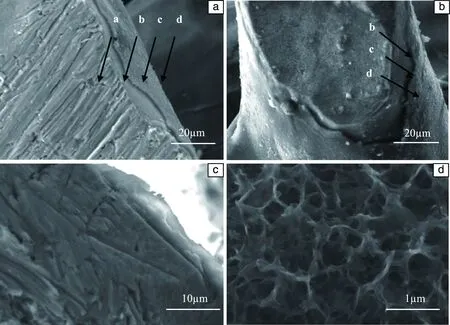
图1 多孔钛表面胶原/HA复合涂层SEM照片:(a)横截面,(b)纵截面,(c) 放大倍数下横截面,(d) HA涂层缺损处Fig.1 SEM images of the collagen/hydroxyapatite composite coating: (a) cross section, (b) longitudinal surface, (c) magnified cross section, (d) HA coating defect

表2 多孔钛表面复合涂层EDS所测元素的原子百分比Table 2 The atomic percents of elements of composite coating analyzed by EDS(at%)
胶原/HA复合涂层的形成机理如图2所示,碱热处理后多孔钛表面形成非晶的钛胶层,热处理后表面形成钛酸钠,预钙化过程中样品表面的钛酸钠水解,形成带负电的活性Ti—OH,Ca2+被静电引力均匀吸附到表面的活性羟基位上。在浸泡SBF过程中,PO43-与Ca2+发生反应,均匀附着在Ca2+表面,同时,又有Ca2+均匀吸附到PO43-表面,层层叠加吸附,形成了均匀分布的HA,随后浸泡到胶原溶液中,表面沉积均匀的类人胶原层。
对不同方法处理后的样品进行细胞培养5 d,后进行MTT检测,对照组(control)为无多孔钛的样品孔,所得结果列于表3,各样品孔中光密度(OD)值均小于对照组,且有显著性差异。以control组细胞存活率为100%,表面活化、HA涂层及胶原/HA复合涂层上细胞存活率分别为8.07%、33.03%、45.68%。可以看到可溶性胶原的添加增加了细胞的成活率,提高了多孔钛支架的生物相容性。由于基体为多孔材料,内部结构复杂,胰酶不能将材料上附着的细胞全部消化下来,数据存在误差,但可以参考其变化趋势。
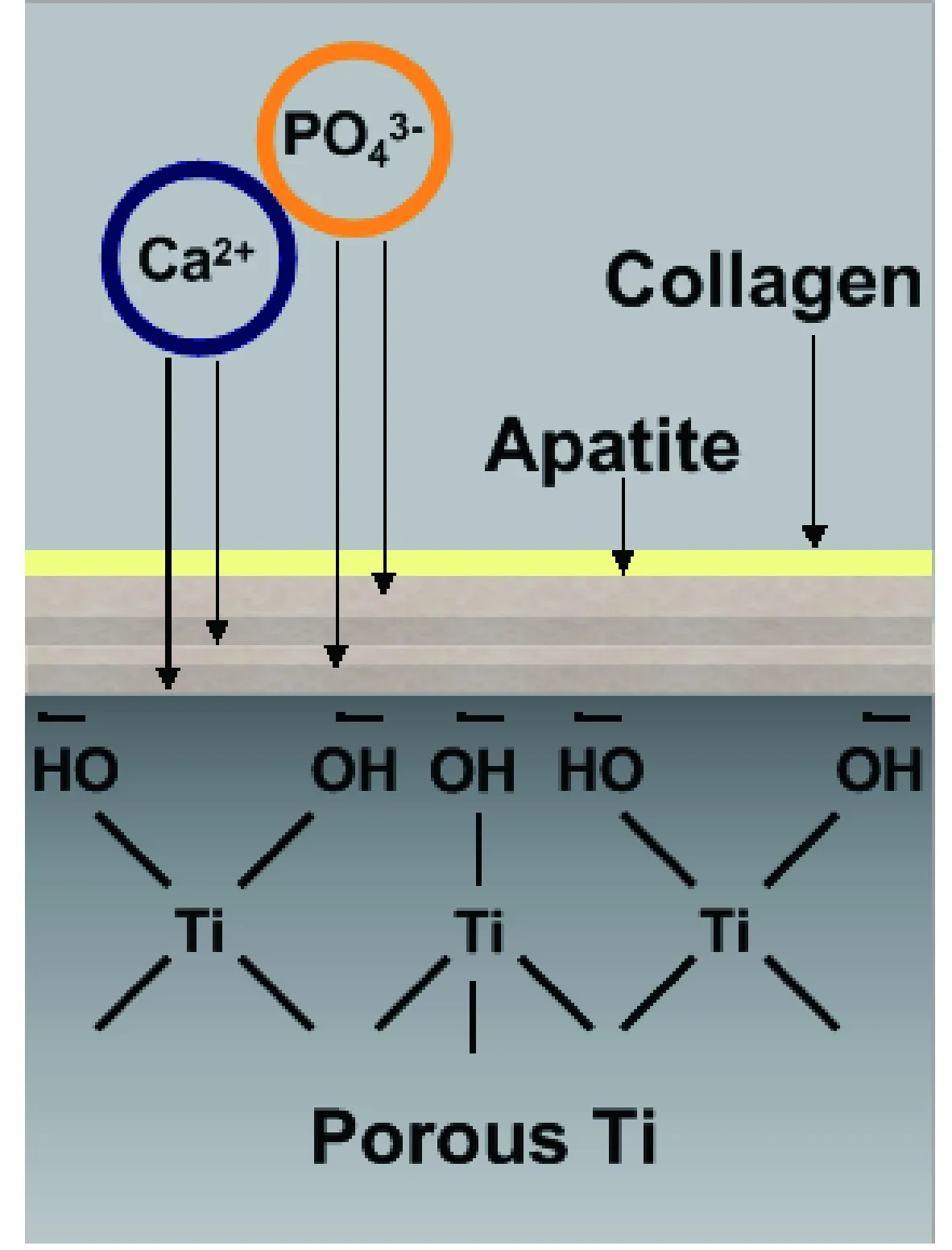
图2 多孔钛表面胶原/HA复合涂层形成机理示意图Fig.2 The mechanism schematic of the collagen/hydroxyapatite composite coating on porous titanium

表3 不同表面处理状态多孔钛MTT检测的光密度(OD)值Table 3 Optical density value of porous titanium samples with different surface conditions through MTT test
对不同方法处理后的样品进行细胞培养5 d,后进行表面形貌观察,图3a为对照组孔洞中粘附的MC3T3-E1细胞的显微照片,图3b为表面活化后多孔钛表面的SEM照片,图3c为HA改性后多孔钛表面的SEM照片,图3d为胶原+HA改性后多孔钛表面的SEM照片,通过对比发现,多孔钛表面的阴影与对照组中粘附的MC3T3-E1细胞形态一致,并结合MTT测试结果,可断定此阴影为多孔钛表面粘附的MC3T3-E1细胞。细胞在表面活化后的多孔钛表面可以粘附,但成骨细胞很难铺展,生长缓慢。沉积HA可以有效提高细胞成活率,但是对比发现,胶原/HA复合涂层表面细胞增殖最多,更有利于成骨细胞的铺展和生长,且在短时间内实现多孔钛纤维中跨丝生长,缩短成骨细胞跨纤维孔内填充生长所需时间,加速骨愈合,与MTT检测所得结果相互印证。

图3 对照组中细胞培养5 d后的细胞形貌(a)及不同表面处理状态多孔钛样品与细胞共培养5 d后的样品表面照片: (b) 表面活化,(c) HA涂层,(d) 胶原/HA涂层Fig.3 The morphology of cells in control group after incubating for 5 days (a), surface morphologies of porous titanium samples with different surface conditions after cell incubated for 5 days: (b) surface activated, (c) HA coating, (d) collagen/HA coating
4 结 论
胶原/HA复合涂层在钛纤维表面均匀附着,胶原的填充连接可修复HA涂层表面的微裂纹。胶原蛋白改性的HA表面有利于细胞附着,可提高小鼠前成骨细胞MC3T3-E1的黏附、增殖及分化,促进细胞在孔内跨纤维生长。复合涂层可以得到更好的细胞响应,对于促进早期骨与植入体的固定有很大的帮助。

