锰(II)催化甲苯胺蓝-高碘酸钾动力学反应条件的优化
韩小燕,刘彤彤
安徽公安职业学院公安科学技术系,合肥,230000
1 相关研究与问题提出
微量元素锰等在人体内含量极微,但具有重要的生物学作用,是人体代谢过程中不可缺少的微量元素,被称为“生命攸关的元素”[1]。二价锰含量的测定在日常生产和生活中有着广泛应用,不同含锰体系可以采用相应的测定方法进行分析检测。
测定锰的常用方法有分光光度法[2,3]和原子吸收光谱法[4],但普通分光光度法灵敏度低。催化动力学光度法具有灵敏度高、仪器廉价、操作简便、分析成本低、便于推广等优点。近年来,测定锰的催化动力学光度法已有不少报道[5-10]。本实验发现:在稀硫酸介质中,锰(II)对高碘酸钾氧化甲苯胺蓝褪色反应具有明显的催化效果,据此探索了测定锰(II)的催化反应的最佳条件,建立了催化光度法测定锰(II)的方法。
2 实 验
2.1 主要仪器和试剂
分光光度计(723A型,上海精密科学仪器有限公司);超级恒温槽(CS501型,重庆实验设备厂);电子天平(FA1604型,上海精密科学仪器有限公司)。
锰(II)标准溶液:准确称取分析纯MnSO4(相对分子质量:169.01) 0.100 0 g,于100 0 mL容量瓶中定容,配成浓度为1.0 g·L-1标准储备液。
甲苯胺蓝(TB)溶液:称取0.305 8 g(±0.000 1 g)甲苯胺蓝溶于少量水中,待完全溶解后移入100 0 mL容量瓶中,并用二次蒸馏水定容,即得到1×10-3mol·L-1甲苯胺蓝溶液;硫酸溶液:0.2 mol·L-1;高碘酸溶液:0.01 mol·L-1;实验所用试剂均为分析纯,水为二次蒸馏水。
2.2 实验方法
选取25 mL具塞比色管三支,第一支加入甲苯胺蓝0.8 mL,稀硫酸1.0 mL。第二支加入甲苯胺蓝0.6 mL,稀硫酸1.0 mL,高碘酸钾2.0 mL。第三支加入甲苯胺蓝0.8 mL,稀硫酸1.0 mL,高碘酸钾2.0 mL 和1 mg·mL-1锰(II)标准工作液1.5 mL。用二次水将三支比色管定容至10 mL处,摇匀半启盖,置于沸水浴中加热8 min,流水冷却5 min。用1 cm比色皿测定催化反应的最佳波长。
选取25 mL具塞比色管两支,在其中一支加入1.0 μg·L-1锰(II)标准工作液1.0 mL(催化体系),另一支比色管中不加(非催化体系)。之后在两支比色管中依次加入甲苯胺蓝0.6 mL,稀硫酸1.0 mL,高碘酸钾2.0 mL,用二次水将两支比色管定容至10 mL处,摇匀半启盖,置于沸水浴中加热8 min,流水冷却5 min。用1 cm比色皿以二次水为参比在590 nm波长下测定非催化反应溶液体系的吸光度A0和催化反应溶液的吸光度A,计算相应的ΔA=A0-A值。
3 结果与讨论
3.1 吸收光谱
图1是依据本文实验方法测得的数据绘制的各体系的吸收曲线。可见曲线 1、2 和3的最大吸收波长均为590 nm,但KIO4的加入使TB 的吸光度下降,表明在酸性介质中 KIO4可缓慢氧化甲苯胺蓝; 当在此非催化体系中加入Mn( II)后,体系的吸光度下降的幅度较大,表明锰(II)对甲苯胺蓝褪色反应具有明显的催化效果。故本实验选用590 nm为测定波长。

图1 吸收曲线
3.2 试剂用量的影响
3.2.1 酸度
分别考察中性介质(水)以及稀H2SO4对Mn2+反应体系的影响。结果表明,中性介质中无催化作用;选用浓度为0.2 mol·L-1的稀硫酸溶液作介质,催化指示反应体系有明显的效应。取2支比色管编号为1、2,加入适量甲苯胺蓝、高碘酸钾和0.5 mL稀硫酸,在2号中加入1.5 mL Mn2+(1 g·L-1),求算两者的吸光度之差为第一组。用第一组的方法改变稀硫酸的用量1.0 mL,1.5 mL,2.0 mL为第二组,第三组和第四组。实验结果发现1.5 mL的效果最好,见图2。

图2 硫酸用量的影响
3.2.2 KIO4的用量
按照3.2.1的实验方法,改变KIO4溶液的用量为0.5 mL、1.0 mL、1.5 mL、2.0 mL、2.5 mL进行测定。实验结果发现,当高碘酸钾溶液用量为2.0 mL时,ΔA最大,效果最好,见图3。

图3 KIO4用量的影响
3.2.3 甲苯胺蓝的用量
按照3.2.1的实验方法,改变甲苯胺蓝溶液的用量为0.4 mL、0.6 mL、0.8 mL、1.0 mL进行测定。实验结果发现,当甲苯胺蓝溶液的用量为0.6 mL时,ΔA最大,效果最好,见图4。
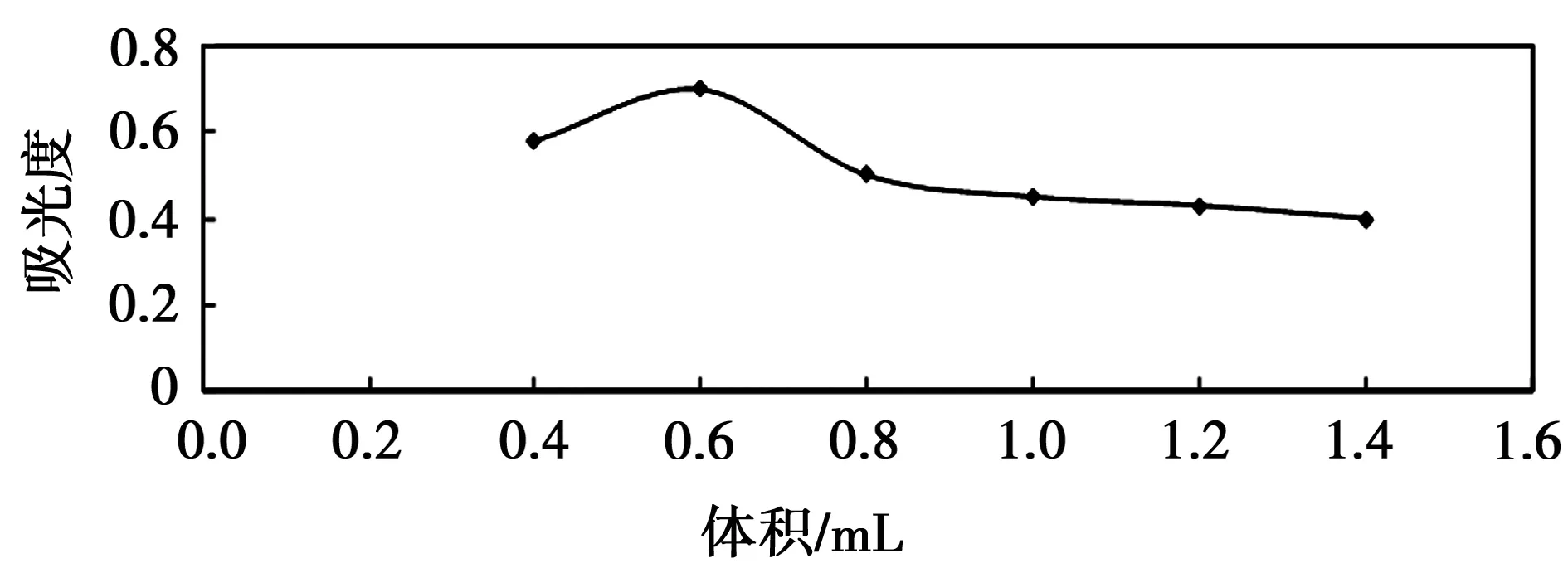
图4 甲苯胺蓝用量的影响
3.3 反应温度
在上述实验选定的条件下,按照3.2.1的实验方法,改变加热温度为50 ℃、60 ℃、70 ℃、80 ℃、90 ℃、95 ℃、98 ℃、100 ℃进行测定。结果表明:催化反应和非催化反应在50 ℃以下几乎不进行;在50 ℃~70 ℃范围内,随着温度升高,反应速率缓慢增加;在70 ℃以上,随着温度升高,反应速率急剧加快,100 ℃时达到最快。故本文采用沸水浴加热,流水冷却5 min以终止反应。在固定浓度和时间的情况下,将50~100 ℃的数据进行处理,见图5。

图5 温度对催化反应速率的影响
催化反应速率与反应时间(t)呈线性关系, 以-lnΔA对1/t作图,得到直线回归的方程为-lnΔA=740.870 8×1/t-19.673 0,相关系数为r=0.975 1 ,由此计算出反应表观活化能E=14.19 kJ·mol-1。
3.4 加热时间和表观速率常数
在实验条件确定的条件下,按照3.2.1的实验方法,改变加热时间为5 min、10 min、15 min、20 min,测定ΔA。实验结果表明,在沸水浴中,反应时间在10分钟时ΔA最大,反应时间在1~10 min范围内,ΔA随反应时间(t)呈现良好的线性关系,说明反应为一级反应,将实验数据log(A0/A)对t回归处理得动力学曲线方程:
ΔA= 0.079 5t+0.187 8,相关系数r=0.990 0。
由此求得催化反应的表观速率常数为0.078 5 s-1。
3.5 工作曲线和检出限
甲苯胺蓝0.6 mL,稀硫酸1.0 mL,高碘酸钾2.0 mL,用二次水将比色管定容,摇匀半启盖置于沸水浴中加热8 min,流水冷却5 min,在590 nm波长的条件下,准确移取Mn2+标准溶液,按实验方法测定吸光度并绘制标准曲线。结果表明,ΔA与锰(II)在2~20 μg·L-1范围内与ΔA呈良好的线性关系,其线性回归方程为:
ΔA=0.989 0 g-0.787 6,相关系数r=0.993 6
对空白进行11次平行测定的标准偏差为1.28× 10-2,检出限D=3S/K =0.039 μg·L-1。
3.6 共存离子的影响
对于10 mL溶液中10 μg·L-1Mn2+的测定,控制相对误差±5%,对常见共存离子进行干扰实验,结果表明:本催化反应有一定的选择性,大多数常见离子没有干扰,少数贵金属离子有一定的允许存在量,500倍的Mg2+、Ca2+;300倍的Ag+、NO3-; 200倍的Pb2+、Al3+;50倍的Cu2+、Cr3+、C2O42-;20倍的Zn2+、Bi3+;10倍的Sc3+、F-没有干扰,Fe3+等量时有干扰,一般所测实验中不超过这个量。
4 结 语
微量元素在人体内含量虽然极微小,但具有重要的生物学作用,大脑皮层、肾、胰、乳腺都含有锰,锰对人体的生理作用主要为:激活大量的酶类,参与多种物质代谢,能促进人体的发育且具有抗癌作用。因此,二价锰的测定方法研究一直被关注。
本研究利用锰(II)对高碘酸钾氧化甲苯胺蓝的催化作用建立了测定二价锰的催化光度法,考察了催化反应的最佳条件以及动力学参数。在最佳反应条件下,二价锰的检出限为0.039 μg·L-1,低于国家标准,选择性好。

