不同NaCl浓 度条件下亚麻籽胶对肌原纤维蛋白凝胶作用力及乳化特性的影响
冯美琴,刘雯燕,孙 健,*,徐幸莲,周光宏
(1.金陵科技学院动物科学与技术学院,江苏 南京 210038;2.南京农业大学食品科技学院,国家肉品质量安全控制工程技术研究中心,江苏 南京 210095)
肌原纤维蛋白(myofibrillar protein,MP)作为肌肉中的结构蛋白质群,除了影响肌肉的收缩及嫩度外,它也是参与乳化的主要物质,并且其受热形成的凝胶对乳化肉制品的质构、黏着性、保油保水性和出品率有直接的影响[1]。因此,MP在重组肉制品和糜类肉制品加工过程中起着重要作用[2]。另外,MP乳化凝胶作用受其理化性质的影响,例如肌肉类型、蛋白质浓度、温度、pH值和离子强度,同时受其他添加物的影响。其中,食盐是肉类加工过程中必需的辅料之一[3-4],它可以改善肉制品的保水保油能力,产品质构以及感官品质[5]。Whiting[6]研究发现在法兰克福香肠中降低NaCl含量可以增加脂肪和水在蒸煮过程中的损失。吴菊清[7]研究发现低盐条件会影响MP乳化物及乳化凝胶的水分分布,降低凝胶保水性。据报道[8]食盐的过多摄入会影响人类健康。因此在实际生产中,常常通过添加亚麻籽胶(f l axseed gum,FG)等亲水胶体改善低盐条件下造成的肉制品品质劣变。
FG是从亚麻籽中提取的一种阴离子多糖,具有良好的胶凝、发泡、乳化、保水和流变特性。Chen Haihua等[9]研究FG与肉蛋白间相互作用,发现添加FG能够显著提高蛋白质的热变性温度,并且增加保水性和硬度。孙健[10]研究发现添加FG的猪肉MP凝胶结构变得更加致密连续。Feng Meiqin等[11]研究发现MP的保水性随着FG的添加量的提高而增强。MP热诱导凝胶的功能特性(比如凝胶保水性)主要取决于化学作用力[12]。目前报道主要集中于单一理化条件下对MP的影响,本实验创新性地通过在不同NaCl浓度条件下加入FG研究其能否提高低浓度NaCl条件下的乳化凝胶特性。另外,以猪油为油相模拟简单的肉糜体系研究FG-MP的乳化作用也鲜见报道。
本实验在不同NaCl浓度条件下,研究FG-M凝胶的作用力(离子键、氢键、疏水相互作用、二硫键和非二硫键)和FG-MP凝胶的作用机理,同时以猪油为油相研究FG-MP乳液的乳析指数、脂肪微粒粒度分布、ζ-电位以及显微观察研究NaCl浓度对FG-MP乳化体系稳定性的影响,从而确定FG对MP乳化凝胶的作用机制,促进FG在肉制品中的应用。
1 材料与方法
1.1 材料与试剂
宰后24 h(pH 5.6~5.8)的猪肉背最长肌,购于南京苏果超市;猪背膘熬制,用纱布过滤得到猪油,真空包装,置于-20 ℃保存。
FG(纯度99.8%,含有16.09%蛋白质、5.10%水和4.35%灰分) 新疆绿旗公司;氯化钠、氯化钾、氯化镁、乙二醇二乙醚二胺四乙酸、Triton X-100、酒石酸钾钠、磷酸氢钾、磷酸二氢钾、氢氧化钠、牛血清白蛋白、三羟甲基氨基甲烷-盐酸、乙二胺四乙酸二钠、甲醇、十二烷基硫酸钠、尿素、碳酸钠、硫酸铜等均为分析纯。
1.2 仪器与设备
Ultra-Turrax T25 basic数显型高速分散机 德国IKA公司;AR64型高速冷冻离心机 美国Beckman-Coulter公司;M2e多功能酶标仪 美国MD公司;AUY120型天平 日本岛津公司;Worcestershire激光粒度分析仪、Nano ZS90电位仪 英国Malvern公司;DP12倒置显微镜日本Olympus公司。
1.3 方法
1.3.1 MP的提取
参照Han Minyi等[13]的方法并进行改进。称取100 g肉,用绞肉机搅碎后,加入400 mL pH值为7.0提取液(其中含20 mmol/L K2HPO4-KH2PO4、100 mmol/L KCl、2 mmol/L MgCl2、1 mmol/L乙二醇二乙醚二胺四乙酸)于1 000×g离心10 min后收集沉淀,重复2 次,期间用匀浆机处理30 s。然后向离心后的沉淀中加入400 mL提取液,再加入4 mL Triton X-100,充分混匀后1 500×g离心10 min,再向沉淀中加入400 mL 0.1 mol/L KCl溶液,1 500×g离心10 min收集沉淀,重复2 次。最后沉淀加入400 mL去离子水,1 500×g离心10 min收集沉淀,重复2 次。由以上操作得到无盐的MP,用双缩脲法测其蛋白质量浓度,密封置于4 ℃保存备用。上述过程均在4 ℃条件下进行。
将提取的蛋白分别溶于含有不同浓度的NaCl(0、0.2、0.4、0.6 mol/L)的磷酸盐缓冲液(0.05 mol/L K2HPO4-KH2PO4,pH 6.5)中,根据实验要求配制相应浓度的MP溶液,置于4 ℃保存备用。
1.3.2 FG-MP凝胶的制备
将FG与猪肉MP用匀浆机混合均匀,使MP最终质量浓度为40 mg/mL,加入质量分数0.4% FG。将配好的样品放入水浴锅,以约1 ℃/min的速率从20 ℃升温到70 ℃,保温30 min。冷却后测定相关指标。
1.3.3 FG-MP复合凝胶体系分子间相互作用力测定
有轨电车联通线类似于地铁联络线,但又不同于地铁联络线。有轨电车要实现网络化运营,需在联通运营的线路之间设置联通线。联通线宜采用互通道岔连接,由于多条线路在此交汇运营,在一定行车密度下不同运营线路的车辆可能同时到达,因此,接轨站站位和配线的设计应结合信号控制需求,以保障车辆不会由于排队而影响交叉口的正常通行为准则。
参照兰冬梅[14]的方法,称取凝胶样品3 g,加S1(0.6 mol/L NaCl,30 mL),用5 000 r/min匀浆2 min,然后放置1 h,10 000×g离心25 min后上清液保存。离心后的沉淀加S2(0.6 mol/L NaCl+1.5 mol/L尿素,30 mL),重复上述步骤,将沉淀继续加S3(0.6 mol/L NaCl+8 mol/L尿素,30 mL),重复上述步骤,向沉淀加S4(0.6 mol/L NaCl+8 mol/L尿素+0.5 mol/L β-巯基乙醇,30 mL),重复上述步骤,最后所得的沉淀加2 mL 1 mol/L NaOH溶液保存。并且所得的所有上清液分别加入相同体积的20%三氯乙酸溶液,5 500×g离心15 min,取其沉淀,向沉淀中加入2 mL 1 mol/L NaOH溶液保存,然后用Lowry法测定蛋白质的含量。上述过程均在4 ℃条件下进行。其中,S1蛋白含量代表离子键,S2蛋白含量代表氢键,S3蛋白含量代表疏水相互作用,S4蛋白含量代表二硫键,S4离心后沉淀的蛋白含量代表非二硫共价键。
1.3.4 乳化液的制备
FG添加量是依据前期研究结果[15]所得,研究发现添加质量分数0.4% FG条件下,乳液能够保持相对稳定,并且在低离子强度(0、0.2 mol/L NaCl)条件下没有发生乳析现象。
将质量分数0.4% FG溶解于0、0.2、0.4、0.6 mol/L不同浓度NaCl的MP溶液中,使MP最终质量浓度为10 mg/mL。再分别将含有FG和不含FG的MP溶液中加入10%猪油,8 000×g匀浆制成乳状液。上述过程均在40 ℃条件下进行。准备的乳化液要在24 h之内使用。
1.3.5 乳化稳定性的测定
将待测样品置于玻璃试管(1.0 cm×15 cm)中,在常温条件下静置3 h及30 d记录乳析界面高度的变化。乳析指数按下式计算:
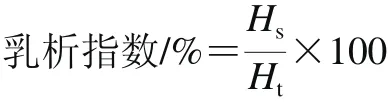
式中:Hs为清液的高度/cm;Ht为乳化液的初始高度/cm。
1.3.6 ζ-电位的测定
1.3.7 脂肪微粒粒度分布测定
参考Ahmed等[16]的方法并进行修改。其中,颗粒折射率为1.520,分散剂为水,分散折射率为1.330,颗粒吸收率为0.001,分析模式为通用球形,进样器名为Hydro 2000 MU(A),噪音为30 s。采用Mastersizer 3000型激光粒度分析仪进行测定,得到脂肪微粒粒度分布图谱。数据结果用平均粒径D4,3表示。
1.3.8 光学显微镜
乳液的微结构研究使用光学显微镜观察。将乳液滴到载玻片上并用盖玻片覆盖。使用显微镜数字照相机(OlympusDP12,Tokyo,Japan)连接到软件(Olympus DP12,Tokyo,日本)安装在计算机上。
1.4 数据统计分析
每个实验重复3 次,采用SAS 9.2统计软件计算。采用Duncan’s multiple range test程序分析平均值和差异,并在显著性水平P值小于0.05时进行单因素方差分析和t检验,评估样本组之间的差异。
2 结果与分析
2.1 不同NaCl浓度条件下FG对MP凝胶体系分子间相互作用力的影响
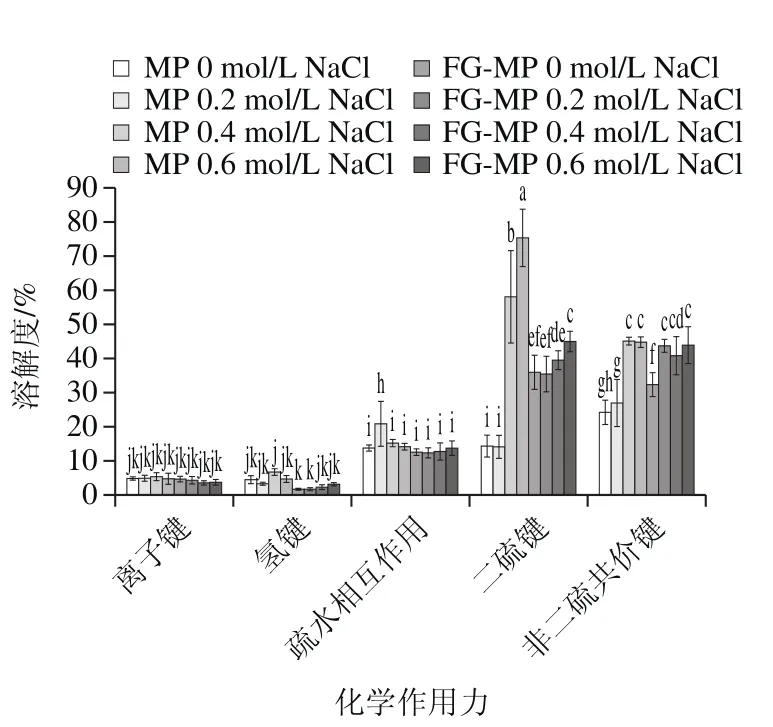
图1 不同NaCl浓度条件下FG对MP凝胶体系分子间相互作用力的影响Fig. 1 Effects of different NaCl concentrations and FG on the chemical interactions of MP gel
如图1所示,MP凝胶中疏水相互作用、二硫键以及非二硫共价键所占的比例较大,而离子键和氢键所占比例较小。兰冬梅[14]在研究罗非鱼肌肉蛋白凝胶过程中也发现了类似的结果。随着NaCl浓度的提高,可以看出二硫键和非二硫共价键的含量是随之升高的(P<0.05)。并且当NaCl浓度达到0.6 mol/L时,在不含FG的MP凝胶中二硫键含量是最高的。关于疏水相互作用,不含FG的MP凝胶出现了先升高后降低的现象,在0.2 mol/L NaCl条件下达到最大。而在实验范围内,离子键和氢键的含量无显著变化(P>0.05)。另外,相对于对照组,FG-MP凝胶的作用力随着NaCl浓度的变化相对平稳。
研究FG和MP间的化学作用力可以对FG在肉制品的应用具有更好的指导作用。随着MP凝胶的形成,MP分子开始变性并有序聚集,形成三维网状结构,而最终体系中蛋白分子的相互作用力会达到一种新的平衡状态[17-18]。其中,蛋白分子间的相互作用力主要包括离子键、氢键、二硫键、疏水相互作用、非二硫共价键等[19]。在凝胶形成的前期,离子键和氢键开始断裂,蛋白变性,疏
水基团和活性巯基开始外露[20]。在热处理过程中,疏水基团和活性巯基逐渐从分子内部暴露,体系产生疏水相互作用,造成肌球蛋白分子聚集[21]。而此时活性巯基发生氧化或—SH/S—S交换反应[22],形成二硫键。与此同时,非二硫共价键也开始形成[23],最终形成凝胶的网络结构。随着NaCl浓度的提高,二硫键和非二硫共价键的含量随之升高(P<0.05),这主要与MP的盐溶性有关。从图1可以看出,MP凝胶中疏水相互作用、二硫键以及非二硫共价键所占的比例较大,而离子键和氢键所占比例较小。这说明形成凝胶体系的关键是二硫键和非二硫共价键的贡献。而离子键与氢键不是维持MP凝胶及FG-MP凝胶稳定构象的主要化学作用力。据报道,这可能是由于在凝胶形成过程中,离子键和氢键参与肌球蛋白分子尾部的缠绕,而不参与头部的聚集[24]。
2.2 不同NaCl浓度条件下FG对MP乳液乳析指数的影响
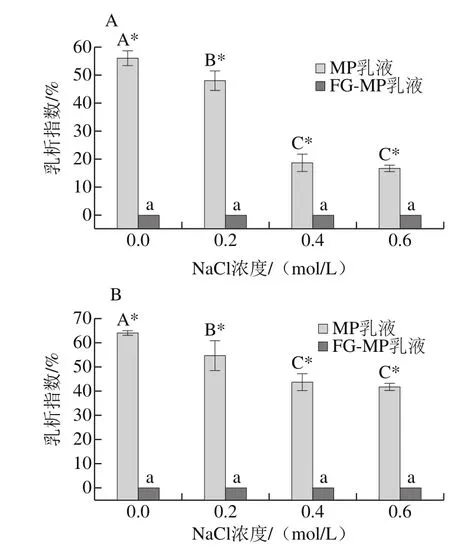
图2 不同NaCl浓度条件下FG对MP乳液3 h(A)和30 d(B)乳析指数的影响Fig. 2 Effects of different NaCl concentrations in the absence and presence of FG on the creaming index of emulsions with MP at 3 h (A) and 30 d (B)
乳析指数可以从宏观角度表征乳液的乳化稳定性,乳析指数越低,说明乳化液越稳定。从图2可以看出,MP乳液受NaCl浓度的影响显著(P<0.05),并且随着NaCl浓度的提高,乳析指数显著降低,乳液更加稳定。如图2A所示,NaCl浓度为0、0.4、0.6 mol/L时,乳析指数为56%、18.67%、16.67%。这可能是由于盐离子增大了MP的溶解度,使MP更好地包裹在油滴表面,从而提高了乳化稳定性[25]。贾娜等[26]也报道了相似的现象,研究发现MP-混合食用胶乳液在低盐条件下,随着盐浓度的提高,乳化稳定性也随着增加。值得注意的是,FG-MP乳液不受NaCl浓度的影响,并且在贮存期间没有发生乳析现象(P>0.05),一直保持稳定状态。FG添加到MP乳液后,具有乳化作用的FG包裹在油滴表面或者部分FG包裹在MP膜的表面,使油滴更加稳定。并且据Wang Meng等[27]研究报道,FG还可以增强流动相的黏度,降低油分子的运动,防止其碰撞造成乳液的絮凝。另外,对比图2A、B可以发现,当乳液放置30 d后,MP乳液在0.4 mol/L和0.6 mol/L NaCl条件下乳析指数明显升高,即乳化稳定性明显降低。如0.2 mol/L NaCl条件下,乳液的乳析指数从48%升高至54.7%,而0.4 mol/L NaCl条件下,乳液的乳析指数从18.67%升高至43.7%。这说明高浓度NaCl条件下,MP乳液受贮藏时间影响较大。这可能是由于高浓度NaCl条件下,静电斥力的减小使得乳化颗粒更容易聚集形成大颗粒,从而发生乳析现象。
2.3 不同NaCl浓度条件下FG对MP乳液ζ-电位的影响
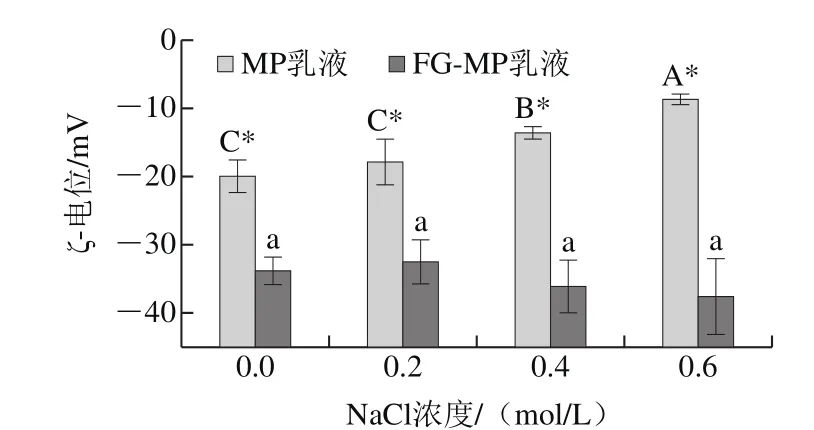
图3 不同NaCl浓度条件下FG对MP乳液ζ-电位的影响Fig. 3 Effects of different NaCl concentrations in the absence and presence of FG on the zeta potential of emulsions with MP
含有10%猪油的乳化液在不同NaCl浓度条件下电位的变化,如图3所示。在实验范围内,所有乳化液都处于负电荷状态。FG-MP乳液比MP乳液电位的绝对值更大,这可能与FG是阴离子多糖有关[28]。而MP乳液的电位值比FG-MP乳液受NaCl浓度的影响更大,这与图1中乳析指数的结果相一致。并且对于MP乳化液,随着NaCl浓度的提高,电位的绝对值逐渐减少(P<0.05),在0.6 mol/L NaCl达到最小值。而对于FG-MP乳液,其电位的绝对值随着NaCl浓度的提高略有升高(P>0.05)。表面电位是用于评价乳化稳定性的重要参数。电位的绝对值越大则说明油滴之间的静电斥力越大,防止油滴聚集成大颗粒,有助于乳化液的稳定性。结果表明,Na+浓度不对FG-MP乳液的稳定性起着重要的作用(P>0.05)。这可能是由于FG包裹在MP表面,使其受NaCl浓度的影响较小。Abdolmaleki等[29]报道了类似的结果,研究发现NaCl浓度对黄蓍胶乳液稳定性没有显著影响。而在MP乳化液中,MP受NaCl浓度影响较大(P<0.05)。据悉,羧基在蛋白质分子外围非常活跃,创造一种阴离子环境[30]。随着盐加入到乳液中,Na+与羧基基团结合,从而导致负电荷减少。
2.4 不同NaCl浓度条件下FG对MP乳液粒径的影响
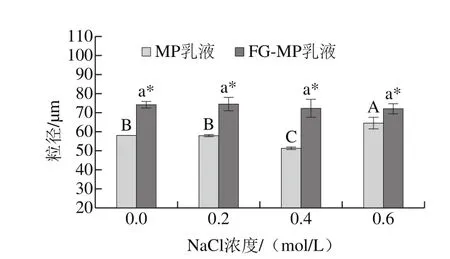
图4 不同NaCl浓度条件下FG对MP乳液粒径D4,3的影响Fig. 4 Effects of different NaCl concentrations in the absence and presence of FG on the particle size (D4,3) of emulsions with MP
如图4所示,含有FG的乳液微粒粒径均高于不含FG的乳液微粒粒径。并且含有FG的乳液微粒的粒径随NaCl浓度的增高略有降低,但是变化不显著(P>0.05),可能与多糖受NaCl影响较小有关[29]。而不含FG的MP乳液的粒径受NaCl浓度的影响显著(P<0.05)。随着NaCl浓度的增加,D4,3呈现了先减小后增大的趋势,在0.4 mol/L NaCl条件下,颗粒粒径达到最小值。其趋势与前人研究结果相似[31]。这可能是因为MP的溶解度随着NaCl浓度的提高而增大,使得更多的MP包裹在油滴表面,导致油滴粒径的降低。但是当NaCl浓度提高到一定值,静电斥力的降低使得油滴靠近,从而形成更大的粒径。
2.5 MP乳液及FG-MP乳液的显微观察结果
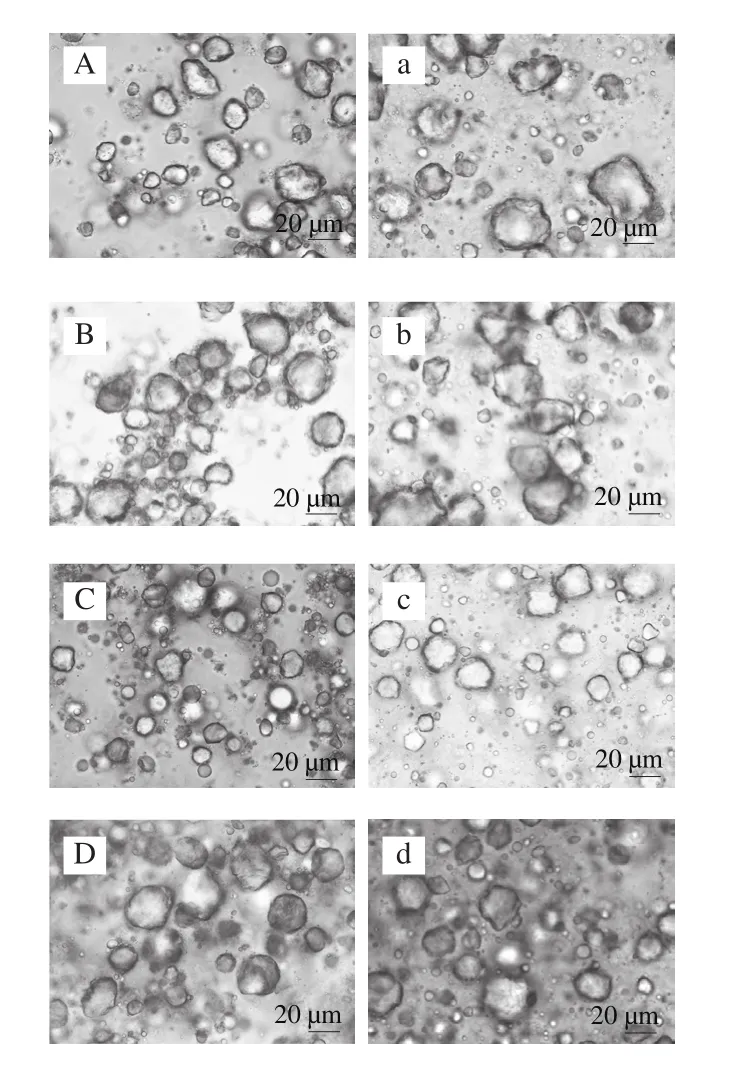
图5 MP乳液和FG-MP乳液在不同浓度NaCl条件下的微观图Fig. 5 Light micrographs of emulsions containing MP and FG
由图5可以看出,猪脂肪颗粒被分散成球状油滴分散在连续相中,并且颗粒大小与图4结果基本一致。不含FG的MP乳液随着NaCl浓度的增加,颗粒大小呈现了先减小后增大的趋势,在0.4 mol/L NaCl条件下,颗粒粒径达到最小值。含有FG的乳液微粒的粒径随NaCl浓度的增高,变化不明显。并且发现,虽然不含FG的乳液粒径小于含有FG的乳液粒径,但是出现了相互聚集的趋势。这可能与电位有关,静电斥力减少,使得颗粒相互靠近,出现了聚集的现象。
3 结 论
本实验通过凝胶作用力的测定发现维持MP凝胶及FG-MP凝胶稳定构象的关键是二硫键和非二硫共价键的贡献。另外,通过测定乳液的相关指标发现虽然MP乳液随着NaCl浓度的提高,乳化稳定性得到明显提高,但是在高浓度NaCl条件下容易受到贮藏时间的影响。而FG-MP乳液在所有NaCl浓度范围内均没有发生乳析现象,尤其是低浓度NaCl条件下FG-MP乳液的稳定性显著高于MP乳液。相对于对照组,添加FG的MP乳液的电位值和粒径大小受NaCl浓度变化不显著,说明FG可以抵抗NaCl浓度的变化对电位及粒径的影响。显微观察发现FG的加入可以改善MP乳液出现的液滴聚集的现象。这说明添加FG可以显著提高MP乳液的乳化稳定性,并且能够大大提高其抗盐能力。因此,可以在实际生产应用中通过添加FG,改良肉制品品质,减少食盐摄入量,达到促进人体健康的目的,为低盐肉制品的开发提供了一定的理论依据。

