耐高盐碱蓬对湿地土壤中金属元素的富集特征研究
张乐添,李景喜,温永红,孙承君,郑 立,蒋凤华,陈发荣
(1.青岛科技大学 化学与分子工程学院,山东 青岛 266042;2.国家海洋局第一海洋研究所 海洋生态研究中心,山东 青岛 266061;3.青岛海洋科学与技术国家实验室海洋药物与生物制品功能实验室,山东 青岛 266071)
湿地是地球上水陆相互作用形成的独特生态系统,作为水陆过渡带,具有巨大的环境调节功能和生态效益[1-2]。近年来由于自然因素和人类生产活动的影响,各地的湿地处于不断退化或即将退化的过程中。目前,随着环境科学的不断发展,湿地重金属污染已成为国内外湿地环境污染的一项重要研究内容,湿地中重金属是一类难降解、易积累的持久性有毒污染物,通常由自然因素和人为因素所致,其中自然因素包含岩石的风化、酸雨等;人为因素有工农业生产、化肥的使用、汽车尾气的排放等[3-4]。湿地中某些重金属元素(Cd、Pb、Hg、Cr、As)的含量高于自然背景水平,可导致湿地生态环境的破坏。较高浓度的重金属可抑制植物对Ca、Mg的吸收,使植物表现出叶片发黄甚至坏死,根系不发达,以及植株矮小等症状[5];并且重金属可通过植物的吸收进入食物链,对生态系统构成一定的威胁[6]。
湿地中重金属的分布特征及修复技术已有报道,特别是植物对湿地中的重金属修复已成为研究重点,植物修复湿地中重金属主要基于植物可耐受或超积累某些特定的重金属污染物。目前植物修复技术主要分为3类:①植物挥发:利用植物将吸收到体内的重金属转化成气态物质,释放到大气中,从而减少土壤中的一些挥发性污染物;②植物提取:利用植物吸收、积累重金属的特性,通过植物自身或人为诱导的方法使植物将土壤中的重金属转移到地上部分,再通过收割的方式减少土壤中的重金属含量;③植物稳定:利用植物的根吸附积累重金属或利用其分泌物将重金属沉淀或还原,使重金属的生物有效性降低,减少被其他植物吸收的可能性等[7-8]。
因此,基于湿地中的植物对重金属的吸收、代谢和累积作用,其对重金属的富集能力决定了湿地的净化能力和植物的配置原则,且不同科属的湿地植物对重金属的富集能力不同。一年生草本植物耐高盐碱蓬一般生长在荒野滩涂,适应能力较强,能在易富集重金属的湿地、沿海滩涂和潮滩等高盐碱环境中正常生长[9],并对Cu、Pb、Zn、Cd、Ni和As等重金属有着很好的耐受性[10],将该植物用于湿地修复,在净化土壤的同时,还能起到固土护堤[11]、调节气候的作用。本文通过在秦皇岛滨海湿地种植耐高盐碱蓬,观测湿地土壤沉积物及耐高盐碱蓬中不同金属元素的含量与变化,分析耐高盐碱蓬根、茎、叶对金属元素的富集特征,以及不同金属元素在碱蓬中的迁移规律,以期为利用碱蓬进行湿地中重金属的修复提供技术支撑及理论基础。
1 实验部分
1.1 仪器与试剂
Agilent 7500a电感耦合等离子体质谱(美国安捷伦公司);MARS密闭微波消解仪(美国CEM公司);Milli-Q超纯水处理系统(美国Millipore公司,电阻率18.2 MΩ·cm);真空冷冻干燥机(美国Labconco公司);AL104 型电子天平(瑞士Mettler-Toledo 公司)。
浓HNO3、H2O2、HF(优级纯,德国Merck公司);多元素混合标准溶液10 mg·L-1及50 μg·L-1Li、Sc、Ge、Y、In、Tb和Bi混合内标溶液(美国SPEX CertiPrep公司);液氩(纯度99.999%);土壤、沉积物成分分析标准物质(GBW07434)及灌木枝叶成分分析标准物质(GBW07603(GSV-2)(国家标准物质中心)。
1.2 试验区及样品的采集
试验区为秦皇岛滨海湿地(119°30′49.57″E~119°31′3.30″E,39°50′20.11″N~39°50′10.33″N,图1),布设16个站位采取沉积物样品(Q01~Q16),其中在Q01、Q08、Q11、Q13、Q15站位分别采集碱蓬植物(每站3~5株)。碱蓬选取生长状态良好的植株,生长周期为4个月,株高约18 cm,采集时保持根部完整,现场采集的植物与沉积物样品于密封袋中密封保存。
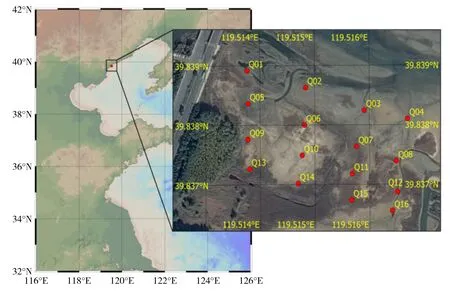
图1 样品采集站位图Fig.1 Sampling stations
1.3 样品预处理及测定
碱蓬样品用水洗净后,用超纯水洗涤3次,风干,将同一站位采集的不同株碱蓬按根部、茎部、叶片分类混合,在真空冷冻干燥机中冷冻干燥、粉碎后混合均匀,称取0.20 g干样品于聚四氟乙烯(PTFE)消解罐中,加入6 mL HNO3+2 mL H2O2,按表1程序进行消解;待样品消解完毕后,用超纯水定重至20.00 g,待测。

表1 微波消解工作参数Table 1 Working parameters of microwave digestion
沉积物样品冷冻干燥、粉碎过筛(80目)后,准确称取0.10 g干样品于聚四氟乙烯(PTFE)高压密封罐中,加入5 mL HNO3+2 mL H2O2+1 mL HF,于80 ℃消解2 h,放气稳定后于120 ℃再消解2 h,冷却、赶酸后用超纯水定重至20.00 g,待测。
沉积物与植物消解溶液均利用Agilent 7500a ICP-MS进行测定,标准溶液和样品溶液测定时均在线加入内标进行仪器校准,内标溶液为50 μg·L-1Li、Sc、Ge、Y、In、Tb、Bi。为考察方法的可靠性与准确度,在相同实验条件下对土壤、沉积物成分分析标准物质(GBW07434)和灌木枝叶成分分析标准物质(GBW07603(GSV-2))进行金属元素测定。
1.4 数据处理与分析
利用富集系数(Enrichment factor,EF)和转移系数(Translocation factor,TF)对研究区域中植物的富集特征进行评估,其计算公式分别为:富集系数(EF)=CX/C沉积物;转移系数(TF)=CX1/CX2。CX为植物不同部位中重金属的浓度,C沉积物为植物附近沉积物中重金属浓度。植物对重金属的富集系数可反映出植物对土壤中不同重金属的吸附效果[12]。CX1、CX2分别为植物不同部位的重金属浓度。重金属在植物体内的转移系数能够提示重金属在植物体内的迁移过程和积累情况[13]。
2 结果与讨论
2.1 湿地沉积物中重金属含量分析
为考察湿地表层沉积物中重金属的分布特征,首先对16个站位沉积物中的Cr、Fe、Mn、Ni、Cu、Zn、As、Mo、Cd和Pb 10种金属元素含量进行测定(表2)。结果显示,沉积物中不同金属元素的平均含量由高至低顺序为Fe>Mn>Zn>Cr>Pb>Ni>Cu>As>Mo>Cd,平均值与中位数近似,表明采样数据在高浓度与低浓度之间分布较平均,不同重金属含量的变化范围不大,最大值与最小值之间比值较大的为Cd、Ni、Cu、Mo和Pb,其值分别为4.25、2.88、2.81、2.75与2.20。相对标准偏差可反映采样总体中各样点之间的平均变异程度[12],从结果可知Cd的相对标准偏差最大(为58.51%),在空间变异程度中属于强变异类型,表明Cd在空间中分布不均匀,离散性较大,其他9种金属元素(Cr、Fe、Mn、Ni、Cu、Zn、As、Mo、Pb)的变异程度较小,相对标准偏差分别为15.72%、7.04%、10.81%、25.35%、23.26%、15.91%、11.74%、29.92%、20.74%,空间分布较均匀,波动较小。
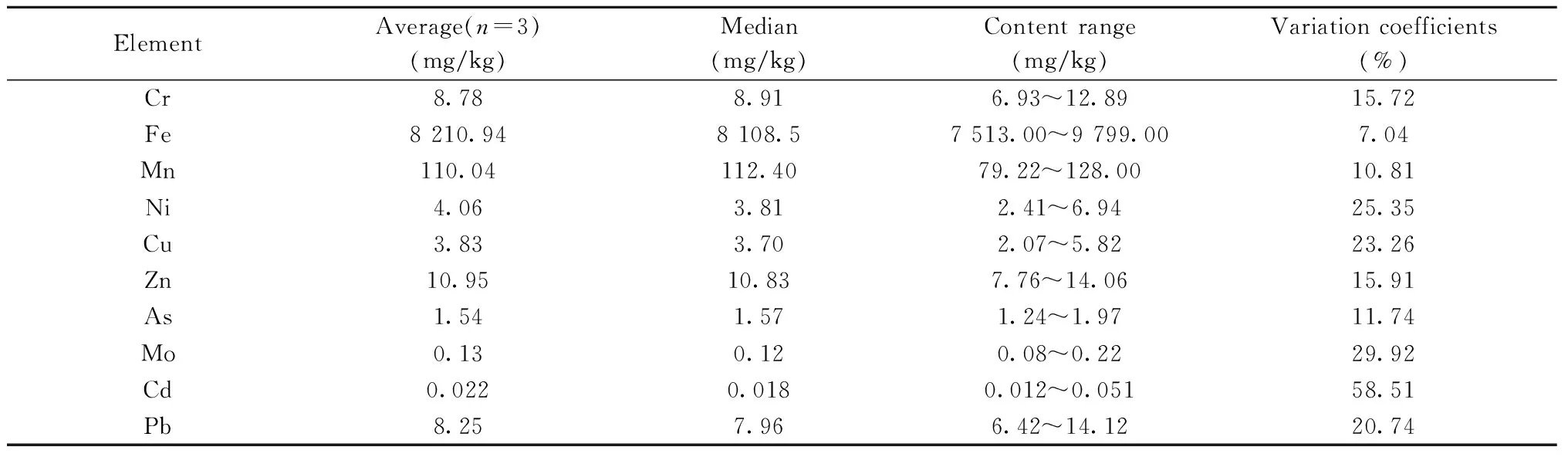
表2 湿地沉积物中的重金属含量Table 2 Levels of heavy metal in sediment from wetland
2.2 碱蓬中不同部位重金属的含量分析
碱蓬体内不同部位的重金属含量如表3所示,由平均值可知,碱蓬不同部位的重金属含量存在差异,Mn、Ni、Cu、As、Cd和Pb的含量大小顺序为根>叶>茎,Fe的含量顺序为根>茎>叶,Cr的含量顺序为茎>根>叶,Zn和Mo的含量顺序为叶>根>茎。比较各站位数据可知,在根中Q01站位的Fe、Mn、Ni、As、Mo、Pb和Q15站位的Cd含量明显高于平均含量,在茎中Q01站位的Fe、Mn、Cu和Q15站位的Cr含量明显高于其他站位,在叶中Q08站位的Mo和Q11站位的Mn含量明显高于平均含量,而Q01站位的Cd含量明显低于平均含量。不同金属元素在沉积物及碱蓬中的含量相关性分析显示[13],根、茎、叶中重金属含量与不同站位沉积物中重金属含量之间呈显著正相关,相关系数大于0.999 5。
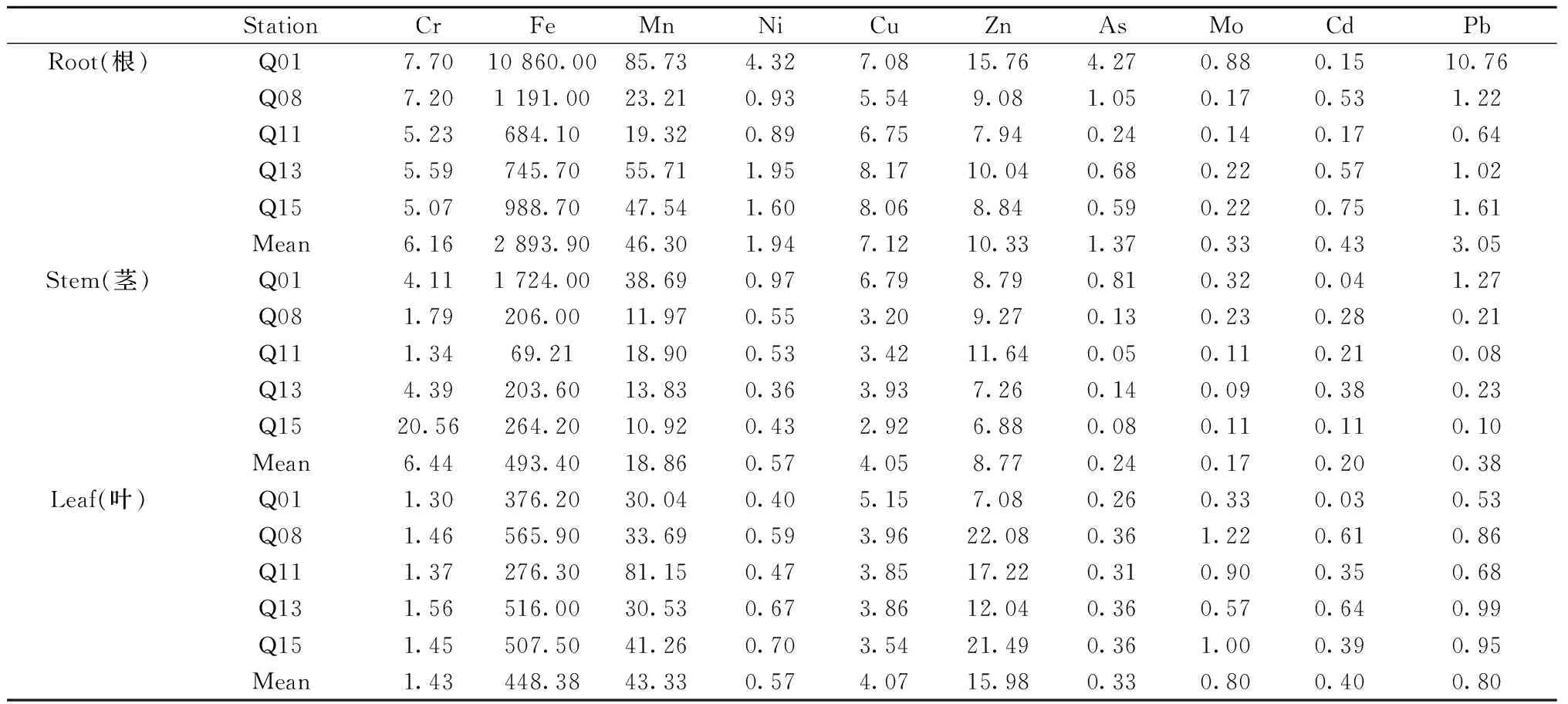
表3 重金属在碱蓬不同部位的分布Table 3 Distribution of heavy metal in different plant organs (mg/kg,n=3)
2.3 方法学考察
测得土壤、沉积物成分分析标准物质中的金属元素含量为:Cr 89.2 mg/kg(标准值94.0±3.0 mg/kg),Fe 4.10 mg/kg(标准值4.45±0.04 mg/kg),Mn 0.54 mg/kg(标准值0.60±0.01 mg/kg),Ni 39.5 mg/kg(标准值41.3±1.9 mg/kg),Cu 30.1 mg/kg(标准值28.8±2.0 mg/kg),Zn 80.1 mg/kg(标准值77.2±3.2 mg/kg),As 17.2 mg/kg(标准值15.9±1.0 mg/kg),Mo 1.12 mg/kg(标准值1.08±0.06 mg/kg),Cd 0.033 mg/kg(标准值0.037±0.008 mg/kg)和Pb 28.9 mg/kg(标准值30.8±1.4 mg/kg),各元素的回收率为89.2%~108%,相对标准偏差(RSD)小于10%。测得灌木枝叶成分分析标准物质中的金属元素含量为:Cr 2.4 mg/kg(标准值2.6±0.2 mg/kg),Mn 59 mg/kg(标准值61±5 mg/kg),Ni 1.5 mg/kg(标准值1.7±0.3 mg/kg),Cu 7.2 mg/kg(标准值6.6±0.8 mg/kg),Zn 21.6 mg/kg(标准值20.6±2.2 mg/kg),As 1.33 mg/kg(标准值1.25±0.15 mg/kg),Mo 0.26 mg/kg(标准值0.28±0.05 mg/kg),Cd 0.35 mg/kg(标准值0.38 mg/kg),Pb 44 mg/kg(标准值47±3 mg/kg),各元素的回收率为88.2%~109%,RSD小于8%,表明检测方法的准确度和重现性较好。

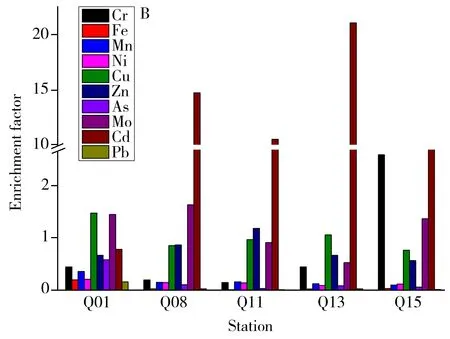
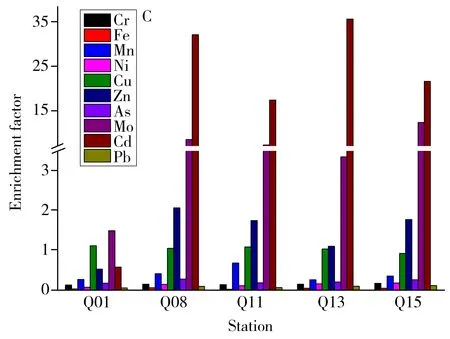
图2 碱蓬不同部位的金属富集系数Fig 2 Enrichment factors of different organsA.root;B.stem;C.leaf
2.4 碱蓬不同部位对金属的富集系数
土壤中植物不同部位对重金属的富集系数(EF)可反映其对不同重金属的吸附效果[14],EF数值越大,说明植物对重金属的吸收效果越好。研究结果显示:碱蓬根部(图2A)的金属富集系数平均值由大到小的顺序为:Cd>Mo>Cu>As>Zn>Cr>Ni>Mn>Pb>Fe,平均值分别为22.53、2.08、1.86、0.99、0.90、0.68、0.47、0.43、0.38、0.34。Q01站位,碱蓬根部对Cd的富集系数均远小于其他站位,对Fe的富集系数远大于其他站位,根部对其他元素的富集系数在各站位变化不大,Cu和Mo的富集系数高于Cr、Fe、Mn、Ni、Zn、As、Pb,而Fe的富集系数最低。碱蓬茎部(图2B)的金属富集系数平均值由大到小的顺序为:Cd>Mo>Cu>Zn>Cr>Mn>As>Ni>Fe>Pb,平均值分别为10.65、1.18、1.03、0.79、0.77、0.18、0.17、0.14、0.06、0.05。由平均值可知,碱蓬茎对Cd的富集系数最高,对Pb的富集系数最低,其中Mn、Ni、Cu、Zn、Mo在各站位的富集系数分布较为平均,Q15中Cr和Q01中Fe、As、Pb的富集系数远高于其他站位,而Q01中Cd的富集系数远低于其他站位。在叶中(图2C)的富集系数平均值由大到小的顺序为:Cd>Mo>Zn>Cu>Mn>As>Cr>Ni>Pb>Fe,平均值分别为20.02、6.71、1.45、1.05、0.41、0.23、0.16、0.15、0.10、0.05。在碱蓬叶中,Cd的富集系数最大,Fe的富集系数最小,Q15中Mo的富集系数远高于其他站位,Q01中Cd的富集系数远低于其他站位,Cr、Fe、Mn、Ni、Cu、Zn、As和Pb的富集系数在各站位变化不大。由平均值可知,碱蓬茎的富集系数除Cr外均低于根和叶中的富集系数,除Zn和Mo外,在根中的富集系数高于叶中的富集系数。
另外,植物地上部分对重金属的富集系数>1时,能够通过收获植物地上部分的方式将重金属元素移出生态系统[15]。由表4可知,所有站位中碱蓬地上部分的富集系数由高到低依次为Cd>Mo>Zn>Cu>Cr>Mn>As>Ni>Pb>Fe,Cd的平均富集系数最大(32.13),Fe的富集系数平均值最小(0.11),其中Cd、Mo、Zn和Cu富集系数的平均值>1,由此可以看出,碱蓬地上部分对Cd和Mo的富集效果最好,Zn和Cu次之,富集Cr、Mn、As、Ni 、Pb和Fe的效果相对较差。

表4 生物富集系数(C地上部分/C沉积物)Table 4 Bioconcentration factor(Caboveground/Csediment)
2.5 重金属在植物体内的迁移与积累
重金属在植物体内的转移系数(TF)显示了重金属在植物体内的迁移过程和积累情况[16],制约金属离子从根部转移到茎部有两个因素:①碱蓬根系的吸收蛋白将重金属元素吸收到根部的细胞中,再通过转运蛋白转移到木质部中,在此过程中,重金属离子需通过专一通道或由特异性蛋白转运进入木质部,木质部装载的选择性导致了不同重金属积累在碱蓬体内的不同部位;②叶部叶肉细胞随蒸腾流吸收重金属。表5的研究结果表明,一些重金属在碱蓬体内TF叶/根<1且TF叶/茎>1(如Fe、Ni、Pb、As、Cu),说明碱蓬根部中这些重金属含量明显高于叶和茎中的含量,另一些重金属在碱蓬中TF叶/根>1且TF茎/根<1(如Mn、Zn、Mo、Cd),说明碱蓬将这些重金属储存在叶中,而只有Cr被储存在茎中(TF茎/根>1且TF叶/根<1),说明碱蓬中根和叶是主要重金属积累器官,碱蓬将Fe、Ni、Pb、As、Cu固定在根部,而Mo、Zn、Cd、Mn能够由根部迁移到叶中,并在叶中储存。一般情况下,普通植物体内重金属含量过高会导致植物植株矮小,叶片发黄,甚至死亡,但重金属耐受性植物能够通过根部细胞分泌的有机酸与重金属络合,使重金属的毒性降低,同时增加重金属的溶解性和可移动性,提高重金属运输到根系的速率,并且植物细胞的分区室化也能使重金属的毒害作用降低;液泡能够通过主动运输的方式吸收重金属,将之与其中的有机酸和蛋白质结合而储存在液泡中,通过挥发或落叶等形式将重金属排出体外[17-20]。因此,本研究中不同重金属的迁移与富集特征,可为耐高盐碱蓬对湿地重金属的修复提供理论基础。

表5 重金属的转移系数Table 5 Translocation factor of heavy metal
3 结 论
本文通过对秦皇岛湿地沉积物中的重金属含量以及耐高盐碱蓬对重金属元素的富集和迁移的研究,得出以下结论:研究选取的湿地修复试验区内土壤沉积物中金属元素的分布较均匀,多数金属元素的变异程度较小;金属元素在碱蓬根、茎、叶中的含量分布存在较大差异,其中Fe、Mn、Ni、Cu、As、Cd和Pb的含量在根中最高,Cr的含量在茎中最高,Zn和Mo的含量在叶中最高,植物的根、茎、叶与沉积物中重金属含量呈显著正相关。从碱蓬的富集系数可见,碱蓬叶片对Cd的富集能力最强,并且Cu、Zn、Mo、Cd的吸收系数均大于1,说明碱蓬能将土壤中的Cu、Zn、Mo、Cd移出。Fe、Ni、Pb、As、Cu等重金属在碱蓬体内的迁移效率较低,被储存在碱蓬的根部,Mo、Zn、Mn、Cd等重金属在碱蓬体内传输效率较高,能从根部转移到叶片贮存,可通过挥发或落叶的形式将重金属排出体外。上述研究结果在湿地土壤中重金属的修复方面具有一定应用价值。

