腹主动脉瘤腔内修复术中行移植物旁瘤腔栓塞预防Ⅱ型内瘘疗效分析
陈宏宇,戴贻权,庄 晖,詹腾辉,陈 诚,郭平凡
(福建医科大学附属第一医院血管外科,福建 福州 350004)
近年来,对符合适应证范围的腹主动脉瘤患者,腹主动脉瘤腔内修复(endovascular aortic aneurysm repair, EVAR)治疗已逐渐取代开放手术修复(open surgical repair, OSR)成为最主要的治疗方式。与OSR相比,EVAR具有围手术期并发症少、手术相关死亡率低和患者住院时间短等优势[1-3],但EVAR移植物相关并发症不容忽视,EVAR术后60%的并发症均由内瘘所致[1]。有研究[4]报道,EVAR术后1个月内Ⅱ型内瘘发生率为7%~44%。临床对持续存在且导致瘤腔扩张的Ⅱ型内瘘多采取积极的治疗方式[5],干预方式多样,但目前尚无公认的最佳处置方案。本研究评估EVAR术中移植物旁瘤腔栓塞预防Ⅱ型内瘘的有效性和安全性。
1 资料与方法
1.1 一般资料 回顾性分析2011年1月—2017年6月我院收治的69例腹主动脉瘤患者的资料,其中男52例,女17例,年龄55~88岁,中位年龄71(65,76)岁;均接受EVAR治疗,其中33例(研究组)EVAR术中接受移植物旁瘤腔栓塞,36例(对照组)接受单纯EVAR。研究组中,男24例,女9例,年龄57~86岁,中位年龄74(68,77)岁;对照组中,男28例,女8例,年龄55~88岁,中位年龄70(64,76)岁。2组间年龄(Z=1.125,P=0.264)、性别(χ2=2.326,P=0.127)差异均无统计学意义。
1.2仪器与方法 采用Toshiba INFX-8000C DSA机引导EVAR治疗。术前常规通过CTA评估腹主动脉瘤,观察腰动脉、肠系膜下动脉位置并测量其直径,选取远端锚定区,测量髂股动脉直径。术中患者取平卧位。对照组中,全身麻醉4例,双侧腹股沟区局部麻醉32例;研究组中,全身麻醉3例,双侧腹股沟区局部麻醉30例。根据术前CTA判断的腰动脉位置、瘤腔大小等选择适当手术入路及支架移植物。
对照组:8例(8/36,22.22%)为经皮穿刺双侧股总动脉入路,25例(25/36,69.44%)切开暴露双侧股动脉,3例(3/36,8.33%)切开暴露单侧股动脉并经皮穿刺另一侧股动脉,行标准EVAR术式;术中支架移植物使用情况: 7例(7/36,19.44%)采用Gore Excluder或Gore C3 Excluder 型(Gore & Associates公司),20例(20/36,55.56%)选用Endurant型(Medtronic公司),3例(3/36,8.33%)选用Zenith型(Cook公司),3例(3/36,8.33%)选用Ankura型(先健科技公司),3例(3/36,8.33%)采用Ageis型[上海微创医疗器械(集团)有限公司]。
研究组:23例(23/33,69.70%)为经皮穿刺双侧股总动脉入路,10例(10/33,30.30%)切开暴露双侧股动脉;EVAR术中支架移植物使用情况: 19例(19/33,57.58%)选用Gore Excluder或Gore C3 Excluder 型(Gore & Associates公司),14例(14/33,42.42%)选用Endurant型(Medtronic公司)。常规于瘤腔内留置导管,完成EVAR后,根据EVAR术中移植物释放后造影及术前CTA表现(主要为开放的腰动脉直径、数量及肠系膜下动脉直径)判断栓塞的密度及位置,经留置导管植入Interlock-35弹簧圈(BSC公司)行瘤腔栓塞(图1)。
1.3 术后随访与疗效评价 对2组患者均于术后12个月随访复查CTA,观察支架移植物位置及完整性,记录内瘘发生情况。
疗效评价指标包括技术成功率及临床治疗率。将术中完成栓塞腹主动脉瘤且未出现异位栓塞等并发症定义为技术成功,术后影像学随访未见瘤腔扩大及内瘘形成定义为临床成功。
1.4 统计学分析 采用SPSS 19.0统计分析软件。计量资料符合正态分布以±s表示,非正态分布则以中位数(上下四分位数)表示;计数资料以百分率表示。采用χ2检验比较2组间患者性别、EVAR治疗技术成功率及临床成功率、术后Ⅱ型内瘘发生率,对患者年龄比较采用Mann-WhitneyU检验。以P<0.05为差异有统计学意义。
2 结果
2组技术成功率均为100%,围术期均未出现肾动脉覆盖、弹簧圈异位栓塞、动脉瘤破裂等严重并发症及死亡病例。对研究组每例患者EVAR术中移植物旁瘤腔栓塞所用弹簧圈为1~6个,平均(2.32±1.16)个。
研究组临床成功率为81.82%(27/33,图1);术后12个月发生Ⅰ型内瘘2例、Ⅱ型内瘘2例、Ⅲ型内瘘2例;术后Ⅱ型内瘘发生率为6.06%(2/33)。对照组临床成功率为69.44%(25/36);术后12个月发生Ⅰ型内瘘2例、Ⅱ型内瘘9例(图2),无Ⅲ型内瘘;术后Ⅱ型内瘘发生率为25.00%(9/36)。2组临床成功率差异无统计学意义 (χ2=1.420,P=0.233),但研究组术后12个月Ⅱ型内瘘发生率明显低于对照组(χ2=4.609,P=0.032)。
3 讨论
EVAR具有早期并发症少及死亡率低等优势,目前已广泛应用于治疗腹主动脉瘤[1-3],但EVAR治疗腹主动脉瘤仍存在一定并发症风险,对部分患者需再干预或转为开放修复手术[6-7]。Schanzer等[8]的一项10 228例大型队列研究结果显示,EVAR术后5年后瘤腔扩大比例为41%,主要原因在于存在不同种类内瘘,其中以Ⅱ型内瘘最为常见。EVAR术后移植物外瘤腔内持久血流灌注即发生内瘘,Ⅱ型内瘘指血流通过侧支动脉(如腰动脉、肠系膜下动脉)灌注瘤腔。根据持续时间和复发情况,内瘘又可分为:①持续性内瘘,即内瘘持续6个月不能自愈;②复发型内瘘,即与原有内瘘来源相同的再发内瘘,且与原有内瘘是否已经自愈或复发时间长短无关。有学者[9-11]认为持续性Ⅱ型内瘘临床结局变化多样,约25%动脉瘤瘤腔可逐渐缩小甚至自愈,50%相对保持稳定,另25%则持续增大;复发性Ⅱ型内瘘EVAR术后再干预率较高和转为开放修复手术比例较高,均与瘤腔扩大有关。Zhou等[12]报道,EVAR术后12个月内Ⅱ型内瘘的发生率高达41%,发生内瘘与瘤腔扩大显著相关。
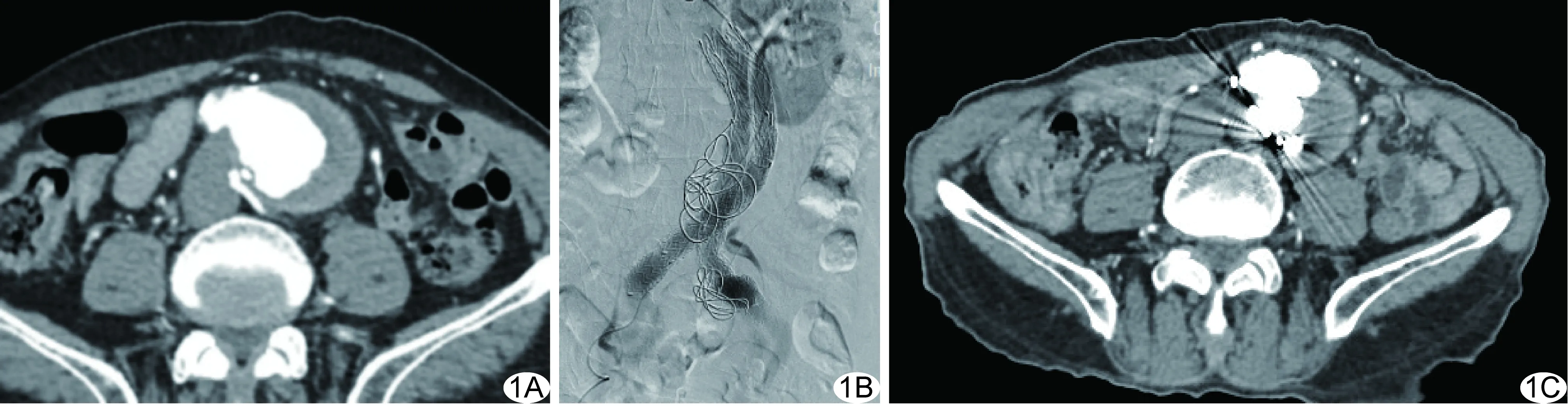
图1 患者男,78岁 A.EVAR术前CTA可见粗大的腰动脉; B.EVAR术中采用弹簧圈行移植物旁瘤腔栓塞; C.术后12个月随访复查CTA未见内瘘发生
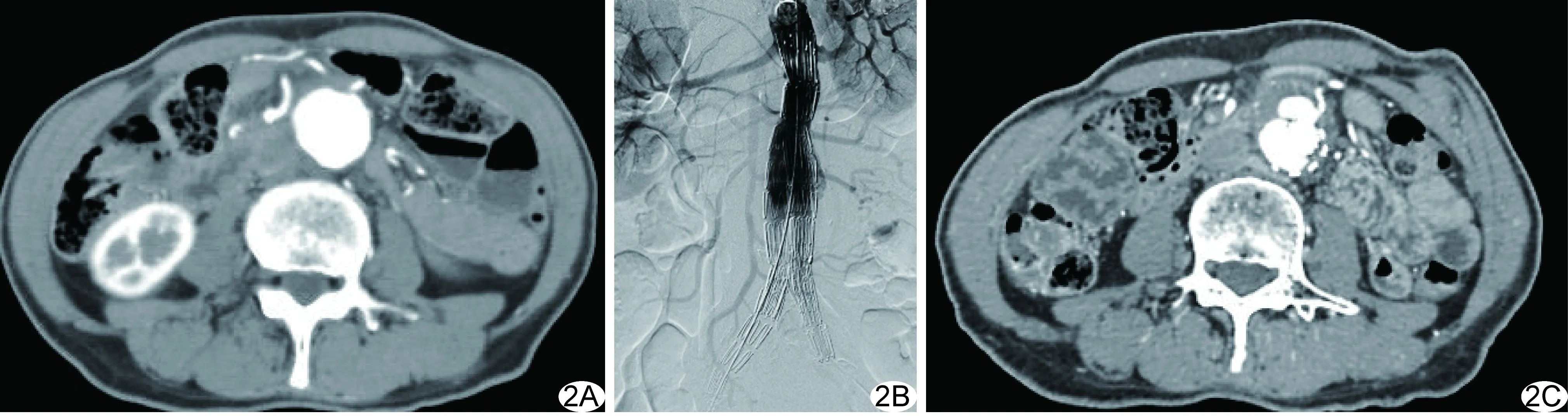
图2 患者男,72岁 A.EVAR术前CTA可见开放的肠系膜下动脉; B.EVAR术中未采用弹簧圈行移植物旁瘤腔栓塞; C.术后12个月随访复查CTA可见来源于肠系膜下动脉的Ⅱ型内瘘
Ⅰ、Ⅲ型内瘘被视为恶性内瘘,2017年美国血管外科协会腹主动脉瘤实践指南[5]推荐应对其及时进行治疗。Ⅱ型内瘘是最常见的内瘘,修复术后即时发现率高达25%。术中发现Ⅱ型内瘘时,通常无需即刻治疗,因为部分Ⅱ型内瘘可自行消失[13-14];但Ⅱ型内瘘并非均为良性,也可能引起瘤腔扩大而影响EVAR疗效,甚至导致危及生命的并发症。目前对Ⅱ型内瘘的治疗原则尚未达成广泛共识,2017年美国血管外科协会腹主动脉瘤实践指南[5]仅建议治疗与动脉瘤扩张相关的Ⅱ型内瘘(Grade 2,Level C),治疗方案包括采用弹簧圈或组织胶栓塞肠系膜下动脉或腰动脉[14]、直接经皮瘤腔内弹簧圈栓塞[15]、经下腔静脉栓塞[16]、腹腔镜下结扎IMA及腰动脉[17]等。目前尚无公认的治疗Ⅱ型内瘘的最佳方案,如何有效治疗Ⅱ型内瘘仍然是一个挑战。此外,即使再干预成功,仍有72%的患者再发内瘘[18]。有效预防Ⅱ内瘘具有重要临床意义。已有研究[19]报道,EVAR术中联合或不联合弹簧圈栓塞向瘤腔内注射纤维蛋白可促进瘤腔血栓化,预防Ⅱ型内瘘。Pilon等[20]也研究证实,向瘤腔内注射纤维蛋白及弹簧圈栓塞能够显著降低EVAR术后Ⅱ型内瘘风险。另有学者[21]认为栓塞瘤腔对预防Ⅱ型内瘘安全、有效。本研究结果显示,EVAR术中移植物旁瘤腔栓塞的技术成功率为100%,且未增加围术期并发症风险,提示采用弹簧圈进行预防性瘤腔栓塞可有效降低术后Ⅱ型内瘘的发生率[6.06%(2/33) vs 25.00%(9/36);χ2=4.609,P=0.032],所用Interlock-35可解脱带纤维毛弹簧圈,有助于促进瘤腔血栓化。
本研究中,对每例患者EVAR术中移植物旁瘤腔栓所用弹簧圈平均为(2.32±1.16)个。为不增加手术难度和治疗费用,鉴别Ⅱ型内瘘的高危因素、仅针对高危内瘘瘤腔进行栓塞十分重要。为预防来源于肠系膜下动脉的内瘘,瘤体内超选择并栓塞肠系膜下动脉具有一定手术难度,会增加X线曝光量,延长手术时间。基于Ⅱ型内瘘的血流动力学机制,动脉瘤的瘤腔类似于血管畸形的瘤巢,通过栓塞瘤腔、促进瘤腔血栓化可达到治疗目的,同时避免肠系膜下动脉栓塞可能导致的相关并发症。
有学者[21]建议通过测量瘤腔内压力来决定是否栓塞瘤腔及栓塞密度,EVAR术中应用压力传感器测量瘤腔内和体循环动脉压,将二者比值>0.16作为瘤腔栓塞的指征。本研究结合EVAR术中移植物释放后造影及术前CTA表现进行评估,根据开放腰动脉的直径、数量及肠系膜下动脉的直径判断瘤腔栓塞的密度及位置。
本研究为回顾性分析,存在选择性偏倚,单中心研究也存在样本量小的局限性,今后将进行更多随机对照研究,并对高危Ⅱ型内瘘进行栓塞治疗的亚组分析。
总之,EVAR术中移植物旁瘤腔栓塞用以预防Ⅱ型内瘘安全、有效。