超声引导经皮腹膜后穿刺置管引流前腹腔穿刺引流治疗重症急性胰腺炎
李 盈,刘明辉,王国涛,陈钦奇,刘洁玉,赵白桦
(中南大学湘雅二医院超声科,湖南 长沙 410011)
急性胰腺炎是由多种病因造成胰腺自身组织消化所致的胰腺组织水肿、出血及坏死等炎症损伤。近年来,临床诊治急性胰腺炎虽已取得一定进展,但重症急性胰腺炎仍为尚未被攻克的难题,患者死亡率居高不下[1-3]。目前对于重症急性胰腺炎的治疗模式已转变为“升阶梯治疗”,但该模式并未涉及对重症急性胰腺炎病程早期出现的腹腔及盆腔积液的处理。本研究探讨于超声引导经皮腹膜后穿刺置管引流(percutaneous retroperitoneal catheter drainage, PRCD)前先行腹腔穿刺引流(abdominal paracentesis drainage, APD)对重症急性胰腺炎的临床价值。
1 资料与方法
1.1 一般资料 回顾性分析2012年1月—2017年12月我院收治的88例重症急性胰腺炎患者的临床资料,男43例,女45例,年龄18~74岁,平均(47.9±14.0)岁。纳入标准:①年龄18~75岁;②结合临床症状和增强CT、MR等影像学检查及实验室检查,确诊为重症急性胰腺炎;③病程2周内出现腹腔及盆腔积液;④首诊于我院或在外院治疗期间未接受穿刺引流及抗生素治疗;⑤于我院接受超声引导APD和/或PRCD治疗。排除标准:①因急腹症开腹探查被诊断为急性腹膜炎;②继发于其他疾病(如胆道蛔虫)或因药物引起的急性胰腺炎;③接受内镜治疗;④超声引导ADP治疗后接受腹膜后坏死组织清除术;⑤胆源性急性胰腺炎合并胆道梗阻、有明确的胰周感染指征,因脓毒血症等原因早期接受手术治疗。88例中,42例接受单纯超声引导PRCD(单纯PRCD组),男20例,女22例,年龄20~74岁,平均(48.8±13.5)岁;46例于超声引导PRCD前接受APD(APD+PRCD组),男23例,女23例,年龄18~73岁,平均(47.0±14.6)岁。
1.2 仪器与方法 采用SuperSonic Imagine Aixplorer超声诊断仪,SC 6-1凸阵探头,频率2~5 MHz。引流导管为8~16F一次性引流导管(邦特公司)。所有患者均接受超声引导PRCD治疗,APD+PRCD组患者于PRCD前14~29天接受超声引导APD治疗。APD治疗指征:①腹腔积液、盆腔积液>50 ml;②急性胰腺炎发病2周左右;③有适当穿刺路径;需同时满足上述3条。PRCD治疗指征:①急性胰腺炎发病4周以后;②经液体复苏抗生素治疗和/或超声引导APD治疗后出现持续高热或外周血白细胞增高;③原器官衰竭症状加重或新发器官衰竭;④术前CT显示胰床区出现气体;需满足条件①并同时满足其他至少1条。APD及PRCD穿刺前,超声扫查确认最佳穿刺点,并进行标记。APD常用穿刺部位为肝周(图1)、脾周、腹腔及盆腔积液的最低位置;PRCD常用穿刺部位为左肾前间隙(图2)、右肾前间隙、胰周、小网膜囊等。常规消毒皮肤、探头,铺无菌洞巾,以2%利多卡因局部麻醉,在相应部位皮肤做1~2 cm切口。实时超声引导下进行穿刺,根据积液部位实时调整进针的角度和方向,确定针尖到达最佳位置后,操作者一手固定针芯,一手推送引流管,将引流管送至适当位置后拔出针芯(图3),以注射器回抽液体,观察抽出液体的颜色,如为黄绿色脓液,则用甲硝唑溶液冲洗,直至引流液清亮,而后于引流管外接引流袋。
1.3 评价指标 对术后患者死亡情况、并发器官衰竭和感染及恢复情况、医疗成本进行评价,指标包括死亡率、器官衰竭发生率、器官衰竭持续时间、并发感染情况(单一病原微生物感染、多种病原微生物感染、无感染)、外周血白细胞水平恢复正常所需时间、住院治疗时间、治疗期间入住重症监护室(intensive care unit, ICU)时间以及治疗费用。
1.4 统计学分析 采用SPSS 17.0统计分析软件。计量资料以±s表示,组间比较采用独立样本t检验;计数资料以百分率表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
APD+PRCD组患者术后死亡率为2.17%(1/46),单纯PRCD组为14.29%(6/42),2组间差异有统计学意义(χ2=4.40,P=0.04)。单纯PRCD组6例(6/42,14.29%)死亡患者中,4例(4/42,9.52%)死因为多器官衰竭,2例(2/42,4.76%)为严重感染;APD+PRCD组1例患者死于严重感染。
2组患者术后并发器官衰竭和感染及恢复情况、医疗成本见表1。2组间术后并发器官衰竭发生率、器官衰竭持续时间、外周血白细胞水平恢复正常所需时间、住院治疗时间、治疗期间入住ICU时间及治疗费用差异均有统计学意义(P均<0.05),并发感染情况(单一病原微生物感染、多种病原微生物感染、无感染)差异无统计学意义(P>0.05)。
3 讨论
重症急性胰腺炎为一种病理机制尚未明确的急腹症,起病急,病情进展迅速,并发症多,常危及患者生命[4-5]。急性胰腺炎病情初期,由于血管通透性增加,大量体液进入腹腔,早期即可形成大量胰腺炎相关的腹腔积液,其中含有的多种毒性物质及炎症介质可对肺脏、肾脏、肠道等重要脏器造成损害。此外,大量腹腔积液可严重影响正常肠道菌群的生态平衡,肠道黏膜屏障被破坏后,多种肠道菌群移至腹腔和腹膜,进而可引发腹腔及腹膜后感染[6-8]。既往研究[9-10]报道,约5%~15%的胰腺炎液体积聚会发展为胰腺假性囊肿,约15%胰腺炎可能合并胰腺坏死,约33%坏死胰腺炎合并感染。虽然有学者[11-12]认为急性胰腺炎早期腹腔积液为无菌积液,不必给予特殊处理,但更多学者[13-15]提出相反观点。Garcia等[15]报道,急性胰腺炎患者早期腹腔及盆腔积液的无菌液体是细菌繁衍的天然培养基,且重症急性胰腺炎患者肠道菌群失调,肠道正常菌群易移位至腹腔,引起腹腔感染。
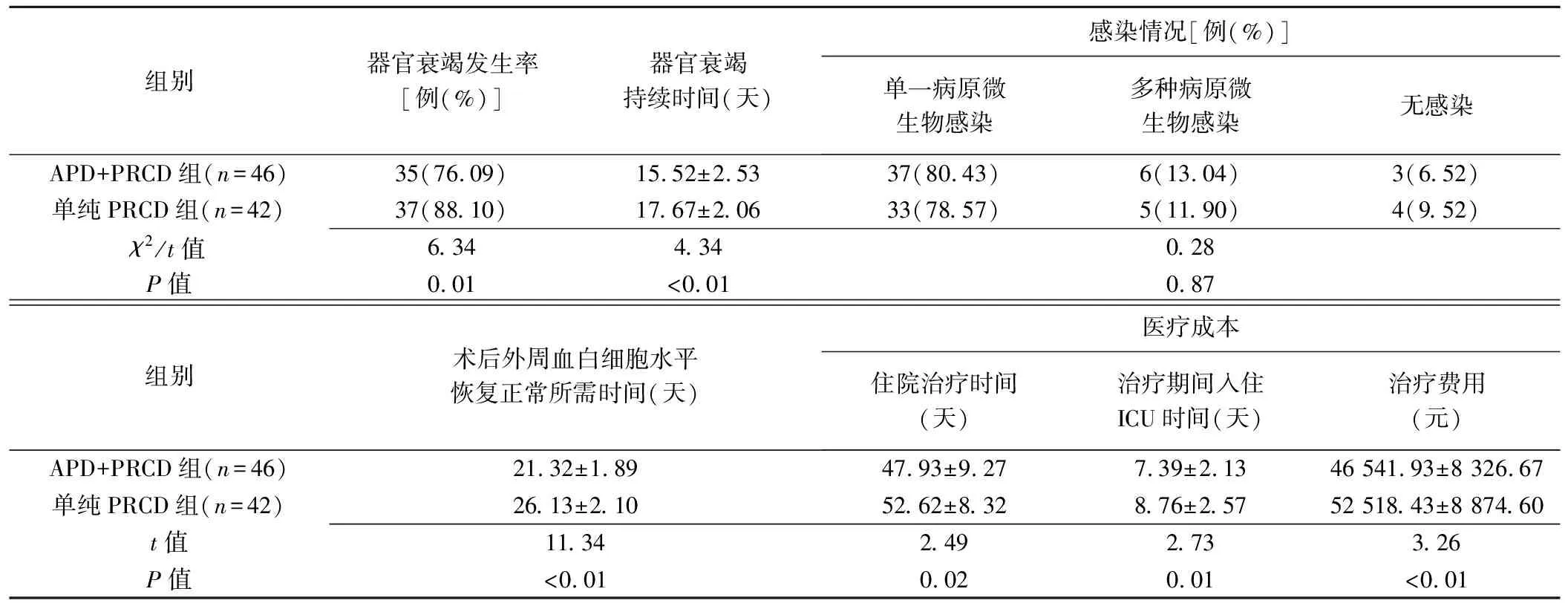
表1 2组患者器官衰竭及感染发生、治疗情况及医疗成本比较
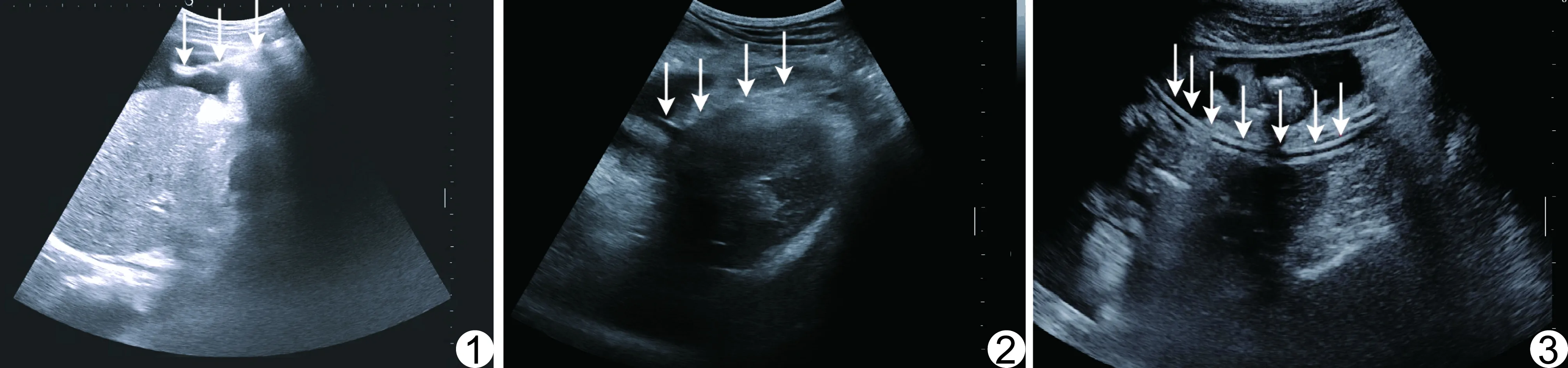
图1 重症急性胰腺炎患者,男,52岁,超声引导APD 穿刺部位为肝周,箭示穿刺针 图2 重症急性胰腺炎患者,男,54岁,超声引导PRCD 穿刺部位为左肾前间隙,箭示穿刺针 图3 重症急性胰腺炎患者,女,61岁,超声引导PRCD 箭示引流管
结合既往工作经验,笔者认为在急性胰腺炎病程早期(发病2周以内)妥善处理胰腺炎相关腹腔积液对重症急性胰腺炎患者的预后具有重要意义。Liu等[6]采用PRCD前先行APD的方法治疗中重度急性胰腺炎,患者死亡率为6.5%。本研究中APD+PRCD组患者死亡率仅为2.17%(1/46),明显低于单纯PRCD组[14.29%(6/42),χ2=4.40,P=0.04],表明超声引导PRCD前先行APD有利于降低患者死亡率,与既往研究[16]报道相符。本研究中,APD+PRCD组内无多器官衰竭导致死亡者,而单纯PRCD组中死于多器官衰竭者占9.52%(4/42),表明先行APD能够有效减少器官衰竭带来的损害,APD+PRCD组并发器官衰竭的发生率较单纯PRCD组更低(χ2=6.34,P=0.01),器官衰竭持续时间较单纯PRCD组更短(t=4.34,P<0.01),也验证了这一观点。Huang等[17]对132例患者进行回顾性和前瞻性研究,其中APD组68例,47例发生感染;非APD组64例,46例发生感染,2组间感染发生率差异无统计学意义(P>0.05)。本研究中APD+PRCD组与纯PRCD组并发感染情况(单一病原微生物感染、多种病原微生物感染、无感染)差异无统计学意义(P>0.05),表明早期APD并未增加并发的感染风险。作为一种有创操作,虽然APD在理论上有引发局部感染或全身感染及心血管并发症的风险,但早期APD实际用于治疗重症急性胰腺炎时感染风险并未更加,分析原因可能为:①目前腹腔穿刺操作技术已较为成熟,可做到全无菌操作,从而有效避免穿刺所引起的感染;②置管后通过专业的护理可减少甚至避免引流管逆行感染。
总之,超声引导PRCD前先行APD可有效减少重症急性胰腺炎患者早期腹腔及盆腔积液,减轻全身和局部炎症反应,减少并发器官功能衰竭的发生并缩短器官衰竭的持续时间,从而降低患者死亡率,但早期APD减低多器官功能衰竭风险的机制尚不十分明确,仍需进一步研究。

