土壤产电信号与线性扫描伏安法联用模拟监测湿地铜污染①
邓 欢,许 静,郭颖颖,蒋玉颖,魏琳钧,钟文辉
土壤产电信号与线性扫描伏安法联用模拟监测湿地铜污染①
邓 欢1,2,许 静1,郭颖颖1,蒋玉颖1,魏琳钧1,钟文辉2,3*
(1 南京师范大学环境学院,南京 210023;2 江苏省物质循环与污染控制重点实验室,南京 210023;3 南京师范大学地理科学学院,南京 210023)
本研究采用产电信号与线性扫描伏安法(LSV)联用,探索快速响应和鉴定湿地铜污染的方法。采集湖岸土壤并淹水用以模拟湿地环境,构建土壤产电体系并实时连续记录土壤产电电压。土壤产电60 h后,分别向体积为145 ml的淹水层中加入5 ml Cu2+浓度为300(T1)、600(T2)、1 200(T3)、2 400 mg/L(T4)的溶液。铜加入后,T1和T2处理的电压迅速降低,T3和T4处理的电压迅速上升,之后所有电压缓慢回到加铜前的水平。加铜后2 h,在淹水土壤中设置三电极体系并采用线性扫描伏安法(LSV)对污染物进行定性检测,结果显示,LSV曲线在0.162 ~ 0.182 V范围内出现单个氧化峰,峰电流值随溶液中Cu2+浓度增加而升高。为解释土壤产电信号变化特征,对加铜前后电流、阴极电势和内阻进行了检测,结果显示,加铜后T1处理电流降低,阴极电势无明显变化;T2处理电流无明显变化,阴极电势上升;而T3、T4处理电流和阴极电势都出现了明显的升高,且T4处理的内阻最低。本研究为实现土壤产电信号在监测污染方面的实际应用提供了参考。
土壤;污染监测;三电极体系;氧化峰;电压
重金属污染是湿地面临的主要污染之一。重金属通过矿山开采、金属冶炼和加工以及化工生产废水输入到湿地水体中[1-2]。传统的湿地水质检测方法依赖于人工的定期或不定期采样检测,耗时费力而且不能做到实时连续监测,导致对湿地污染事件的发现比较滞后。
土壤和底泥等沉积物中含有大量具有产电能力的细菌,包括梭菌属[3-4]、地杆菌属,以及希瓦氏菌属等多种产电细菌[5]。这些产电细菌能够将胞内分解有机质产生的电子通过位于细胞外膜上的细胞色素传递到胞外的电子受体。如果将电极材料分别埋设在沉积物内和沉积物上方的淹水层中,并采用导线将两块电极加以连接,便会有电流从导线流过(图1)。其产电原理类似于土壤微生物燃料电池[6]。
本课题在前期工作中,将Cu2+、Cd2+和芘直接加入到土壤中,抑制了土壤产电细菌活性,因此土壤产电电压峰值和产电电量随污染物浓度增加而降低[7-8],产电启动时间随污染物浓度增加而延迟[9]。这表明产电细菌能够响应重金属污染,并通过产电信号的波动及时“报告”污染事件[10]。但是对于湿地环境,重金属污染物先进入水体,再进入沉积物。因此可以设想,重金属离子进入水体后会首先扰动阴极的电化学性质,从而改变湿地产电信号,实现产电信号对重金属污染的快速响应,而不是首先扰动底泥中的产电细菌。

图1 土壤产电体系
在前期工作中,还发现土壤产电信号只与污染物毒性和浓度有关,而不能反映出污染物的类型。因此,需要与某种检测方法联用,实现对污染的定性检测。能够定性检测重金属的方法很多,例如原子吸收光谱(AAS)法、电感耦合等离子体质谱(ICP-MS)法等。这些方法的检测灵敏度高、准确性好,但是所需仪器体积大、成本高、操作复杂。采用电化学方法也可以实现对重金属的定性定量检测,包括阳极溶出伏安检测法、线性扫描伏安法(LSV)等[11]。电化学方法所需仪器成本低、操作简单。其中LSV法检测不使用化学试剂,检测时间短(扫描只需5 min)。LSV与产电信号联用有望实现快速响应和快速鉴定湿地的重金属污染,从而有助于及时发现和处理污染事件。
铜是一种主要的湿地污染物[12]。本研究以铜污染为例并采用淹水土壤模拟湿地,探索产电信号与LSV联用监测湿地铜污染的可行性。由于土壤产电信号与电流、电极电势和内阻关系密切,所以本研究检测了加铜前后的一系列电化学性质以便解释产电信号响应铜污染的机理。
1 材料与方法
1.1 土壤采集
土壤采集于南京师范大学仙林校区湖岸,土壤含水率 30%,采样深度 0 ~ 20 cm。采样地位于亚热带湿润气候区,年平均降水量1 100 mm,年平均温度15℃。土壤带回实验室阴干后,过2 mm 筛并充分混匀,部分样品自然风干后进行理化性质的测定。土壤总碳和总氮通过元素分析仪(Vario EL III,Elementar,Germany)测定;土壤pH以土水比1∶2.5由pH计测定;土壤电导率(EC)使用电导率仪(DDSJ-308F,上海雷磁)测定;土壤总Cu含量通过原子吸收光谱法(AVANTA,GBC,Australia)测定。结果为:总碳16.7 mg/g,总氮0.61 mg/g,pH 7.66,EC 65.9 μS/cm,总Cu 33.8 μg/g。
1.2 土壤产电体系构建
本研究采用淹水土壤模拟湿地。向5只250 ml玻璃烧杯中分别加入相当于120 g干重的新鲜土样,之后缓缓地向烧杯中加入蒸馏水,保持淹水土壤上方的水层体积为145 ml。两块直径为3.5 cm的圆形碳毡分别埋设在土壤底部作为阳极,放置在上层水中作为阴极。阳极和阴极使用钛丝与1 000 Ω的外阻串联。图1为本研究的土壤产电体系示意图。外阻与数据采集卡(7660B,中泰研创)并联,每隔30 min记录一次电压数据,并且每12 h对蒸发的水分进行补充。运行60 h之后进行加铜试验。为了详细记录土壤产电电压对铜污染的响应特征,加铜前将数据采集卡记录的频率从每30 min 1个电压数据调整为每1 min 1个电压数据。为了模拟野外监测的实际状况,土壤产电在自然温度下运行。
1.3 加铜试验
用CuSO4·5H2O分别配制Cu2+浓度为300、600、1 200和2 400 mg/L的溶液。分别取5 ml缓缓加入到淹水土壤的上层水中,此时上层水中理论上Cu2+浓度达到10、20、40 和80 mg/L。将加入300、600、1 200和2 400 mg/L Cu2+溶液的4只烧杯分别命名为T1、T2、T3和T4处理。对照加入5 ml蒸馏水。加铜前10 min,将数据采集卡的记录频率调整为每1 min 1个电压数据,连续记录至加铜后130 min,停止记录。依次进行内阻检测和LSV检测。LSV检测结束后,取出上层水,采用原子吸收光谱法检测其中Cu2+浓度。
1.4 电流和阴极电势检测
为了观察加铜前后电流的变化,分别采用通用型源表(2400,Keithley,USA)检测导线上的电流,以及采用Ag/AgCl参比电极检测阴极的电势。电流和阴极电势检测的时间范围为加铜前10 min至加铜后20 min,记录频率为每1 min 1个电流和电势数据。
1.5 内阻检测
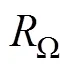
1.6 线性扫描伏安
内阻检测结束后,在土壤产电体系中直接构建三电极体系。引入铂电极为工作电极,埋设在淹水土壤中的阳极碳毡作为对电极,Ag/AgCl电极为参比电极。其中铂电极和参比电极固定在上层水中。采用多通道恒电位仪(CHI1040c,上海辰华)进行LSV检测,初始电位-0.9 V,结束电位0.5 V,扫速5 mV/s。
2 结果与分析
2.1 土壤产电电压变化
加铜前的60 h产电过程中,电压数据表现出随气温波动的特征,即中午气温较高(20 ℃左右),电压也较高(4.5 mV左右);夜晚气温较低(10 ℃左右),电压进入低谷(2.5 mV左右)。向上层水中加入CuSO4溶液之后,土壤产电电压立刻发生剧烈变化。其中,向上层水中加入5 ml 300 mg/L Cu2+和600 mg/LCu2+溶液之后,产电电压分别在7 min和4 min内降低到1.9 mV和–0.9 mV,之后缓慢回升至加铜前的电压水平;向上层水中加入1 200 mg/LCu2+和2 400 mg/LCu2+之后,产电电压分别在7 min和9 min时间内上升到8.9 mV和12.7 mV,之后缓慢回落至加铜前的电压水平。需要说明的是,因为加铜前后每个处理要检测30 min电流,而所用的Keithley 2400通用型源表每次只能检测一个处理,所以图2中的加铜时间从CK到T4处理依次延后30 min 至1 h左右。

(图中黑色箭头表示加铜,CK加入等量蒸馏水;加铜前10 min将电压数据记录频率从每30 min 1个调整为每1 min 1个。T1、T2、T3和T4分别表示加入300、600、1 200、2 400 mg/L Cu2+ 溶液,下同)
2.2 电流和阴极电势检测
加入5 ml 蒸馏水和300 mg/LCu2+溶液之后,电流呈现降低的趋势;加入600 mg/L Cu2+溶液之后,电流逐渐升高,而加入1 200和2 400 mg/L Cu2+溶液之后,电流出现快速升高(图3)。原因可能是加入600、1 200和2 400 mg/L Cu2+溶液之后,大大增加了溶液的导电性,从而提高了电流。随着加入的具有氧化性的Cu2+浓度升高,阴极电势也呈现上升趋势(图4)。但加入蒸馏水和300 mg/LCu2+溶液导致电流降低的原因尚不清楚。
2.3 内阻检测
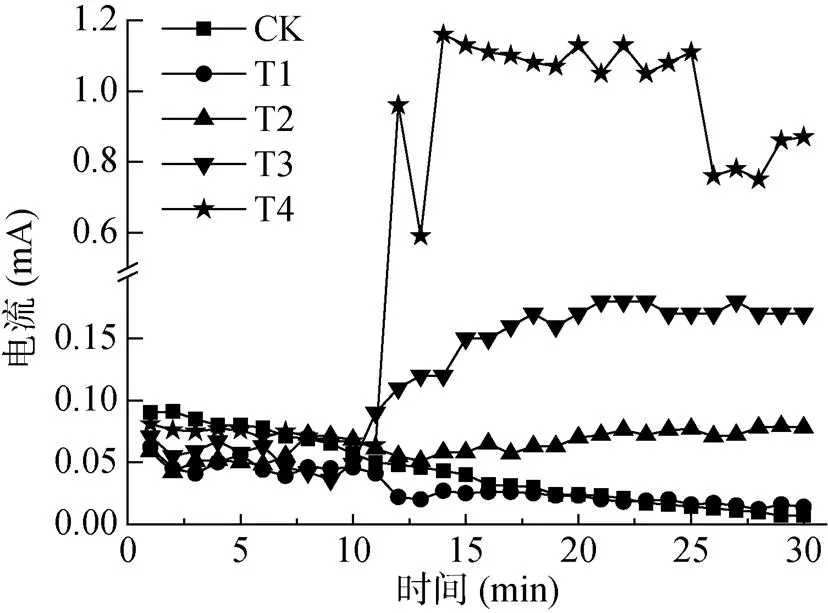
(第11 min加铜,CK加入等量蒸馏水;记录频率为每1 min 1个电流数据;下图同)
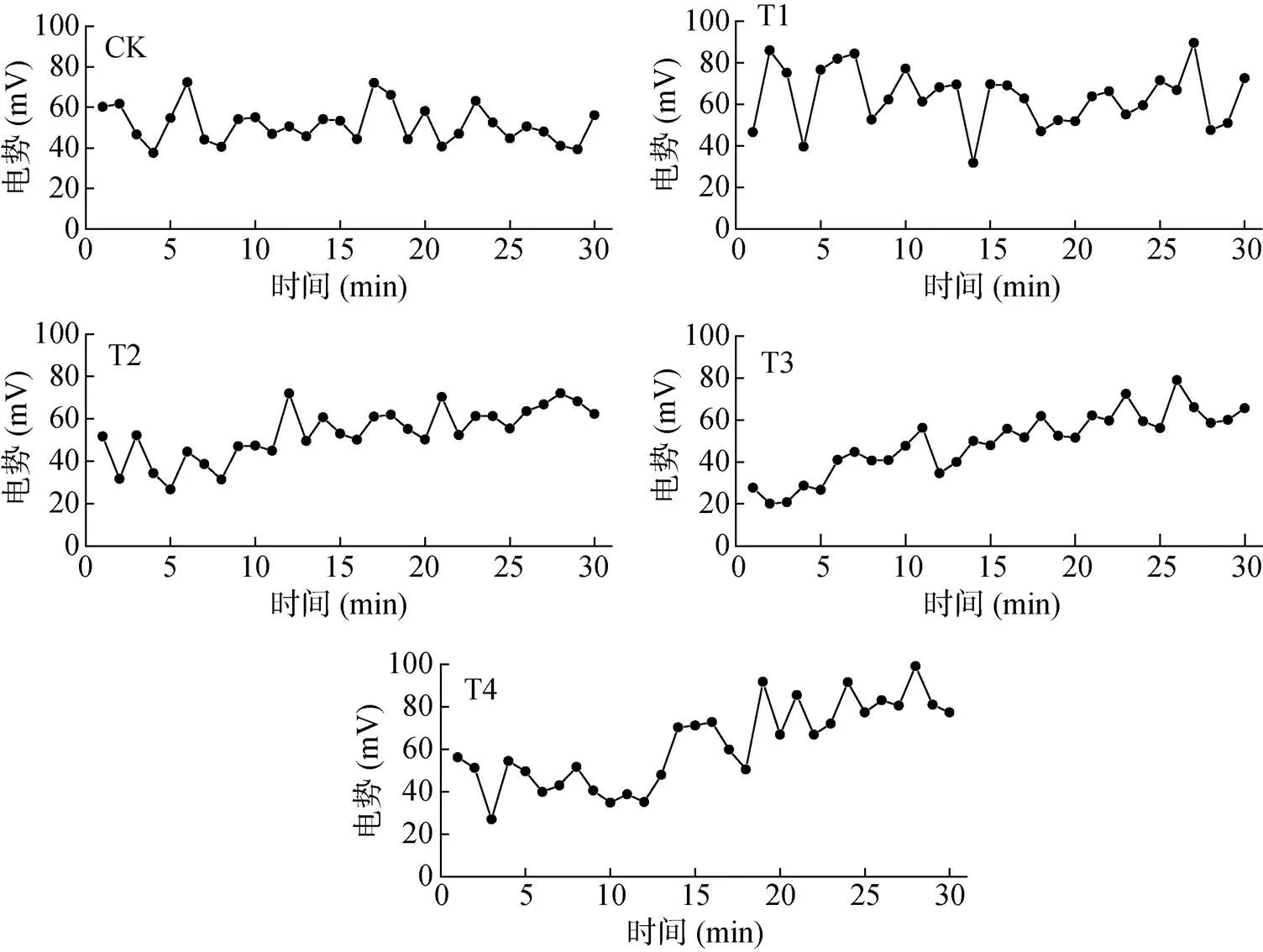
图4 加铜前后阴极电势曲线

(、和分别代表欧姆阻抗、阳极电荷传递电阻和阴极电荷传递电阻;CPE代表常相角元件)
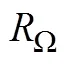
表1 不同处理的欧姆阻抗 ()、阳极电荷传递电阻()、阴极电荷传递电阻()以及内阻(R)
2.4 线性伏安扫描
加铜处理的LSV曲线在0.162 ~ 0.182 V范围内出现单个氧化峰(图6),未出现其他杂峰。各处理原子吸收法测定的Cu2+浓度值、峰电流值随溶液中Cu2+浓度增加而升高,峰电流对应的峰电位随Cu2+浓度增加逐步从0.162 V偏移至0.182 V(表2)。
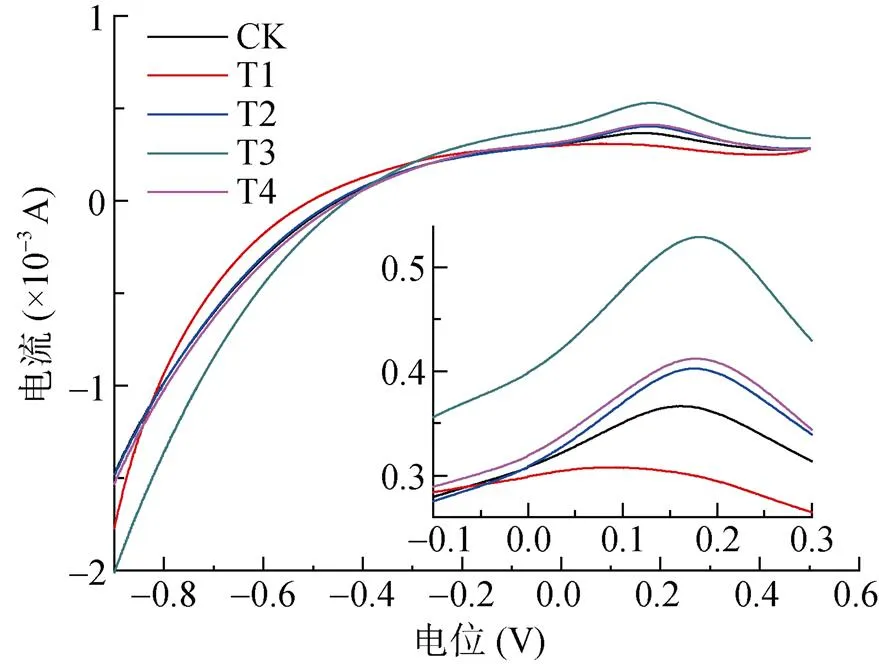
(图中小坐标图显示不同处理的峰电流局部图)

表2 线性扫描伏安曲线的峰电流和峰电位与水中Cu2+浓度的对应关系
3 讨论
本研究采用淹水土壤模拟湿地,显示土壤或底泥产生的电压信号能够对湿地水体质量进行实时连续的监测,并且能够对重金属污染做出快速响应,但电压信号不能反映出重金属污染种类。而采用LSV与产电信号联用能够弥补产电信号的这一缺陷,较好地实现对湿地铜污染的快速响应和快速定性。除此之外,电压信号对不同Cu2+浓度的响应特征存在差异;LSV峰电流也随着Cu2+浓度增加而上升,表明电压信号和LSV还能对重金属污染进行大致的定量检测。
土壤产电信号在无污染的状态下随着气温的变化而波动,这与本课题组之前的研究结果是一致的,即土壤产电电压与气温具有极显著的相关关系[14]。另外,Dai 等[15]也发现湿地底泥产电电流与气温变化的相关关系。这与产电微生物活性随温度变化有关。虽然气温和重金属输入都会造成电压信号波动,但是气温造成的波动较为缓慢和温和,而污染造成的波动较为迅速和剧烈,两类波动容易区分。因此,本研究认为电压信号对湿地重金属污染的监测不太可能受到气温的干扰。
本研究显示,在较低浓度污染下,电压信号向下波动;而较高浓度污染下,电压信号向上波动。由于阳极埋在土壤下,可以假设加入铜污染的瞬间,Cu2+还无法穿过土壤到达阳极表面,因此电压信号的变化主要与阴极电势、电流和内阻有关。为了解释电压信号响应污染的机制,本研究检测了铜污染前10 min和污染后20 min的电流和阴极电势,发现加入5 ml 1 200 mg/L和2 400 mg/L Cu2+溶液之后,阴极电势和电流上升幅度较大。在本课题组的另一项研究中,采用了铂网作为阴极,不锈钢管作为阳极,电压信号对不同Cu2+浓度的响应表现为始终向上波动[16]。原因包括Cu2+具有较强的氧化性,可作为电子受体在阴极被还原[17],以及CuSO4溶液具有酸性,能够促进以下阴极反应[18]:O2+ 4H++ 4e = 2H2O;O2+ 2H++ 2e = H2O2。
同时,本研究也显示加入5 ml 300 mg/L 和600 mg/L Cu2+溶液之后,电压信号降低。推测可能的原因是这两个铜浓度抑制了阴极碳毡上参与氧气还原的电化学活性细菌,而且由于铜浓度相比T3和T4处理的更低,对于电压的促进作用无法抵消对电化学活性细菌的抑制作用,因此表现为电压信号降低。相比于铂网电极,碳毡结构复杂,因此采用碳毡作为阴极时,电压信号对铜污染的响应特征和机制也比采用铂网电极更为复杂。
从内阻的结果和电压曲线的结果可以判断,铜污染2 h后,电压基本回复到加铜前的水平,而内阻尤其是阳极电荷传递电阻并未发生大的变化,表明阳极表面的产电细菌及其产电能力未受到明显的影响。这一方面得益于土壤对Cu2+的吸附[19];另一方面,具有产电能力的细菌多为铁还原细菌,土壤中Fe(III) 矿物在被这类细菌还原时,吸附的重金属也会释放出来,因此在长期的进化中铁还原细菌普遍具有一定的抗重金属能力。有文献表明,具有铁还原功能的地杆菌和梭菌能耐受100 μmol/L Cu2+甚至更高浓度的Co2+、Ni2+和 Zn2+[20]。本课题组从土壤中分离到的生孢梭菌()在Cu2+浓度为10 mg/L的培养液中,其产电能力与未加铜的培养液相比未显著降低[4],也印证了这一点。
在标准状态下,Cu2++ 2e →Cu,这一反应的标准电极电势为+0.342 V(相对于标准氢电极)。本研究所采用的Ag/AgCl参比电极电位高于标准氢电极+0.199 V,因此理论上,Cu2+浓度达到1 mol/L时的峰电位应为+0.143 V(相对于Ag/AgCl参比电极)。本研究中Cu2+浓度远低于标准状态,根据能斯特方程,LSV曲线的峰电位理论上应出现在0 V附近。这表明实际检测时,峰电位出现了偏移。峰电位的正向偏移或负向偏移在研究中普遍存在,与电极材料、溶液离子组成以及pH等许多因素有关[21]。例如本研究中土壤pH偏碱性,这会造成峰电位向正电位方向偏移。而且LSV的测定是在土壤产电体系中进行,LSV检测所用的对电极仍为土壤产电信号检测所用的阴极碳毡,目的是尽可能方便产电信号检测与LSV的对接,减少操作,增加实用性,但这样也引起了土壤中复杂成分对LSV检测的干扰。未来还可以改进操作,包括研究并采用修饰电极,提高对各类重金属离子检测的灵敏度和准确性[22]。
4 结论
湿地底泥产生的电压信号能够对湿地水体质量进行实时连续的监测,并且能对重金属污染做出快速响应,电压的响应特征与重金属浓度有关,但电压信号本身不能反映出重金属污染种类。而采用伏安扫描等电化学检测方法与底泥产电信号联用能够弥补产电信号的这一缺陷,并且线性伏安扫描法的峰电流强度与重金属浓度存在相关,具备一定的定量功能。因此,电压信号与伏安扫描联用有望实现对湿地重金属污染的快速响应、定性和定量。另外,虽然气温和重金属输入都会造成电压信号波动,但是气温造成的波动较为缓慢和温和,而污染造成的波动较为迅速和剧烈,因此电压信号对湿地重金属污染的监测不太可能受到气温的干扰。
[1] 高磊, 陈建耀, 王江, 等. 东莞石马河沿岸土壤重金属污染及生态毒性研究[J]. 土壤学报, 2014, 51(3): 538–546
[2] 张玉娇, 陈敏瑶, 张旭辉, 等. 不同程度重金属污染对水稻土团聚体组成的影响[J]. 土壤, 2017, 49(2): 337–344
[3] Jiang Y B, Zhong W H, Han C, et al. Characterization of electricity generated by soil in microbial fuel cells and the isolation of soil source exoelectrogenic bacteria [J]. Frontiers in Microbiology, 2016, 7: 1776
[4] Deng H, Xue H J, Zhong W H. A novel exoelectrogenic bacterium phylogenetically related to clostridium sporogenes isolated from copper contaminated soil[J]. Electroanalysis, 2017, 29(5): 1294
[5] Kim S J, Koh D C, Park S J. Molecular analysis of spatial variation of iron-reducing bacteria in riverine alluvial aquifers of the Mankyeong river[J]. The Journal of Microbiology, 2012, 50(2): 207–217
[6] 邓欢, 薛洪婧, 姜允斌, 等. 土壤微生物产电技术及其潜在应用研究进展[J]. 环境科学, 2015, 36(10): 3926– 3934
[7] Deng H, Jiang Y B, Zhou Y W, et al. Using electrical signals of microbial fuel cells to detect copper stress on soil microorganisms[J]., 2015, 66: 369–377
[8] 姜允斌, 钟文辉, 薛洪婧, 等. 土壤微生物产电信号评价芘污染毒性的研究[J]. 土壤学报, 2014, 51(6): 1332– 1341
[9] Jiang Y B, Deng H, Sun D M, et al. Electrical signals generated by soil microorganisms in microbial fuel cells respond linearly to soil Cd2+pollution[J]. Geoderma, 2015, 255/256: 35–41
[10] 邓欢, 王日, 许静, 等. 小型化土壤微生物燃料电池电信号放大电路的设计与运行[J]. 土壤, 2017, 49(3): 588– 591
[11] Nurhayati E, Juang Y, Rajkumar M, et al. Effects of dynamic polarization on boron-doped NCD properties and on its performance for electrochemical-analysis of Pb (II), Cu (II)and Hg (II) in aqueous solution via direct LSV[J]. Separation and Purification Technology, 2015, 156: 1047– 1056
[12] 潘科, 朱艾嘉, 徐志斌, 等. 中国近海和河口环境铜污染的状况[J]. 生态毒理学报, 2014, 9(4): 618–631
[13] Manohar A K, Bretschger O, Nealson K H,et al. The use of electrochemical impedance spectroscopy (EIS) in the evaluation of the electrochemical properties of a microbial fuel cell[J]. Bioelectrochemistry, 2008, 72(2): 149–154
[14] Deng H, Wu Y C, Zhang F, et al. Factors affecting the performance of single-chamber soil microbial fuel cells for power generation[J]. Pedosphere, 2014, 24(3): 330–338
[15] Dai J N, Wang J J, Chow A T, et alElectrical energy production from forest detritus in a forested wetland using microbial fuel cells[J]. GCB Bioenergy, 2015, 7(2): 244–252
[16] 吴少松, 邓欢, 刘丽, 等. 沉积物产电信号原位在线监测水体铜污染研究[J]. 环境科学学报, 2018, 38(6): 2454– 2461
[17] Wu D, Huang L P, Quan X, et al. Electricity generation and bivalent copper reduction as a function of operation time and cathode electrode material in microbial fuel cells[J]. Journal of Power Sources, 2016, 307: 705–714
[18] Wang Z J, Deng H, Chen L H, et al. In situ measurements of dissolved oxygen, pH and redox potential of biocathode microenvironments using microelectrodes[J]. Bioresource Technology, 2012, 132: 387–390
[19] Deng H, Li XF, Cheng W D, et al. Resistance and resilience of Cu-polluted soil after Cu perturbation, tested by a wide range of soil microbial parameters[J]. FEMS Microbiology Ecology, 2009, 70: 293–304
[20] Burkhardt E M, Bischoff S, Akob D M. Heavy metal tolerance of Fe(III) reducing microbial communities in contaminated creek bank soils[J]. Applied and Environmental Microbiology, 2011, 77: 3132–3136
[21] 刘雅旋. 氧还原生物阴极微生物燃料电池制备氢氧化钴[D]. 大连: 大连理工大学, 2014
[22] Cui L, Wu J, Ju H X. Electrochemical sensing of heavy metal ions with inorganic, organic and bio-materials[J]. Biosensors and Bioelectronics, 2015, 63: 276–286
Combining Use of Soil Generated Electrical Signals and Linear Sweep Voltammetry to Stimulate Copper Pollution Monitoring in Wetland
DENG Huan1,2, XU Jing1, GUO Yingying1, JIANG Yuying1, WEI Linjun1, ZHONG Wenhui2,3*
(1 College of Environment, Nanjing Normal University, Nanjing 210023, China; 2 Jiangsu Provincial Key Laboratory of Materials Cycling and Pollution Control, Nanjing 210023, China; 3 College of Geography Sciences, Nanjing Normal University, Nanjing 210023, China)
This study combines the use of soil generated electrical signals and linear sweep voltammetry to explore a way to quickly response and identify copper pollution in wetland. Soil was collected in a forest in Nanjing City and flooded to simulate the wetland. The systems for soil to generate electricity were constructed and soil generated voltage data were recorded in time and continuously. Sixty hours after soil started to generate electricity, a volume of 5 ml Cu2+solution was added into the overlaying water above the flooded soil to stimulate an event of copper pollution in wetland. The designed Cu2+concentrations of the solution were 300 (T1), 600 (T2), 1 200 (T3) and 2 400 mg/L (T4), respectively. Soil generated voltage showed response immediately after Cu2+addition, including the sudden decline for T1 and T2 treatments, and quick increase for T3 and T4 treatments. Later the voltage went back to the level before Cu2+addition. Two hours after Cu2+addition, a three-electrode mode was set in the flooded soil followed by the LSV to identify copper pollution, and the results showed that single oxidative peak appeared within the range from 0.162 V to 0.182 V in LSV curve and the peak current increased with increasing Cu2+concentration. In order to interpret the response of soil generated voltage to Cu2+addition, soil generated current, cathodic potential and impedance were measured before and after copper addition. After the addition of Cu2+, the current of T1 treatment decreased while its cathodic potential was not dramatically changed; the current of T2 treatment did not changed while its cathodic potential increased; the current and cathodic potential increased for both T3 and T4 treatment, and the internal resistance was the lowest for T4 treatment. This study may provide a reference for using soil generated electrical signals to monitor pollution.
Soil; Pollution monitoring; Three-electrode mode; Oxidative peak; Voltage
国家自然科学基金项目(41671250)和江苏省高校自然科学研究面上项目(16KJB210007)资助。
(zhongwenhui@njnu.edu.cn)
邓欢 (1982—),男,江苏南京人,博士,副教授,主要从事土壤电化学活性微生物的研究。E-mail: hdeng@njnu.edu.cn
10.13758/j.cnki.tr.2018.05.013
S153
A

