羊口疮病毒ORFV/GD-QY/01株的分离鉴定
向 蓉,翟少伦,王晓虎,陈 晶,黄 元,黄 忠,向 华
(广东省农业科学院动物卫生研究所/广东省畜禽疫病防治研究重点实验室,广东 广州 510640)
羊口疮,又称羊传染性脓疱,是由羊口疮病毒(Orf virusk, ORFV)引起的绵羊和山羊的一种接触性传染病,具有嗜上皮性,以口唇、舌、鼻、乳房等部位形成丘疹、水疱、脓疱和结成疣状结痂为特征。ORFV属于痘病毒科副痘病毒属,是一种人兽共患病原,羔羊对其最为敏感,麝牛、鹿和人也可感染[1]。羊口疮最早发现于欧洲,现已广泛分布于全世界[2]。我国也越来越常见该病的报道,新疆、甘肃、青海、内蒙古及东北三省主要养羊地区均有该病发生和流行[3-8]。随着养羊业的发展以及羊只引种等交易频繁,广东省也陆续有羊口疮的发病报道[9-10]。羊口疮传染性强,流行迅速,一只羊患病即可感染全群,导致巨大的经济损失。因此对该病及早诊断和治疗尤为重要。羊口疮病变特异,初步诊断不难,但要确诊还需进一步诊断。目前已建立不同类型的PCR检测方法,扩增的靶基因主要是B2L囊膜蛋白基因等。ORFV基因组中,BamH I酶切片段的B2L基因是一个完整的阅读框,又称为ORFV011,蛋白编码蛋白质大小为42 ku。该蛋白是病毒囊膜蛋白,可刺激淋巴细胞诱导强烈的抗体反应,B2L基因在ORFV中相对保守,能够刺激淋巴细胞增殖,引发机体产生较强的免疫应答,是ORFV重要的保护性抗原[11-13]。
2016年6月,广东省清远市某羊场的羊只疑似发病,本课题组赴羊场采样,发现病羊在口唇和舌头处发生溃疡、生疮,有的已形成痂皮或疣状病变(桑葚状痂垢),发病率较高,但死亡率低。根据临床特征、病理变化和PCR检测,诊断为羊口疮。为了获得致病毒株,本试验对病毒进行了系统的分离鉴定,并对该病毒的B2L基因与其他毒株的序列进行比对分析和遗传进化分析,以期了解广东地区ORFV流行毒株的基因分子特征,以及与其他毒株的亲缘关系。
1 材料与方法
1.1 试验材料
阳性对照为购自山东泰丰的疫苗毒。MDBK细胞株由本实验室保存,病料为广东省清远市某羊场疑似羊口疮发病山羊的唇部痂皮。
主要试剂和仪器:Premix TaqTM、100 bp NDA Ladder(Dye Plus)、DNA Marker DL2000、pMD-18T载体等购自TaKaRa公司,病毒RNA/DNA提取试剂盒、琼脂糖凝胶DNA回收试剂盒购自美基生物科技有限公司,DMEM高糖培养基、胎牛血清为Gibco公司产品。PCR扩增仪为美国BIO-RAD公司产品,凝胶成像分析系统(Tanon 1600)为上海天能科技有限公司产品。
1.2 试验方法
1.2.1 病料处理 将采回的病羊痂皮病料用无菌剪刀剪成适宜大小,无菌1×PBS缓冲液反复漂洗3次,完全剪碎后加PBS缓冲液进行研磨,研磨液制成1∶10的悬液,加青霉素、链霉素各2 000单位/mL,-20℃反复冻融3次,然后4℃浸毒过夜,3 000 r/min离心30 min,取上清液,再用孔径0.45 µm的滤器过滤,备用。
1.2.2 病毒分离和培养 MDBK细胞用含10%FBS的DMEM培养基传代培养至状态良好,待细胞铺满细胞瓶单层,用1×PBS缓冲液清洗细胞2~3次,弃掉缓冲液。接种1.2.1中处理好的病毒液1 mL,37℃ CO2培养箱中感作1 h,弃去病毒液,1×PBS缓冲液清洗细胞1~2次,再加入含2%FBS的DMEM维持液37℃继续培养,此后每天观察细胞生长和细胞病变情况,同时设正常细胞对照。当出现80%细胞病变时收毒,-20℃冻融3次,收集病毒液,同时继续传代。若细胞在接种病料后5 d内未出现病变则连续盲传3代,若第5代仍未病变视为阴性。
1.2.3 引物设计与合成 参照文献[14]针对羊口疮病毒的免疫囊膜蛋白B2L基因设计1对特异性引物,由Invitrogen公司合成。
上游引物 B2L(UP):5' ATG TGG CCG TTC TCC TC 3'
下游引物 B2L(DN):5' TTA ATT TAT TGG TTT GCA GAA CT 3'
1.2.4 病毒PCR鉴定 按照病毒RNA/DNA提取试剂盒说明书操作,从疫苗毒、病料痂皮和第1~6代传代细胞病毒液中提取DNA。以提取的病毒基因组DNA为模板扩增目的片段,PCR扩增反应体系为:2×Premix TaqTM25 µL、B2L上下游引物各2 µL、DNA模板6 µL、ddH2O 15 µL,反应条件为 94℃ 5 min;94℃ 30 s、53℃30 s、72℃90 s,30个循环;72℃10 min。取6 µL PCR产物在8 g/L琼脂糖凝胶上电泳,检测扩增结果并拍照。
对PCR产物进行切胶回收后与pMD-18T载体连接,挑取阳性克隆送Invitrogen公司测序。将测序结果在NCBI中进行BLAST比对分析,同时应用DNA Star软件的MegAlign对分离株B2L基因的测序结果进行生物信息学分析,包括将获得毒株的B2L基因核苷酸序列和NCBI中其他羊口疮毒株B2L基因进行多序列比对以及构建系统发育进化树等。
2 结果与分析
2.1 病毒分离及培养
病料悬液接种MDBK细胞后第1代未出现病变,72 h时收毒并盲传第2代,从第2代开始出现细胞病变,病变时间出现在48 h左右,继续传到第6代时细胞病变时间变得规律,细胞病变时间出现在40 h左右,细胞病变表现为:胞核浓缩、变圆、团聚、拉网、最后脱落,对照细胞表现正常(图1)。继续传代至第12代,且随着传代次数的增加出现细胞病变也更加规律,将该病毒分离株命名为ORFV/GD-QY/01。
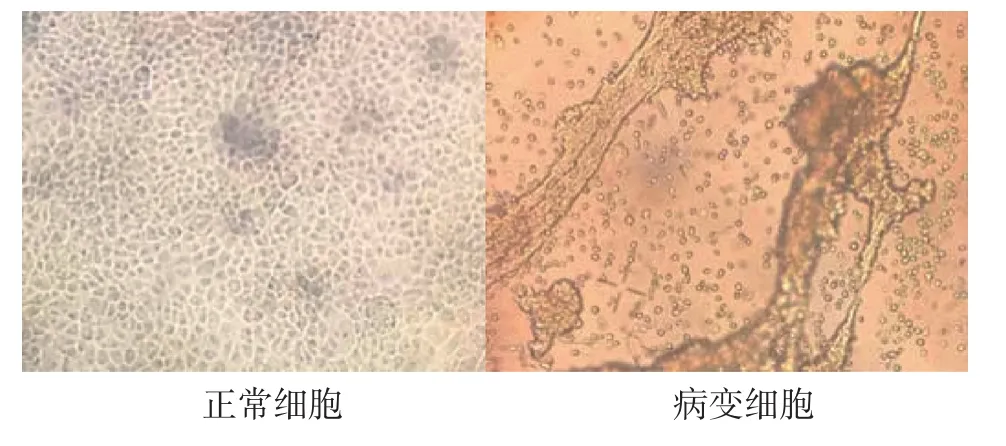
图1 MDBK细胞接种前后表现
2.2 PCR检测及测序结果
以疫苗毒阳性对照、原病料痂皮和分离毒第1~6代病毒液分别提取的病毒基因组DNA为模板进行PCR扩增,结果(图2)显示,扩增出1 137 bp左右的目的基因片段,与预期片段长度相符。目的片段测序结果见图3,序列经BLAST核酸序列搜索后,显示与测序序列相似性高的均为ORFV核酸序列,说明分离病毒为ORFV。
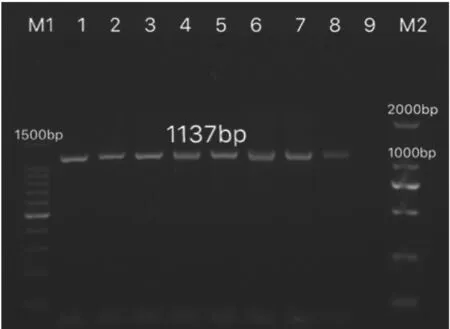
图2 痂皮及细胞毒中B2L基因PCR扩增结果

图3 ORFV/GD-QY/01的B2L基因全序列
2.3 序列分析及系统进化树构建结果
从NCBI中下载国内外发布的ORFV不同毒株B2L基因序列,与分离株ORFV/GD-QY/01的B2L基因序列进行比较分析,利用DNAStar软件计算遗传距离,根据遗传距离绘制遗传进化树。遗传进化树(图4)结果显示,ORFV/GD-QY/01分离株与台湾分离毒株(EU935106、DQ904351)的亲缘关系最近,处于同一分支上。
3 结论与讨论
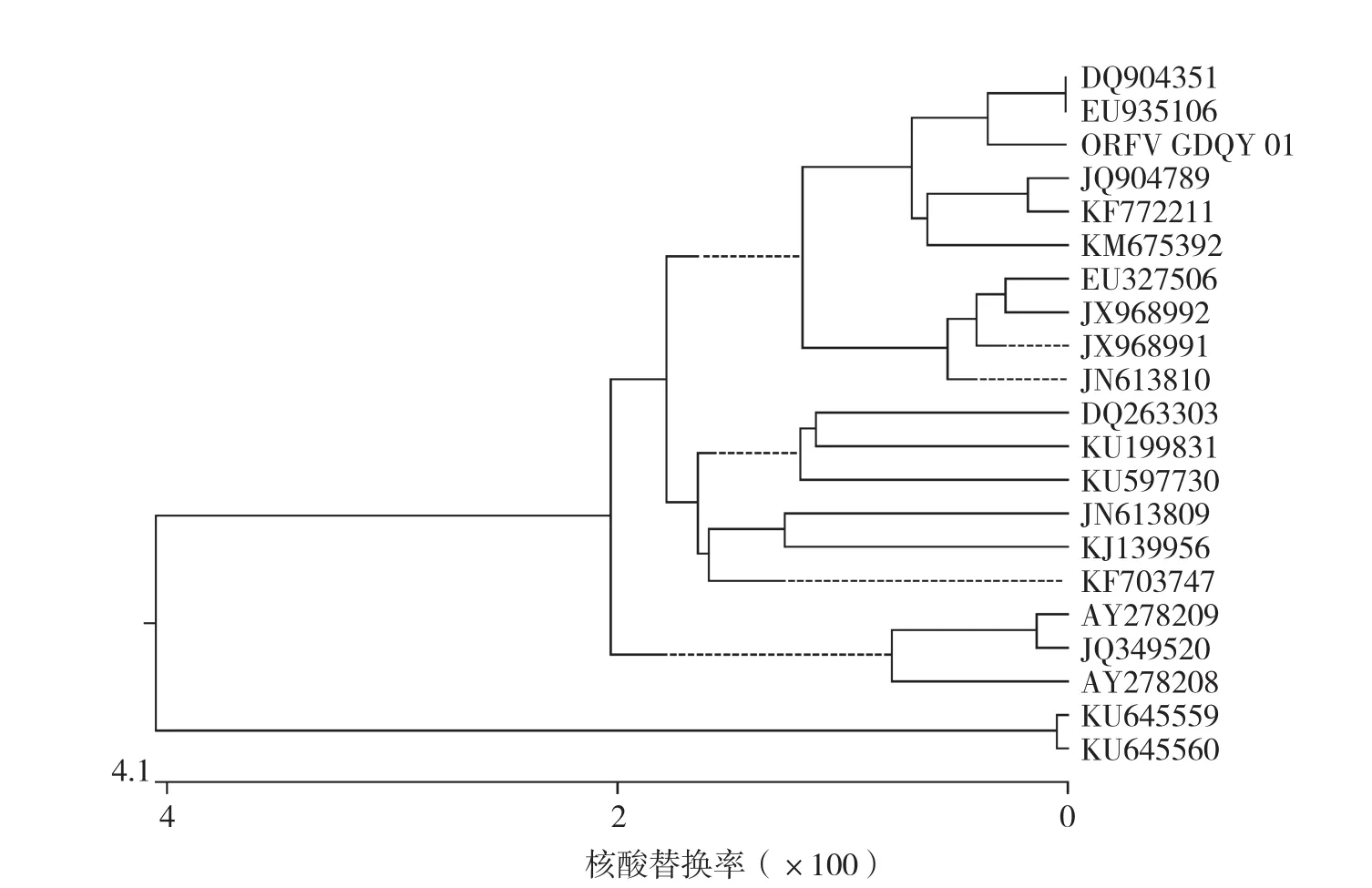
图4 B2L基因系统进化发育树
ORFV的B2L基因序列高度保守,有文献报道,不同来源的羊口疮病毒B2L基因仅有个别碱基的差别。因此,保守的B2L基因常用于鉴定该病毒。本研究根据病羊表现的典型临床症状初步诊断为羊口疮,为确诊病原,针对B2L基因设计1对特异性引物对病毒进行检测和鉴定。病料痂皮样本的PCR扩增结果显示,产物条带与预期目的基因大小一致,测序结果也证实序列为ORFV的B2L基因,因此可以确定病料中含有羊口疮病毒。将病料研磨上清液接种MDBK细胞,从第2代开始出现典型的CPE,一直传代到第12代,一直存在规律的CPE。第1~6代的细胞毒同时进行PCR检测,扩增条带均与预期目的基因大小一致,经测序鉴定为ORFV的B2L基因,表明从清远羊场病羊痂皮中分离获得1株羊口疮病病毒(ORFV/GD-QY/01)。
B2L基因产物经回收测序后,将测序结果与国内外发表的ORFV不同毒株相应的核苷酸序列进行遗传进化分析,结果表明ORFV/GDQY/01株B2L基因与台湾山羊分离株(DQ904351和EU935106)亲缘关系最近,相似性为99.2%,其次是国内福建株和陕西株等,分别为99.0%和98.4%,与国外如北美和拉丁美洲等的分离株的同源性较低,低于93.0%。这表明B2L基因虽然高度保守,但随着空间距离的扩大,在遗传上仍存在一定差异,可能是由于病毒在不同地域环境下进化过程中的变异所致。
广东省养羊规模逐渐壮大,尤其政府对牛羊养殖的鼓励政策刺激了养羊业的蓬勃发展,但目前依然存在肉羊上市量满足不了市场需求的现状[15],其中一个重要原因就是各种羊病频发,以及缺乏对疾病防治的技术和经验。羊口疮是一种人兽共患病,其病原体具有高度的嗜上皮性,引起感染部位皮肤以及粘膜增生性病变。目前,对该病的发病机制尚不清楚,但各国已经使用分子生物学的方法进行疾病诊断,并加紧进行病毒分子生物学研究和基因工程苗研究[16-17]。本研究利用MDBK细胞从发病羊场成功分离到一株羊口疮病毒,为今后进一步研制羊口疮疫苗和检测试剂打下了良好的基础,进而为该病的防控提供了技术保障。

